由稳定或短暂稳定的氮杂环卡宾(NHCs)合成配合物的早期研究大部分集中于过渡金属,包括对NHCs-金属配合物的配位和催化化学的系统研究[1].但是随着NHCs-金属配合物研究的迅速发展,NHCs作为一类超级配体,几乎影响了周期表中所有金属的配位模式和催化化学,并且涉及催化、光物理、生物有机金属化学和材料等研究领域[2].虽然NHCs-金属配合物的研究主要在催化领域,但近年来,NHCs及NHCs-金属配合物在药物化学领域的研究工作也得了蓬勃发展[3].而且科研工作者还通过向NHCs杂环引入新的官能团[4]开发具有特定性能的NHCs及NHCs-金属配合物.碳水化合物天然含量丰富,价廉易得、无毒副作用,并且具有独特的生物相容性、手性、水溶性,因而被广泛应用,是非常好的官能团[5].如将碳水化合物基团引入NHCs及NHCs-金属配合物中,可以引入手性结构,增加其水溶性和促进其生物相容性,这样结构新颖的糖基-NHCs及糖基-NHCs-金属配合物在催化和药物化学领域均显示出广阔的应用前景[6].到目前为止,糖基-NHCs及糖基-NHCs-金属配合物中的碳水化合物基团通常是基于D-吡喃葡萄糖的单糖.尽管只含单糖D-吡喃葡萄糖,但由于存在多个手性碳,因而化学结构较为复杂,特别是吡喃葡萄糖稠环上碳氢化学位移较为接近[6].文献报道的大部分糖基-NHCs-金属配合物利用核磁共振(NMR)技术进行结构确证时,通常采用一维1H NMR和13C NMR谱图进行表征,然后结合已有文献数据对糖基-NHCs-金属配合物的特征信号进行归属,详细的NMR数据归属报道较少[7-13].而设计特定功能的材料时,详细的NMR数据除了可以用于解析材料结构外,还可用于探究其机理[14].因此,利用2D NMR技术对1H NMR和13C NMR数据进行准确归属是非常重要的[15, 16].
我们曾报道溴化1-(2, 3, 4, 6-四-O-乙酰基-β-D-吡喃葡萄糖基)-3-丁基咪唑盐(化合物1)不仅能够作为配体促进钯催化的Suzuki偶联反应[17],还可以作为配体稳定钯纳米粒子,制备得到2 nm左右的NHCs-钯纳米粒子[18],也对化合物1的1H NMR和13C NMR信号进行了详尽归属[16].本文以化合物1、吡啶和醋酸钯为原料,进一步制备了空气中稳定的1-(2, 3, 4, 6-四-O-乙酰基-β-D-吡喃葡萄糖基)-3-丁基-咪唑-2-亚基]-溴化钯(Ⅱ)-吡啶(Glu-NHCs-Pd(Ⅱ)-Py,配合物2).用元素分析对其组成进行了确认;然后用液体1D和2D NMR技术,包括1H NMR、13C NMR、DEPT135、DEPT90、DEPT45、COSY、1H-13C HSQC和1H-13C HMBC对配合物2的结构进行分析和详尽归属.在配合物2结构解析时,采用了对比法,通过对比原料化合物1的NMR数据发现,NHCs作为供电子配体,吡啶环上氮原子具有吸电子作用,由于NHCs-Pd-(Ⅱ)-Py金属键的形成,1H NMR与13C NMR化学位移均有不同程度的变化,变化最大的是NHCs环上的1H NMR与13C NMR信号,分别向高场移达到0.61 ppm和向低场位移达到14.1 ppm.本文首次合成和详尽归属了手性Glu-NHCs-Pd(Ⅱ)-Py的1H NMR和13C NMR波谱数据,对手性糖基-NHCs-金属配合物的制备和结构归属具有较好的参考价值.
1 实验部分 1.1 试剂二氯甲烷、甲醇和乙腈等试剂均购于国药集团化学试剂有限公司.柱层析硅胶(300~400目)、GF薄层层析硅胶板等购于青岛海洋化工有限公司.溶剂CDCl3(99.8%氘代)、NMR样品管(ST-500,NORELL)购于青岛腾龙微波科技有限公司.
1.2 配合物2的合成化合物1按文献[17]方法合成.氮气保护下,将化合物1(1.0 mmol)、醋酸钯(1.0 mmol)、溴化钾(2.0 mmol)、吡啶(3.0 mL)依次加入25.0 mL干燥四氢呋喃中,回流反应6 h,并使用薄层色谱法(TLC)监测反应;待反应结束后,除去四氢呋喃,残余物通过柱层析分离提纯(流动相:二氯甲烷/甲醇,体积比30/1或20/1),真空干燥,得空气稳定的配合物2:淡黄色粉末,0.743 g,产率为93%.配合物2的合成见图 1所示.

|
图 1 配合物2的合成 Fig. 1 Synthesis of complex 2 |
元素分析使用德国Elementar公司Vario Micro cube元素分析仪测试.
NMR谱图均在室温[(293.0±0.1) K]条件下使用Bruker Avance III-400型超导NMR谱仪测定,使用PABBO-5 mm多核宽带探头,以CDCl3为溶剂,以TMS为内标.1H和13C NMR的工作频率分别为400.13和100.76 MHz,谱宽分别为8 223.69 Hz和24 038.46 Hz.COSY、HSQC及HMBC实验均采用标准脉冲程序.COSY的F2(1H)和F1(1H)维谱宽均为6 009.61 Hz,采样数据点阵t2×t1=2 048×256;HSQC的F2(1H)和F1(13C)维谱宽分别为6 398.86 Hz和22 136.58 Hz,采样数据点阵t2×t1=2 048×256;HMBC的F2(1H)和F1(13C)维谱宽分别为6 393.86 Hz和22 138.80 Hz,采样数据点阵t2×t1=4 096×256.
2 结果与讨论 2.1 配合物2的元素分析配合物2的元素分析理论值(%):C 39.05,H 4.41;实测值(%):C 39.06,H 4.40.两者吻合.
2.2 NMR谱图分析 2.2.1 1D NMR谱图分析1H NMR谱(图 2)显示,配合物2和化合物1在结构上存在部分共性,但由于形成了Glu-NHCs-Pd(Ⅱ)-Py配合物,两者结构上也出现了较大差异,本文结合化合物1的NMR数据[16],对配合物2的NMR谱图进行详尽解析.

|
图 2 化合物1和配合物2的1H NMR谱图(CDCl3) Fig. 2 1H NMR spectra of compound 1 and complex 2 in CDCl3 |
首先,化合物1中H-9[δH 10.82 (s, 1H)]由于配合物2中NHCs-Pd(Ⅱ)键的形成而消失,同时结合信号峰的峰型、化学位移、对应的积分面积及文献值进行解析发现,配合物2咪唑杂环上H-7和H-8的化学位移和峰型均发生了巨大的变化,由化合物1对应的δH 7.59(s, 2H)大幅度往高场移动的同时,分为两组独立的双峰δH 7.20(d, J=2.2 Hz, 1H)和δH 6.98(d, J=2.3 Hz, 1H),分别向高场区移动了0.39 ppm和0.61 ppm,这可能受到吡啶氮杂环的各向异性效应,但进一步归属需要借助2D NMR技术及参考文献数据[16].结合峰型、化学位移、对应的积分面积,可以对几个较为明显的特征峰进行归属:δH 6.78(d, J=9.5 Hz, 1H)归属为H-1,与化合物1相比向低场移动了0.21 ppm;δH 9.06(m, 2H)归属为H-22;δH 7.37(m, 2H)归属为H-23;δH 7.79(m, 1H)归属为H-24;δH 1.03(t, J=8.1 Hz, 3H)归属为H-21,向低场移动了0.05 ppm.
图 3为配合物2的13C NMR谱,由于NHCs-Pd(Ⅱ)-Py配合物的生成,改变了配合物的电子云密度,因此显著地影响了配合物中碳原子的化学位移,与化合物1相比,大部分碳原子的化学位移向低场发生移动,特别是距离Pd(Ⅱ)较近的C-1、C-9和C-18,其中C-1(δC 86.2)的化学位移向低场移动2.5 ppm;原料化合物1的四个乙酰基由中两组信号峰靠得太近,难以区分,配合物2中呈现出4个独立信号峰.

|
图 3 化合物1和配合物2的13C NMR谱图(CDCl3) Fig. 3 13C NMR spectra of compound 1 and complex 2 in CDCl3 |
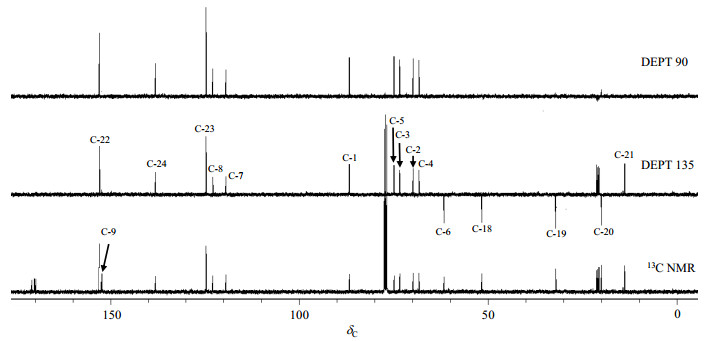
通过图 4的DEPT谱可以判断配合物2有5个伯碳(δC 13.7、20.1、20.2、20.5、20.8),4个仲碳(δC 20.6、31.4、51.3、61.3),10个叔碳(δC 67.9、69.4、72.9、74.4、86.2、119.0、122.6、124.2、137.7、152.3),4个季碳(δC 169.2、169.5、169.6、170.3)和1个Pd-C(δC 151.5).详尽归属配合物2的NMR数据需要结合其2D NMR谱,特别是HSQC和HMBC谱.
|
图 4 配合物2的13C NMR和DEPT谱图(CDCl3) Fig. 4 13C NMR and DEPT spectra of complex 2 in CDCl3 |
在配合物2的COSY NMR谱(图 5)中,δH 5.47(t, J=8.0 Hz, 1H)与H-1存在交叉峰,可归属为H-2,与化合物1相比向低场移动了0.19 ppm;δH 5.59(t, J=8.0 Hz, 1H)与H-2存在交叉峰,归属为H-3,向低场移动了0.14 ppm;δH 5.22(t, J=8.0 Hz, 1H)与H-3和H-2同时存在交叉峰,归属为H-4,化学位移几乎不变.它们向低场位移的距离随着对应质子与Pd(Ⅱ)中心的距离增大而减小.H-5与H-4存在交叉峰,C-5是不对称碳原子,δH 4.11(m, 1H)归属为H-5,向高场移动了0.18 ppm.但是H-6与H-5未见交叉峰,H-6上存在两个质子,由于糖分子的稠环结构,H-6a与H-6e是不等价的,在COSY谱上呈现交叉峰,参考文献[16]及1H-13C HSQC(图 6)和1H-13C HMBC(图 7)谱图将δH 4.28(m, 1H)归属为H-6a,化学位移几乎没有变化,δH 4.17(m, 1H)归属为H-6e,向低场移动了0.04 ppm.在COSY谱中,δH 1.49(m, 2H)与H-21存在交叉峰,归属为H-20,向低场移动了0.16 ppm;δH 2.04(m, 2H)和H-20存在交叉峰,归属为H-19,向低场移动了0.15 ppm;出人意外的是,H-18裂分为两组独立的信号峰,H-19和H-18的两组氢均存在交叉峰,结合COSY、HSQC和HMBC谱,将δH 4.75(m, 1H)和δH 4.26(m, 1H)归属为H-18,分别向低场移动了0.36 ppm和向高场移动了0.13 ppm.基于上述解析,对大部分NHCs-Pd(Ⅱ)-Py配合物2骨架氢原子化学位移进行了归属.从以上解析可以看出,化学位移基本上向低场移动,其移动幅度一般随质子与Pd(Ⅱ)中心的距离增大而减小.

|
图 5 配合物2的COSY谱(CDCl3) Fig. 5 COSY spectrum of complex 2 in CDCl3 |
|
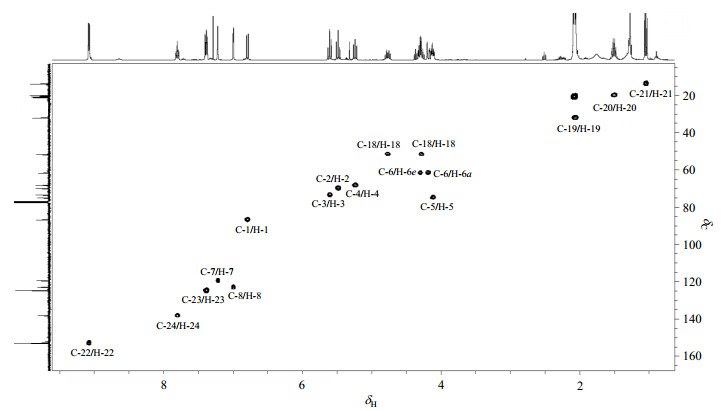
图 6 配合物2的1H-13C HSQC谱图(CDCl3) Fig. 6 1H-13C HSQC spectrum of complex 2 in CDCl3 |
|
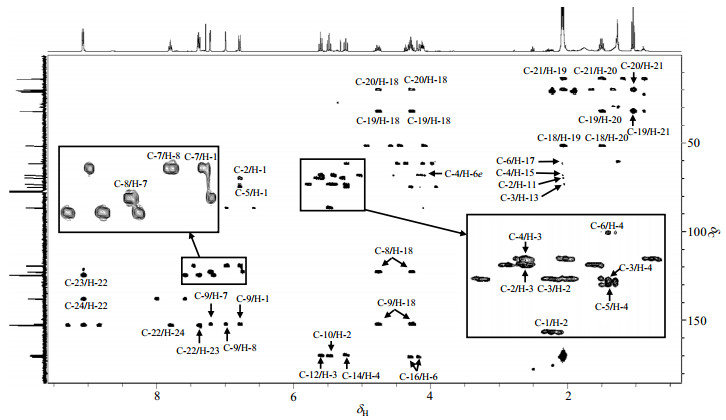
图 7 配合物2的1H-13C HMBC谱图(CDCl3) Fig. 7 1H-13C HMBC spectrum of complex 2 in CDCl3 |
在HSQC谱中,δC 152.3与H-22相关,归属为C-22;δC 124.2与H-23相关,归属为C-23;δC 137.7与H-24相关,归属为C-24;δC 122.6和119.0与H-7和H-8相关,具体归属尚需借助HMBC谱;δC 86.2与H-1相关,归属为C-1;δC 72.9与H-3相关,归属为C-3;δC 69.4与H-2相关,归属为C-2;δC 67.9与H-4相关,归属为C-4;δC 74.4与H-5相关,归属为C-5.δC 61.3与H-6a和H-6e均有相关,归属为C-6;δC 51.3与H-18相关,归属为C-18;δC 31.4与H-19相关,归属为C-19;δC 20.6与H-20相关,归属为C-20;δC 13.7与H-21相关,归属为C-21.
综上,咪唑环上2个叔碳(C-7和C-8,δC 119.0和122.6)、乙酰基上4个羰基季碳(C-10、C-12、C-14和C-16,δC 170.3、196.5、196.2和169.6)和4个伯碳(C-11、C-13、C-15和C-17,δC 20.8、20.5、20.2和20.1)的化学位移无法准确归属,需要参考文献同时辅以HMBC谱进行解析.
利用配合物2的HMBC谱对咪唑环上2个叔碳(δC 119.0和122.6)进行归属,δC 119.0是咪唑环上C-7或C-8,它与H-1有交叉峰,归属为C-7,δC 122.6归属为C-8.通过HSQC谱图将7.20(d, J=2.2 Hz)归属为H-7,δH 6.98(d, J=2.3 Hz)归属为H-8.HMBC谱上显示C-8与δH 4.75(m, 1H)和δH 4.26(m, 1H),即H-18有交叉峰.4个羰基季碳(C-10、C-12、C-14和C-16)可以通过它们与糖稠环上质子的相关信号来解析.在HMBC谱中,δC 169.6与H-2相关,归属为C-10;δC 169.5与H-3相关,归属为C-12;δC 169.2与H-4相关,归属为C-14;δC 170.3与H-6a与H-6e相关,归属为C-16.
利用HMBC图谱,有两种方法可以对乙酰基上4个甲基质子进行归属.(1)通过糖稠环上碳的相关峰来解析,δH 2.05(s, 3H)与C-2有交叉峰,归属为H-11;δH 2.04(s, 3H)与C-3有交交叉峰,归属为H-13;δH 2.06(s, 3H)与C-4有交叉峰,归属为H-15;δH 2.07(s, 3H)与C-6有交叉峰,归属为H-17.(2)通过它们与乙酰基上4个羰基碳的相关峰来解析,δH 2.05(s, 3H)与C-10有交叉峰,归属为H-11;δH 2.04(s, 3H)与C-12有交叉峰,归属为H-13;δH 2.06(s, 3H)与C-14有交叉峰,归属为H-15;δH 2.07(s, 3H)与C-16存在交叉峰,归属为H-17.通过HSQC谱图,将δC 20.2归属为C-11、δC 20.1归属为C-13、δC 20.5归属为C-15、δC 20.8归属为C-17.至此,所有的1H和13C NMR信号均得到了归属,详细数据见表 1.
| 表 1 化合物1和配合物2的1H和13C NMR归属 Table 1 1H and 13C NMR assignments of compound 1 and complex 2 |
NHCs作为经典的供电子配体,其咪唑杂环2号位的碳原子具有良好的配位能力,吡啶环上的氮原子具有吸电子作用,是sp2杂化,同时具有孤对电子,整体上是平面六元环结构.化合物1为原料,其分子内含有阴、阳离子基团,它与醋酸钯、吡啶反应,NHCs与吡啶的共同配位而得到稳定配合物2.化合物1和配合物2的化学位移对比见表 1,从对比数据可以看出,1H NMR化学位移相差较大的是H-7和H-8,差值分别为0.39 ppm和0.61 ppm.由配合物2的糖环和丁基链上质子化学位移变化可以看出,与化合物1相比,配合物2糖环上质子的化学位移变化也有一定的规律,如糖环上H-1、H-2和H-3均向低场移动,且随着距离变大而变小,分别向低场移动0.21,0.19和0.14 ppm,当距离进一步加大时,如H-4基本上没有明显变化,由于杂原子氧的存在,H-5向高场移动了0.18 ppm.H-6a基本没变化,H-6e向低场位移.丁基链上质子向低场位移较多,β-和γ-位碳上质子递减.同样,H-18的位移裂分成两组多重峰,分别向低场移动了0.36 ppm和向高场移动了0.13 ppm,H-19和H-20均向低场位移,其变化规律与文献报道[7]类似,可能是由吡啶环的屏蔽和去屏蔽效应引起的.
13C NMR化学位移相差最大的是C-9,向低场位移了14.1 ppm;而咪唑环上的C-7和C-8,仅向高场位移了0.4 ppm和0.1 ppm.由于糖基的稠环上存在多个弱配位的氧,同时乙酰基氧原子上也有两对孤电子对,相比不存在共轭键的丁基来说,NHCs-Pd(Ⅱ)-Py金属键的形成对糖基电子云的变化影响较大,比如与咪唑环相连的糖基稠环C-1的化学位移向低场移动2.5 ppm,C-2的化学位移向高场移动1 ppm,而丁基上的C-18的化学位移向低场移动1 ppm,C-19的化学位移向高场移动仅为0.4 ppm.
3 结论本文首次制备了手性1-(2, 3, 4, 6-四-O-乙酰基-β-D-吡喃葡萄糖基)-3-丁基-咪唑-2-亚基]-溴化钯(Ⅱ)-吡啶配合物.用元素分析对其组成进行了确认,运用液体1D和2D NMR技术对其结构进行分析和全归属.发现在供电子配体氮杂环卡宾,和具有屏蔽和去屏蔽效应的吡啶环,以及糖基稠环上存在的多个弱配位氧质子和乙酰基氧原子孤电子对的共同作用下,配合物2的D-吡喃葡萄糖稠环骨架和丁基的1H NMR与13C NMR化学位移的变化较为明显;相对而言,糖基稠环上碳氢化学环境变化更大.变化最大的是NHCs环上的1H NMR与13C NMR信号,分别向高场移达到0.61 ppm和向低场位移达到14.1 ppm.
| [1] | BIFFIS A, CENTOMO P, DEL ZOTTO A, et al. Pd metal catalysts for cross-couplings and related reactions in the 21st century:a critical review[J]. Chem Rev, 2018, 118(4): 2249-2295. DOI: 10.1021/acs.chemrev.7b00443. |
| [2] | DANOPOULOS A A, SIMLER T, BRAUNSTEIN P. N-heterocyclic carbene complexes of copper, nickel, and cobalt[J]. Chem Rev, 2019, 119(6): 3730-3961. DOI: 10.1021/acs.chemrev.8b00505. |
| [3] | DODDI A, PETERS M, TAMM M. N-heterocyclic carbene adducts of main group elements and their use as ligands in transition metal chemistry[J]. Chem Rev, 2019, 119(12): 6994-7112. DOI: 10.1021/acs.chemrev.8b00791. |
| [4] | AN Y Y, YU J G, HAN Y F. Recent advances in the chemistry of N-heterocyclic-carbene-functionalized metal-nanoparticles and their applications[J]. Chin J Chem, 2019, 37(1): 76-87. DOI: 10.1002/cjoc.201800450. |
| [5] | MARRADI M, CHIODO F, GARCíA I, et al. Glyconanoparticles as multifunctional and multimodal carbohydrate systems[J]. Chem Soc Rev, 2013, 42(11): 4728-4745. DOI: 10.1039/c2cs35420a. |
| [6] | ZHAO W, FERRO V, BAKER M V. Carbohydrate-N-heterocyclic carbene metal complexes:synthesis, catalysis and biological studies[J]. Coord Chem Rev, 2017, 339: 1-16. DOI: 10.1016/j.ccr.2017.03.005. |
| [7] | NISHIOKA T, SHIBATA T, KINOSHITA I. Sugar-incorporated N-heterocyclic carbene complexes[J]. Organometallics, 2007, 26(5): 1126-1128. DOI: 10.1021/om061128d. |
| [8] | HENDERSON A S, BOWER J F, GALAN M C. Carbohydrate-based N-heterocyclic carbenes for enantioselective catalysis[J]. Org Biomol Chem, 2014, 12(45): 9180-9183. DOI: 10.1039/C4OB02056A. |
| [9] | HENDERSON A S, BOWER J F, GALAN M C. Carbohydrates as enantioinduction components in stereoselective catalysis[J]. Org Biomol Chem, 2016, 14(17): 4008-4017. DOI: 10.1039/C6OB00368K. |
| [10] | TEWES F, SCHLECKER A, HARMS K, et al. Carbohydrate-containing N-heterocyclic carbene complexes[J]. J Organomet Chem, 2007, 692(21): 4593-4602. DOI: 10.1016/j.jorganchem.2007.05.007. |
| [11] | SHI J C, LEI N, TONG Q S, et al. Synthesis of chiral imidazolinium carbene from a carbohydrate and its Rhodium(I) complex[J]. Eur J Inorg Chem, 2007, 2007(15): 2221-2224. DOI: 10.1002/ejic.200700027. |
| [12] | SHIBATA T, ITO S, DOE M, et al. Dynamic behaviour attributed to chiral carbohydrate substituents of N-heterocyclic carbene ligands in square planar nickel complexes[J]. Dalton Trans, 2011, 40(25): 6778-6784. DOI: 10.1039/c0dt01833c. |
| [13] | IMANAKA Y, HASHIMOTO H, KINOSHITA I, et al. Incorporation of a sugar unit into a C-C-N pincer Pd complex using click chemistry and Its dynamic behavior in solution and catalytic ability toward the Suzuki-Miyaura coupling in water[J]. Chem Lett, 2014, 43(5): 687-689. DOI: 10.1246/cl.140017. |
| [14] | ASENSIO J M, TRICARD S, COPPEL Y, et al. Knight shift in 13C NMR resonances confirms the coordination of N-heterocyclic carbene ligands to water-soluble palladium nanoparticles[J]. Angew Chem Int Ed, 2016, 129(3): 883-887. |
| [15] |
ZHOU Z G, LIU P, TONG Q S, et al. NMR studies on methyl 4, 6-O-benzyl idene-3-deoxy-3-(salicylideneamino)-α-D-altropyranoside[J].
Journal of Fujian Normal University, 2009, 5: 78-80.
周中高, 刘沛, 童庆松, 等. 甲基3-脱氧-3-(2-羟基苄叉氨基)-4, 6-O-苄叉基-α-D-阿卓吡喃糖苷的NMR研究[J]. 福建师范大学学报, 2009, 5: 78-80. |
| [16] |
ZHOU Z G, YUAN Y Y, HUANG L, et al. Spectral analysis of glucose-based chiral N-heterocyclic carbene precursors[J].
Chinese J Magn Reson, 2018, 35(2): 215-225.
周中高, 元洋洋, 黄丽, 等. 葡糖衍生手性N-杂环卡宾前体波谱学数据分析[J]. 波谱学杂志, 2018, 35(2): 215-225. |
| [17] | ZHOU Z G, QIU J, XIE L, et al. Synthesis of chiral imidazolium salts from a carbohydrate and their application in Pd-catalyzed Suzuki-Miyaura reaction[J]. Catal Lett, 2014, 144(11): 1911-1918. DOI: 10.1007/s10562-014-1323-4. |
| [18] | ZHOU Z G, LI M, LIU G S, et al. Ultra-small sugar-substituted N-heterocyclic carbenes protected Pd nanoparticles and catalytic activity[J]. Appl Organomet Chem, 2019, 33(7): e4942. |
 2020, Vol. 37
2020, Vol. 37 
