2. 大连理工大学 化学分析测试中心 辽宁 大连 116024;
3. 大连理工大学 精细化工国家重点实验室, 辽宁 大连 116023
2. Chemistry Analysis and Inspection Center, Dalian University of Technology, Dalian 116024, China;
3. State Key Laboratory of Fine Chemicals, Dalian University of Technology, Dalian 116023, China
N-酰腙(NAH)骨架(-CONHN=)是药物设计和药物化学中常用且很有前途的骨架,N-酰腙类化合物是药物化学中的重要化合物,具有抗癌、抗糖尿病、抗炎、抗惊厥、抗结核、抗抑郁、抗HIV、抗血小板聚集等广谱的生物学活性[1-3].咔唑(Cz)和三嗪并吲哚(Ti)骨架也是重要的药效团,其衍生物具有多种重要的生物活性.如咔唑衍生物具有抗癌[4, 5]、抗糖尿病[5-7]、抗病毒[8]、抗结核[9]、抗菌[10]和抗炎[11]等药理活性;三嗪并吲哚衍生物在抗癌[12, 13]、抗糖尿病[14, 15]、抗惊厥、抗菌[16]、抗抑郁[16-18]、抗疟疾[19]和抗结核[20]等方面有着重要的应用前景.若将N-酰腙、咔唑和三嗪并吲哚这三个药效团杂交,形成的新杂交化合物有望改善其生物活性、拓宽其应用前景.鉴于此,本课题组在前期工作[5, 21]的基础上,设计并合成了一个基于咔唑-三嗪并吲哚的新型N-酰腙衍生物3,即2-(5H-[1, 2, 4]三嗪[5, 6-b]吲哚-3-硫基)-N'-(9-乙基咔唑-3-亚甲基)乙酰肼.
本文利用元素分析、红外光谱(IR)、1D和2D核磁共振(NMR)技术(包括1H NMR、13C NMR、1H-1H COSY、1H-13C HSQC、1H-13C HMBC和NOESY)确定了化合物3的结构,并对其两种异构体(A和B)的1H和13C NMR数据进行了全归属,测量了其偶合常数(J值)及异构体所占的比例.本文对此类化合物的结构解析以及构效关系的研究具有参考意义.
1 实验部分 1.1 新化合物3的合成向干燥的三口瓶中,加入自行合成[22]的0.3 mmol 9-乙基-3-甲酰基咔唑(2)、10.0 mL无水乙醇和3滴冰醋酸(约为10 μL),室温下搅拌0.5 h后,再加入自行合成[21]的0.3 mmol 3-肼羰基甲基硫代-5H-1, 2, 4-三嗪[5, 6-b]吲哚(1),继续室温搅拌0.5 h,再加热回流6 h.反应结束后,抽滤出固体,得到乳白色片状粗产品.空气中晾干后,用N, N-二甲基甲酰胺(DMF)重结晶,得到0.124 g浅黄色粉末状晶体目标化合物3,产率为86.1%,熔点 > 280 ℃.化合物3的合成和结构如图 1所示.

|
图 1 2-(5H-[1, 2, 4]三嗪[5, 6-b]吲哚-3-硫基)-N'-(9-乙基咔唑-3-亚甲基)乙酰肼(新化合物3)的合成路线 Fig. 1 Synthetic route of 2-(5H-[1, 2, 4]triazine[5, 6-b]indol-3-ylthio)-N'-(9-ethylcarbazol-3-ylmethylene)acetylhydrazine (new compound 3) |
IR光谱在TENSOR 27型红外分光光度计(德国)上完成,KBr压片;元素分析在Vario EL III元素分析仪(德国Elementar公司)上完成.
1D和2D NMR实验均在Bruker AVANCE III 500 MHz型超导NMR谱仪上完成,以四甲基硅烷(TMS)为内标,以DMSO-d6(氘化率为99.9%,CIL,含0.03% TMS,购自北京恒思锐科贸有限公司)为溶剂.实验温度为298.0 K,1H和13C NMR的工作频率分别为500.03 MHz和125.73 MHz,谱宽分别为10 330.6 Hz和29 761.9 Hz.2D NMR(1H-1H COSY、1H-13C HSQC、1H-13C HMBC和NOESY)实验均采用标准脉冲序列.1H-1H COSY的F2(1H)和F1(1H)维谱宽均为7 246.4 Hz,采样数据点阵为t2×t1=2 048×256;1H-13C HSQC的F2(1H)和F1(13C)维谱宽分别为6 410.3 Hz和20 827.8 Hz,采样数据点阵为t2×t1=2 048×256;1H-13C HMBC的F2(1H)和F1(13C)维谱宽分别为6 410.3 Hz和27 927.4 Hz,采样数据点阵为t2×t1=2 048×256;NOESY的F2(1H)和F1(1H)维谱宽为6 410.3 Hz,混合时间为0.6 s,采样数据点阵为t2×t1=2 048×256.
2 结果与讨论 2.1 元素分析和IR光谱元素分析C26H21N7OS实测值(%):C 64.87,H 4.59,N 20.23;理论值(%):C 65.12,H 4.41,N 20.45.
IR光谱:3 202(vN-H),3 060(v=CH),2 977和2 868(vC-H),1 656(vC=O),1 627(vC=N),1 598、1 580、1 493和1 475(vC=C).
元素分析和IR光谱数据与新化合物3的结构相符,初步证明了此化合物的结构.
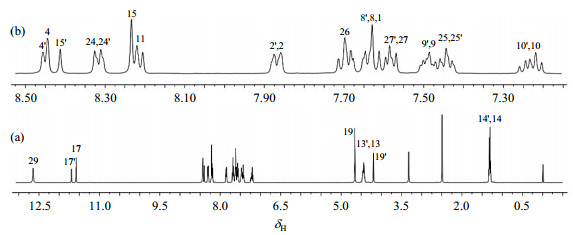
2.2 NMR谱分析与结构确定观察新化合物3的1H NMR谱(图 2)发现,高场区SCH2(δH 4.00~5.00)和低场区CONH(δH 11.50~12.00)的1H NMR信号数目均大于理论数目,且成对出现;其13C NMR谱图(图 3)也出现了谱线增多的现象.这说明新化合物3在DMSO-d6溶剂中可能存在异构体.此外,观察1H和13C NMR谱发现,咔唑和三嗪并吲哚环的1H或13C NMR信号因化学位移比较接近而归属困难.
|
图 2 新化合物3的1H NMR谱. (a)全谱;(b)局部放大谱(δH 7.1~8.5) Fig. 2 1H NMR spectra of the new compound 3. (a) Full spectrum; (b) Partial enlarged spectrum (δH 7.1~8.5) |
|
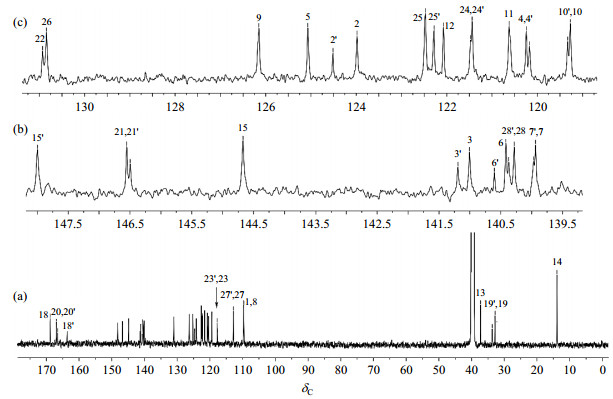
图 3 新化合物3的13C NMR谱图. (a)全谱;(b)和(c)分别为δC 139.5~148.5和δC 119~131的局部放大谱 Fig. 3 13C NMR spectra of the new compound 3. (a) Full spectrum; (b) and (c) Partial enlarged spectrum at δC 139.5~148.5 and δC 119~131 |
根据文献[23, 24]可知,N-酰腙可能存在四种异构体,两个关于亚胺键(C=N)的几何异构体(E/Z)和两个关于酰胺N-C(O)键的构象异构体(cis/trans).在极性较大的溶剂中(如DMSO-d6),C=N双键主要以E异构体的形式存在,因为空间位阻,Z异构体存在的可能性小,E异构体比Z异构体更稳定;而N-C(O)基团在cis/trans旋转异构体之间相互转化(即CO的氧原子与NH的氢原子处于顺式/反式),因此存在着cis/trans两种构象异构体,即发生图 4中的A(E/cis)和B(E/trans)两种异构体之间的相互转化.所以,新化合物3的1H和13C NMR谱中有谱线增多的现象.

|
图 4 新化合物3的两种异构体A和B的结构及原子编号 Fig. 4 Structures and atomic labels for isomers A and B of the new compound 3 |
2D NMR技术对于确定复杂化合物的结构及1H和13C NMR信号峰的归属非常有效[25-27].因此,本文利用1D和2D NMR(包括1H NMR、13C NMR、1H-1H COSY、1H-13C HSQC、1H-13C HMBC和NOESY)技术对新化合物3进行了结构确定,并对其1H和13C NMR数据进行了全归属.
根据电子云密度可知,13C NMR谱中最低场δC 168.7处的峰,可直接归属为C-18.根据HMBC谱(图 5)可知,C-18与δH 11.59和δH 4.67、δH 11.59与δC 144.7,δH 4.67与δC 166.7存在着远程相关,由此可归属δH 11.59和δH 4.67分别为H-17和H-19,δC 144.7和δC 166.7可分别归属为C-15和C-20.根据HSQC谱(图 6)即可归属出H-15(δH 8.23)和C-19(δC 32.7).

|
图 5 新化合物3的1H-13C HMBC谱. (a)全图;(b)部分放大图 Fig. 5 1H-13C HMBC spectra of the new compound 3. (a) Full spectrum; (b) Partial enlarged spectrum |

|
图 6 新化合物3的1H-13C HSQC谱. (a)全图;(b)部分放大图 Fig. 6 1H-13C HSQC spectra of the new compound 3. (a) Full spectrum; (b) Partial enlarged spectrum |
根据文献[23, 24]可知,在极性较大的溶剂中(如DMSO-d6),E/cis为主要异构体,E/trans为次要异构体.在1H NMR谱中,δH 4.67和δH 4.21的积分面积分别为0.62和0.38.由此可知,δH 4.21为H-19'.同理δH 11.71可归属为H-17'.由HMBC谱可知,H-17'与δC 148.0和δC 163.4、H-19'与δC 163.4和δC 166.4存在远程耦合,所以δC 148.0、δC 163.4和δC 166.4可分别归属为C-15'、C-18'和C-20'.由HSQC谱可归属出H-15'(δH 8.41)和C-19'(δC 33.5).
根据电子云密度,可直接将13C NMR谱中高场区的δC 37.1和δC 13.7分别归属为C-13和C-14.由HSQC谱可知,C-13和C-14分别与δH 4.44/δH 4.47(q, J=7.0 Hz)和δH 1.32/δH 1.33(t, J=7.5 Hz)存在交叉峰,因此,δH 4.44/δH 4.47和δH 1.32/δH 1.33可分别归属为H-13/H-13'和H-14/H-14'.观察13C NMR谱可知,C-13和C-14旁未出现相应的异构体信号峰,这说明C-13与C-13'及C-14与C-14'信号峰重叠.
咔唑环的归属:由HMBC谱可知,C-15与δH 7.867(d, J=8.5 Hz)和δH 8.44,δH 7.867与δC 140.4,δH 8.44与δC 140.4和δC 122.1,δC 122.1与δH 7.22(t, J=7.5 Hz)分别存在着远程耦合,所以δH 7.867和δH 8.44可分别归属为H-2和H-4,δC 140.4和δC 122.1分别归属为C-6和C-12,δH 7.22归属为H-10.由1H-1H COSY谱(图 7)可知,H-2与δH 7.62(d, J=8.5 Hz)、H-10与δH 8.21(d, J=7.5 Hz)和δH 7.486(td, J=7.8, 1.0 Hz)、δH 7.486与δH 7.637(d, J=8.5 Hz)存在相关,因此δH 7.62、δH 8.21、δH 7.486和δH 7.637可分别归属为H-1、H-11、H-9和H-8.再根据HSQC谱可分别归属出相应的C-1(δC 109.5)、C-2(δC 124.0)、C-4(δC 120.24)、C-8(δC 109.4)、C-9(δC 126.2)、C-10(δC 119.27)和C-11(δC 120.6).由HMBC谱可知,H-1和H-11与δC 125.1,H-9与δC 139.9存在远程耦合,因此δC 125.1和δC 139.9可分别归属为C-5和C-7.同理,由HMBC谱可知,C-15'与H-2'(δH 7.872)(d, J=8.5 Hz)和H-4'(δH 8.45),H-2'(δH 7.872)与C-6'(δC 140.6),C-12与H-10/H-10'(δH 7.24)(t, J=7.5 Hz)和H-8/H-8'(δH 7.644)(d, J=8.5 Hz)存在着远程耦合.再根据HSQC谱,可分别归属出相应的C-2'(δC 124.5)、C-4'(δC 120.17)和C-10'(δC 119.33).根据1H-1H COSY谱可知,H-10'与δH 7.492(td, J=7.8, 1.0 Hz)存在交叉峰,因此δH 7.492归属为H-9'.由HMBC谱可知,H-9'与δC 140.0存在着远程相关,δC 140.0可归属为C-7'.

|
图 7 新化合物3的部分放大1H-1H COSY谱 Fig. 7 Partial enlarged 1H-1H COSY spectrum of the new compound 3 |
观察1H和13C NMR谱发现(图 2和图 3),主要异构体H-1和H-11信号峰旁未出现次要异构体的信号峰,这说明H-1与H-1'、H-11与H-11'信号峰重叠;C-1、C-5、C-8、C-9、C-11和C-12信号峰也不是成对出现的峰,这说明次要异构体与主要异构体的相应信号峰重叠.此外,在1H-13C HMBC谱中,未观察到H-1与C-3存在远程偶合相关峰,而H-1'与H-1又重叠,所以C-3和C-3'暂时无法归属,将其放置于最后归属.
1, 2, 4-三嗪并[5, 6-b]吲哚环归属:1H NMR谱中,在δH 8.15~8.50范围内尚有两组双峰未归属(δH 8.25~8.35).由新化合物3的结构可知,它们可能是H-24/H-24'或H-27/H-27'.因H-27/H-27'邻位连有NH基团,共轭效应的结果使H-27/H-27'上的电子云密度增大,H-24/H-24'较H-27/H-27'位于低场.所以根据电子云密度可知,1H NMR谱中δH 8.32和/或δH 8.31(d, J=8.0 Hz)可直接归属为H-24和/或H-24'.由1H-1H COSY谱可知,H-24与δH 7.443(t, J=7.5 Hz),δH 7.443与δH 7.70(td, J=7.5, 1.0 Hz),δH 7.70与δH 7.58(d, J=8.0 Hz),H-24'与δH 7.438(t, J=7.5 Hz)存在交叉峰,所以δH 7.443、δH 7.70、δH 7.58和δH 7.438可分别归属为H-25、H-26、H-27和H-25'.由HSQC谱可归属出相应的C-24(δC 121.4)、C-24'(δC 121.5)、C-25(δC 122.5)、C-26(δC 130.8)、C-27(δC 112.67)和C-25'(δC 122.3).根据HMBC谱可知,H-24与δC 130.9和δC 140.3,H-26与δC 140.3,H-25与δC 117.62存在着远程相关,因此δC 130.9、δC 140.3、δC 117.62可分别归属为C-22、C-28、C-23.此外,由HMBC谱还观察到,H-24'与δC 140.4,C-25'与δH 7.59,δH 7.59与δC 117.57存在远程耦合,因此δC 140.4、δH 7.59和δC 117.57可分别归属为C-28'、H-27'和C-23'.根据HSQC谱可归属出C-27'(δC 112.71).
观察1H NMR谱发现,H-26(td, J=7.5, 1.0 Hz)信号峰的峰面积显示为1个质子,这说明H-26与H-26'信号峰重叠.观察13C NMR谱发现,在δC 130.5~131.0范围内只有C-22和C-26信号峰,再无其它峰,这说明C-22与C-22'、C-26与C-26'信号重叠.
13C NMR谱中还剩余δC 146.6、δC 146.5、δC 141.0和δC 141.2尚未归属.由新化合物3的结构可知,C-21/C-21'直接与两个氮原子相连,而C-3/C-3'则是与碳原子相连,诱导效应的结果使C-21/C-21'的核外电子云密度低于C-3/C-3',因此C-21/C-21'较C-3/C-3'在低场出峰.根据电子云密度,δC 146.6、δC 146.5、δC 141.0和δC 141.2它们可直接归属为C-21、C-21'、C-3和C-3'.1H NMR谱中还剩余δH 12.66尚未归属,可直接归属为H-29.由1H NMR谱可知,H-29积分面积显示其为1个氢原子,说明H-29'与H-29信号峰重叠.
至此,新化合物3的两种异构体(A和B)的1H和13C NMR信号峰归属完毕(表 1).
| 表 1 新化合物3的1H和13C NMR归属(DMSO-d6, 500 MHz) Table 1 1H and 13C NMR data of the new compound 3 (DMSO-d6, 500 MHz) |
新化合物3的构型及咔唑环的取向确定:由NOESY谱(图 8)可以看出,H-17与H-15,H-17'与H-15'存在着交叉峰,说明这些氢原子在空间上距离比较近,新化合物3的A和B两种异构体中关于亚胺键(C=N)均是以E构型存在.H-15与H-4存在交叉峰,由此可以确定A异构体(主要异构体)中咔唑环的取向如图 4所示.在NOESY谱中H-17与H-19无交叉峰存在,说明A异构体中关于酰胺N-C(O)键是以cis构型存在,即CO中的氧原子与NH中的氢原子处于同侧.而H-17'与H-19'存在交叉峰,说明B异构体(次要异构体)中关于酰胺N-C(O)键是以trans构型存在,即CO中的氧原子与NH中的氢原子处于异侧.在1H NMR谱中,由于H-4'较H-4处于低场,说明H-4'与N-16'存在着分子内氢键,据此可确定出B异构体中咔唑环的取向如图 4所示.由上述分析可确定新化合物3的A和B两种异构体的构型,即在DMSO-d6中,室温下,新化合物3的A异构体是以E/cis形式存在,B异构体是以E/trans形式存在,且A异构体是主要的,它们的空间结构如图 4所示.

|
图 8 新化合物3的NOESY谱 Fig. 8 NOESY spectrum of the new compound 3 |
根据1H NMR谱中H-17/H-17'和H-19/H-19'峰面积的平均值,可计算出新化合物3的两种异构体A和B的含量分别为62.8%和37.2%.
3 结论综合利用元素分析、IR光谱、NMR技术对新化合物3,即基于咔唑-三嗪并吲哚的N-酰腙衍生物的两种异构体(A和B)的1H和13C NMR信号进行了全归属,给出了相应的偶合常数(J值)及异构体所占的比例,确定了它们的空间结构.实验结果表明,新化合物3在DMSO-d6中,室温下,存在着E/cis(A)和E/trans(B)两种异构体,并且E/cis为主要异构体,其含量为62.8%.本文的研究结果对此类化合物1H和13C NMR信号的归属以及结构与活性关系的研究具有重要意义.
| [1] | KUMAR V. Hydrazone:A promising pharmacophore in medicinal chemistry[J]. J Pharmacogn Phytochem, 2018, 7(2): 40-43. |
| [2] | JADNA SILVA FREDERICO M, JHONATAN GOMES CASTRO A, MASCARELLO A, et al. Acylhydrazones contribute to serum glucose homeostasis through dual physiological targets[J]. Curr Top Med Chem, 2012, 12(19): 2049-2058. DOI: 10.2174/156802612804910232. |
| [3] | CERQUEIRA J V, MEIRA C S, DE SOUZA SANTOS E, et al. Anti-inflammatory activity of SintMed65, an N-acylhydrazone derivative, in a mouse model of allergic airway inflammation[J]. Int Immunopharmacol, 2019, 75: 105735. DOI: 10.1016/j.intimp.2019.105735. |
| [4] | ISSA S, PRANDINA A, BEDEL N, et al. Carbazole scaffolds in cancer therapy:a review from 2012 to 2018[J]. J Enzyme Inhib Med Chem, 2019, 34(1): 1321-1346. DOI: 10.1080/14756366.2019.1640692. |
| [5] |
LI Y J, WANG S Y, JIN K, et al. Synthesis and Cdc25B/PTP1B inhibitory activity evaluation of novel acylhydrazone derivatives containing carbazole moity[J].
Chin J Org Chem, 2019, 39(2): 491-499.
李英俊, 王思远, 靳焜, 等. 新型含咔唑环酰腙衍生物的合成及Cdc25B/PTP1B抑制活性评价[J]. 有机化学, 2019, 39(2): 491-499. |
| [6] |
LI Y J, ZHAO Y, JIN K, et al. Synthesis and PTP1B/TCPTP Inhibitory Activity Evaluation of Novel 2, 5-Disubstituted-1, 3, 4-thiadiazolamide Derivatives Containing Carbazole/Benzimidazole Moity[J].
Chin J Org Chem, 2019, 39(9): 2599-2608.
李英俊, 赵月, 靳焜, 等. 含咔唑/苯并咪唑环的2, 5-二取代-1, 3, 4-噻二唑酰胺衍生物的合成及对PTP1B/TCPTP抑制活性的评价[J]. 有机化学, 2019, 39(9): 2599-2608. |
| [7] | TANG Y B, LIU J Z, ZHANG S E, et al. 3-Phenylpropanoic acid-based phosphotyrosine (pTyr) mimetics:Hit evolution to a novel orally active protein tyrosine phosphatase 1B (PTP1B) inhibitor[J]. Chem Med Chem, 2014, 9(5): 918-921. DOI: 10.1002/cmdc.201400007. |
| [8] | CARUSO A, CERAMELLA J, IACOPETTA D, et al. Carbazole derivatives as antiviral agents:An overview[J]. Molecules, 2019, 24(10): 1912. DOI: 10.3390/molecules24101912. |
| [9] | SHAIKH M S, KANHED A M, CHANDRASEKARAN B, et al. Discovery of novel N-methyl carbazole tethered rhodanine derivatives as direct inhibitors of Mycobacterium tuberculosis InhA[J]. Bioorg Med Chem Lett, 2019, 29(16): 2338-2344. DOI: 10.1016/j.bmcl.2019.06.015. |
| [10] | TAMENE D, ENDALE M. Antibacterial activity of coumarins and carbazole alkaloid from roots of clausena anisata[J]. Adv Pharmacol Sci, 2019: 5419854. |
| [11] | MAHAPATRA D K, DADURE K M, SHIVHARE R S. Edema reducing potentials of some emerging Schiff's bases of murrayanine[J]. MOJ Bioorg Org Chem, 2018, 2(4): 171-174. |
| [12] | ZHANG Q, DING D, ZENG S X, et al. Structure and activity analysis of Inauhzin analogs as novel antitumor compounds that induce p53 and inhibit cell growth[J]. PLoS one, 2012, 7(10): e46294. DOI: 10.1371/journal.pone.0046294. |
| [13] | ALI R, SAAD H. Synthesis of some novel fused pyrimido[4", 5":5', 6']-[1, 2, 4] triazino[3', 4':3, 4] [1, 2, 4] triazino[5, 6-b]indoles with expected anticancer activity[J]. Molecules, 2018, 23(3): 693. DOI: 10.3390/molecules23030693. |
| [14] | ZHAN J Y, MA K, ZHENG Q C, et al. Exploring the interactional details between aldose reductase (AKR1B1) and 3-mercapto-5H-1, 2, 4-triazino[5, 6-b]indole-5-acetic acid through molecular dynamics simulations[J]. J Biomol Struct Dyn, 2019, 37(7): 1724-1735. DOI: 10.1080/07391102.2018.1465851. |
| [15] | RAHIM F, TARIQ S, TAHA M, et al. New triazinoindole bearing thiazole/oxazole analogues:Synthesis, α-amylase inhibitory potential and molecular docking study[J]. Bioorg Chem, 2019, 92: 103284. DOI: 10.1016/j.bioorg.2019.103284. |
| [16] | SHRUTHI N, POOJARY B, KUMAR V, et al. Synthesis and biological evaluation of N-(substituted phenyl)-2-(5H-[1, 2, 4] triazino[5, 6-b] indol-3-ylsulfanyl)acetamides as antimicrobial, antidepressant, and anticonvulsant agents[J]. Russ J Bioorg Chem, 2015, 41(2): 223-230. DOI: 10.1134/S1068162015020144. |
| [17] | SHELKE S M, BHOSALE S H, MAHADIK K R. 3-(5H-[1, 2, 4] Triazino[5, 6-b]indol-3-ylthio)-N-(substituted phenyl)propionamides:Synthesis and antidepressant activity evaluation[J]. Der Pharma Chemica, 2010, 2(4): 169-177. |
| [18] | ASWAR U M, KALSHETTI P P, SHELKE S M, et al. Effect of newly synthesized 1, 2, 4-triazino[5, 6-b]indole-3-thione derivatives on olfactory bulbectomy induced depression in rats[J]. Asian Pac J Trop Biomed, 2012, 2(12): 992-998. DOI: 10.1016/S2221-1691(13)60012-X. |
| [19] | KGOKONG J L, SMITH P P, MATSABISA G M. 1, 2, 4-Triazino[5, 6-b]indole derivatives:effects of the trifluoromethyl group on in vitro antimalarial activity[J]. Bioorg Med Chem, 2005, 13(8): 2935-2942. DOI: 10.1016/j.bmc.2005.02.017. |
| [20] | SIVENDRAN S, JONES V, SUN D, et al. Identification of triazinoindol-benzimidazolones as nanomolar inhibitors of the Mycobacterium tuberculosis enzyme TDP-6-deoxy-D-xylo-4-hexopyranosid-4-ulose 3, 5-epimerase (RmlC)[J]. Bioorg Med Chem, 2010, 18(2): 896-908. DOI: 10.1016/j.bmc.2009.11.033. |
| [21] |
LI Y J, LIU X J, LIU J H, et al. Synthesis and PTP1B inhibitory activity evaluation of novel carbazole-based carbohydrazone derivatives[J].
Chin J Org Chem, 2020, 40(2): 478-488.
李英俊, 刘雪洁, 刘季红, 等. 基于咔唑的新型碳酰腙衍生物的合成及PTP1B抑制活性评价[J]. 有机化学, 2020, 40(2): 478-488. |
| [22] | HAMID H M A. Functionalised 1, 2, 4-triazino[5, 6-b]indoles[J]. J Chem Res, 2004, 2004(3): 183-185. DOI: 10.3184/0308234041640735. |
| [23] | ZHOU M, EUN Y J, GUZEI I A, et al. Structure-activity studies of divin:an inhibitor of bacterial cell division[J]. ACS Med Chem Lett, 2013, 4(9): 880-885. DOI: 10.1021/ml400234x. |
| [24] | HIZLIATEŞ C G. Arylidene carbazole carbohydrazides:Synthesis and characterization[J]. Hacettepe J Biol Chem, 2018, 46(2): 169-175. |
| [25] |
LI Y J, YANG K D, JIN K, et al. NMR study of a novel carbazole-isatin based bis-thiocarbohydrozone derivative[J].
Chinese J Magn Reson, 2019, 36(1): 83-92.
李英俊, 杨凯栋, 靳焜, 等. 基于咔唑-靛红双-硫代碳酰腙衍生物的NMR研究[J]. 波谱学杂志, 2019, 36(1): 83-92. |
| [26] |
YIN T P, WANG Z, CHEN Y, et al. An NMR analysis of 10-indol cytochalasin chaetoglobosin F[J].
Chinese J Magn Reson, 2019, 36(1): 74-82.
尹田鹏, 汪泽, 陈阳, 等. 10-吲哚细胞松弛素chaetoglobosin F的NMR解析[J]. 波谱学杂志, 2019, 36(1): 74-82. |
| [27] |
LI Y J, LI J Y, JIN K, et al. An NMR study of a novel N-acylhydrazone derivative containing benzimidazole moiety[J].
Chinese J Magn Reson, 2017, 34(1): 25-34.
李英俊, 李继阳, 靳焜, 等. 含苯并咪唑环N-酰腙衍生物的NMR研究[J]. 波谱学杂志, 2017, 34(1): 25-34. |
 2020, Vol. 37
2020, Vol. 37 