丁氟螨酯(结构如图 1所示),英文名为Cyflumetofen,商品名为Danisaraba(Otsuka),化学名为2-甲氧乙基(R, S)-2-(4-叔丁基苯基)-2-氰基-3-(α, α, α-三氟邻甲苯基)丙酸酯,CAS登录号为400882-07-7,分子式为C24H24F3NO4,分子量为447.45.其原药为白色或乳白色固体颗粒,纯品为白色固体,为日本大冢化学公司开发的新型酰基乙腈类杀螨剂.丁氟螨酯为非内吸性杀螨剂,主要是起到触杀作用[1].该药剂对哺乳动物、水生植物、有益生物及红蜘蛛的天敌等非靶标生物均十分安全,且其在土壤和水中代谢迅速、残留较少,是对环境十分友好的农药[2].

|
图 1 丁氟螨酯结构式 Fig. 1 The chemical structure of cyflumetofen |
已有文献报道丁氟螨酯的应用研究、残留问题及色谱分析方法:冯开阳等[3]研究了丁氟螨酯的抗性问题,乔岩等[4]介绍了丁氟螨酯防治草莓二斑叶螨的效果,Hayashi等[5]研究了丁氟螨酯的作用方式,李敏敏、刘新刚等[6-8]研究了丁氟螨酯的环境降解行为及色谱检测方法;但尚未见到其波谱学数据的报道.而对化合物结构进行分析,波谱学数据的归纳是必要的.近年来有很多关于化合物波谱学数据解析的研究:张明光等[9]确证了盐酸贝西沙星的结构,林云良等[10]对卢立康唑的波谱学数据做了全归属,梁向晖等[11]分析了阿伐他汀钙的核磁共振(NMR)数据,吉小龙等[12]对依卡倍特钠进行了波谱学数据分析.对于物质结构的确证,NMR、质谱、红外吸收(IR)光谱、紫外吸收(UV)光谱这四类谱图的数据尤为重要.
本文对丁氟螨酯的NMR波谱(包括1H NMR、13C NMR、DEPT、COSY、HSQC、HMBC)、UV光谱、IR光谱及高分辨质谱(HR-MS)进行了分析,测定了其分子量,讨论了其红外特征吸收峰所对应的各官能团的振动形式,对1H和13C NMR信号进行了归属,并指认了相关基团在结构中的位置及其连接顺序,确证了该化合物的结构.波谱学的信息及结构的确证对于农药生产过程中的质量管控有着非常重要的意义,并可为同类型物质的合成以及其他杂质的确认提供参考,本文的工作将对丁氟螨酯和同类物的开发应用,以及鉴定合成过程中的其他副产物提供参考.
1 实验 1.1 仪器与试剂MS谱图通过配备电喷雾离子源的AB SCIEX Triple Quad 5500三重四级杆质谱仪(美国AB SCIEX公司)获得.UV光谱通过紫外可见分光光度计UV-2550(日本岛津公司)获得.IR光谱通过傅里叶变换红外光谱仪NICOLET 6700(美国赛默飞世尔科技有限公司)获得.NMR谱图通过配备正相宽带BBO探头的Bruker Avance 600超导型傅里叶变换NMR谱仪(瑞士Bruker公司)获得.
氘代甲醇(CD3OD)购自美国CIL公司,丁氟螨酯样品由华南农业大学农药学系徐汉虹课题组提供,多次重结晶提纯后,经高效液相色谱(HPLC)-UV面积归一化测得纯度 > 99.5%,符合结构鉴定要求.
1.2 NMR实验样品溶于CD3OD,以甲醇溶剂峰定标(δH 3.31,δC 49.0),1H和13C NMR的工作频率分别为600.13和150.95 MHz,实验温度为25 ℃,谱宽分别为12 376.24和35 971.22 Hz,DEPT135谱的工作频率为150.95 MHz,谱宽35 971.22 Hz.1H-1H COSY、1H-13C HSQC和1H-13C HMBC实验分别采用COSYGPMFSW、HSQCEDETGP和HMBCGPND标准脉冲程序.1H-1H COSY的F2维(1H)和F1维(1H)谱宽均为4 844.96 Hz,采样数据点阵t2×t1=2 048×128,累加次数为12;HSQC的F2维(1H)和F1维(13C)谱宽分别为4 844.96 Hz和24 997.29 Hz,采样数据点阵t2×t1=1 024×256,累加次数为24;HMBC的F2维(1H)和F1维(13C)谱宽分别为4 844.96 Hz和33 518.11 Hz,采样数据点阵t2×t1=4 096×128,累加次数为64.NMR谱图处理通过Bruker Topspin 2.1及MestReNova 9.0.1上完成.
2 结果与分析 2.1 UV光谱分析丁氟螨酯丙酮溶液的UV谱图在200 nm附近有较强吸收带,206 nm处吸收峰为K吸收带;同时250~300 nm处存在较强吸收带,261 nm吸收峰处为B吸收带,说明结构中存在苯环或者杂环结构,这与丁氟螨酯的结构相符.
2.2 IR光谱分析IR光谱(图 2)中,1 128 cm-1和1 168 cm-1处有较强吸收峰,是C-O-C伸缩振动的特征吸收峰;1 225 cm-1和1 319 cm-1处吸收峰是由同一个碳原子连有多个氟原子C-F伸缩振动引起的,表明分子中可能含有-CF3基团;1 734 cm-1处较强吸收峰表明分子中存在RCOR'基团;而1 764 cm-1处的强吸收峰为C=O振动,表明分子中存在RCOOR'结构;2 892 cm-1处的吸收峰为饱和碳原子-CH3上的C-H伸缩振动;2 821 cm-1处吸收峰是RCOOCH2中-CH2上的碳氢伸缩振动;1 449 cm-1、1 506 cm-1、1 587 cm-1、1 607 cm-1的四个特征吸收峰为芳环上C=C的骨架振动,表明分子中含有芳环结构;2 972 cm-1处有较强的吸收峰,为C-H伸缩振动,说明结构中含有-CH基团.

|
图 2 丁氟螨酯的红外吸收光谱 Fig. 2 IR spectrum of cyflumetofen |
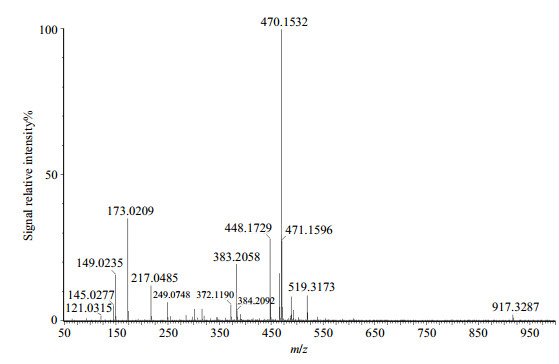
丁氟螨酯的HR-MS谱图(图 3)显示在正离子检测模式下,得到了质荷比(m/z)为448.172 9的离子峰[M+H]+、470.153 2的离子峰[M+Na]+,及其他相应碎片,这与丁氟螨酯(分子式为C24H24F3NO4,精确分子质量447.166 0)一致.
|
图 3 正离子检测模式下,丁氟螨酯的高分辨质谱图 Fig. 3 High resolution mass spectrum of cyflumetofen at positive ion mode |
丁氟螨酯的1H NMR谱图(图 4)共给出10种质子信号:δH 7.84(1H,d,J=7.91 Hz)、7.71(1H,m)、7.61(1H,m)、7.56(2H,m)、7.53(2H,m)、7.27(1H,d,J=7.74 Hz)、4.46(2H,m)、3.62(2H,t,J=4.51 Hz)、3.33(3H,s)、1.35(9H,s),可对应该化合物的24个质子.

|
图 4 丁氟螨酯的1H NMR谱图 Fig. 4 1H NMR spectra of cyflumetofen |
丁氟螨酯的13C NMR谱图(图 5)共给出20种碳信号:δC 191.7、164.9、154.7、136.5(q,3JCF=2.20 Hz)、133.1、133.0、129.4(q,2JCF=32.86 Hz)、129.0、128.4(q,3JCF=4.93 Hz)、128.2、128.0、127.4、124.7(q,1JCF=272.64 Hz)、116.5、71.0、68.3、67.4、59.3、35.7、31.7.DEPT是无畸变极化转移增益法(Distortionless Enhancement by Polarization Transfer)的简称[13].联合DEPT和13C NMR谱可确定碳原子的级数.在DEPT135中,叔碳及伯碳为正峰,而仲碳为负峰[11].结合13C NMR和DEPT135谱及HSQC谱可推断其含有2种伯碳信号、2种仲碳信号、6种叔碳信号及10种季碳信号.其中δC 31.7含有三个伯碳,δC 129.0及δC 127.4均含有两个叔碳;δC 124.7(q,1JCF=272.64 Hz)、δC 129.4(q,2JCF=32.86 Hz)、δC 136.5(q,3JCF=2.20 Hz)、δC 128.4(q,3JCF=4.93 Hz)均裂分为四重峰,是因为受到三个氟原子的影响.

|
图 5 丁氟螨酯的13C NMR和DEPT135谱图 Fig. 5 13C NMR and DEPT135 spectra of cyflumetofen |
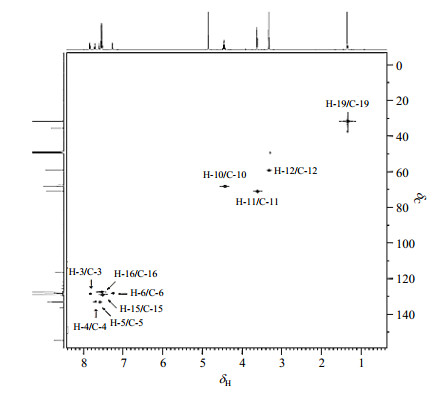
1H NMR谱中,根据积分面积、化学位移规律及DEPT135谱图给出的信息,δH 3.33(3H,s)归属为末端甲基的质子信号H-12;在HSQC谱(图 6)中,δC 59.3与H-12相关,归属为C-12.δH 3.62(2H,t,J=4.51 Hz)与δH 4.46(2H,m)在COSY谱(图 7)中相关;在HMBC图(图 8)中,δH 3.62与C-12相关,而δH 4.46与δC 164.9相关,结合化学位移规律、DEPT135谱图和丁氟螨酯结构,δC 164.9可归属为酯基的碳原子C-9,因此可认为δH 3.62处于靠近末端甲氧基的位置,而δH 4.46处于靠近酯基的位置,分别归属为H-11和H-10;通过HSQC谱可归属δC 71.0为C-11,δC 68.3为C-10.
|
图 6 丁氟螨酯HSQC谱图 Fig. 6 HSQC spectrum of cyflumetofen |

|
图 7 丁氟螨酯的COSY(a)全谱和(b)局部放大图
Fig. 7 (a) COSY and (b) partial enlarged spectra of cyflumetofen
|

|
图 8 丁氟螨酯的HMBC(a)全谱和(b)局部放大图
Fig. 8 (a) HMBC and (b) partial enlarged spectra of cyflumetofen
|
1H NMR谱中最高场的单峰δH 1.35(9H,s),结合积分面积、化学位移规律及DEPT135谱,可归属为叔丁基上9个化学环境相同的甲基质子H-19,其对应的碳原子C-19为δC 31.7.在HMBC谱中,δC 35.7、δC 154.7与H-19相关,可分别归属为C-18和C-17.δH 7.56(2H,m)与δH 7.53(2H,m)在COSY谱(图 6)中相关,由峰型和化学位移可判断为苯对位取代后剩余质子的信号;在HMBC谱中,δH 7.56与C-18和C-19均相关,归属为H-16,则δH 7.53归属为H-15;通过HSQC谱,可归属δC 127.4为C-16,δC 129.0为C-15.在HMBC谱中,季碳δC128.0和δC 67.4与H-15、H-16相关,根据化学位移,可判定δC 128.0为C-14,δC 67.4为C-8.季碳δC 116.5在HMBC中无任何相关出现,结合化学位移规律和丁氟螨酯的结构,可归属为C-13.
该化合物含氟原子,距离氟原子较近的碳原子,会受到氟原子的作用而在碳谱中产生裂分;且随着相隔键数的增加,耦合常数会减小[11].据此可归属δC 124.7(q,1JCF=272.64 Hz)为C-20;δC 129.4(q,2JCF=32.86 Hz)为C-2;在HSQC谱中,δH 7.84(1H,d,J=7.91 Hz)与δC 128.4(q,3JCF=4.93 Hz)相关,分别归属为H-3和C-3;另一个受氟原子影响而产生裂分的季碳δC 136.5(q,3JCF=2.20 Hz)则归属为C-1.在COSY谱中,δH 7.71(1H,m)与H-3相关,而且是3J耦合,归属为H-4;在HSQC谱中,δC 133.0与H-4相关,归属为C-4.δH 7.61(1H,m)与H-4在COSY谱中相关,且为3J耦合,归属为H-5;δC 133.1在HSQC谱中与H-5相关,归属为C-5.δH 7.27(1H,d,J=7.74 Hz)与H-5在COSY谱中相关,且为3J耦合,归属为H-6;δC 128.2在HSQC谱中与H-6相关,归属为C-6.季碳δC 191.7在HMBC谱中与H-6有相关,结合其化学位移数值,归属为C-7.HMBC谱中,H-3与C-1及C-5、H-4与C-6及C-2、H-6与C-2及C-4、H-5与C-3及C-1的相关可验证上述分析.
具体的1H和13C NMR信号归属见表 1.
| 表 1 丁氟螨酯的1H和13C NMR归属 Table 1 The 1H and 13C NMR assignments of cyflumetofen |
本文测定了丁氟螨酯的UV光谱、IR光谱、HR-MS谱图,以及1H NMR、13C NMR、1H-1H COSY、1H-13C HSQC和1H-13C HMBC等NMR谱图,分析了其UV和IR光谱的特征吸收峰与各官能团之间的对应关系,通过HR-MS谱图确定了丁氟螨酯的精确分子量,并归属了其1H和13C NMR信号.上述波谱学数据证明了丁氟螨酯的结构,并为今后关于丁氟螨酯及其同类物的其他研究提供了参考.
| [1] |
YANG G Z. Insecticidal acaricidal-cyflumetofen[J].
World Pesticides, 2013, 35(6): 59-60.
杨国璋. 杀虫杀螨剂-丁氟螨酯[J]. 世界农药, 2013, 35(6): 59-60. DOI: 10.3969/j.issn.1009-6485.2013.06.013. |
| [2] |
ZHANG Y B. New acaricide cyflumetofen development history[J].
World Pesticides, 2007, 29(2): 1-4, 18.
张一宾. 新颖杀螨剂cyflumetofen的开发沿革[J]. 世界农药, 2007, 29(2): 1-4, 18. DOI: 10.3969/j.issn.1009-6485.2007.02.001. |
| [3] | FENG K Y, WEN X, HE X L, et al. Resistant inheritance and cross-resistance of cyflumetofen in tetranychus cinnabarinus (boisduval)[J]. Pestic Biochem Physiol, 2018, 148: 28-33. DOI: 10.1016/j.pestbp.2018.03.013. |
| [4] |
QIAO Y, ZHANG Z W, ZHANG T, et al. Integrating phytoseiulus persimilis and cyflumetofenin for control of tetrangchus urticae on strawberry[J].
Chinese Journal of Biological Control, 2018, 34(4): 514-519.
乔岩, 张正伟, 张涛, 等. 联合应用智利小植绥螨与丁氟螨酯防治草莓二斑叶螨[J]. 中国生物防治学报, 2018, 34(4): 514-519. |
| [5] | HAYASHI N, SASAMA Y, TAKAHASHI N, et al. Cyflumetofen, a novel acaricide-its mode of action and selectivity[J]. Pest Manag Sci, 2013, 69(9): 1080-1084. DOI: 10.1002/ps.3470. |
| [6] | 李敏敏.杀螨剂丁氟螨酯残留分析及环境降解行为研究[D].哈尔滨: 东北农业大学, 2013: 68-69. http://cdmd.cnki.com.cn/Article/CDMD-10224-1013207595.htm |
| [7] | LI M M, LIU X G, DONG F S, et al. Determination of cyflumetofen residue in water, soil, and fruits by modified quick, easy, cheap, effective, rugged, and safe method coupled to gas chromatography/tandem mass spectrometry[J]. J Sep Sci, 2015, 5(20): 2743-2749. |
| [8] | WANG P P, LI M M, LIU X G, et al. Degradation of cyflumetofen and formation of its main metabolites in soils and water/sediment systems[J]. Environ Sci Pollut Res Int, 2016, 23(22): 23114-23122. DOI: 10.1007/s11356-016-7523-2. |
| [9] |
ZHANG M G, FENG X H, YU S T, et al. Spectral analysis and structural elucidation of besifloxacin hydrochloride[J].
Chinese J Magn Reson, 2018, 35(3): 374-384.
张明光, 冯小虎, 于水涛, 等. 盐酸贝西沙星的波谱学数据与结构确证[J]. 波谱学杂志, 2018, 35(3): 374-384. |
| [10] |
LIN Y L, GAO H M, LI F, et al. Spectral analysis and structural elucidation of besifloxacin hydrochloride[J].
Chinese J Magn Reson, 2018, 35(3): 385-392.
林云良, 高红梅, 李锋, 等. 卢立康唑的波谱学特征和结构确证[J]. 波谱学杂志, 2018, 35(3): 385-392. |
| [11] |
LIANG X H, ZHONG W Q, MAO Q P. Analysis of molecular structure of atorvastatin calcium by NMR technology[J].
Experimental technology and management, 2018, 35(8): 46-50.
梁向晖, 钟伟强, 毛秋平. 核磁共振技术解析阿伐他汀钙的分子结构[J]. 实验技术与管理, 2018, 35(8): 46-50. |
| [12] |
JI X L, YU S T, CHEN Z X, et al. Spectral analyses of ecabet sodium[J].
Chinese J Magn Reason, 2018, 35(1): 109-118.
吉小龙, 于水涛, 陈再新. 依卡倍特钠的波谱学数据解析[J]. 波谱学杂志, 2018, 35(1): 109-118. |
| [13] | DODDRELL D M, PEGG D T, BENDALL M R. Distortionless enhancement of NMR signals by polarization transfer[J]. J Magn Reson, 1982, 48(2): 323-327. |
 2020, Vol. 37
2020, Vol. 37 
