2. 河北省电磁场与电器可靠性重点实验室(河北工业大学 电气工程学院), 天津 300130;
3. 中国科学院 电工研究所, 北京 100190;
4. 北京纳志医疗科技有限公司, 北京 100089
2. Key Laboratory of Electromagnetic Field and Electrical Apparatus Reliability of Hebei Province, School of Electrical Engineering, Hebei University of Technology, Tianjin 300130, China;
3. Institute of Electrical Engineering, Chinese Academy of Sciences, Beijing 100190, China;
4. Beijing Nazhi Health Care Co., Ltd., Beijing 100089, China
磁共振成像(Magnetic Resonance Imaging,MRI)是对生物体内核自旋在射频场作用下产生的核磁共振(Nuclear Magnetic Resonance,NMR)信号进行重建的一种成像技术,近年来发展十分迅速.由于其具有无损伤、免接触及无辐射等特点,被广泛应用在人体全身各部位的成像诊断中.实验表明,正常和癌变组织之间具有较大的电特性差异[1-4],使均匀分布的射频场变得不均匀.射频场映像(B1 mapping)就是通过对射频场进行重现来反映生物组织电特性的一种图像重建方法.
早在1925年,Fricke[5]就提出用介电常数检测早期癌症的方法.1991年,Haacke等人[6]提出在磁共振图像中提取人体组织电特性分布的方法.2003年,Wen等人[7]建立了高场MRI人体组织电特性和射频场关系的算法,并进行了实验.2009年,Katscher[8]在电磁场基础上提出新的算法,并实现了人体头部电特性磁共振断层成像(3 T).近些年来,虽然新的电特性算法不断被提出[9],但都是基于高场鸟笼线圈展开的,而对低场永磁体相控阵线圈的研究很少.与高场超导鸟笼线圈相比,低场永磁体磁共振造价成本低[10],而且在高信噪比条件下,相控阵线圈具有单个线圈能够获得较大的成像区域的优点.随着磁共振电特性研究的发展,低场永磁体相控阵线圈射频场映像必将被进一步研究.
磁共振图像分辨率除与主磁场的均匀性有关外,还与射频场有直接关系.永磁体磁共振设备在主磁场固定的情况下,射频线圈直接决定着图像质量,射频场映像技术也可以从实验数据评价射频线圈的质量,为永磁体磁共振的射频场评价提供了依据.
本文针对低场永磁体磁共振射频场进行研究.首先,建立了四通道相控阵线圈仿真模型,通过对线圈模型调谐,分析比较了谐振线圈空载和负载情况下射频场的分布情况.然后,利用四通道相控阵线圈进行MRI实验,使用相应算法分析低场相控阵线圈在空载和负载下射频场均匀性的变化,证实了低场永磁体射频场在负载时均匀度发生明显变化,可为低场磁共振电特性研究提供一定参考.
1 射频场映像原理射频线圈包括发射线圈和接收线圈两部分.射频发射线圈在某一个确定的断层面施加射频脉冲,经过生物组织后,射频接收线圈可以接收反映组织结构特性(T1、T2,或质子密度)的自由感应衰减(Free Induction Decay,FID)信号或者自旋回波(Spin Echo,SE)信号,经模数转换等处理后,得到各个体素发出的大小不等的磁共振信号,这些信号用来获得磁共振图像.医用磁共振图像绝大部分是黑白单色图像,对于成像目标体内不同组织的区分依赖图像黑白亮度的差异[11].接收信号的幅值强度就是图像中的灰度,体素的磁共振信号越强,它所对应图像的像素就越亮.
在MRI设备中除了主磁场和射频场外,还会有梯度(Gradient,G)场的存在,它与Z轴方向的主磁场平行,使得Z轴方向每个断层面的共振频率不同,因此可根据射频脉冲频率选择成像断层面.射频接收线圈接收到的信号是选定断层面上所有体素共振信号叠加的时域信号,需要对其进行频率编码和相位编码来区分各个体素.在断层平面X方向施加一个梯度场,使得断层面内不同列体素的共振频率不同,以此来区分列体素.在断层平面Y方向施加另外一个梯度磁场,断层面上各个行体素质点的进动速度会有差别,进动速度的不同必然导致相位不同,以此来区分行体素.值得一提的是,在实际实验中先施加相位编码之后再施加频率编码.
在断层面各个体素的信号经编码处理后,提取到直角坐标体空间的傅里叶对偶空间(K Space,K空间),K空间是将质子密度图像和采集到的原始数据联系起来的一座桥梁.在成像过程中,K空间是对断层面进行频率编码和相位编码后的数据储存空间.对K空间进行矩阵转换以及二维傅里叶反变换后,得到目标体二维图像的灰度值;随后分别进行MRI和B1 mapping实验.
双角度法(Double Angle Method,DAM)是一种常用的B1 mapping方法.它采用同一平面、同一序列的两个不同的翻转角,即脉冲序列由翻转角为α和2α的脉冲组成,通过自旋回波序列或者梯度回波序列来实现.由Bloch方程,可知自旋回波序列的信号强度SI为[12, 13]:
| $ SI={{M}_{\text{0}}}\frac{\text{sin}{{\alpha }_{\text{SE}}}\cdot \left[ 1-\text{cos}{{\beta }_{\text{SE}}}\cdot {{E}_{1}}-(1-\text{cos}{{\beta }_{\text{SE}}})\cdot {{E}_{1}}\cdot {{\text{e}}^{\frac{TE}{2{{T}_{1}}}}} \right]}{1-\text{cos}{{\alpha }_{\text{SE}}}\text{cos}{{\beta }_{\text{SE}}}\cdot {{E}_{1}}}\cdot {{\text{e}}^{\frac{TE}{{{T}_{2}}}}}\cdot S(r) $ | (1) |
(1) 式中
| $ SI={{C}_{\text{SE}}}\cdot S(r)\cdot \text{sin}{{\alpha }_{\text{SE}}}\cdot \text{si}{{\text{n}}^{2}}\frac{{{\beta }_{\text{SE}}}}{2} $ | (2) |
(2) 式中,
| $ SI={{C}_{\text{SE}}}\cdot S(r)\cdot \text{si}{{\text{n}}^{3}}{{\alpha }_{\text{SE}}} $ | (3) |
为了得到所求射频场,需要对同一目标体进行两次分别施加不同翻转角的实验,以消去
| $ \lambda =\frac{S{{I}_{1}}}{S{{I}_{2}}}=\frac{\text{si}{{\text{n}}^{3}}{{\alpha }_{\text{1SE}}}}{\text{si}{{\text{n}}^{3}}{{\alpha }_{\text{2SE}}}} $ | (4) |
其中
| $ B_{\text{1}}^{+}(r)=\frac{1}{\gamma {{T}_{\text{p}}}}\text{arccos}{{(\frac{\lambda }{8})}^{\frac{1}{3}}} $ | (5) |
为了更清楚地了解低场永磁体射频线圈的磁场分布,文章从仿真和实验两个方面对射频场在有无负载下的均匀度进行说明.有限元仿真软件使用COMSOL公司的5.0版本,志愿者的MRI扫描由北京纳志医疗科技有限公司0.4 T磁共振设备完成.
2.1 有限元仿真在多物理场耦合软件COMSOL射频模块下对相控阵线圈进行简单仿真.本文针对主磁场场强为0.4 T时射频发射线圈进行了初步研究.单个线圈根据感兴趣区域大小及谐振频率确定线圈的长和宽,以及谐振的电容.在单个线圈基础上,建立17.8 MHz四通道相控阵线圈模型,通过有限元分析计算射频场的大小.
2.2 MRI扫描实验MRI扫描实验使用北京纳志医疗科技有限公司生产的0.4 T低场永磁体磁共振设备,射频线圈选用对应四通道的相控阵线圈.实验扫描一名健康志愿者头部,提取磁共振设备的原始K空间数据, 以获得磁共振图像和射频场映像图像.
3 结果与讨论 3.1 相控阵线圈仿真在COMSOL 3D空间中建立单线圈电磁仿真模型(图 1).线圈由半径为0.3 m,弧度π/4的扇形曲面矩形线圈构成,铜片宽度设置为1.5 cm、长度设置为56.4 cm,材料均为理想金属导体.

|
图 1 单线圈仿真模型 Figure 1 Single coil simulation model |
线圈上分布着三个电容,包含两个等值电容C1和一个电容C2,数值上满足C1=2C2.在17.8 MHz谐振频率下,回路中的电感值L(单位为μH)可近似化简[14]为:
| $ L = \frac{{{\mu _0}l}}{{2{\rm{ \mathit{ π} }}}}({\rm{ln}}\frac{{2l}}{w} + \frac{1}{2}) $ | (6) |
其中w为导体的宽度,l为导体的总长度.将仿真模型的长与宽代入(6)式,计算得到L≈1.876 μH,再根据串联电路关于谐振的公式
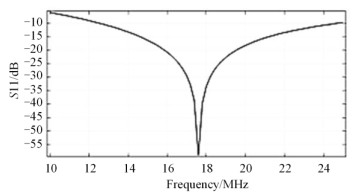
通过有限元仿真软件对上述结果进行验证. 图 2是通过有限元仿真软件计算得到的反射系数(S11)与频率之间的关系曲线,线圈在计算得到的电容值时的谐振频率近似为17.8 MHz,仿真与计算结果一致,即单线圈在17.8 MHz频率下发生谐振.
|
图 2 反射系数(S11)和频率的关系 Figure 2 The relationship between reflection coefficient (S11) and frequency |
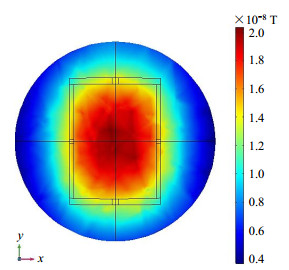
谐振时反射系数达到最小值,根据反射系数找到谐振频率. 图 3为在端口激励施加17.8 MHz的1 V激励电压时,单个发射线圈谐振的射频场分布.
|
图 3 单个发射线圈在17.8 MHz谐振频率工作的磁场分布 Figure 3 Magnetic field distribution of single transmitting coil working at 17.8 MHz resonant frequency |
由图 2和图 3可以看出,通过计算得到的电容值可使单个发射线圈在谐振频率下有效工作,采用三维有限元电磁仿真软件可粗略得知该线圈的磁场分布以及磁通密度均匀度.
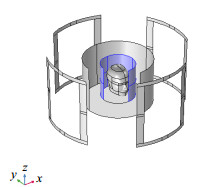
在单个线圈基础上,仿真了四通道相控阵线圈(图 4).在每个曲面矩形线圈分别设置相位差为π/2的单位激励电压,由于四通道相邻线圈在空间上呈正交分布,相互之间耦合作用较小,可通过微调曲面矩形线圈的电容大小实现线圈在17.8 MHz谐振频率的调谐.在线圈内部放置人体头部模型,头部模型外围由半径为0.15 m的完美电导体包围,图 4中蓝色标注部分为感兴趣区域(Region of Interest,ROI).头部模型内电参数设置为:电导率为0.9 s/m、相对介电常数为60,相对磁导率为1.
|
图 4 四通道相控阵线圈仿真模型 Figure 4 Simulation model of four-channel phase array coil |
通过有限元分析可计算磁场的大小,观察磁场的分布情况,研究相控阵线圈磁通密度的均匀度.射频场左旋分量是代表射频线圈发射场中与自旋相互作用的分量,通过一定的算法可以用其反演得到电特性分布图.图 5(a)和5(b)分别为空载和头部负载下的相控阵线圈射频场左旋分量相位云图分布.由图 5(a)可知,四通道相控阵线圈的磁通密度有良好均匀度,可以满足低场射频场映像需求.射频场经过头部负载后,仿真结果显示磁场强度发生了显著改变.图 5(c)和5(d)分别为射频场左旋分量在空载和负载情况下的幅值云图.

|
图 5 四通道相控阵线圈在17.8 MHz谐振频率工作时的射频场左旋分量分布仿真.(a)射频场左旋分量相角,空载;(b)射频场左旋分量相角,人体头部模型负载;(c)射频场左旋分量幅值,空载;(d)射频场左旋分量幅值,人体头部模型负载 Figure 5 Left-handed component of radiofrequency field distribution simulation for four-channel phase array coil working at 17.8 MHz resonant frequency. (a) Left-handed component phase angle of radiofrequency field, no-load; (b) Left-handed component phase angle of radiofrequency field, human head model load; (c) Left-handed component amplitude of radiofrequency field, no-lad; (d) Left-handed component amplitude of amplitude radiofrequency field, human head model load |
从仿真结果可知,低场永磁体磁共振四通道相控阵发射线圈在有负载情况下,射频磁场经过电特性不同的材料时会发生较为明显的变化,通过一定的算法可反衍计算出生物组织电特性.这表明低场磁共振可以满足磁共振电特性映像的要求,增大了磁共振电特性研究的应用范围.
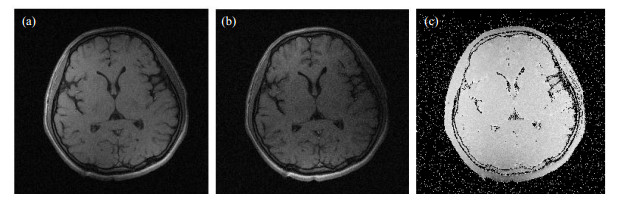
3.2 射频场映像实验通过对四通道相控阵线圈射频场分布仿真结果可知,相控阵线圈在有效位置内有较好的磁通密度均匀度.我们进一步利用四通道相控阵线圈在0.4 T永磁体磁共振设备上进行了MRI实验.两组实验均采用标准自旋回波序列,对一名健康志愿者(23岁)的头部进行MRI扫描:TR为1 000 ms、TE为14.0 ms、层厚为4 mm、层间距为1 mm、像素矩阵大小为256×256、视野(Field of View, FOV)为240×240 mm2.其中一组实验的脉冲翻转角设置为60˚,另一组实验的脉冲翻转角设置为120˚.在满足TR > > T1 > > TE情况下采集了志愿者头部ROI的K空间数据.然后对K空间数据进行快速傅里叶变换等处理得到磁共振图像[图 6(a)和6(b)]的灰度值.最后利用DAM理论求解射频场经生物组织共振后的磁场分布,即射频场映像[图 6(c)],结果显示射频场在通过不同电导率和介电常数的目标体后发生明显改变.
|
图 6 志愿者头部感兴趣区域同一段断层面的磁共振图像和射频场映像. (a)磁共振图像,翻转角为60˚;(b)磁共振图像,翻转角为120˚;(c)射频场映像 Figure 6 MR images and B1 mapping of the volunteer's head. (a) MR image, flip angle=60˚; (b) MR image, flip angle=120˚; (c) B1 mapping |
由于磁共振信号幅值量级小,且两幅磁共振图像未在同一时刻测量,所以生物组织周围数据会有差异,在DAM处理过程中,差异会被随机放大或者减弱,表现出随机噪声.为了定量分析射频场均匀度,本文进一步研究了相控阵线圈仿真实验和射频场映像实验中空载和负载下的射频场的不均匀度,采用公式如(7)式所示:
| $ {B_{{\rm{1\_uniform}}}} = \frac{{\left\| {{B_{1\_{\rm{max}}}}} \right\| - \left\| {{B_{1\_{\rm{min}}}}} \right\|}}{{\left\| {{B_{{\rm{1\_center}}}}} \right\|}} $ | (7) |
(7) 式中,
| 表 1 射频场振幅的不均匀度 Table 1 The inhomogeneity of the radiofrequency field amplitude |
在射频场映像实验中,采用0.4 T的主磁场,四通道相控阵发射线圈射频场在人体头部负载条件下的不均匀度远远高于空载下的不均匀度,即相控阵线圈的射频场在负载下发生明显变化,能够区分出不同电特性的脑组织,可进一步根据这种变化计算脑组织的电特性[14].仿真头部模型设置同一电特性参数,与实际实验相比,均匀性要更好.
通过进一步研究,我们还发现随着主磁场增加,生物组织氢核共振频率增加,施加的射频场频率也随之增加,电特性参数对射频场分布的影响更加明显.
4 结论本文介绍了射频场映像的原理,对低场永磁体相控阵线圈,从有限元仿真和磁共振扫描两个方面分别进行空载和头部负载的实验,并对射频场幅值均匀度进行分析.结果表明:低场相控阵线圈在有负载时,射频场均匀度发生了较大的变化,可在一定程度上反映负载生物组织的电特性.对组织早期病变的诊断有一定参考价值,对早期癌症诊断有着一定的意义.
目前,基层临床使用的低场磁共振设备以是相控阵射频线圈为主.随着磁共振电特性的发展,相控阵线圈电特性成像需要进一步的研究,相控阵线圈射频场映像的研究为未来电特性成像提供更广泛的新诊断参考,在疾病早期诊断中具有广阔的应用前景.
| [1] | JOINES W T, ZHANG Y, LI C X, et al. The measured electrical properties of normal and malignant human tissues from 50 to 900 MHz[J]. Med Phys, 1994, 21(4): 547-550. DOI: 10.1118/1.597312. |
| [2] | LIU J E, ZHANG X T, VAN DE MOORTELE P F, et al. Determining electrical properties based on B1 fields measured in an MR scanner using a multi-channel transmit/receive coil:a general approach[J]. Phys Med Biol, 2013, 58(13): 4395-4408. DOI: 10.1088/0031-9155/58/13/4395. |
| [3] | KATSCHER U, ABE H, IVANCEVIC M, et al. Systematic brain tumor conductivity study with optimized EPT sequence and reconstruction algorithm[C] 201321th Annual International Conference of the ISMRM. Salt Lake City: 2013: 33-40. |
| [4] | HAEMMERICH D, STAELIN S T, TSAI J Z, et al. In vivol electrical conductivity of hepatic tumours[J]. Physiol Meas, 2003, 24(2): 251-260. DOI: 10.1088/0967-3334/24/2/302. |
| [5] | FRICKE H. The electric capacity of suspensions with special reference to blood[J]. J Gen Physiol, 1925, 9(2): 137-152. DOI: 10.1085/jgp.9.2.137. |
| [6] | HAACKE E M, PETROPOULOS L S, NILGES E W, et al. Xtraction of conductivity and permittivity using magnetic resonance imaging[J]. Phys Med Biol, 1991, 36(6): 723-734. DOI: 10.1088/0031-9155/36/6/002. |
| [7] | WEN H. Noninvasive quantitative mapping of conductivity and dielectric distributions using RF wave propagation effects in high field MRI[C]. Proc SPIE 5030, Medical Imaging 2003: Physics of Medical Imaging, 2003, doi: 10.1117/12.480000. |
| [8] | KATSCHER U, VOIGT T, FINDEKLEE C, et al. Determination of Electric conductivity and local SAR Via B1 mapping[J]. IEEE Trans Med Imaging, 2009, 28(9): 1365-1374. DOI: 10.1109/TMI.2009.2015757. |
| [9] | ZHANG X T, SCHMITTER S, VAN DE MOORTELE P F, et al. From complex B1 mapping to local SAR estimation for human brain MR imaging using multi-channel transceiver coil at 7T[J]. IEEE Trans Med Imaging, 2013, 32(6): 1058-1067. DOI: 10.1109/TMI.2013.2251653. |
| [10] |
YANG B L. Future of ultra high field MRI in basic research and clinical applications[J].
Chinese J Magn Reson, 2015, 32(4): 707-714.
杨保联. 超高场磁共振人体成像应用研究和医学前景[J]. 波谱学杂志, 2015, 32(4): 707-714. |
| [11] | 赵喜平. 磁共振成像[M]. 北京: 科学出版社, 2004. |
| [12] |
ZHOU Z K, HU L Z, JIANG R R, et al. Rapid B1+ mapping based on actual flip-angle imaging[J].
Chinese J Magn Reson, 2016, 33(4): 515-527.
周子堃, 胡凌志, 蒋瑞瑞, 等. 基于AFI的快速发射场B1+成像方法[J]. 波谱学杂志, 2016, 33(4): 515-527. |
| [13] | HE X W, YUAN R B, LI B K, et al. The design of an open MRI 4-channel receive-only phased array knee coil[J]. Appl Magn Reson, 2016, 47(5): 499-510. DOI: 10.1007/s00723-016-0768-6. |
| [14] |
XIN X G. Technological progresses of the magnetic resonance electrical property tomography of human tissues[J].
Chinese Journal of Biomedical Engineering, 2015, 34(1): 83-90.
辛学刚. 人体组织电特性磁共振断层成像(MR EPT)技术进展[J]. 中国生物医学工程学报, 2015, 34(1): 83-90. DOI: 10.3969/j.issn.0258-8021.2015.01.012. |
 2018, Vol. 35
2018, Vol. 35 
