2. 中国科学院大学, 北京 100049
2. University of Chinese Academy of Sciences, Beijing 100049, China
两种及以上表面活性剂的混合以及其他添加剂的使用被称为表面活性剂的复配[1-3].实际生产应用中使用的表面活性剂通常都不是单一的表面活性剂,而是表面活性剂复配的体系.一方面是为了降低生产成本;另一方面,表面活性剂的复配使用往往比单一表面活性剂具有更加优良的性能,如具有更低的临界胶束浓度(CMC)和更高的表面活性、润湿性、发泡性等,这种现象称之为表面活性剂间的“协同效应”.由于表面活性剂的复配具备诸多的特殊性能,被广泛应用于化工、材料、生物、医药、环境等科学领域[3-9],因此对表面活性剂复配规律的研究具有重要的价值和意义.
Rubingh等[10]首次将规则溶液理论应用于混合胶束的形成,建立了表征非理想混合体系偏离理想混合程度的相互作用参数(β)理论,用于表征二元表面活性剂混合体系中组分间相互作用的性质与大小.随后Rosen等[11, 12]又进一步将该理论与表面活性剂吸附平衡理论相结合,推导出了二元混合表面活性剂在降低表面张力的效率、CMC和表面张力等方面产生协同效应的条件.然而这些理论未能明确描述二元混合表面活性剂体系组分间相互作用的规律,原因在于它是根据宏观测试方法测得的“混合溶液的CMC”来推测的,实际上混合体系中各组分有各自的行为,所以用这个理论来分析和描述表面活性剂之间具体的相互作用是不准确的.
核磁共振(NMR)波谱技术可以在不破坏体系的条件下对多组分体系中的各个组分进行单独观测,从分子或原子水平获取相关信息,在研究混合溶液组分间的相互作用方面具有独特的优势[13-15].本文通过1H NMR实验,测定了3种表面活性剂——十六烷基三甲基溴化铵(CTAB)、辛基苯基聚氧乙烯醚(TX-100)和十二烷基硫酸钠(SDS)组成的CTAB/TX-100、SDS/TX-100以及CTAB/TX-100/SDS等二元和三元表面活性剂复配体系中各组分的CMC,对比分析了空间效应对混合表面活性剂中组分间相互作用的影响.
1 实验部分 1.1 仪器与试剂NMR实验在Bruker AVANCE500型NMR谱仪上进行,质子共振频率为500.13 MHz.重水(D2O,氘代率为99.9%)购自Sigma-Aldrich公司;表面活性剂CTAB购自Acros Organics公司,TX-100购自Nacalai Tesque公司,SDS购自Alfa Aesar公司.各表面活性剂的分子式和质子编号如图 1所示.

|
图 1 3种表面活性剂CTAB、TX-100和SDS的分子结构式和质子编号 Figure 1 Chemical structures and proton number of CTAB, TX-100 and SDS |
用重水配制母液浓度为40 mmol/L的各单一表面活性剂溶液.然后按照既定的摩尔比例混合各单一表面活性剂母液,得到一定摩尔配比的二元和三元母液.用重水逐步稀释各复配母液,得到一系列浓度梯度的表面活性剂复配溶液.
1.3 NMR实验实验温度为298.0 K,1H NMR谱采用30˚小角度激发代替常规单脉冲序列中的90˚激发,以减少采样时间和获得更高的信噪比,利用水峰(δH 4.70)进行定标.求取各复配溶液中CTAB、TX-100和SDS的CMC值,主要依据3种表面活性剂的特征峰T-6、H-1和S-1的化学位移随浓度倒数的变化.
2 结果与讨论 2.1 表面活性剂复配体系中各组分的CMC本次实验中所涉及到的混合胶束体系均属于NMR尺度上的快交换体系(微秒量级),在达到CMC后,在1H NMR谱图中观测到的是融合的权重峰,观察到的化学位移值(δobsd)为单体态表面活性剂分子的化学位移值(δmon)与胶束态表面活性剂分子的化学位移值(δmic)的加权平均值[13, 16]:
| $ {{\delta }_{\rm{obsd}}}=\frac{{{C}_{\rm{mon}}}}{{{C}_{\rm{T}}}}{{\delta }_{\rm{mon}}}+\frac{{{C}_{\rm{mic}}}}{{{C}_{\rm{T}}}}{{\delta }_{\rm{mic}}} $ | (1) |
(1) 式中,CT表示表面活性剂分子的总浓度,Cmon和Cmic分别表示单体态和胶束态的表面活性剂分子的浓度,且Cmic=CT-Cmon.(1)式可转换为:
| $ {{\delta }_{\rm{obsd}}}=\frac{CMC}{{{C}_{\rm{T}}}}({{\delta }_{\rm{mon}}}-{{\delta }_{\rm{mic}}})+{{\delta }_{\rm{mic}}} $ | (2) |
在表面活性剂浓度低于CMC时,溶液中的表面活性剂分子以单体态存在:
| $ {{\delta }_{\rm{obsd}}}={{\delta }_{\rm{mon}}} $ | (3) |
由(2)式和(3)式可以发现,在表面活性剂分子的浓度达到CMC以上和低于CMC时,表观化学位移值(δobsd)与表面活性剂分子中浓度的倒数(1/CT)分别呈两条直线,通过这两条直线可以得到一个交叉点,这个交叉点即为CMC的倒数值,从而可以获得表面活性剂的CMC.由此得到的各混合表面活性剂复配体系中各个组分的CMC列于表 1和表 2,表中αX代表表面活性剂X在复配体系中的摩尔分数.由于阴阳离子表面活性剂混合容易产生沉淀,三元混合体系中只得到了CTAB与SDS比例比较极端的两种结果.
| 表 1 CTAB/TX-100和SDS/TX-100二元表面活性剂复配体系中各组分的CMC Table 1 CMC values of each surfactant in CTAB/TX-100 and SDS/TX-100 binary mixtures |
| 表 2 CTAB/TX-100/SDS三元表面活性剂复配体系中各组分的CMC Table 2 CMC values of each surfactant in CTAB/TX-100/SDS ternary mixtures |
混合表面活性剂体系中一个组分的CMC降低越明显,说明体系中其他组分对它的协同作用越强.由表 1和表 2可以发现,混合表面活性剂中各组分的CMC均随着自身摩尔分数的增大而增大,而随着其他组分摩尔分数的增大是减小的.
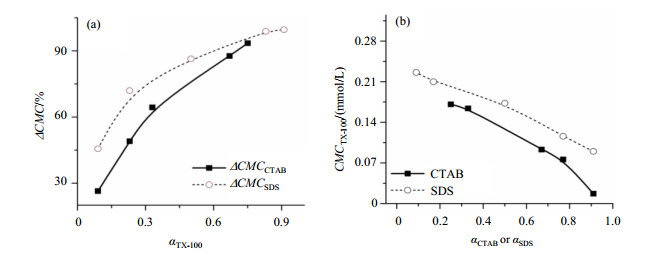
2.2 空间效应对混合表面活性剂中组分间协同效应的影响表面活性剂协同效应理论认为静电作用是影响组分间协同效应的主要因素,在存在多种影响因素时,静电作用对协同效应的强弱起决定性作用,一般情况下二元混合表面活性剂体系中的协同效应存在这样的关系:阴离子/聚氧乙烯型非离子(POE)>阳离子/POE[17].通过图 2,我们对CTAB/TX-100和SDS/TX-100两组二元混合体系中组分间的协同效应进行了分析,由于CTAB和SDS的CMC相差一个数量级,为了更准确地对二者与TX-100混合后CMC降低的程度进行比较,用ΔCMC(%)来表示,即在TX-100为某摩尔分数时,离子型表面活性剂的CMC相对于其纯溶液时降低的百分数.
|
图 2 二元混合体系中(a) CTAB与SDS的CMC降低百分比(ΔCMC)随TX-100摩尔分数增加的变化;(b) TX-100的CMC随着离子型表面活性剂(CTAB或SDS)摩尔分数的增加的变化曲线 Figure 2 (a) ΔCMC values of CTAB or SDS in CTAB/TX-100 or SDS/TX-100 mixtures; (b) CMC values of TX-100 in CTAB/TX-100 or SDS/TX-100 mixtures |
图 2(a)中表明SDS的CMC比CTAB降低更显著,说明TX-100与SDS间旳静电作用主导协同效应;但是图 2(b)中,与CTAB混合后TX-100的CMC降低得更多,说明CTAB对TX-100的协同作更强,这是因为CTAB与SDS头基大小与尾链长度的不同,导致了CTAB的分子截面积明显大于SDS,充分说明协同效应的影响因素不仅包含静电相互作用,空间效应在一定的情况下也会起到关键的作用.通过对比三元混合表面活性剂体系的数据(图 3),可以更明显地发现空间效应在其中所产生的影响.
|
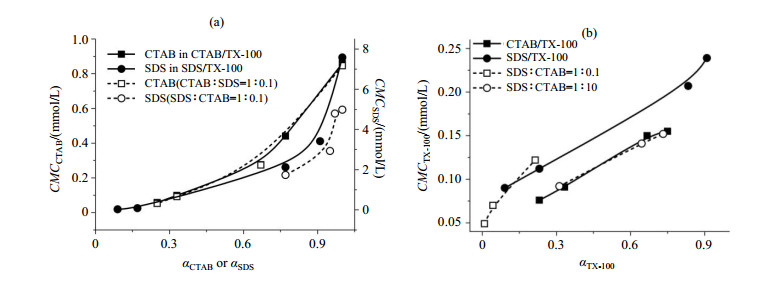
图 3 (a) CTAB或SDS的CMC随各自和TX-100混合体系中(实线)自身摩尔比例增加的变化与三元混合体系中(虚线)变化的对比;(b) TX-100的CMC在各二元(实线)或三元(虚线)混合体系中随自身摩尔分数的变化 Figure 3 (a) CMC values of CTAB or SDS against their mole fractions in binary (solid) and ternary (dash) surfactant mixtures; (b) CMC values of TX-100 against its mole factions in binary (solid) and ternary (dash) surfactant mixtures |
三元表面活性剂复配体系整体体现出与过量离子型/非离子型表面活性剂复配体系相似的性质,所以三元混合体系中各组分CMC的变化趋势与相应的二元混合体系是一致的(如图 3所示).然而从图 3(a)中不难发现,往CTAB/TX-100混合体系中加入少量的SDS,并没有对CTAB的CMC变化造成大的影响;但是少量CTAB的加入却能使SDS的CMC相比SDS/TX-100二元混合体系中的发生显著的降低.同样,为了更准确地描述CTAB和SDS的CMC下降的相对程度,把二元和三元体系中CTAB(或SDS)与TX-100混合比例相等时的CMC值做了对比,表示为三元体系中离子型表面活性剂的CMC值相对二元体系中对应值的降低百分比(如表 3所示),所得结果与图形结果相一致.这是因为CTAB的分子截面积远大于SDS,在反电荷离子加入量较少的情况下,SDS对CTAB的空间效应很小,CTAB的CMC变化不大;而CTAB对SDS的空间效应不可忽略,使SDS的CMC变化曲线降低明显.
| 表 3 离子型表面活性剂(CTAB与SDS)在三元混合表面活性剂体系中的CMC值较相应二元混合体系降低的百分比(ΔCMC) Table 3 Comparison of the CMC percentage changes (ΔCMC) of CTAB and SDS between ternary mixtures and binary mixtures |
本文利用1H NMR分别测量了摩尔比例不同的表面活性剂复配体系CTAB/TX-100、SDS/TX-100、CTAB/TX-100/SDS中各组分的CMC值,通过对比不同体系中各组分CMC随摩尔分数的变化曲线,发现了空间效应对表面活性剂复配体系中协同效应的影响在一定的情况下也不逊于静电相互作用:表面活性剂分子的截面积越大,对体系中其他组分的协同作用越强;当组分间存在弱的静电相互作用时,空间效应对协同作用起到更主要的影响.
| [1] | JONSSON B. Surfactants and polymers in aqueous solution[M]. 2nd ed. New York: John Wiley & Sons Inc, 1998. |
| [2] | HOLLAND P M, RUBINGH D N. Mixed surfactant systems:An overview[M]. Washington DC: American Chemical Society, 1992. |
| [3] | JOST F, LEITER H, SCHWUGER M J. Synergisms in binary surfactant mixtures[J]. Colloid Polym Sci, 1988, 266(6): 554-561. DOI: 10.1007/BF01420767. |
| [4] | SOLANS C, IZQUIERDO P, NOLLA J, et al. Nano-emulsions[J]. Curr Opin Colloid In, 2005, 10(3, 4): 102-110. |
| [5] | PARIA S. Surfactant-enhanced remediation of organic contaminated soil and water[J]. Adv Colloid Interface, 2008, 138(1): 24-58. DOI: 10.1016/j.cis.2007.11.001. |
| [6] | GARTI N, SPERNATH A, ASERIN A, et al. Nano-sized self-assemblies of nonionic surfactants as solubilization reservoirs and microreactors for food systems[J]. Soft Matter, 2005, 1(3): 206-218. DOI: 10.1039/b506233k. |
| [7] | HAN F, LI S M, YIN R, et al. Effect of surfactants on the formation and characterization of a new type of colloidal drug delivery system:Nanostructured lipid carriers[J]. Colloids and Surfaces A:Physicochem Eng Aspects, 2008, 315(1-3): 210-216. DOI: 10.1016/j.colsurfa.2007.08.005. |
| [8] | GIESY J P, KANNAN K. Peer reviewed:Perfluorochemical surfactants in the environment[J]. Environ Sci Technol, 2002, 36(7): 146A-152A. DOI: 10.1021/es022253t. |
| [9] | YANG J. Viscoelastic wormlike micelles and their applications[J]. Curr Opin Colloid In, 2002, 7(5): 276-281. |
| [10] | HOLLAND P M, RUBINGH D N. Nonideal multicomponent mixed micelle model[J]. J Phys Chem, 1983, 87(11): 1984-1990. DOI: 10.1021/j100234a030. |
| [11] | ROSEN M J, HUA X Y. Surface concentrations and molecular interactions in binary mixtures of surfactants[J]. J Colloid Inter Sci, 1982, 86(1): 164-172. DOI: 10.1016/0021-9797(82)90052-2. |
| [12] | ROSEN M J, ZHU Z H. Synergism in binary mixtures of surfactants[J]. J Colloid Inter Sci, 1993, 133(2): 473-478. |
| [13] | CUI X, JIANG Y, YANG C, et al. Mechanism of the mixed surfactant micelle formation[J]. J Phys Chem B, 2010, 114(23): 7808-7816. DOI: 10.1021/jp101032z. |
| [14] | GAO H, ZHU R, YANG X, et al. Properties of polyethylene glycol (23) lauryl ether with cetyltrimethylammonium bromide in mixed aqueous solutions studied by self-diffusion coefficient NMR[J]. J Colloid Inter Sci, 2004, 273(2): 626-631. DOI: 10.1016/j.jcis.2003.12.047. |
| [15] |
YANG C S, CUI X H, JIANG Y, et al. Mixed micelles of sodium dodecyl sulfate and triton X-100 in aqueous solution studied by 1H NMR[J].
Chinese J Magn Reson, 2009, 26(4): 466-475.
杨春升, 崔晓红, 蒋艳, 等. 表面活性剂SDS/TX-100混合体系的NMR研究[J]. 波谱学杂志, 2009, 26(4): 466-475. |
| [16] |
YU G J, LIU J, MAO S Z, et al. Exchange kinetics of surfactants TX-100 and CTAB investigated by 1H NMR spectroscopy[J].
Chinese J Magn Reson, 2016, 33(3): 422-431.
俞刚金, 刘君, 毛诗珍, 等. TX-100和CTAB交换动力学的核磁共振研究[J]. 波谱学杂志, 2016, 33(3): 422-431. DOI: 10.11938/cjmr20160307. |
| [17] | ROSEN M J, KUNJAPPU J T. Surfactants interfacial phenomena[M]. 4th ed. New York: John Wiley & Sons Inc, 2012. |
 2018, Vol. 35
2018, Vol. 35 
