2. 同济大学 材料科学与工程学院, 上海 201804
2. College of Materials Science and Engineering, Tongji University, Shanghai 201804, China
锂离子电池作为一种高效的储能电池,具有高能量密度和高功率的优点,被广泛的应用在各个领域[1, 2].但是目前广泛使用的液体/凝胶锂离子电池存在易漏液、可燃、易爆炸等安全隐患.相对于液体/凝胶锂离子电池,基于固体电解质的全固态锂离子电池具有更好的安全特性,并且具有高温下稳定、易成型加工等优点[3].研发新型高性能的固体电解质一直是相关研究领域的热点[4].从化学结构来说,目前研究的固体电解质主要可以分为两类:以陶瓷材料为基本结构的无机固体电解质[5]以及以聚醚类高分子与无机锂盐络合的有机固体电解质[6].这两类固体电解质各有优缺点.有机固体电解质具有很强的可塑性,但是室温下电导率太低,难以达到实际应用的要求;无机固体电解质相对于有机固体电解质具有电导率高的优点[7],但是无机固体电解质的主要缺点是电解质和电极之间的界面层在低电压下容易被还原,中等电压下容易被氧化[8, 9].因此,为了消除电极材料对固体电解质的加速氧化还原反应,在固态电解质表面采用喷涂沉积等方法加入缓冲层可以有效地提高电池性能[10-15].或者在电极和电解质之间增加一层聚合物隔膜以降低界面层对电池性能的影响[16].Zhou等[17]合成了一种高分子/陶瓷/高分子的三明治结构的固体电解质,在陶瓷固体电解质和电极之间加入高分子膜,改善了全固态电池的电化学稳定性,证明高分子对于提高固体电解质的稳定性具有较好的效果.
将有机固体电解质用于无机固体电解质表面进行改性提供了一种高性能固体电解质设计的新思路.在这一研究领域,目前的研究主要集中在尝试不同的无机和有机固体电解质混合以获得性能优良的电解质材料.对于无机和有机固体电解质混合后材料的结构变化,特别是无机和有机固体电解质表界面的结构变化,相关研究还很不充分,文献中也鲜有报道.然而,很多理论工作表明固体电解质中材料颗粒的表界面对于电化学性能具有重要影响[18].研究发现,固体电解质表界面的形成会降低锂离子的迁移动力学[19],导致电池化学稳定性变差[20],界面层的厚度会直接影响电池的界面电阻和循环稳定性[21, 22].
固体核磁共振(NMR)方法是一种研究材料结构及动力学性能的有效手段,可以清晰地反映材料微观结构对分子运动性的影响[23, 24].通过对固体电解质表界面结构和分子运动的研究,有助于我们在分子层次理解表界面对材料电化学性能影响的来源.本文将通过固体NMR方法对无机和有机固体电解质中表界面的结构和分子运动进行深入研究.我们选取了一种常见的无机有机固体电解质——三嵌段共聚物聚乙二醇-聚丙二醇-聚乙二醇(PEG-PPG-PEG)和NASICON型固体电解质——Li1.5Al0.5Ge1.5P3O12(简称LAGPO)及一种常见的锂盐——三氟甲基磺酸锂(CF3SO3Li)合成了一种复合物.通过静态变温1H NMR谱,我们研究了样品中高分子链的分子运动;通过2D 1H-7Li宽线分离(WISE)NMR实验,我们实现了对无机/有机材料表界面上高分子的选择性观测,并研究了其不同于本体的分子运动.
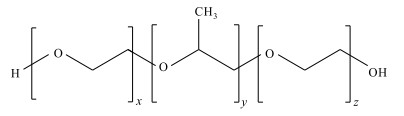
1 实验部分 1.1 试剂与合成方法三嵌段共聚物PEG-PPG-PEG:(C3H6O-C2H4O)x,购买于美国的Sigma-Aldrich公司.图 1为这种样品的结构式,平均分子量为8.4 k,氧化乙烯(EO)链段和氧化丙烯(PO)链段的数量比为3.82: 1;CF3SO3Li购买于Sigma-Aldrich公司;LAGPO购买于合肥科晶材料技术有限公司;乙腈(C2H3N),购买于百灵感科技有限公司.
|
图 1 PEG-PPG-PEG分子式 Figure 1 Molecular formula of PEG-PPG-PEG |
高分子-锂盐-陶瓷复合体系PEG-PPG-PEG-CF3SO3Li-LAGPO合成方法:按照EO/PO链段和锂盐摩尔数之比为3: 1的比例,称量CF3SO3Li 0.159 2 g、PEG-PPG-PEG 0.142 0 g,溶解于30 mL乙腈溶液中,室温下搅拌24 h,称量LAGPO 2.700 0 g,加入上述溶液中继续搅拌24 h后,室温下放置在通风橱内使溶液缓慢蒸发,溶液蒸发后得到白色粉末,在真空烘箱中40 ℃烘干12 h除去残余溶剂.此样品中PEG-PPG-PEG+CF3SO3Li的质量占混合样品总质量的10%,后面的实验所用的样品皆为此比例.
PEG-PPG-PEG-CF3SO3Li的合成方法:CF3SO3Li 0.474 8 g、PEG-PPG-PEG 0.525 2 g,溶解于200 mL乙腈溶液中,室温下搅拌24 h后,室温下放置在通风橱内使溶液缓慢蒸发,溶液蒸发后得到白色粉末,在真空烘箱中40 ℃烘干12 h除去残余溶剂.
1.2 仪器及参数宽角X-射线衍射(XRD)实验:XRD实验用Bruker D8 ADVANCE型衍射仪进行记谱扫描.测试条件:Cu-Ka射线作为射线源(λ = 0.154 06 nm),管电压为35 kV,管电流为25 mA,扫描范围2θ = 5°~90°,扫描速度30°/min,所有XRD实验均在室温下进行.
扫描电子显微镜(SEM)实验:SEM实验在S4800 HITACHI仪器上进行,加速电压为5.0 kV.
固体高分辨NMR实验:固体静态变温NMR实验在Bruker AVANCE Ⅲ 300型NMR谱仪上进行,采用4 mm探头和转子,1H核共振频率为300.16 MHz.其它固体NMR实验均在Bruker AVANCE Ⅲ 600型NMR谱仪上进行,1H和7Li核的共振频率分别为600.44 MHz和233.23 MHz,1H NMR谱的化学位移是以金刚烷(Adamantane)定标(δH 1.46),7Li的化学位移是以浓度为1 mol/L的氯化锂溶液(LiCl)定标(δLi 0).对于1H/7Li交叉极化(CP)实验,用样品优化条件,所有的CP接触时间为1 ms,转速为10 kHz.2D 1H-7Li WISE NMR实验采用接触时间为1 ms,1H 90°脉宽为4 μs,F1维谱宽为240 kHz,F2维谱宽为178.65 kHz,转速为3 kHz.
2 结果与讨论 2.1 高分子和陶瓷复合状态的SEM、XRD研究本文通过SEM实验研究了材料的表面形貌和结晶状态.如图 2所示,图 2(a)、2(b)、2(c)分别为LAGPO、复合物PEG-PPG-PEG-CF3SO3Li-LAGPO和PEG-PPG-PEG-CF3SO3Li的SEM照片,从图 2(a)可以明显看出LAGPO是呈颗粒状均匀分布的,大部分颗粒尺度在3 μm左右.通过图 2(b)复合物PEG-PPG-PEG-CF3SO3Li-LAGPO的SEM图和LAGPO的SEM图的对比来看,可以发现复合物的表面形貌和LAGPO的基本相同,也存在LAGPO颗粒的分布,这主要由于LAGPO在乙腈中无法溶解,在分散搅拌的过程中LAGPO的晶格没有受到破坏.不同的是图 2(b)中LAGPO颗粒存在一定的团聚现象,初步推断是PEG-PPG-PEG和LAGPO颗粒表面发生了相互作用,促使一部分LAGPO颗粒团聚.图 2(c)为PEG-PPG-PEG-CF3SO3Li的SEM照片,可以发现PEG-PPG-PEG-CF3SO3Li的结晶形貌和LAGPO以及复合物PEG-PPG-PEG-CF3SO3Li-LAGPO有显著差别.比较图 2(b)和2(c),我们认为复合物PEG-PPG-PEG-CF3SO3Li-LAGPO中并不存在PEG-PPG-PEG-CF3SO3Li单独的结晶相,这意味着高分子主要以非晶状态存在于LAGPO颗粒之间.这一点也得到了XRD实验结果的证实.

|
图 2 室温下(a) LAGPO、(b)复合物PEG-PPG-PEG-CF3SO3Li-LAGPO和(c) PEG-PPG-PEG-CF3SO3Li的SEM照片 Figure 2 SEM images of (a) LAGPO, (b) PEG-PPG-PEG-CF3SO3Li-LAGPO and (c) PEG-PPG-PEG-CF3SO3Li at room temperature |
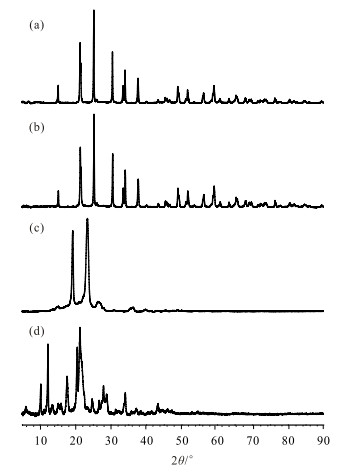
图 3分别为LAGPO、复合物PEG-PPG-PEG-CF3SO3Li-LAGPO、高分子PEG-PPG-PEG和PEG-PPG-PEG-CF3SO3Li的XRD谱图.比较图 3(a)和3(b),我们发现其XRD衍射峰完全相同,并且与文献[25]报道的LAGPO的XRD谱图基本符合,说明在复合物中不存在高分子的结晶相,证明复合物中大部分高分子以非晶状态存在.图 3(c)和3(d)中高分子以及高分子/锂盐的衍射峰在图 3(b)中都没有出现.表明复合物中不存在高分子以及高分子/锂盐的结晶相,证明高分子大部分以非晶状态存在.
|
图 3 室温下(a) LAGPO、(b) PEG-PPG-PEG-CF3SO3Li-LAGPO、(c) PEG-PPG-PEG和(d) PEG-PPG-PEG-CF3SO3Li的XRD谱图 Figure 3 XRD spectra of (a) LAGPO, (b) PEG-PPG-PEG-CF3SO3Li-LAGPO, (c) PEG-PPG-PEG and (d) PEG-PPG-PEG-CF3SO3Li at room temperature |
上述SEM、XRD表明,高分子嵌段共聚物在复合体系处于非晶状态.通过样品的SEM谱图我们可以发现LAGPO在和高分子复合之后发生了部分的团聚,因此推测高分子和LAGPO颗粒表面具有一定的相互作用.接下来我们将通过一系列固体NMR方法对高分子和LAGPO颗粒表界面的相互作用进行较为系统的研究.
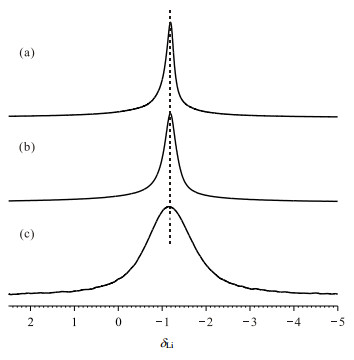
2.2 固体NMR谱的信号归属图 4分别LAGPO、PEG-PPG-PEG-CF3SO3Li-LAGPO、PEG-PPG-PEG-CF3SO3Li的单脉冲7Li NMR谱.图 4(a)谱峰半高宽为55.1 Hz,图 4(b)谱峰半高宽为56.7 Hz,而图 4(c)中PEG-PPG-PEG-CF3SO3Li的谱峰半高宽(251.0 Hz)明显大于图 4(a)和4(b).通过图 4(b)和4(c)对比可以看出结晶状态的PEG-PPG-PEG-CF3SO3Li的7Li NMR信号在复合物中不存在,也就说明复合物中的高分子大部分是非晶状态,印证了前面的SEM和XRD的观测结果.
|
图 4 室温下(a) LAGPO、(b) PEG-PPG-PEG-CF3SO3Li-LAGPO和(c) PEG-PPG-PEG-CF3SO3Li的7Li NMR谱图 Figure 4 7Li NMR spectra of (a) LAGPO, (b) PEG-PPG-PEG-CF3SO3Li-LAGPO and (c) PEG-PPG-PEG-CF3SO3Li at room temperature |
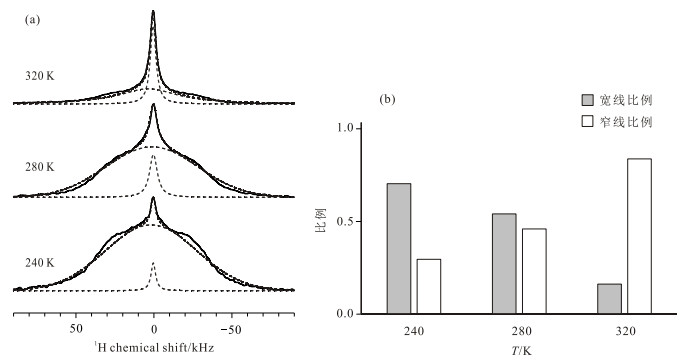
图 5(a)为复合物PEG-PPG-PEG-CF3SO3Li-LAGPO的变温静态1H NMR谱图.为了消除探头的背景信号,我们使用了1H EASY脉冲序列对1H NMR信号进行了采集[26, 27].分析图 5(a)的信号,我们发现样品中的高分子链段在240 K温度时明显存在宽线和窄线两个信号.由于上述XRD结果已经证实材料中高分子并不结晶,所以,我们把宽线归属为运动性较差的高分子链段,把窄线归属为运动性较强的高分子链段.图 5(a)中虚线部分为通过Dmfit进行拟合后的谱峰,通过拟合我们还可以得出不同温度下宽窄信号的相对比例如图 5(b)所示.从图中可以知道随着温度的升高,窄线的比例逐渐升高,而宽线的比例逐渐降低.这一现象说明,随着温度的升高,体系内的两种分子链段的运动性都明显增强.对于复合物PEG-PPG-PEG-CF3SO3Li-LAGPO的静态1H NMR谱中宽线和窄线的来源,我们根据材料的性质进行了推测:在复合物PEG-PPG-PEG-CF3SO3Li-LAGPO中,由于高分子并不结晶,所以对应于宽线、运动性较差的高分子链段很可能是受到LAGPO作用的分子链段;而对应于窄线、运动性较高的高分子链段很可能是高分子本体,或者是较少受到LAGPO作用的分子链段.接下来我们将通过变温1H/7Li CP/MAS和1H-7Li WISE实验对上述信号进行归属,并对高分子和LAGPO颗粒表界面的结构和分子运动进行系统研究.
|
图 5 (a) 复合物PEG-PPG-PEG-CF3SO3Li-LAGPO的变温静态1H NMR谱图;(b)拟合得到的不同温度下(a)图中宽线和窄线的强度比例 Figure 5 (a) Static1H NMR spectra of complex PEG-PPG-PEG-CF3SO3Li-LAGPO at different temperatures; (b) The change of the intensity ratio of the broad and narrow peak in fig. (a) at different temperatures by fitting |
图 5的信号是通过单脉冲获得,通过设置足够长的循环等待时间使自旋能够完全弛豫,所以是体系内包含的高分子本体,以及高分子和LAGPO颗粒表界面高分子在内的所有信号.对于高分子和LAGPO复合物来说,LAGPO本身含质子量极低,质子的最主要来源是高分子.基于这一结构模型,我们可以通过1H/7Li的CP过程选择性的获得高分子和LAGPO颗粒表界面7Li核和高分子的信号.
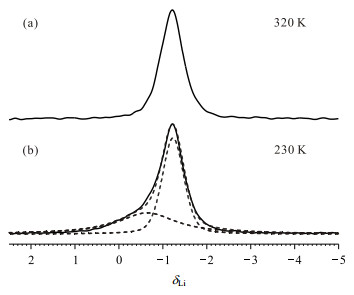
图 6为复合物PEG-PPG-PEG-CF3SO3Li-LAGPO的变温1H/7Li CP/MAS谱图.由于导电陶瓷LAGPO中基本不含有质子信号,所以1H/7Li CP/MAS中出现的7Li NMR信号是由于界面高分子中的质子和界面上的7Li核的偶极相互作用产生,因此,该7Li NMR信号反映了界面上7Li核的信号.图 6(a)是复合物在320 K下的1H/7Li CP/MAS谱图.该谱图中7Li NMR信号与相同温度下单脉冲谱图中的信号类似,只是半高宽略宽.图 6(b)是复合物在230 K下的1H/7Li CP/MAS谱图,通过Dmfit拟合我们发现在δLi -0.8处又出现一个半高宽较宽的信号.通过图 7和图 8的1H-7Li WISE实验,我们发现这两种7Li NMR信号对应于材料中不同运动性的高分子链段,详细的讨论将在后文展开.
|
图 6 复合物PEG-PPG-PEG-CF3SO3Li-LAGPO的在(a) 320 K和(b) 230 K下的1H/7Li CP/MAS谱图 Figure 6 1H/7Li CP/MAS spectra of complex PEG-PPG-PEG-CF3SO3Li-LAGPO at (a) 320 K and (b) 230 K |
|
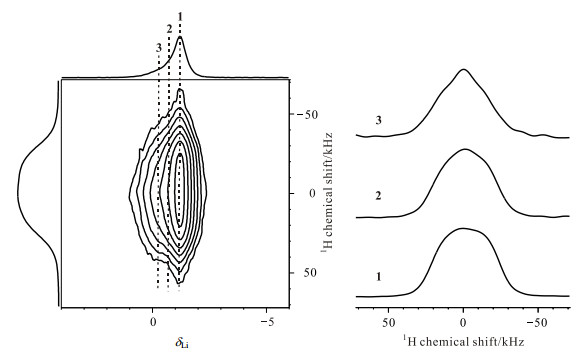
图 7 左图为复合物PEG-PPG-PEG-CF3SO3Li-LAGPO 230 K下的2D 1H-7Li WISE谱图;右图为按照左图1、2、3标示纵向抽出的F1维切片谱图 Figure 7 Left: the 2D 1H-7Li WISE spectrum of complex PEG-PPG-PEG-CF3SO3Li-LAGPO at 230 K; Right: 1, 2, 3 are slices in the F1 dimension according to the mark on the left spectrum |
|
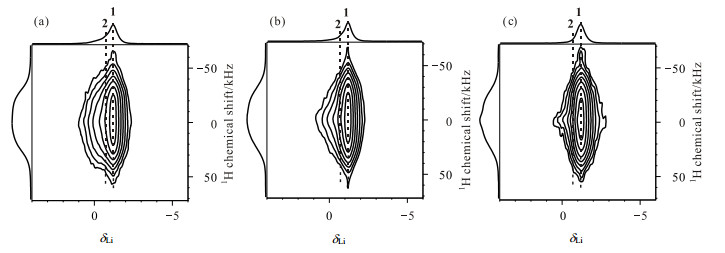
图 8 复合物PEG-PPG-PEG-CF3SO3Li-LAGPO在(a) 230 K、(b) 280 K、(c) 320 K下的2D 1H-7Li WISE谱图 Figure 8 2D 1H-7Li WISE spectra of the complex PEG-PPG-PEG-CF3SO3Li-LAGPO at (a) 230 K, (b) 280 K and (c) 320 K |
2D 1H-7Li WISE谱是一种研究分子运动的有效的方法.该谱图的直接维(F2维)是7Li NMR谱,间接维(F1维)是1H NMR谱.通过WISE谱中1H与7Li NMR信号的相关,我们可以了解不同的7Li NMR所对应的1H NMR信号的线形,进而可以知道7Li核相近的不同含氢基团的运动性差别[28, 29]. 图 7为PEG-PPG-PEG-CF3SO3Li-LAGPO在230 K下的2D 1H-7Li WISE谱,在1、2、3三个位置纵向抽出3条1H NMR的切片谱,这三张1H NMR谱分别对应于化学位移为δLi -1.2、-0.8、-0.1的7Li核.对比发现,这三条1H NMR谱的谱峰线形存在着明显差别:1是一个宽的近似高斯宽线,而2、3是接近洛伦兹宽线上叠加了一个窄峰.不同的线形说明和材料中与7Li核距离不同的高分子链段运动存在差异.1对应的7Li核的化学位移是δLi -1.2,与LAGPO本体的信号相同.在WISE谱里这个信号对应的1H NMR谱最宽.表明高分子链受到的束缚作用大.2的线性接近洛伦兹线形,说明2对应的高分子链段运动性高于1.3的线形相比于2更尖,半高宽更窄,说明3对应的高分子链段运动性高于2.根据样品的特点,我们认为1对应的高分子链可能是在陶瓷颗粒表面的高分子链段,这部分高分子链段和LAGPO颗粒存在着较强的界面作用,因此受到束缚作用较大.3对应于受到束缚作用较小的高分子链,相对于1对应的高分子链段来说,这部分高分子链段和LAGPO颗粒存在着相对较弱的界面作用,因此受到束缚作用较小.而2代表的高分子运动性介于1、3之间,表明这部分高分子链段和LAGPO颗粒存在的界面作用也是处于1、3之间.
基于上述归属,我们可以研究在复合物PEG-PPG-PEG-CF3SO3Li-LAGPO中陶瓷与高分子相表界面不同位置上高分子的运动情况.图 8中(a)、(b)、(c)分别为230 K、280 K、320 K下的1H-7Li WISE谱图.我们选取了化学位移为位置1(δLi -1.2)、位置2(δLi -0.8)的7Li核对应的1H NMR谱,如下图 9所示.
|
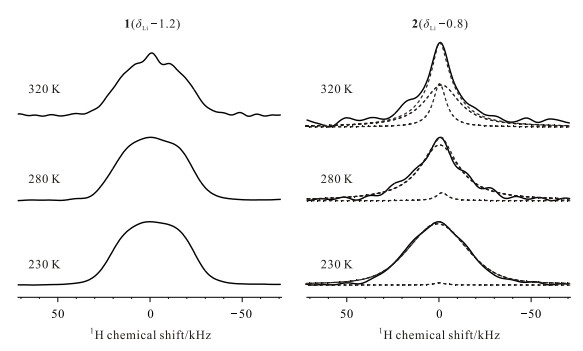
图 9 不同温度的2D 1H-7Li WISE谱图按照图 8标示的相同位置抽出的的F1维切片谱 Figure 9 Slices in the F1 dimension according to the mark on fig. 8 of 2D 1H-7Li WISE spectra at different temperatures |
从图 9可以看到,随着温度的升高,1谱的线宽没有明显的变化, 但是在320 K时出现了一个窄峰.1谱的线形在温度升高时所表现的这种稳定性,说明这部分高分子链段由于和陶瓷距离最近,受到的束缚作用强,导致高分子链运动性很差.在320 K出现的窄峰可能是来源于对应于1谱的部分高分子链段运动性的提高,也可能是其他高分子链段上的1H核通过自旋扩散传递而来.与图 9中1谱不同,2谱中的信号在230 K时接近高斯宽线.随着温度的升高,可以明显看到高斯宽线在逐渐减弱,而一个窄峰在逐渐增强.说明该信号对应的高分子随着温度的升高其运动能力逐步加强.从上面的讨论中我们已经知道:1谱(δLi -1.2)对应的高分子链可能是在陶瓷颗粒表面,与LAGPO颗粒存在着较强的界面作用;而2谱(δLi -0.8)对应的高分子链与LAGPO颗粒的界面作用较弱,因此与陶瓷颗粒表面距离相对较远.图 9中1、2谱图充分说明在我们制备的复合物材料中高分子与陶瓷颗粒的表界面上具有较为复杂的结构,而且这些表界面结构中高分子链段具有显著的运动性差异.考虑到高分子链段与锂离子的络合作用,上述NMR结果所揭示的表界面结构中高分子链段运动特点对我们理解表界面锂离子的运动具有非常重要的意义.
3 结论本文采用多种固体NMR技术并结合其他表征方法,如XRD、SEM等,研究了高分子-陶瓷复合物PEG-PPG-PEG-CF3SO3Li-LAGPO体系中高分子-陶瓷界面的性质.XRD和SEM的实验结果表明,高分子-陶瓷复合物PEG-PPG-PEG-CF3SO3Li-LAGPO中高分子大部分为非晶状态,高分子没有单独成相.固体1H-7Li WISE NMR实验揭示了复合物PEG-PPG-PEG-CF3SO3Li-LAGPO中高分子-陶瓷界面的结构和分子动力学特点:(1)复合物PEG-PPG-PEG-CF3SO3Li-LAGPO中高分子和LAGPO之间存在着明显的、具有复杂分子运动的界面;(2)按链段运动性进行区分,上述高分子-陶瓷界面中存在受限和严重受限的两层高分子层,从7Li NMR的化学位移推测,这两层高分子层中的锂离子可能具有不同的络合结构;(3)两层高分子层中的分子链段具有明显不同的温度依赖性.上述研究结果加深了我们对高分子-陶瓷复合物中界面结构和性质的理解.同时,本文所采用1H-7Li WISE实验展示出在表界面结构和分子运动研究方面的巨大潜力,这为该类材料表界面研究提供了一个新的思路和手段.
| [1] | GOODENOUGH J B, PARK K. The Li-ion rechargeable battery:A perspective[J]. J Am Chem Soc, 2013, 135(4): 1167-1176. DOI: 10.1021/ja3091438. |
| [2] | TARASCON J M, ARMAND M. Issues and challenges facing rechargeable lithium batteries[J]. Nature, 2001, 414(6861): 359-367. DOI: 10.1038/35104644. |
| [3] | ROBINSON A L, JANEK J. Solid-state batteries enter EV fray[J]. MRS Bulletin, 2014, 39(12): 1046-1047. DOI: 10.1557/mrs.2014.285. |
| [4] | KAMAYA N, HOMMA K, YAMAKAWA Y, et al. A lithium superionic conductor[J]. Nat Mater, 2011, 10(9): 682-686. DOI: 10.1038/nmat3066. |
| [5] | TREVEY J E, GILSDORF J R, MILLER S W, et al. Li2S-Li2O-P2S5 solid electrolyte for all-solid-state lithium batteries[J]. Solid State Ionics, 2012, 214: 25-30. DOI: 10.1016/j.ssi.2012.02.034. |
| [6] | SMITHA B, SRIDHAR S, KHAN A A. Solid polymer electrolyte membranes for fuel cell applications-a review[J]. J Membrane Sci, 2005, 259(1, 2): 10-26. |
| [7] | MANUEL STEPHAN A, NAHM K S. Review on composite polymer electrolytes for lithium batteries[J]. Polymer, 2006, 47(16): 5952-5964. DOI: 10.1016/j.polymer.2006.05.069. |
| [8] | LUNTZ A C, VOSS J, REUTER K. Interfacial challenges in solid-state Li ion batteries[J]. J Phys Chem Lett, 2015, 6(22): 4599-4604. DOI: 10.1021/acs.jpclett.5b02352. |
| [9] | ZHU Y Z, HE X F, MO Y F. Origin of outstanding stability in the lithium solid electrolyte materials:insights from thermodynamic analyses based on first-principles calculations[J]. ACS Appl Mater Interfaces, 2015, 7(42): 23685-23693. DOI: 10.1021/acsami.5b07517. |
| [10] | SAKUDA A, HAYASHI A, OHTOMO T, et al. All-solid-state lithium secondary batteries using LiCoO2 particles with pulsed laser deposition coatings of Li2S-P2S5 solid electrolytes[J]. J Power Sources, 2011, 196(16): 6735-6741. DOI: 10.1016/j.jpowsour.2010.10.103. |
| [11] | OHTA N, TAKADA K, ZHANG L Q, et al. Enhancement of the high-rate capability of solid-state lithium batteries by nanoscale interfacial modification[J]. Adv Mater, 2006, 18(17): 2226-2229. DOI: 10.1002/(ISSN)1521-4095. |
| [12] | SAKUDA A, HAYASHI A, TATSUMISAGO M. Interfacial observation between LiCoO2 electrode and Li2S-P2S5 solid electrolytes of all-solid-state lithium secondary batteries using transmission electron microscopy[J]. Chem Mater, 2010, 22(3): 949-956. DOI: 10.1021/cm901819c. |
| [13] | OHTA N, TAKADA K, SAKAGUCHI I, et al. LiNbO3-coated LiCoO2 as cathode material for all solid-state lithium secondary batteries[J]. Electrochem Commun, 2007, 9(7): 1486-1490. DOI: 10.1016/j.elecom.2007.02.008. |
| [14] | DOKKO K, HOSHINA K, NAKANO H, et al. Preparation of LiMn2O4 thin-film electrode on Li1+xAlxTi2-x(PO4)3 NASICON-type solid electrolyte[J]. J Power Sources, 2007, 174(2): 1100-1103. DOI: 10.1016/j.jpowsour.2007.06.137. |
| [15] | HOSHINA K, YOSHIMA K, KOTOBUKI M, et al. Fabrication of LiNi0.5Mn1.5O4 thin film cathode by PVP sol-gel process and its application of all-solid-state lithium ion batteries using Li1+xAlxTi2-x(PO4)3 solid electrolyte[J]. Solid State Ionics, 2012, 209, 210(8): 30-35. |
| [16] | KOTOBUKI M, HOSHINA K, KANAMURA K. Electrochemical properties of thin TiO2 electrode on Li1+xAlxGe2-x(PO4)3 solid electrolyte[J]. Solid State Ionics, 2011, 198(1): 22-25. DOI: 10.1016/j.ssi.2011.07.003. |
| [17] | ZHOU W D, WANG S F, LI Y T, et al. Plating a dendrite-free lithium anode with a polymer/ceramic/polymer sandwich electrolyte[J]. J Am Chem Soc, 2016, 138(30): 9385-9388. DOI: 10.1021/jacs.6b05341. |
| [18] | TIKEKAR M D, CHOUDHURY S, TU Z Y, et al. Design principles for electrolytes and interfaces for stable lithium-metal batteries[J]. Nature Energy, 2016, 1(9): 16114-16120. DOI: 10.1038/nenergy.2016.114. |
| [19] | MAIER J. Ionic conduction in space charge regions[J]. Prog Solid State Chem, 1995, 23(3): 171-263. DOI: 10.1016/0079-6786(95)00004-E. |
| [20] | ONG S P, MO Y F, RICHARDS W D, et al. Phase stability, electrochemical stability and ionic conductivity of the Li10±1MP2X12 (M=Ge, Si, Sn, Al or P, and X=O, S or Se) family of superionic conductors[J]. Energy Environ Sci, 2012, 6(1): 148-156. |
| [21] | WENZEL S, WEBER D A, LEICHTWEISS T, et al. Interphase formation and degradation of charge transfer kinetics between a lithium metal anode and highly crystalline Li7P3S11, solid electrolyte[J]. Solid State Ionics, 2016, 286: 24-33. DOI: 10.1016/j.ssi.2015.11.034. |
| [22] | WENZEL S, RANDAU S, LEICHTWEIß T, et al. Supporting information for:direct observation of the interfacial in-stability of the fast ionic conductor Li10GeP2S12 at the lithium metal anode[J]. Chem Mater, 2016, 28(7): 2400-2407. DOI: 10.1021/acs.chemmater.6b00610. |
| [23] | BOTTKE P, RETTENWANDER D, SCHMIDT W, et al. Ion dynamics in solid electrolytes:NMR reveals the elementary steps of Li+ hopping in the garnet Li6.5La3Zr1.75Mo0.25O12[J]. Chem Mater, 2015, 27(19): 6571-6582. DOI: 10.1021/acs.chemmater.5b02231. |
| [24] | MICHAN A L, LESKES M, GREY C P. Voltage dependent solid electrolyte interphase formation in silicon electrodes:Monitoring the formation of organic decomposition products[J]. Chem Mater, 2016, 28(1): 385-398. DOI: 10.1021/acs.chemmater.5b04408. |
| [25] | HE K, WANG Y H, ZU C K, et al. High-temperature X-ray analysis of phase evolution in lithium ion conductor Li1.5A10.5Ge1.5(PO4)3[J]. Mater Charact, 2013, 80: 86-91. DOI: 10.1016/j.matchar.2013.03.012. |
| [26] | JAEGER C, HEMMANN F. EASY:A simple tool for simultaneously removing background, deadtime and acoustic ringing in quantitative NMR spectroscopy. Part Ⅱ:Improved ringing suppression, application to quadrupolar nuclei, cross polarisation and 2D NMR[J]. Solid State Nucl Magn Reson, 2014, 63-64: 13-19. DOI: 10.1016/j.ssnmr.2014.08.001. |
| [27] | JAEGER C, HEMMANN F. EASY:A simple tool for simultaneously removing background, deadtime and acoustic ringing in quantitative NMR spectroscopy-Part Ⅰ:Basic principle and applications[J]. Solid State Nucl Magn Reson, 2014, 57-58: 22-28. DOI: 10.1016/j.ssnmr.2013.11.002. |
| [28] | CALUCCI L, GALLESCHI L, GEPPI M, et al. Structure and dynamics of flour by solid state NMR:effects of hydration and wheat aging[J]. Biomacromolecules, 2004, 5(4): 1536-1544. DOI: 10.1021/bm0499177. |
| [29] | BRUS J, DYBAL J, SCHMIDT P, et al. Order and mobility in polycarbonate-poly(ethylene oxide) blends studied by solid-state NMR and other techniques[J]. Macromolecules, 2000, 33(17): 6448-6459. DOI: 10.1021/ma000533s. |
 2017, Vol. 34
2017, Vol. 34 
