2. 波谱与原子分子物理国家重点实验室, 武汉核磁共振中心(中国科学院 武汉物理与数学研究所), 湖北 武汉 430071
2. State Key Laboratory of Magnetic Resonance and Atomic and Molecular Physics, National Center for Magnetic Resonance in Wuhan(Wuhan Institute of Physics and Mathematics, Chinese Academy of Sciences), Wuhan 430071, China
动态核极化(DNP)[1, 2]因可以极大地增强核磁共振(NMR)信号而引起了研究者的广泛关注.DNP是一种电子与核双共振技术,通过微波照射来饱和自由基中的未配对电子,由于电子与核之间存在偶合作用,从而使得与其偶合的核自旋能级布居数发生变化,把电子的高自旋极化度转移到核上,进而使核自旋获得高极化度,提高NMR检测灵敏度.DNP最大增强倍数E为:
| $ E=1-\rho fs\frac{|{{\gamma }_{\text{s}}}|}{{{\gamma }_{\text{I}}}} $ | (1) |
其中γs、γI分别代表电子和核的旋磁比.ρ为偶合因子,表征的是标量偶合与偶极偶合的相对贡献,其范围为-1~0.5.当只存在标量偶合时,ρ=-1;当只存在偶极偶合时,ρ=0.5.f为泄漏因子,表示电子自旋引起的核弛豫率与核总弛豫速率之比,其范围为0~1.当电子与核的偶合不存在弛豫时,f=0;当电子与核不存在其他弛豫机制时,f=1.s为饱和因子,表示电子极化的饱和程度,其范围为0~1.当电子完全饱和时,s=1;当不存在微波照射时,s=0.ρ、f、s是DNP实验的3个重要参数,决定了极化转移的最终结果.在溶液DNP中,电子与核之间的极化转移是通过弛豫完成的,而弛豫的强弱强烈依赖于核自旋与未配对电子间相互作用,即偶极偶合和超精细偶合.
Marin-Montesinos等[3]曾报道利用氢键作用使两个三苯甲游基自组装成二聚体,结果显示15N标记的胆碱的15N DNP增强效率提高了60%,这表明分子与自由基通过氢键作用后有效的提高了DNP的极化效率.那么,与氢键类似的一种相互作用——卤键(XB),是否也会同氢键一样对DNP极化效率造成影响呢?近年来,卤键已经在工程材料[4]和生命化学[5, 6]等领域展示了广泛的应用潜力.卤键[7]是指卤素原子和电负性原子或p体系之间的一种分子间弱相互作用.卤键的表达形式[8]为D-X…Y,其中D是C、N、卤素等元素;X为Lewis酸,是指Cl、Br、I等卤元素,它是电子受体位点,是卤键的供体;Y为Lewis碱,是指N、O、S等元素或p电子体系,它是电子供体位点,是卤键的受体.卤键概念的提出,不仅开辟了一个新的化学研究领域,也给从事合成化学的工作者提供了引入卤素的理论指导,更能在一定程度上促进了基于卤键合成的分子构筑学的发展.
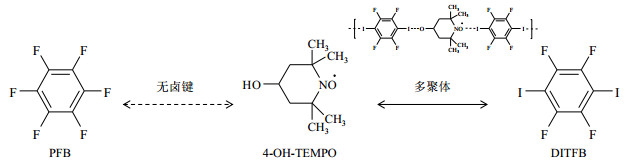
为研究卤键对DNP极化效率的影响,我们选择了DNP实验中最常用的自由基——4-羟基-2, 2, 6, 6-四甲基吡啶-1-氧自由基(4-OH-TEMPO),它具有性质稳定、化学惰性、在有机溶液中溶解性良好、电荷密度较高等特点,可以作为良好的卤键受体[9].在所有卤素中,碘原子是最强的卤键给体,最易形成卤键作用,其中碘代全氟碳是最理想和最常用到的卤键给体[10].本文在自主研制的DNP实验平台上,利用19F NMR、电子顺磁共振(EPR)以及DNP实验技术,通过比较观察存在卤键相互作用体系——1, 4-二碘四氟苯(DITFB)/4-OH-TEMPO与无卤键作用对照组——六氟苯(PFB)/4-OH-TEMPO的19F DNP极化效率的差异,对卤键体系19F DNP增强进行研究.两种体系的自组装示意图如图 1所示.
|
图 1 1, 4-二碘四氟苯(DITFB)、六氟苯(PFB)与4-羟基-2, 2, 6, 6-四甲基吡啶-1-氧自由基(4-OH-TEMPO)自由基的自组装示意图[11] Figure 1 Self-assembly of DITFB and PFB with 4-OH-TEMPO |
4-OH-TEMPO(纯度为98%)、DITFB(纯度为99%)、PFB(纯度为98%)、CDCl3(纯度大于99.0%)均购于百灵威试剂公司.
分别配制DITFB/4-OH-TEMPO和PFB/4-OH-TEMPO的系列CDCl3溶液,其中DITFB和PFB的浓度为1.5 mol/L,4-OH-TEMPO浓度分别为20 mmol/L、50 mmol/L、70 mmol/L、100 mmol/L、200 mmol/L,以三氟甲苯(C6H5CF3)作为外标(δF -63.7).
1.2 19F NMR实验19F NMR实验在实验室自主研制的500 MHz NMR谱仪(WIPM-I 500MHz NMR)上完成.19F核观测频率为470.65 MHz,采样温度为25 ℃,样品不旋转,采用s1pul脉冲序列(d1-90°-ACQ),实验参数如下:DITFB/4-OH-TEMPO溶液采样时谱宽(SW)为71 510 Hz,PFB/4-OH-TEMPO溶液采样时谱宽为100 116 Hz,DITFB/4-OH-TEMPO溶液采样时90°脉宽约为6 μs,PFB/4-OH-TEMPO溶液采样时90°脉宽约为8 μs;等待时间(d1)为5 s,采样时间为2 s,累加次数(NS)为1.
纵向弛豫时间(T1)采用反转恢复法进行测试(d1-180°-d2-90°-ACQ),实验参数如下:DITFB/4-OH-TEMPO溶液采样时谱宽为69 500 Hz,PFB/4-OH-TEMPO溶液采样时谱宽为110 386 Hz;DITFB/4-OH-TEMPO溶液采样时90°脉宽约为6 μs,PFB/4-OH-TEMPO溶液采样时90°脉宽约为8 μs;等待时间为10 s,采样时间为2 s,累加次数为1;自由基浓度为20 mmol/L、50 mmol/L、70 mmol/L时,d2阵列为0.062 5 s,0.125 s,0.25 s,0.5 s,1 s,2 s,4 s,8 s,16 s,32 s;自由基浓度为100 mmol/L和200 mmol/L时,d2阵列为0.016 s,0.032 s,0.064 s,0.128 s,0.256 s,0.512 s,1.024 s,2.048 s.
1.3 连续波-电子顺磁共振(CW-EPR)实验CW-EPR实验在JES-FA200型谱仪(日本JEOL公司)上进行,精确测定样品质量及填充长度,取分析样品装入EPR专用石英玻璃管中,然后放入仪器测量室,使磁场扫描中心对准样品中央. X-Band扫描频率为9.0~9.5 GHz,功率为3.0 mW,磁场扫描范围为276~376 mT.
1.4 19F DNP增强实验DNP增强实验在自主研制的DNP谱仪上进行,静磁场下质子共振频率为2.62 MHz.使用图 2所示的脉冲序列测试19F核的增强情况,分别在打开和关闭微波功放的情况下采集自由感应衰减(FID)信号.微波对应于EPR谱的其中一条谱线,且采用连续波激发,采样点数为2 048,微波照射时间为0.8 s,微波功率为158 W(谐振腔输入端),采样温度控温在25 ℃.

|
图 2 DNP 90°脉冲序列 Figure 2 DNP 90° pulse sequence |
自由电子的存在会影响到原子核的NMR化学位移和弛豫,而卤键的作用有可能会改变电子对核NMR信号的影响程度.本研究以DITFB/4-OH-TEMPO卤键体系为考察对象,与无卤键对照组—PFB/4-OH-TEMPO进行对比,观测卤键存在对19F NMR的化学位移及T1的影响.表 1为DITFB与PFB在CDCl3溶液中随着自由基浓度增加的化学位移变化情况.溶液中4-OH-TEMPO自由基能和众多的化合物形成瞬时的“碰撞络合物”,而使化合物产生顺磁位移.当DITFB与PFB溶液中不存在自由基时,它们的化学位移分别为δF -118.54和δF -163.04.从表 1中可以看出:(1)当DITFB与PFB溶液引入自由基,DITFB和PFB的19F NMR均产生了顺磁位移,化学位移向低场移动;并且随着自由基浓度的增大,化学位移向低场移动越来越显著,即化学位移差(DδF=δ有自由基-δ无自由基)逐渐增大.(2)存在卤键相互作用的DITFB/4-OH-TEMPO体系与不存在卤键相互作用的PFB/4-OH-TEMPO对照组的19F NMR化学位移变化并没有显著的差异,此结果与Cavallotti等[12]的研究报道不一致.Cavallotti等以卤代全氟碳/TEMPO自由基为研究体系,利用19F NMR研究电子受体/电子供体摩尔比分别为1: 1、1: 3、1: 6、1: 9和1: 12时的化学位移变化情况,发现存在卤键相互作用的样品体系相对于不存在卤键样品体系化学位移向低场移动地更加显著,即化学位移差更加明显.两者不一致的原因可能是本实验中电子受体DITFB和PFB的浓度较高,但电子供体4-OH-TEMPO自由基浓度较低,DITFB与4-OH-TEMPO自由基间只形成了少量卤键.对于卤键较少的情况,19F NMR可能并不能检测出有或无卤键相互作用两种体系中化学位移变化的差异.
| 表 1 DITFB与PFB随着自由基浓度增加的化学位移差和T1(CDCl3) Table 1 Chemical shift differences and T1 of DITFB and PFB at different radical concentration (CDCl3) |
TEMPO自由基这类顺磁性物质和待研究的逆磁性分子发生络合时,它不仅会使得逆磁性分子中原子核NMR信号产生很大的顺磁位移,且将大大缩短核的弛豫时间,并使得NMR谱线产生不同程度的增宽.从表 1中可以看出,在不存在自由基时,DITFB与PFB的T1分别为2.226 s与2.637 s.随着自由基浓度的增加,DITFB与PFB两种物质中19F核的弛豫随之不断加快,即T1越来越小.与自由基分子存在卤键作用的DITFB比PFB对照组的19F核的T1减少得更加显著,说明了卤键作用加快了19F NMR弛豫.
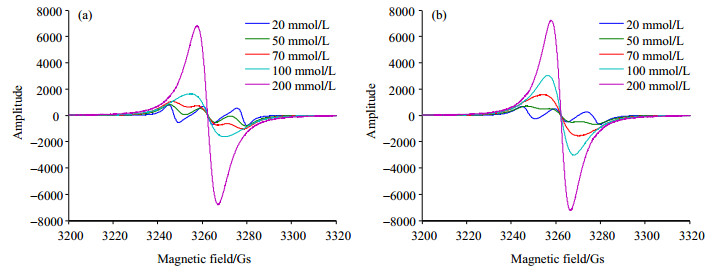
2.2 CW-EPR结果与分析如果在未成对电子附近存在具有磁性的原子核,通过二者自旋磁距的相互作用,使单一的共振吸收谱线分裂成多重谱线,它们被称为超精细偶合结构,偶合作用大小用AN表示.氮氧自由基中氮原子核(I=1,I为自旋量子数)的自旋与未成对电子的自旋相互作用,使得超精细裂分符合(2nI+1)规律.图 3为DITFB与PFB在CDCl3溶液中随着自由基浓度变化的EPR谱图.如图 3所示,在自由基浓度为20 mmol/L时,溶液中均呈现超精细分裂现象.通过测量得知,卤键作用存在体系——DITFB/4-OH-TEMPO组和无卤键作用体系——PFB/4-OH-TEMPO组的超精细偶合常数分别为15.30 Gs和14.46 Gs(1 Gs=10-4 T).卤键相对于无对照组卤键存在体系的超精细偶合常数明显增大.对于氮氧自由基,增加氮原子上的电子自旋密度或者减小氧原子上的电子自旋密度都能使氮原子的超精细偶合常数增加[13].卤键是电子给体与受体之间的相互作用,是电子密度从密集区到贫瘠区的供给[14].卤素原子为吸电子基团,当DITFB与自由基形成I…O卤键时,使单电子定域在氮原子上,增加了氮原子周围的电子自旋密度,降低了氧原子周围的电子自旋密度,因此超精细偶合常数也随之增大.
|
图 3 不同自由基浓度时,DITFB/4-OH-TEMPO (a)和PFB/4-OH-TEMPO (b)的EPR谱图 Figure 3 EPR spectra of (a) DITFB/4-OH-TEMPO and (b) PFB/4-OH-TEMPO at different radical concentration |
从图 3可以看出,自由基浓度对EPR谱线有显著影响.在自由基浓度较低时,EPR波谱表现出三重峰.随着自由基浓度的不断增大,自由基分子间自旋-自旋相互作用增加,EPR谱线逐渐变宽,超精细结构的分辨率逐渐降低,直至出现对称的单峰.在自由基浓度为50 mmol/L时[图 4(a)],可以明显观察到卤键作用存在体系与无卤键作用的对照组之间EPR谱线的差别:不存在卤键作用的对照组中,PFB与自由基仅是瞬时的“碰撞络合物”,自由基分子间具有强烈的自旋-自旋相互作用,EPR谱线增宽,超精细结构逐渐消失;在相同自由基浓度的情况下,在存在卤键相互作用时,DITFB与4-OH-TEMPO形成多聚体,自由基与自由基被DITFB隔开,自旋-自旋相互作用相对较弱,自由基EPR波谱的超精细结构仍相对明显.自由基浓度为70 mmol/L [图 4(b)]时,两种体系的EPR谱图也证实了上述现象.而当自由基浓度继续增大时,电子与电子相互作用占主导地位,两种体系的EPR谱均不再存在超精细分裂.

|
图 4 自由基浓度为50 mmol/L (a)和70 mmol/L (b)时,DITFB/4-OH-TEMPO与PFB/4-OH-TEMPO的EPR谱线 Figure 4 EPR spectra of DITFB/4-OH-TEMPO and PFB/4-OH-TEMPO at radical concentration of (a) 50 mmol/L and (b) 70 mmol/L |
EPR实验结果表明卤键的存在对电子与电子之间的相互作用产生了显著影响,而DNP是通过电子-核极化转移提高核的NMR信号的检测灵敏度的技术.那么,电子与电子相互作用的改变对DNP增强倍数的影响又会是怎样的呢?
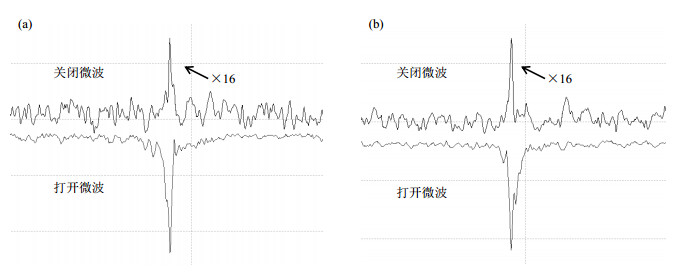
图 5为19F DNP增强结果对比,从图 5中我们可以看出,总体上,在没有微波作用时,采集到的信号非常弱,而在有微波的情况下,信号明显得到极大的提高.在自由基浓度为20 mmol/L时,DITFB/4-OH-TEMPO体系的增强约为-43倍,PFB/4-OH-TEMPO体系的增强倍数约为-28倍.因此,通过DNP增强能够有效提高NMR的检测灵敏度.并且,DNP增强与未成对电子浓度有关.如图 6所示,无论是PFB/4-OH-TEMPO体系还是DITFB/4-OH-TEMPO体系,在自由基浓度较低范围内,随着自由基浓度的增加,19F DNP信号增强的倍数也越来越大;但当自由基浓度大于100 mmol/L后,DITFB/4-OH-TEMPO体系的19F DNP信号增强的倍数略有下降,PFB/4-OH-TEMPO体系的19F DNP信号增强的倍数仍在缓慢增加.总体而言,在自由基浓度相对较低时,有卤键作用的DITFB/4-OH-TEMPO体系19F DNP增强倍数比没有卤键作用的PFB/4-OH-TEMPO体系高;而且两者间19F DNP增强倍数的差别在自由基浓度小于100 mmol/L时最大.在DNP实验中,增强因子与饱和因子呈正比关系,而饱和因子同电子弛豫亦呈正比关系,电子的弛豫时间(T1e和T2e)越长,饱和因子越大[15].由卤键作用使得EPR线宽变窄(图 4)可知,卤键的存在削弱了自由基电子与电子之间的自旋-自旋相互作用,使得自旋-自旋作用的时间变长,T2e增大,饱和因子变大,因而使DITFB/4-OH-TEMPO体系的DNP增强倍数增大.
|
图 5 自由基浓度为20 mmol/L时,DITFB/4-OH-TEMPO (a)和PFB/4-OH-TEMPO (b) 19F DNP增强结果对比 Figure 5 19F DNP enhancement with 20 mmol/L radical of DITFB/4-OH-TEMPO (a) and PFB/4-OH-TEMPO (b) |

|
图 6 DITFB/4-OH-TEMPO与PFB/4-OH-TEMPO体系随着自由基浓度增加的19F DNP极化增强倍数(CDCl3) Figure 6 19F DNP enhancement of DITFB/4-OH-TEMPO and PFB/4-OH-TEMPO with the increasing of radical concentration (CDCl3) |
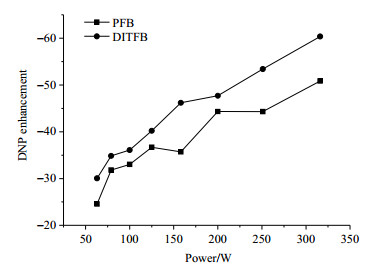
从图 7可以看出,微波功率从63 W逐渐增加到316 W的过程中,PFB/4-OH-TEMPO与DITFB/4-OH-TEMPO的19F DNP信号增强都在不断增加,可知实验过程中电子并未达到饱和.但是从NMR实验结果(表 1)可知,随着自由基浓度逐渐增加,体系中T1不断缩短,但T1过短会严重影响电子的高自旋极化度转移到核的效率,可能造成DNP倍数不再继续增加而是降低.因此,在自由基浓度大于100 mmol/L时,由于DITFB/4-OH-TEMPO的T1比PFB更短,因此DITFB/4-OH-TEMPO增强倍数略有降低,而PFB/4-OH-TEMPO增强倍数增加缓慢.
|
图 7 DITFB/4-OH-TEMPO与PFB/4-OH-TEMPO体系随着微波功率增加的19F DNP极化增强倍数 Figure 7 19F DNP enhancement of DITFB/4-OH-TEMPO and PFB/4-OH-TEMPO with the increasing of microwave power |
本文以卤键存在体系——DITFB/4-OH-TEMPO为研究对象,利用19F NMR、EPR以及19F DNP技术研究卤键作用对自由基电子相互作用的影响.结果表明,少量的卤键相互作用对其NMR信号没有明显影响,而对EPR和DNP的检测则影响显著.相比无卤键作用体系,有卤键作用的体系具有更窄的EPR线宽和更大的19F DNP增强.因此,卤键作用可以通过影响电子自旋-自旋作用来改善核的DNP增强效果.同时,DNP测试核增强倍数的方法为卤键作用提供了一个新的分析表征方法,对于更清晰认识卤键分子间相互作用、药物设计或晶体设计具有重要意义.
| [1] | OVERHAUSER A W. Polarization of nuclei in metals[J]. Phys Rev, 1953, 92(2): 411-415. DOI: 10.1103/PhysRev.92.411. |
| [2] | MALY T, DEBELOUCHINA G T, BAJAJ V S, et al. Dynamic nuclear polarization at high magnetic fields[J]. J Chem Phys, 2008, 128(5): 052211-052219. DOI: 10.1063/1.2833582. |
| [3] | MARIN-MONTESINOS I, PANIAGUA J C, VILASECA M, et al. Self-assembled trityl radical capsules-implications for dynamic nuclear polarization[J]. Phys Chem Chem Phys, 2015, 17(8): 5785-5794. DOI: 10.1039/C4CP05225K. |
| [4] | CINČIĆ D, FRIŠČIĆ T, JONES W. A stepwise mechanism for the mechanochemical synthesis of halogen-bonded cocrystal architectures[J]. J Am Chem Soc, 2008, 130(24): 7524-7525. DOI: 10.1021/ja801164v. |
| [5] | IBRAHIM M A. AMBER empirical potential describes the geometry and energy of noncovalent halogen interactions better than advanced semiempirical quantum mechanical method PM6-DH2X[J]. J Phys Chem B, 2012, 116(11): 3659-3669. DOI: 10.1021/jp3003905. |
| [6] | PARKER A J, STEWART J, DONALD K J, et al. Halogen bonding in DNA base pairs[J]. J Am Chem Soc, 2012, 134(11): 5165-5172. DOI: 10.1021/ja2105027. |
| [7] | METRANGOLO P, NEUKIRCH H, PILATI T, et al. Halogen bonding based recognition processes:A world parallel to hydrogen bonding[J]. Acc Chem Res, 2005, 38(5): 386-395. DOI: 10.1021/ar0400995. |
| [8] | DUMAS J M, GOMEL M, GUERIN M. ChemInform abstract:Molecular interactions involving organic halides[J]. Chem Inform, 1984, 15(34): 985-1020. |
| [9] | PANG X, ZHAO X R, WANG H, et al. Modulating crystal packing and magnetic properties of nitroxide free radicals by halogen bonding[J]. Crystal Growth Des, 2013, 13(8): 3739-3745. DOI: 10.1021/cg400776x. |
| [10] | MUGNAINI V, PUNTA C, LIANTONIO R, et al. Noncovalent paramagnetic complexes:detection of halogen bonding in solution by ESR spectroscopy[J]. Tetrahedron Lett, 2006, 47(19): 3265-3269. DOI: 10.1016/j.tetlet.2006.03.033. |
| [11] | BOUBEKEUR K, SYSSA-MAGALE J L, PALVADEVU P, et al. Self-assembly of nitroxide radicals via halogen bonding-directional NO⋯I interactions[J]. Tetrahedron Lett, 2006, 47(8): 1249-1252. DOI: 10.1016/j.tetlet.2005.12.088. |
| [12] | CAVALLOTTI C, METRANGOLO P, MEYER F, et al. Binding energies and 19F nuclear magnetic deshielding in paramagnetic halogen-bonded complexes of TEMPO with haloperfluorocarbons[J]. J Phys Chem A, 2008, 112(112): 9911-9918. |
| [13] | KNAUER B R, NAPIER J J. The nitrogen hyperfine splitting constant of the nitroxide functional group as a solvent polarity parameter. The relative importance for a solvent polarity parameter of its being a cybotactic probe vs. its being a model process[J]. Chem Inform, 1976, 7(41): 4395-4400. |
| [14] | METRANGOLO P, PILATI T, RESNATI G. Halogen bonding and other noncovalent interactions involving halogens:A terminology issue[J]. Crystengcomm, 2006, 8(12): 946-947. DOI: 10.1039/b610454a. |
| [15] | 张震. 液态杂核的低场DNP-NMR/MRI方法研究[D]. 武汉: 中国科学院武汉物理与数学研究所, 2016. http://cdmd.cnki.com.cn/Article/CDMD-80020-1016090709.htm |
 2017, Vol. 34
2017, Vol. 34 
