2. 中国科学院天然气水合物重点实验室, 中国科学院 广州能源研究所, 广东 广州 510650;
3. 国土资源部天然气水合物重点实验室, 青岛海洋地质研究所, 山东青岛 266071;
4. 青岛海洋科学与技术国家实验室 海洋矿产资源评价与探测技术功能实验室, 山东 青岛 266071;
5. 中国科学院大学, 北京 100049
2. Key Laboratory of Gas Hydrate, Guangzhou Institute of Energy Conversion, Chinese Academy of Sciences, Guangzhou 510650, China;
3. Key Laboratory of Natural Gas Hydrate, Ministry of Land and Resources, Qingdao Institute of Marine Geology, Qingdao 266071, China;
4. Laboratory for Marine Mineral Resources, Qingdao National Laboratory for Marine Science and Technology, Qingdao 266071, China;
5. University of Chinese Academy of Sciences, Beijing 100049, China
天然气水合物形成于低温高压条件下,富存于海洋大陆边缘和陆地的永久冻土区,是一种非常规天然气资源,具有分布广、储量大和能量密度高等特征,被视为未来的替代能源之一,因此被各国政府和科学界高度关注[1].自然界中的天然气水合物以甲烷水合物(CH4·nH2O)最为典型,在自然界的含量达90%以上[2].甲烷水合物是主要由甲烷和水分子构成的固态物质,属于非化学计量的结晶物质.与1 mol甲烷分子生成水合物的水分子摩尔数,即为水合数(n)[3].由水合数和所研究气体水合物的密度可计算出沉积物中水合物的丰度[4].天然气水合物能够存储大量气体,可以用来存储和运输气体.准确测定水合数对水合物资源的研究、开采及工业应用有重要意义.
水合数可通过水合物分解法直接测量得到,但受水合物中冰的影响会导致结果不准确[2].水合数间接测量方法包括差示扫描量热法(DSC)、激光拉曼光谱法和固体核磁共振(NMR)波谱法. Handa等人[5]用DSC法测得天然气水合物的水合数为5.91~6.00.Uchida等人[3]使用激光拉曼光谱法测得平衡态甲烷水合物晶体的水合数为6.20±0.2.Ripmeester等人[6]采集了13C标记的Ⅰ型甲烷水合物和Ⅱ型甲烷丙烷混合气体水合物的固体13C NMR谱图,并计算出甲烷水合物的水合数为6.05±0.06.相对于DSC,固体NMR测试不受冰融化的影响,能够表征气体水合物笼内物质的信息,为气体水合物的研究提供重要参考数据.甲烷水合物中,由于质子的个数较多、天然丰度高、旋磁比大,所以极化较强;而13C核的天然丰度较低(约为1.1%)、旋磁比小,所以极化较弱.交叉极化(CP)能使1H核的磁化强度通过极化转移传递到13C核,从而增强13C NMR信号;而高功率质子去偶(1H HPDEC)能通过射频照射消除质子对13C核的偶极偶合作用,以提高13C核的NMR检测灵敏度.这些固体NMR技术可以进一步提高甲烷水合物的检测灵敏度、改善NMR谱图分辨率,从而提高所得水合数的准确度.
气体水合物按其结构不同分为3类:Ⅰ型水合物、Ⅱ型水合物及H型水合物.Ⅰ型水合物每个晶胞单元含有2个512小笼(5边12面体)和6个51262大笼(14面体),Ⅱ型水合物每个晶胞单元含有16个512小笼和8个51264大笼(16面体),H型水合物每个晶胞含有3个512小笼、2个435663中笼(扁球形12面体)和1个51268大笼(椭球型12面体)[7](图 1).甲烷分子直径较小,单纯甲烷分子形成Ⅰ型水合物,进入512和51262笼,在超高压下也能形成Ⅱ型水合物;而甲烷与乙烷、二氧化碳等以一定比例混合时可形成Ⅱ型水合物,甲烷可进入512和51264笼[8];当甲烷与大分子(如环辛烷、四氢呋喃等)混合时,易形成H型的二元水合物,小分子气体(如甲烷)进入512小笼和435663中笼,而大分子(如环辛烷)进入3种笼型中腔体最大的51268笼[9].填充在不同笼型中的甲烷分子的13C NMR化学位移不同[10]:甲烷分子在Ⅰ、Ⅱ、H型水合物的512笼中的化学位移通常位于δC-4.1~-4.5之间,在Ⅰ型的51262大笼中的化学位移在δC-6.5~-6.7之间,在Ⅱ型的51264大笼的化学位移在δC-8.1~-8.2之间,在H型的435663中笼中的化学位移δC-4.7~-4.9之间[11].2007年,中国地质调查局在南海北部陆坡神狐海域组织实施了首个水合物钻探航次(GMGS1航次),完成钻探站位8个,其中在SH2站位钻获水合物样品,主要富集于稳定带底界上部10~43 m的范围之内,且水合物饱和度最高达48%,平均饱和度为22%,钻探证实水合物分布面积为15 km2[12].本研究利用SH2站位沉积物模拟天然气水合物生成条件,采用低温高分辨13C CP和1H HPDEC两种固体NMR技术表征所合成的甲烷水合物,包括冰粉+甲烷气体和冰粉+沉积物+甲烷气体,并利用激光拉曼光谱验证所测量的甲烷水合物的笼占有率和水合数的准确性,研究沉积物对甲烷水合物结构、笼占有率和水合数的影响.

|
图 1 3种常见气体水合物的晶胞结构 Figure 1 The unit cell structures of three common hydrate gases |
所用仪器主要包括自制的可视化气体水合物合成装置(压力为20 MPa,体积为100 mL)、300 MHz AVANCEⅢ宽腔固体NMR谱仪(瑞士Bruker)、LabRAM HR800激光共焦拉曼光谱仪(法国HORIBA JY,配备波长为532 nm的激光器)、Direct-Q3纯水系统(法国MILLIPORE)、FD-1C-50真空冷冻干燥机(西安太康).
所用试剂主要包括高纯甲烷(纯度为99.999%,购自广州盛盈气体有限公司)、金刚烷(纯度为99%,购自美国Sigma公司).
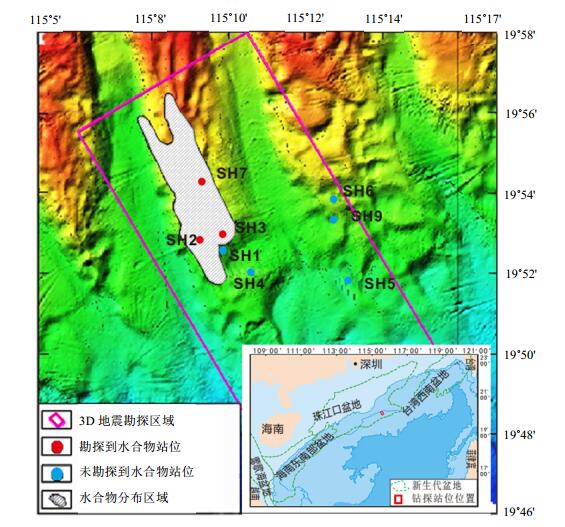
1.2 样品制备沉积物为南海北部陆坡神狐海域,SH2站位(图 2).沉积物经过纯净水分散后,冷冻干燥备用.
甲烷水合物样品由自制可视化气体水合物合成装置合成,具体过程如下:首先将纯净水制成冰粉,研磨,过200目筛;然后称取20 g过筛冰粉于反应釜中,制备冰粉+沉积物+甲烷气体样品时,还需向冰粉中加入10 g冷冻干燥后的沉积物;然后充入高纯甲烷,增压进行甲烷气体置换3次后,充压至10 MPa;在乙二醇-水浴控制的263 K温度下反应4 h后,设置水浴温度为272 K,待温度、压力平衡后继续反应反应7 d;反应结束卸压,在液氮保护下取出水合物,将合成的甲烷水合物于液氮中研磨后,用自制NMR装样工具在液氮中将样品均匀填入转子,并在液氮中装好盖子,将装好样品的定子保存于液氮中待测.
1.3 实验条件优化进行13C NMR实验时,使用7 mm DVT双共振固体NMR高分辨探头,以及7 mm的ZrO2转子和盖子.13C NMR工作频率为75.5 MHz.以金刚烷为外标对化学位移进行定标(δC38.5),并利用金刚烷作为标准物质对13C CP和1H HPDEC实验的参数进行优化.优化后的13C CP实验参数为:1H 90˚脉宽为3.5 μs,13C核接触时间为2 ms;优化后的1H HPDEC实验参数为:去偶序列为tppm15,脉冲重复间隔时间为20 s.首先使用空转子进行魔角旋转,旋转转速为2 kHz.将探头温度降低至170 K后,取出空转子,放入装有样品的转子,继续以2 kHz转速进行魔角旋转,扫描次数为128.
2 结果与讨论 2.1 冰粉与甲烷气体合成的甲烷水合物的13C NMR谱图分析根据化学位移判断甲烷所处的笼的类型,而且水合物的NMR谱峰面积之比可反映大笼和小笼个数之比,因此结合化学位移和大小笼数的峰面积比可判断水合物的类型:Ⅰ型水合物的大小笼数比为3:1,Ⅱ型水合物的大小笼数比为1:2.由13C CP实验测得的冰粉与甲烷气体合成的甲烷水合物的小笼特征峰位于δC-4.14、大笼特征峰位于δC-6.49,小笼和大笼的峰面积比为1:3.81;由1H HPDEC实验测得上述水合物小笼的特征峰位于δC-4.15、大笼特征峰位于δC-6.53,小笼和大笼的峰面积比为1:3.62,表明冰粉与甲烷气体合成的甲烷水合物为Ⅰ型水合物(见图 3).气态甲烷的化学位移为δC -10.2,笼型水合物中水分子的静电场对甲烷客体分子存在扰动,谱峰出现裂分.大笼是14面体,具有不同的形状和大小,笼内甲烷分子具有不同的化学位移,化学位移分布位于高场δC-6.41~-6.53之间;小笼是维度相同的5边12面体,甲烷分子在小笼中的化学位移分布更为集中,出现在低场δC -4.14[6].根据Buckingham的松笼-紧笼理论[14],甲烷分子在大笼中意味着更松的环境,腔体更大,分子运动更快,因此化学位移更接近气体峰;小笼为更紧的环境,甲烷分子运动受束,化学位移与气体峰更远.

|
图 3 由13C CP和1H HPDEC测得的冰粉与甲烷气体合成的甲烷水合物的13C NMR谱图,以及由1H HPDEC测得甲烷与冰粉和SH2站位沉积物气体合成的甲烷水合物的13C NMR谱图 Figure 3 13C NMR spectra of methane hydrates synthesized by mixing ice power without (using 13C CP and 1H HPDEC pulse sequence) and with (using 1H HPDEC pulse sequence) SH2 site sediments and methane gas |
笼占有率(θ)为客体分子占有的笼数与总水合物笼数的比值,可影响水合物晶体的气体容量[15].为了计算晶体水合数,假定甲烷分子的横截面及其极性在大小笼中几乎一致,IL/IS是大小笼NMR特征谱峰面积之比[14],甲烷在大笼和小笼中的笼占有率(θL/θS)之比[16]为:
| $ \frac{{{\theta _L}}}{{{\theta _S}}} = \frac{{{I_L}}}{{3{I_S}}} $ | (1) |
对于Ⅰ型水合物,每个晶胞单元含有46个水分子、2个小笼和6个大笼,甲烷水合物通常可以表述为CH4·nH2O,n为水合数.当甲烷分子填满小笼和大笼时,n接近于理想值5.75,然而,实际甲烷分子不能完全占满小笼和大笼,因此实际水合数(nC)的计算公式[14]为:
| $ {n_C} = \frac{{23}}{{\left( {3{\theta _L} + {\theta _S}} \right)}} $ | (2) |
在没有客体分子间相互作用和主体晶格扭曲时,水分子在空晶格中与冰之间的化学势能差(△μw0)为:
| $ \mathit{\Delta }\mu _w^0 = - {\rm{R}}T\left[ {3\ln \left( {1 - {\theta _L}} \right) - \ln \left( {1 - {\theta _S}} \right)} \right]/23 $ | (3) |
其中Ⅰ型水合物△μw0为1 297 J/mol,R为摩尔气体常数8.314,T为相平衡温度273 K.
由(1)~(3) 式即可计算出θL、θS以及水合数nC.由图 3和(1)~(3) 式计算出的冰粉和和甲烷气体合成的甲烷水合物的θL、θS、nC,及其文献值见表 1.
| 表 1 甲烷水合物的化学位移、小笼占有率、大笼占有率和水合数 Table 1 Chemical shifts, small cage occupancies, large cage occupancies and hydrate numbers of methane hydrates |
表 1显示本文利用冰粉与甲烷气体合成的甲烷水合物为Ⅰ型,其大笼和小笼占有率分别为0.988和0.824,水合数为6.07.甲烷在小笼占有率低于大笼,表明甲烷分子占有小笼的数量相对低于大笼,这与Klapproth报道[21]的人工合成甲烷水合物的小笼偏离理想朗缪尔行为的观点一致,而大笼中甲烷分子的填充情况与理想朗缪尔行为几乎完全相同.
由图 3可见,13C CP法采集的谱图信号较1H HPDEC法弱,主要在于1H HPDEC法可以有效消除1H-13C异核偶极偶合和J偶合,从而提高13C核的检测灵敏度和谱图分辨率.而且CP法在快速魔角旋转条件下,需要严格的实验参数优化才能实现Hartmann-Hahn匹配,从而达到信号增强;偏离匹配条件,非但不能实现13C NMR信号增强,还有可能无法观测到信号[22].由于CP参数优化是在293 K时使用金刚烷进行的,因而甲烷水合物测试条件为170 K,未必完全满足Hartmann-Hahn匹配条件[22];而且气体水合物测试在170 K和2 kHz旋转速率条件下,实现实验参数严格优化比较难,因而13C CP实验难以取得良好效果,故得到的NMR谱图信号和计算得到的水合数准确度相对1H HPDEC法更低.因此气体水合物测试建议使用1H HPDEC法.
2.2 甲烷气体与SH2站位沉积物和冰粉合成的甲烷水合物谱图分析甲烷气体与SH2站位沉积物和冰粉合成的甲烷水合物经过淘洗后,使用1H HPDEC法测得NMR谱图见图 3.小笼和大笼特征峰的化学位移分别为δC-4.14和δC-6.41.少量沉积物的存在对化学位移存在一定干扰,导致大笼峰和小笼峰的化学位移较不含沉积物时向低场位移动.大笼和小笼的峰面积比为3.34:1,为Ⅰ型水合物.由图 3和(1)~(3) 式计算出的甲烷气体与SH2站位沉积物和冰粉合成的甲烷水合物的小笼占有率0.887,大笼占有率为0.987,水合数为5.98(详见表 1).水合数稍低于理想值,却与利用固体NMR测得甲烷水合物水合数在5.8~6.3[12]之间相一致,表明本方法不仅适用于纯甲烷水合物,也适用于沉积物中生成的甲烷水合物.
SH2站位沉积物的存在不影响水合物类型,但提高了甲烷气体在小笼中的占有率和甲烷水合物饱和度、降低了水合物水合数.该水合数比利用激光拉曼光谱测得的SH2站位天然水合物的水合数5.91略高[23],可能是由于测试方法不同引起的,因而本文也利用激光拉曼光谱法对该结果进行了验证.
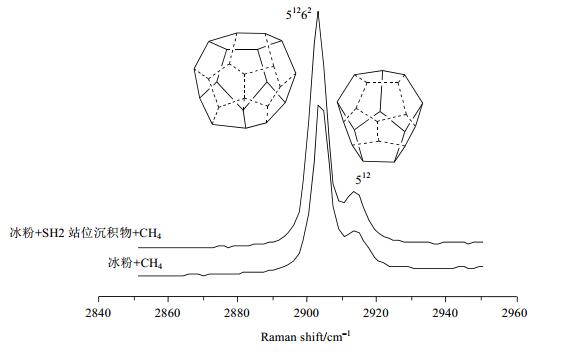
2.3 NMR技术与激光拉曼光谱法测得的水合数对比利用共聚焦激光拉曼光谱仪对不含沉积物和含有沉积物的冰粉与甲烷气体合成的甲烷水合物进行表征(见图 4):大笼峰(51262)出现在2 903 cm–1,小笼峰(512)出现在2 914 cm–1;峰没达到基线,分峰拟合后,冰粉与甲烷气体合成的甲烷水合物大笼和小笼峰面积比为3.51:1,甲烷气体与SH2站位沉积物和冰粉合成的甲烷水合物大笼和小笼峰面积比为3.36:1,也表明这两种水合物均为Ⅰ型水合物.利用(1)~(3) 式计算[24]得到:冰粉与甲烷气体合成的甲烷水合物小笼占有率0.844,大笼占有率0.987,水合数为6.04;甲烷气体与SH2站位沉积物和冰粉合成的甲烷水合物小笼占有率0.881,大笼占有率为0.987,水合数为5.82,低于该站位天然气水合物水合数5.98[23].该结果与使用NMR技术测得的结果相近,进一步验证了SH2站位沉积物的存在降低了甲烷水合物的水合数,提高了甲烷气体在小笼中的占有率和甲烷水合物的饱和度.
|
图 4 不含沉积物和含有SH2站位沉积物的冰粉与甲烷气体合成的甲烷水合物的激光拉曼谱图 Figure 4 Laser Raman spectra of methane hydrates synthesized by mixing ice power without and with SH2 site sediments and methane gas |
利用13C CP和1H HPDEC两种固体NMR方法对无沉积物参与和SH2站位沉积物参与的冰粉和甲烷气体合成的甲烷水合物进行了对比分析可知:1H HPDEC脉冲序列得到的NMR谱图信号和计算得到的水合数准确度相对更高,更适用于气体水合物测试.NMR实验结果显示,两种甲烷水合物均为Ⅰ型,冰粉和甲烷气体合成的甲烷水合物大笼和小笼占有率分别为0.988和0.824,水合数为6.07.甲烷气体与SH2站位沉积物和冰粉合成的甲烷水合物大笼和小笼占有率分别为0.987和0.887,水合数为5.98.该结果说明SH2站位沉积物的存在降低了甲烷水合物的水合数,提高了甲烷气体在小笼中的占有率和甲烷水合物的饱和度.使用激光拉曼光谱法的测试结果证实了上述结论.因此,可使用1H HPDEC固体NMR方法测定甲烷水合物的水合数,该测定可结果为气体水合物资源的研究及气体水合物技术工业应用提供参考.
致谢 感谢北京大学卢海龙教授对NMR测试气体水合物工作的指导.| [1] | PAULL C K, DILLON W P, et al. Natural gas hydrates:occurrence, distribution, and detection[M]. Washington DC: American Geophysical Union, 2001: 131-143. |
| [2] | KIDA M, HACHIKUBO A, SAKAGAMI H, et al. Natural gas hydrates with locally different cage occupancies and hydration numbers in Lake Baikal[J]. Geochem Geophy Geosy, 2009, 10(5): 1-8. |
| [3] | UCHIDA T, HIRANO T, EBINUMA T, et al. Raman spectroscopic determination of hydration number of methane hydrates[J]. AIChE J, 1999, 45(12): 2641-2645. DOI: 10.1002/(ISSN)1547-5905. |
| [4] | LU H L, LORENSON T D, MOUDRAKOVSKI I L, et al. The characteristics of gas hydrates recovered from the Mount Elbert Gas Hydrate stratigraphic test well, Alaska North Slope[J]. Mar Petrol Geol, 2011, 28(2): 411-418. DOI: 10.1016/j.marpetgeo.2010.01.002. |
| [5] | HANDA Y P. A Calorimetric study of naturally occurring gas hydrated[J]. Ind Eng Chem Res, 1988, 27(5): 872-874. DOI: 10.1021/ie00077a026. |
| [6] | RIPMEESTER J A, RATCLIFFEA C I. Low-temperature cross-polarizatlon/magic angle spinning 13C NMR of solid methane hydrates:structure, cage occupancy, and hydration number[J]. J Phys Chem, 1988, 92(2): 337-339. DOI: 10.1021/j100313a018. |
| [7] |
XIA N, LIU C L, YE Y G, et al. Study on determination method of natural gas hydrates by micro-laser raman spectroscopy[J].
Rock and Mineral Analysis, 2011, 30(4): 416-422.
夏宁, 刘昌岭, 业渝光, 等. 显微激光拉曼光谱测定天然气水合物的方法研究[J]. 岩矿测试, 2011, 30(4): 416-422. |
| [8] | OHNO H, TIMOTHY A S, STEVEN F D, et al. Raman studies of methane-ethane hydrate metastability[J]. J Phys Chem A, 2009, 113: 1711-1716. DOI: 10.1021/jp8010603. |
| [9] |
MENG Q G, LIU C L, YE Y G, et al. Measurement of micro-struc ture features of binary CH4-THF clathrate hydrate based on the 13C solid state NMR[J].
Natural Gas Industry, 2015, 35(3): 1-6.
孟庆国, 刘昌岭, 业渝光, 等. 13C固体核磁共振法测定CH4-THF二元水合物的微观结构特征[J]. 天然气工业, 2015, 35(3): 1-6. |
| [10] |
LIU C L, MENG Q G, YE Y G. Applications of solid state NMR in the studies of gas hydrate[J].
Chinese J Magn Reson, 2012, 29(3): 465-474.
刘昌岭, 孟庆国, 业渝光. 固体核磁共振技术在气体水合物研究中的应用[J]. 波谱学杂志, 2012, 29(3): 465-474. |
| [11] | MOUDRAKOVSHI I, LU H L, RIPMEESTER J A. Experimental solid state NMR of gas hydrates:problems and solutions[C]//Vancouver:Proceedings of the 6th International Conference on Gas Hydrates, 2008. |
| [12] |
WU N Y, ZHANG H Q, YANG S X, et al. Preliminary discussion on natural gas hydrate(NGH) reservoir system of Shenhu Area, North Slope of South China Sea[J].
Natural Gas Industry, 2007, 27(9): 1-6.
吴能友, 张海啟, 杨胜雄, 等. 南海神狐海域天然气水合物成藏系统初探[J]. 天然气工业, 2007, 27(9): 1-6. |
| [13] | WU N Y, ZHANG H Q, YANG S X, et al. Gas hydrate system of Shenhu area, Northern South China Sea:Geochemical results[J]. Journal of Geological Research, 2011: 370298. |
| [14] | SUBRAMANIAN S, SLOAN E D. Trends in vibrational frequencies of guests trapped in clathrate hydrate cages[J]. J Phys Chem B, 2002, 106(17): 4348-4355. DOI: 10.1021/jp013644h. |
| [15] | KIDA M, SUZUKI K, KAWAMURA T, et al. Characteristics of natural gas hydrates occurring in pore-spaces of marine sediments collected from the eastern Nankai Trough, off Japan[J]. Energy Fuels, 2009, 23(11): 5580-5586. DOI: 10.1021/ef900612f. |
| [16] | DAVDSON D W, HANDA Y P, RIPMEESTER J A. Xenon129 NMR and the thermodynamic parameters of xenon hydrate[J]. J Phys Chem, 1986, 90: 6549-6552. DOI: 10.1021/j100282a026. |
| [17] | SUSILO R, RIPMEESTER J A, ENGLEZOS P. Characterization of gas hydrates with PXRD, DSC, NMR, and Raman spectroscopy[J]. Chem Eng Sci, 2007, 62(15): 3930-3939. DOI: 10.1016/j.ces.2007.03.045. |
| [18] | LEE J W, LEE J, KANG S P. 13C NMR spectroscopies and formation kinetics of gas hydrates in the presence of monoethylene glycol as an inhibitor[J]. Chem Eng Sci, 2013, 104: 755-759. DOI: 10.1016/j.ces.2013.10.007. |
| [19] | RIPMEESTER J A, LU H, MOUDRAKOVSKI I L, et al. Structure and composition of gas hydrate in sediment recovered from the JAPEX/JNOC/GSC et al. Mallik 5L-38 gas hydrate production research well, determined by X-ray diffraction and Raman and solid-state nuclear magnetic resonance spectroscopy[J]. Geological Survey of Canada Bulletin, 2005, 585: 106. |
| [20] | KIM D Y, UHM T W, LEE H, et al. Compositional and structural identification of natural gas hydrates collected at Site 1249 on Ocean DrillingProgram Leg 204[J]. Korean J Chem Eng, 2005, 22(4): 569-572. DOI: 10.1007/BF02706645. |
| [21] | KLAPPROTH A, GORESHNIK E, STAKOVA D, et al. Structural studies of gas hydrates[J]. Can J Phys, 2003, 81(1, 2): 503-518. |
| [22] |
TANG X Q, ZHANG Z F, YANG J. Heating of biological samples in studies of MAS solid-state NMR[J].
Chinese J Magn Reson, 2015, 32(1): 123-140.
唐新启, 张正逢, 杨俊. 生物固体核磁共振中样品发热的研究进展[J]. 波谱学杂志, 2015, 32(1): 123-140. DOI: 10.11938/cjmr20150114. |
| [23] | LIU C L, YE Y G, MENG Q G, et al. The characteristics of gas hydrates recovered from Shenhu Area in the South China Sea[J]. Mar Geol, 2012, 307-310: 22-27. DOI: 10.1016/j.margeo.2012.03.004. |
 2017, Vol. 34
2017, Vol. 34