文章信息
- 马二倩, 李永肖, 赵瑞格, 张占辉, 杨秋青
- MA Er-qian, LI Yong-xiao, ZHAO Rui-ge, ZHANG Zhan-hui, YANG Qiu-qing
- NP-10与单链、双链季铵盐三种复配体系相互作用规律的NMR研究
- Interactions Between NP-10 and Single/Double Chain Quaternary Ammonium Salts Studied by NMR Spectroscopy
- 波谱学杂志, 2017, 34(1): 16-24
- Chinese Journal of Magnetic Resonance, 2017, 34(1): 16-24
- http://dx.doi.org/10.11938/cjmr20170103
-
文章历史
收稿日期: 2016-01-29
收修改稿日期: 2017-01-04


DOI:10.11938/cjmr20170103
2. 河北师范大学 分析测试中心, 河北 石家庄 050024
2. Analysis and Testing Center, Hebei Normal University, Shijiazhuang 050024, China
双子表面活性剂[1-4]被称作“新世纪表面活性剂”.它的出现为表面活性剂的基础和应用研究开拓了广阔的前景.目前,国内外对该类表面活性剂的研究多是Gemini溴化物季铵盐表面活性剂的胶束体系[5-7].它们利用核磁共振(NMR)、表面张力等方法探讨了14-s-14型Gemini溴化物季铵盐在传统面活性剂存在时交换过程的动力学与机理.但因其自组织行为远比普通的表面活性剂复杂,因此对其性能方面的研究还没有像传统表面活性剂那样具有系统性.在表面活性剂复配体系中,混合胶束的动态行为、分子间相互作用规律及其影响因素等方面的研究更加欠缺,特别是对Gemini氯化物季铵盐的混合体系报道极少.与普通表面活性剂复配,是降低生产成本的重要途径,经过多种实验[8-10]证明,表面活性剂复配体系之所以较单一的表面活性剂性能优越,其中最关键的因素是它们之间产生了相互作用力,即复配体系中形成了混合胶束.因此,混合胶束动力学性能方面的研究,成为表面活性剂研究的重点.
NMR技术具有能探测分子内部而不破坏分子本身的特点,能获得其它波谱方法所不能得到的信息,是近十几年研究分子表面活性剂的热门技术.我们前面已用NMR技术研究了Gemini氯化盐与绿色表面活性剂--十二烷基麦芽糖苷(DM)形成的混合体系[11, 12],得到了表面活性剂复配体系中混合胶束的一些动力学信息.为了获得更普适的规律,本文对普通的非离子表面活性剂壬基酚聚氧乙烯醚(NP-10)与阳离子表面活性剂,包括单链(DTAC)、双链(C12-C4-C12和C12-C8-C12)Gemini氯化物季铵盐形成的复配体系,进行了进一步研究.
1 实验部分NP-10的纯度经薄层色谱法(TLC)测定大于95.0 %,购自Calbiochem公司;DTAC纯度大于99.0 %,购自日本TCI Chemicals公司;氘代率为99.9 %的D2O购自美国CIL公司;双链氯化物季铵盐为自制品,结构通过红外光谱和NMR谱图确认,NP-10、DTAC、C12-C4-C12和C12-C8-C12的临界胶束浓度(cmc)经表面张力测定分别为0.059 mmol/L、20 mmol/L、1.5 mmol/L和0.8 mmol/L.表面活性剂的结构及质子编号见图 1.
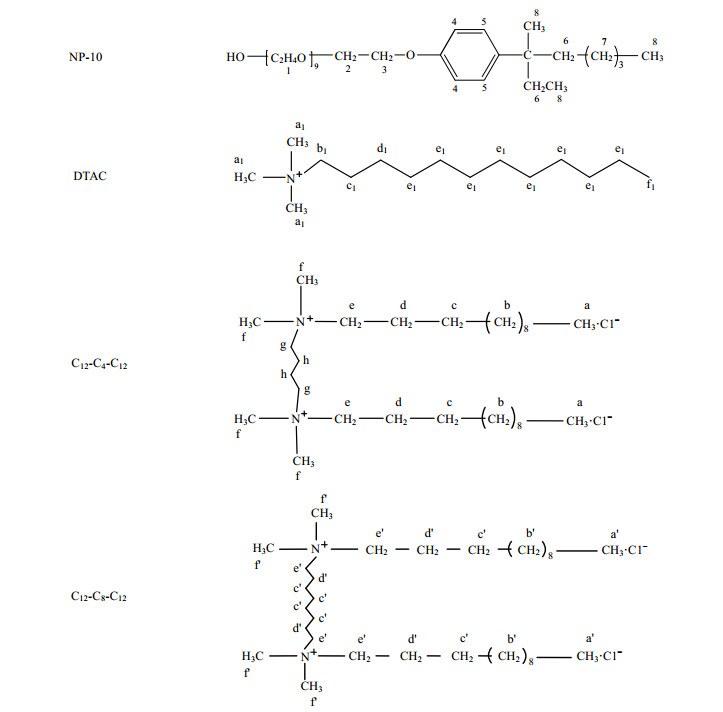
|
| 图 1 4个表面活性剂的分子结构 Fig. 1 Molecular structures of 4 surfactants |
NMR实验均在质子共振频率为500.13 MHz的Bruker DMX-500 NMR谱仪上进行,溶剂为D2O,采样温度为298 K,用二维扩散排序谱(DOSY)测量自扩散系数(D).利用预饱和反转恢复法和CPMG(Carr-Purcell-Meiboom-Gill)脉冲序列分别测量纵向弛豫时间(T1)和横向弛豫时间(T2).2D NOESY谱采用标准三脉冲序列,为确保2D NOESY谱中相关点强度的准确性、避免系统中慢运动导致的自扩散,混合时间(d8)经过优化设为300 ms.
2 结果与讨论 2.1 化学位移的变化表面活性剂1H NMR的化学位移(δH)对所处环境很敏感,是研究表面活性剂的一个重要参数.在单链、双链氯化物季铵盐与NP-10表面活性剂复配体系中,固定NP-10浓度为44 mmol/L,我们发现随着DTAC、C12-C4-C12和C12-C8-C12摩尔浓度的增加,3个复配体系中氯化物季铵盐的化学位移均向低场移动,但变化幅度不同.在NP-10/DTAC复配体系中,随着DTAC浓度的增加,DTAC的化学位移变化比较小,最大位移1 Hz;而在复配体系NP-10/C12-C4-C12和NP-10/C12-C8-C12中,C12-C4-C12和C12-C8-C12的最大位移分别为22 Hz和23 Hz,由此我们可以推断出在3个不同的复配体系中,分子间的相互作用力大小是有差异的,从而导致化学位移变化的幅度不同.双链混合配体较单链混合配体的化学位移变化大,可能是因为双链表面活性剂比单链表面活性剂在复配体系中能表现出更好的协同作用,与NP-10分子间的相互作用更强.此外在复配体系NP-10/C12-C8-C12中,我们还可以看到一个明显的现象(见图 2),当NP-10:C12-C8-C12=1:3时,C12-C8-C12化学位移反而向高场位移,与两者摩尔比小于等于2时规律相反,这表明1:2的配比,是该复配体系中分子间与分子内相互作用力的拐点,或者说1:2是一个较好的复配摩尔比例.该结论我们将会在后面的实验中进一步检验核实.
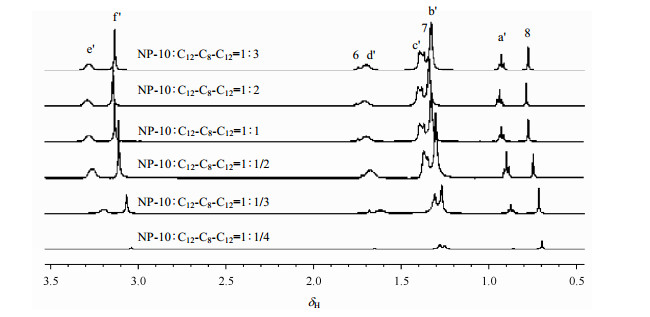
|
| 图 2 不同摩尔比时,C12-C8-C12的1H NMR谱(固定NP-10浓度为44 mmol/L) Fig. 2 1H NMR spectra of C12-C8-C12 at different molar ratios (CNP-10=44 mmol/L) |
分子自扩散是分子热运动的一种,利用脉冲梯度场(PFG)NMR实验测定的自扩散系数(D)是混合溶液中所有分子(既包括溶液中的胶束分子,也包括自由单分子)的平均值,可反映表面活性剂形成胶束的尺寸.在混合溶液中,自由单分子与胶束分子之间存在着快速交换,在浓度大于临界胶束浓度以上的混合溶液中,自扩散系数分析基于(1) 式或(2) 式[13, 14]:
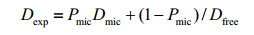
|
(1) |
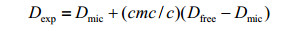
|
(2) |
Dexp是PFG NMR实验所测得的自扩散系数,Dmic和Dfree分别表示混合溶液中的胶束分子和自由单分子的自扩散系数,Pmic表示胶束分子所占的浓度比例,cmc和c分别表示溶液的临界胶束浓度和总浓度.由(1) 式和(2) 式可以看出,Dexp的大小取决于溶液中的胶束分子和自由单分子两部分.根据相分离模型,混合溶液临界胶束浓度(用cmc*表示)可以用(3) 式表示[15]:

|
(3) |
其中α1表示表面活性剂1在混合溶液中所占的摩尔比例,cmc1和cmc2分别表示表面活性剂1和2的临界胶束浓度.实验时3个混合体系溶液浓度均为cmc*的200倍以上,此时溶液中都已经形成胶束,因此Dexp主要是来自胶束分子的贡献,自由单分子的贡献可忽略.
进行实验时,我们固定NP-10浓度为44 mmol/L,通过增加氯化物季铵盐的浓度,将溶液摩尔比从1:1调整至1:6,结果显示3种复配体系的自扩散系数均随着单链、双链氯化物季铵盐的浓度增加而减小,说明混合胶束的水合动力学半径随着单链、双链氯化物季铵盐的浓度增加越来越大.为了进一步明确在形成混合胶束的过程中,哪种表面活性剂对胶束的水合动力学半径起到主导作用,我们又采用了固定总浓度为60mmol/L,分别改变两种表面活性剂相对摩尔比例的方法.NP-10、DTAC、C12-C4-C12和C12-C8-C12纯溶液的自扩散系数分别为2.85×10−11 m2/s、43.54×10−11 m2/s、9.25×10−11 m2/s和10.87×10−11 m2/s.当NP-10与3个阳离子表面活性剂摩尔比为1:1时,其混合体系的的扩散系数与NP-10纯溶液接近,而远离3个单链或双链氯化物季铵盐纯溶液(见表 1),这表明NP-10对3种混合胶束的水合动力学半径的影响大于氯化物季铵盐分子.
| 复配体系 | NP-10:季铵盐 | ||
| 1:1/3 | 1:1 | 1:3 | |
| NP-10/DTAC | 4.33 | 8.78 | 24.34 |
| NP-10/C12-C4-C12 | 3.45 | 3.87 | 5.64 |
| NP-10/C12-C8-C12 | 3.51 | 4.56 | 6.24 |
NMR实验中的弛豫时间包括T1和T2两种[16],是研究表面活性剂的又一重要的动力学参数.T1又称自旋-晶格驰豫时间,对分子局部的高频运动比较敏感;T2又称自旋-自旋弛豫时间,对长分子链的慢运动扩散比较敏感.分子的质子密度越大时,质子间的偶极相互作用就越强,分子链运动就越慢,导致T2较低.单链和双链季铵盐3种阳离子表面活性剂纯溶液情况下,各质子T2的变化规律是相似的,即T2随着表面活性剂浓度的增加缓慢下降.当与NP-10形成复配体系以后,各质子的T2值出现了一致相反的变化(表 2):随着DTAC、C12-C4-C12和C12-C8-C12浓度加大,它们各自的T2呈现上升的趋势,这充分证明了表面活性剂复配体系中发生了分子间相互作用.当NP-10与DTAC和C12-Cs-C12(s=4或8)混合体系的摩尔比分别为1:3和1:2时,T2的变化出现拐点,开始减小,这说明这种相互作用大小会随着混合体系中两种表面活性剂的相对摩尔分数不同而变化.而协同效应也会随着相互作用力的变化而变化:相互作用力大,协同效应就明显;反之亦然.当NP-10/DTAC和NP-10/C12-Cs-C12(s=4或8)的配比分别为1:3和1:2时,其分子间的相互作用力开始减小,分子内作用力开始起主导作用,即混合体系中两种表面活性剂分子的协同效应减弱,此时即使再继续增加DTAC、C12-C4-C12和C12-C8-C12的量,对增加协同效应也是徒劳的.
| 质子 | NP-10:季铵盐 | |||||||
| 1:1/3 | 1:1/2 | 1:1 | 1:2 | 1:3 | 1:4 | |||
| DTAC | H-a1 | 364 | 398 | 437 | 439 | 442 | 437 | |
| H-b1 | 209 | 243 | 249 | 251 | 262 | 254 | ||
| H-c1 | 278 | 321 | 347 | 352 | 359 | 348 | ||
| H-d1 | 60 | 110 | 135 | 152 | 172 | 159 | ||
| H-e1 | 147 | 161 | 174 | 178 | 182 | 179 | ||
| H-f1 | 131 | 137 | 145 | 148 | 153 | 147 | ||
| C12-C4-C12 | H-a | 237 | 261 | 274 | 286 | 271 | 265 | |
| H-b | 115 | 116 | 119 | 124 | 112 | 109 | ||
| H-e | 48 | 51 | 65 | 78 | 72 | 67 | ||
| H-f | 88 | 91 | 101 | 106 | 96 | 93 | ||
| H-g | 49 | 52 | 68 | 99 | 75 | 69 | ||
| H-h | 46 | 49 | 63 | 67 | 65 | 53 | ||
| C12-C8-C12 | H-a′ | 257 | 258 | 284 | 291 | 273 | 267 | |
| H-b′ | 123 | 125 | 147 | 158 | 152 | 141 | ||
| H-c′ | 78 | 99 | 107 | 115 | 97 | 91 | ||
| H-d′ | 50 | 53 | 68 | 87 | 73 | 69 | ||
| H-e′ | 64 | 73 | 78 | 85 | 75 | 71 | ||
| H-f′ | 73 | 96 | 97 | 104 | 99 | 95 | ||
3种复配体系中各质子的T2/T1比值均小于1,说明分子链运动受到限制[17, 18],溶液内形成了胶束.在3种复配体系中,NP-10/C12-C8-C12复配体系中T2/T1≤0.5的质子个数最多,NP-10/C12-C4-C12次之,NP-10/DTAC最少,这说明在3种复配体系中,NP-10/C12-C8-C12复配体系的胶束排列最为紧密;而NP-10/DTAC复配体系胶束排列相对松散,该混合体系的相互作用力相对其它两体系较弱,这一结论得到了后面2D NOESY实验的验证.
2.4 空间距离的变化2D NOESY谱是研究大分子聚集结构中空间距离小于0.5 nm的核间距的重要方法,能够反映混合胶束中两个表面活性剂分子之间相互作用的强弱、质子之间的距离大小以及分子的排列方式[19, 20].依据核Overhanser效应(NOE)强度与质子间距离的关系式[(4) 式][21],可求出质子间距离的变化.
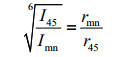
|
(4) |
rmn表示m质子和n质子之间的距离,Imn表示m质子和n质子之间的交叉峰强度.该式表明交叉峰的强度越强,两质子间的距离越近,作用力越强.由此就可以从2D NOESY谱图中定量分析两个表面活性剂的相互作用情况.为方便比较,选择NP-10分子苯环上H-4/H-5为参考距离.依据苯环的空间结构,可以求出H-4/H-5之间的距离是0.240 nm.由(4) 式我们可以计算出其它任何两个质子间的距离.
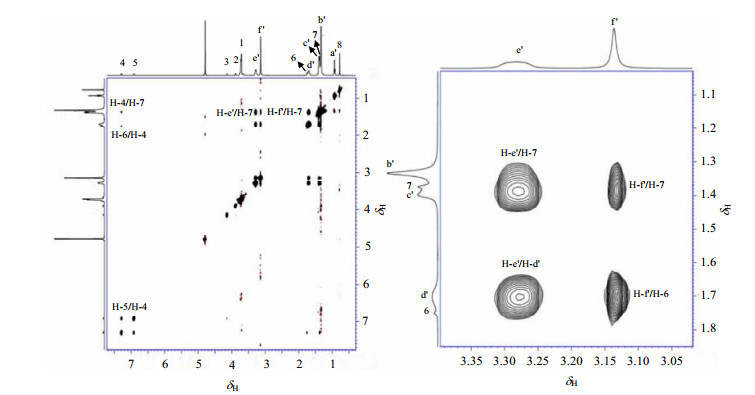
3个复配体系中,除了分子内质子的相互作用点外,均存在分子间质子的相互作用点,但作用点个数不同.在NP-10/DTAC混合体系中,NP-10与DTAC分子有1个相互作用点(H-b1/H-7);而在混合体系NP-10/C12-C4-C12中,有2个相互作用点(H-e/H-7、H-b/H-1);在NP-10/C12-C8-C12混合体系中,也有2个相互作用点(H-e′/H-7、H-f′/H-7),如图 3所示.
|
| 图 3 NP-10/C12-C8-C12摩尔比为1:2时的2D NOESY谱图及局部放大图 Fig. 3 Global and local amplified 2D NOESY spectra for NP-10/C12-C8-C12 mixed micelle at molar ratio of 1:2 |
这3个体系有一个共同作用点,就是与极头(甲基部位)相邻的亚甲基质子和NP-10分子间的相互作用.将该作用点的积分面积代入(4) 式计算得出,在混合摩尔比为1:1时,NP-10/DTAC、NP-10/C12-C4-C12和NP-10/C12-C8-C12的分子间距依次为0.309 nm、0.262 nm和0.246 nm,表明在该比例下它们的分子间相互作用强弱顺序为NP-10/C12-C8-C12 > NP-10/C12-C4-C12 > NP-10/DTAC.从表 3可以看出它们的分子间相互作用是随着两者混合比例的不同而动态变化的:NP-10/DTAC混合胶束随着总浓度的加大,分子间距离越来越小,混合胶束越来越紧凑,在比例为1:3时,质子间距离最小(达到0.250 nm),相互作用最大,协同效应最好,说明在混合体系NP-10/DTAC中1:3为相对理想的混合比例,之后分子间距离开始变大;在NP-10/C12-C4-C12和NP-10/C12-C8-C12混合胶束中,当复配摩尔比为1:2时,质子间距离达到最小值,此时这2个体系中的2个作用点距离分别为0.251 nm、0.314 nm和0.244 nm、0.296 nm,故1:2为NP-10/C12-C4-C12和NP-10/C12-C8-C12两体系相对理想的复配摩尔比.这一结果验证了前面由T2值和化学位移变化规律得到的结论;双链体系中相互作用点数更多说明了双链体系比单链体系协同效应更好的缘由.
| 相互作用位点 | NP-10:季胺盐 | ||||||
| 1:1/4 | 1:1/3 | 1:1/2 | 1:1 | 1:2 | 1:3 | 1:4 | |
| H-7(NP-10)/H-b1(DTAC) | 0.364 | 0.330 | 0.315 | 0.309 | 0.281 | 0.250 | 0.258 |
| H-7(NP-10)/H-e (C12-C4-C12) | 0.273 | 0.268 | 0.263 | 0.262 | 0.251 | 0.302 | 0.308 |
| H-1(NP-10)/H-b (C12-C4-C12) | 0.370 | 0.368 | 0.332 | 0.323 | 0.314 | 0.334 | 0.341 |
| H-7(NP-10)/H-e′(C12-C8-C12) | 0.271 | 0.262 | 0.247 | 0.246 | 0.244 | 0.323 | 0.331 |
| H-7(NP-10)/H-f′(C12-C8-C12) | 0.318 | 0.307 | 0.299 | 0.299 | 0.296 | 0.297 | 0.299 |
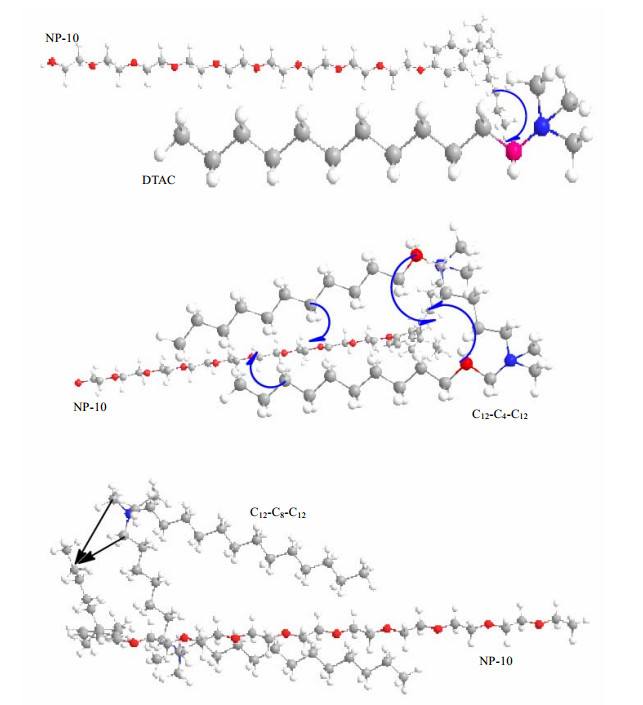
由以上结果除了得知在3种复配体系中,NP-10/C12-C8-C12和NP-10/C12-C4-C12复配体系分子间相互作用较NP-10/DTAC体系强外,根据分子间的相互作用点位置我们还可以推出3种混合胶束的可能的排列方式如图 4所示.
|
| 图 4 混合胶束的排列形状及相互作用点 Fig. 4 The relative arrangement of the three mixed micelles and the point of interaction |
通过各种NMR技术研究了NP-10与单链、双链氯化物季铵盐的3种复配体系,得到了有价值的变化规律:(1)1H NMR的化学位移变化规律得到2D NOESY实验的支持,NP-10/C12-C4-C12和NP-10/C12-C8-C12混合体系中δH的最大变化分别为22 Hz和23 Hz,这是因为双链表面活性剂比单链表面活性剂在混合体系里与NP-10的分子间相互作用协同作用更强;(2)T2在复配前后变化趋势相反,佐证了分子间发生了相互作用,但在NP-10/DTAC和NP-10/C12-Cs-C12的摩尔比分别为1:3和1:2时,T2变化又出现拐点反映出了分子间的相互作用力开始减小,分子内作用开始占主导地位,此时即使再增加DTAC和C12-Cs-C12(s=4, 8)的量,也不会增加分子间相互作用;(3)T2/T1≤0.5的质子个数在双链复配体系中更多,也说明双链比单链复配体系的胶束排列更加紧密,分子间作用更强,这也得到了2D NOESY结果的验证.3种复配体系的分子间相互作用强弱顺序为NP-10/C12-C8-C12 > NP-10/C12-C4-C12 > NP-10/DTAC;且双链复配体系比单链复配体系多一个分子间相互作用点;NP-10/DTAC中相对理想的复配摩尔比为1:3;NP-10/C12-C4-C12和NP-10/C12-C8-C12相对理想的复配摩尔比为1:2;从分子间相互作用点分析得到了它们空间的排列方式;自扩散系数显示NP-10对混合胶束的动力学半径影响大于氯化物季铵盐.
| [1] | TRAWINSKA A, HALLMANN E, MEDRZYCKA K. Synergistic effects in micellization and surface tension reduction in nonionic gemini S-10 and cationic RTAB surfactants mixtures[J]. Colloids and Surfaces A:Physicochem Eng Aspects, 2016, 488: 162-172 DOI:10.1016/j.colsurfa.2015.10.008 |
| [2] | SIDDIQUI H, KAMIL M, PANDA M, et al. Solubilization of phenanthrene and fluorene in equimolar binary mixtures of gemini/conventional surfactants[J]. Chinese J Chem Eng, 2014, 22(9): 1009-1015 DOI:10.1016/j.cjche.2014.06.028 |
| [3] | CARDOSO A M, MORAIS C M, CRUZ A R, et al. New serine-derived gemini surfactants as gene delivery systems[J]. Eur J Pharm Biopharm, 2015, 89: 347-356 DOI:10.1016/j.ejpb.2014.12.013 |
| [4] | HU Z Y, WANG L Q, GUO J F, et al. Interaction of a novel anionic gemini surfactant containing a triazine ring with cetyltrimethyl ammonium bromide in aqueous solution[J]. J Surfact Deterg, 2015, 18(1): 17-24 DOI:10.1007/s11743-014-1610-5 |
| [5] | LIU J, JIANG Y, CHEN H, et al. Probing dynamics and mechanism of exchange process of quaternary ammonium dimeric surfactants, 14-s-14, in the presence of conventional surfactants[J]. J Phys Chem B, 2012, 116(51): 14859-14868 DOI:10.1021/jp3082694 |
| [6] | JIANG Y, CHEN H, CUI X H, et al. 1H NMR study on pre-micellization of quaternary ammonium gemini surfactants[J]. Langmuir, 2008, 24(7): 3118-3121 DOI:10.1021/la703346p |
| [7] | JIANG Y, LU X Y, CHEN H, et al. NMR study of the dynamics of cationic gemini surfactant 14-2-14 in mixed solutions with conventional surfactants[J]. J Phys Chem B, 2009, 113(24): 8357-8361 DOI:10.1021/jp902419u |
| [8] | ZHANG J Z, XIE L, CHAI S G, et al. Interaction in binary mixtures of gemini surfactant G12-6-12 and CTAB by NMR[J]. Chinese J Chem Phys, 2014, 27(3): 307-314 DOI:10.1063/1674-0068/27/03/307-314 |
| [9] | XANG X Y, TANG X L, CHENG G Z, et al. Mixed micelles of sodium 4-decyl naphthalene sulfonate with Triton X-100 and sodium dodecyl sulfonate analyzed by 1H NMR[J]. J Colloid Interf Sci, 2004, 279(2): 533-538 DOI:10.1016/j.jcis.2004.06.091 |
| [10] | DEL BURGO P, JUNQUERA E, AICART E. Mixed micellization of a nonionic-cationic surfactant system constituted by n-octyl-β-Dglucopyranoside/dodecyltrimethylammonium bromide/H2O. An electrochemical, thermodynamic, and spectroscopic study[J]. Langmuir, 2004, 20(5): 1587-1596 DOI:10.1021/la035770d |
| [11] | YANG Q Q, ZHOU Q, SOMASUNDARAN P. Mixed micelles of octane-1, 8 bis (dodecyl dimethyl ammonium chloride) and n-dodecyl-β-maltoside by 1H NMR study[J]. Colloids and Surfaces A:Physicochem Eng Aspects, 2007, 305(1-3): 22-28 DOI:10.1016/j.colsurfa.2007.04.050 |
| [12] | YANG Q Q, ZHOU Q, SOMASUNDARAN P. NMR study of micellar microstructures of cationic single-chain and gemini surfactants and their mixtures with nonionic surfactant n-dodecyl-β-maltoside[J]. Colloids and Surfaces A:Physicochem Eng Aspects, 2008, 322(1-3): 40-46 DOI:10.1016/j.colsurfa.2008.02.026 |
| [13] | LIN J H, CHEN W S, HOU S S. NMR studies on effects of tetraalkyl ammonium bromides on micellization of sodium dodecylsulfate[J]. J Phys Chem B, 2013, 117(40): 12076-12085 DOI:10.1021/jp403616p |
| [14] | ARKHIPOV V P, IDIYATULLIN Z S, POTAPOVA E F, et al. Micelles and aggregates of oxyethylated isononylphenols and their extraction properties near cloud point[J]. J Phys Chem B, 2014, 118(20): 5480-5487 DOI:10.1021/jp502386e |
| [15] | RAUWEL G, LECLERCQ L, CRIQUELION J, et al. Aqueous mixtures of di-n-decyldimethylammonium chloride/polyoxyethylene alkyl ether:Dramatic influence of tail/tail and head/head interactions on co-micellization and biocidal activity[J]. J Colloid Interf Sci, 2012, 374(1): 176-186 DOI:10.1016/j.jcis.2012.02.006 |
| [16] | SONG Y Q. Low field magnetic resonance:Multi-dimensional experiments of relaxation and diffusion[J]. Chinese J Magn Reson, 2015, 32(2): 141-149 |
| [17] | PODO F, RAY A, NEMETHY G. Structure and hydration of nonionic detergent micelles. High resolution nuclear magnetic resonance study[J]. J Am Chem Soc, 1973, 95(19): 6164-6170 DOI:10.1021/ja00800a003 |
| [18] | YUAN H Z, DU Y R, ZHAO S, et al. Self-aggregation of surfactants in water solution by NMR[J]. Sci China Ser A, 1999, 42(3): 319-323 DOI:10.1007/BF02879067 |
| [19] | GAO H C, FANG X W, MAO S Z, et al. Conformation and dynamics of polyoxyethylene lauryl ether (Brij-35) chains in aqueous micellar solution studied by 2D NOESY and 1H NMR relaxation[J]. Sci China Ser B, 2002, 45(2): 143-150 DOI:10.1360/02yb9020 |
| [20] | YANG Q Q, ZHOU Q, SOMASUNDARAN P. 1H NMR study of micelles formed by mixture of nonionic n-dodecyl-β-D-maltoside and cationic gemini surfactants[J]. J Mol Liq, 2009, 146(3): 105-111 DOI:10.1016/j.molliq.2009.02.008 |
| [21] | LIU C D, ZHU G. Quadruplex nucleic acid structure determination by solution NMR[J]. Chinese J Magn Reson, 2015, 32(2): 150-162 |

本作品采用知识共享署名 4.0 国际许可协议进行许可。
 2017, Vol. 34
2017, Vol. 34



