文章信息
- 俞刚金, 刘君, 毛诗珍, 刘买利, 杜有如
- YU Gang-jin, LIU Jun, MAO Shi-zhen, LIU Mai-li, DU You-ru
- TX-100和CTAB交换动力学的核磁共振研究
- Exchange Kinetics of Surfactants TX-100 and CTAB Investigated by 1H NMR Spectroscopy
- 波谱学杂志, 2016, 33(3): 422-431
- Chinese Journal of Magnetic Resonance, 2016, 33(3): 422-431
- http://dx.doi.org/10.11938/cjmr20160307
-
文章历史
收稿日期: 2015-09-09
收修改稿日期: 2016-07-11


DOI:10.11938/cjmr20160307
2. 中国科学院大学, 北京 100049
2. University of Chinese Academy of Sciences, Beijing 100049, China
在溶液中,当表面活性剂的浓度超过其临界胶束浓度(CMC)时,表面活性剂分子会自发聚集形成胶束.胶束溶液处于动态平衡之中,胶束中的表面活性剂分子和溶液中的单体表面活性剂分子时刻发生着快速的交换.这个动态平衡涉及两个动力学弛豫过程[1-5]:一个是快弛豫过程,弛豫时间是τ1,一般在微秒(μs)量级,这个弛豫过程表征的是胶束中表面活性剂分子和溶液中表面活性剂分子发生快速交换的过程;另一个是慢弛豫过程,弛豫时间是τ2,一般在毫秒(ms)量级,这个弛豫过程表征的是胶束的缔合和分解过程.表面活性剂分子在溶液中的动力学过程直接影响胶束的寿命和稳定性,从而极大程度上影响着表面活性剂起泡、乳化、润湿、增溶和去污等功能[6, 7].
1965年,Mijnlief和Ditmarsc在Nature杂志上报道了用压力突降方法得到了表面活性剂十二烷基硫酸钠在水溶液中胶束的形成速率[8].随后,科学工作者们发展了很多其他方法来研究表面活性剂胶束动力学,如超声吸收法[9]、温度突降法[10]和停流法[11]等.相比于这些方法,核磁共振(NMR)方法的最大特点就是在不破坏体系的情况下,能够在分子甚至原子水平上直接获取溶液体系的动力学信息[12-17],因此NMR方法在研究表面活性剂溶液的动力学中具有独特的优势.
1999年,Huc和Oda[18]首次报道了一些阳离子型双子表面活性剂胶束态和单体态的交换过程在NMR时间尺度上为慢交换,并且试图计算其交换特征时间.之后,Cui等人[19]用NMR 1D线型分析方法定量测得了双子表面活性剂C14-s-C14·2Br的交换速率.Liu等人[20]用NMR 1D线型分析方法定量讨论了阳离子型双子表面活性剂C14-s-C14·2Br的交换速率受向溶液中加入传统表面活性剂的影响,认为非离子型、阳离子型和阴离子型传统表面活性剂分别加快、几乎不影响和减慢C14-s-C14·2Br的交换速率.目前,NMR 1D线型分析方法描述表面活性剂动力学性质主要集中在一些NMR时间尺度上慢交换的表面活性剂体系中,对于NMR时间尺度上快交换的表面活性剂体系鲜有报道.Jiang等人[21]通过NMR 1D线宽变化定性分析了TX-100/SDS混合体系与各自的胶束溶液交换速率的变化,认为SDS加快了TX-100胶束溶液的交换速率,而TX-100减慢了SDS胶束溶液的交换速率.对于传统的常规表面活性剂来说,表面活性剂分子在胶束和溶液中的交换为NMR时间尺度上的快交换,NMR 1D线型分析方法对表面活性剂在NMR时间尺度上快交换过程的研究还只是定性分析.本文通过NMR 1D线型分析方法,定量测定了表面活性剂胶束溶液在NMR时间尺度上快交换的平均停留时间,并消除了非交换以外其他因素的影响.
1 实验部分 1.1 仪器及试剂辛基苯基聚氧乙烯醚(TX-100,MW646.86)的NMR实验在BrukerAVANCE Ⅲ 600型NMR谱仪上完成,其质子的共振频率为600.13MHz,实验温度为298K;十六烷基三甲基溴化铵(CTAB,MW364.45,纯度为99%)的NMR实验在BrukerAVANCE Ⅲ 500型NMR谱仪上完成,其质子的共振频率为500.13MHz,实验温度为298K.所有的NMR谱均采用30°小角度激发代替传统的90°激发,以保证磁化矢量在每次采样前能够回到平衡态.
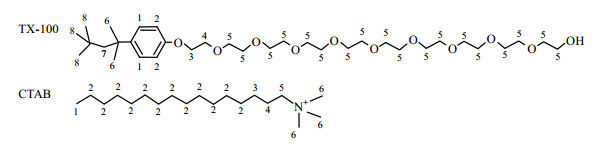
TX-100购买自Nacalai Tesque公司;CTAB购买自Acros公司;D2O(氘代率为99.9%)和TMS(氘代率为98%)购买自美国剑桥同位素实验室(CIL).所有试剂均直接使用,未进一步提纯.TX-100和CTAB的分子结构和质子编号如图 1所示.
|
| 图 1 TX-100和CTAB的分子结构和质子编号 Fig. 1 Molecular formulas and the proton numbering of surfactants TX-100 and CTAB |
样品溶于D2O,配置TX-100(2 mmol/L)和CTAB(5 mmol/L)的母液,逐步稀释母液,得到一系列浓度梯度的样品溶液,以TMS为外标.TX-100和CTAB的1H NMR谱宽分别是6 009.62 Hz和5 500.55 Hz,所有1H NMR谱的采样点数为32 k,累加次数为256,弛豫等待时间为2 s.
1.3 1D线型分析[12-14, 22, 23]1D线型分析方法最早是由Gutowsky等人[23]基于两点交换中磁化矢量Bloch方程得来.对于A、B两点的化学交换A↔B,磁化矢量M表示为:
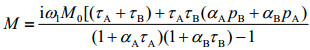 (1)
(1)
式中

ω1表示施加的射频场,M0是平衡时磁化矢量强度,pA和pB分别为A和B的分布分数,τA和τB分别为分子在A、B两点的停留时间,T2为A和B的横向弛豫时间(认为二者相等),Δω为A、B的平均共振频率与射频频率的偏置,δω表示无交换影响下A和B的共振频率的差值.该方程可以简单的表示为:
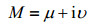 (2)
(2)
只有其虚部υ被作为吸收信号记录,
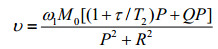 (3)
(3)
式中
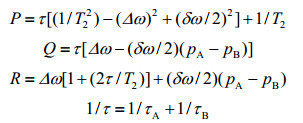
τ表示分子在A、B两点的平均停留时间.
当A、B两点交换为NMR尺度上的快交换,即τ < < δω时,A、B吸收峰融合为一个权重峰,其半峰宽为:
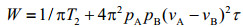 (4)
(4)
νA和νB分别表示A和B的共振频率.
对于表面活性剂溶液体系,在形成胶束后,A和B分别为单体态和胶束态表面活性剂分子,单体态和胶束态的横向弛豫时间存在着一定的差异,因此其半峰宽为:
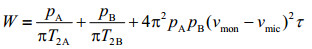 (5)
(5)
T2A和T2B分别为单体态和胶束态的横向弛豫时间,νmon和νmic分别为没有交换时单体态和胶束态的共振频率.
2 结果与讨论 2.1 不同温度下TX-100和CTAB的临界胶束浓度在稀溶液中,表面活性剂一部分在溶液表面吸附,另一部分以单体的形式存在于溶液中,当表面活性剂的浓度达到一定值时,表面活性剂在溶液内部缔合形成胶束,此时表面活性剂浓度称为临界胶束浓度.在胶束溶液中,单体和胶束中的表面活性剂分子处于不同的化学环境,二者之间存在着快速交换的动态平衡,当交换为NMR尺度上的快交换时,根据相分离模型[24],NMR图谱上观察到的化学位移(δobsd)为单体态和胶束态化学位移的加权平均:
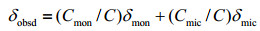 (6)
(6)
式中,δmon和δmic分别表示胶束溶液中单体态和胶束态表面活性剂分子的化学位移,C、Cmon和Cmic分别表示溶液中表面活性剂分子的浓度、单体态表面活性剂分子的浓度和胶束态表面活性剂分子的浓度.基于相分离模型,当表面活性剂分子浓度低于其CMC时,溶液中只有单体态的表面活性剂分子,表观化学位移保持不变,当表面活性剂分子的浓度高于其CMC时,Cmon=CMC,Cmic=C- Cmon得到:
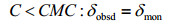 (7)
(7)
 (8)
(8)
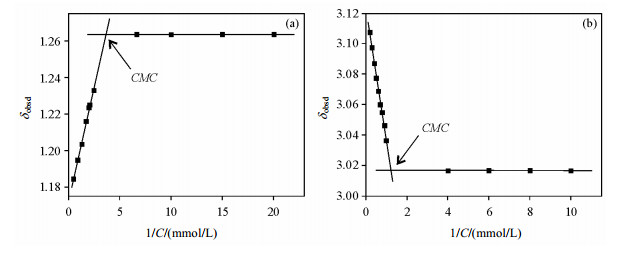
根据(7)式和(8)式,在表面活性剂浓度低于和高于CMC时,表观化学位移随表面活性剂浓度倒数的变化分别遵循两条直线,这两条直线的交点即为其CMC值,图 2为298K下,TX-100和CTAB表观共振频率(δobsd)随表面活性剂浓度的倒数(1/C)的拟合曲线.
|
| 图 2 298 K下,(a) TX-100和(b) CTAB的H-6的表观共振频率(δobsd)与表面活性剂浓度倒数(1/C)的拟合曲线 Fig. 2 The plots of observed resonance frequency (δobsd) as a function of reciprocal of the concentration (1/C) at 298 K. (a) H-6 proton of TX-100; (b) H-6 proton of CTAB |
TX-100和CTAB在不同温度下的CMC值列在表 1中,从表 1可以看出实验值和文献值比较吻合.微小差异一方面来自不同方法带来的系统误差,另一方面可能来自于溶剂D2O和H2O的差异[20].本文通过NMR方法获得的CMC值虽然有些在文献中已经报道,但不同的方法获得的CMC值有不同的系统误差,并且部分温度下的CMC值在文献中还没有报道.此结果一方面为相关研究提供参考数据;另一方面为准确配置该表面活性剂2倍CMC浓度和低于CMC浓度的样品,以用于平均停留时间的测定.
表面活性剂TX-100和CTAB为NMR时间尺度上的快交换体系,其胶束溶液的NMR谱融合为一套权重峰.在胶束溶液中,假设单体态和胶束态的表面活性剂分子之间的交换为准一级化学交换反应.当表面活性剂浓度远低于其CMC时,表面活性剂溶液不形成胶束,没有交换,线宽公式为:
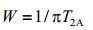 (9)
(9)
当表面活性剂浓度为2倍CMC时,表面活性剂溶液形成胶束,单体态和胶束态的表面活性剂分子的浓度相等,二者的分布分数都为1/2,即PA=PB=1/2,线宽公式为(5)式,有两部分组成,前面一部分为横向弛豫T2弛豫带来的本征线宽项,后一部分为因交换引起的交换展宽项.因此,通过(5)和(9)式就可以得到表面活性剂分子形成胶束后的线宽增宽:
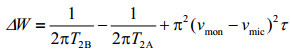 (10)
(10)
通过对单体态和胶束态横向弛豫时间的拟合,结果发现式(10)中,前两项相减后结果远小于交换展宽项,可以忽略,因此可以得到单体态和胶束态表面活性剂分子的交换展宽项:
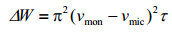 (11)
(11)
利用(11)式对表面活性剂浓度为2倍CMC和远低于CMC的1H NMR谱图的线型分析,可以测定表面活性剂分子浓度在2倍CMC的平均停留时间.TX-100分子的H-6和CTAB分子的H-6均与其分子内的质子无耦合作用(图 1),可以用来线型分析.1H NMR谱图中直接测量获得的TX-100的H-6和CTAB的H-6的半峰宽变化,表示为ΔWH6*,由于表面活性剂浓度为2倍CMC和远低于CMC的线宽变化,除了交换展宽项,还包含两个样品的粘度和场不均匀性的差异带来的变化.粘度和场不均匀性的差异对溶剂HDO有着相同的影响,这些差异引起的变化可以通过HDO半峰宽变化(ΔWHDO)来确定.因此表面活性剂质子半峰宽的变化(ΔWH6)可以通过扣除HDO半峰宽变化得到优化.
(11)式中,νmon为没有交换时,单体态表面活性剂分子H-6的共振频率,可以直接在表面活性剂浓度低于其CMC的1H NMR谱图中读出来.νmic为没有交换时,胶束态表面活性剂分子H-6的共振频率,可以通过νobsd与1/C拟合曲线的截距获得,截距表示表面活性剂浓度无限大时H-6的共振频率,此时可近似认为仅有胶束态质子.表 2列出了表面活性剂TX-100和CTAB不同温度下由ΔWH6*、ΔWHDO、ΔWH6、νmon和νmic以及通过1D线型分析方法计算的平均停留时间(τ).
交换过程的平均停留时间反映了表面活性剂分子进出胶束的快慢程度,平均停留时间越大,说明表面活性剂分子进出胶束越慢;反之,则越快.如表 2所示,表面活性剂TX-100和CTAB分子的平均停留时间随温度的增加逐渐减小,说明TX-100和CTAB分子进出胶束的速率随温度的增加逐渐加快.同一温度下,比较TX-100和CTAB的平均停留时间,TX-100的平均停留时间比CTAB的大,说明同一温度下TX-100进出胶束的速率比CTAB慢.
| Surfactants | T/K | ΔW H6 */Hz | ΔW HDO/Hz | ΔW H6/Hz | ν mon/Hz | ν mic/Hz | Δν a/Hz | τ/(10 -4s) |
| TX-100 | 278 | 10.72 | -0.08 | 10.80 | 511.6 | 472.5 | 39.1 | 7.14 |
| 283 | 10.15 | 0.03 | 10.12 | 543.2 | 502.3 | 40.9 | 6.12 | |
| 288 | 9.93 | 0.11 | 9.82 | 573.3 | 530.2 | 43.1 | 5.36 | |
| 293 | 9.41 | -0.04 | 9.45 | 603.3 | 558.4 | 44.9 | 4.75 | |
| 298 | 8.93 | 0.00 | 8.93 | 631.9 | 586.2 | 45.7 | 4.34 | |
| 303 | 8.26 | -0.07 | 8.33 | 659.6 | 612.0 | 47.5 | 3.74 | |
| CTAB | 288 | 6.06 | 0.39 | 5.67 | 1741.0 | 1810.1 | 69.1 | 1.20 |
| 293 | 4.06 | 0.40 | 3.66 | 1776.5 | 1843.2 | 66.7 | 0.83 | |
| 298 | 2.54 | 0.26 | 2.28 | 1810.4 | 1874.0 | 63.6 | 0.57 | |
| 303 | 1.43 | 0.40 | 1.03 | 1843.0 | 1904.0 | 61.0 | 0.28 | |
| 308 | 0.96 | 0.41 | 0.55 | 1873.7 | 1932.6 | 59.0 | 0.16 | |
| a Δν=|νmon -νmic| | ||||||||
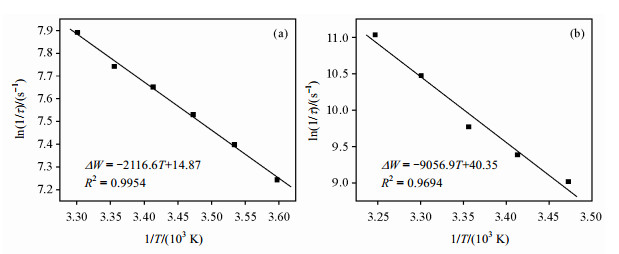
表面活性剂分子交换过程的表观交换活化能根据阿伦尼乌斯公式lnk=-Ea/(RT)+A0获得.Ln(1/τ)与1/T的拟合曲线如图 3所示,结果显示TX-100和CTAB拟合曲线均具有良好线性,它们的线性相关系数R2均大于0.96.
|
| 图 3 TX-100(a)和CTAB(b)的ln(1/τ)与1/T的拟合曲线 Fig. 3 The plots of ln(1/τ) as a function of 1/T. (a) TX-100, (b) CTAB |
计算得到其表观交换活化能,TX-100的表观交换活化能为17.6 kJ/mol,CTAB的表观交换活化能为75.3 kJ/mol.
交换过程活化能的大小在一定程度上反映了表面活性剂分子进出胶束的难易程度,而活化能的大小与表面活性剂分子形成胶束后疏水链的作用强弱密切相关.前面提到,交换过程平均停留时间的大小反映了表面活性剂分子进出胶束的快慢程度.对照各表面活性剂的活化能与它们的平均停留时间发现:TX-100的交换活化能比CTAB的交换活化能小,说明在胶束溶液中,TX-100分子进出胶束比CTAB更容易;但是同一温度下,TX-100的平均停留时间却比CTAB的平均停留时间长,即在胶束溶液中,TX-100分子进出胶束的速率比CTAB分子慢.这说明交换活化能并不是决定表面活性剂进出胶束快慢的唯一因素,还可能与其分子结构有关.
从结构上看(图 1),TX-100分子的疏水链有8个碳原子,且是支链,这8个碳原子的支链又不是直链,是椭圆形的,从而使TX-100分子聚集形成胶束时,排列不像直链那么紧密,整体表现出来的疏水作用比较弱,因此活化能较低.而CTAB分子的疏水链有16个碳原子,并且是直链,形成胶束时,疏水作用相对比较强,另外CTAB亲水头基带正电荷,受静电斥力的影响,因此在形成胶束的过程中,活化能较高.但是TX-100分子具有一个由9~10个氧乙基聚合而成的长的亲水链,整个分子的链长比CTAB长,进出胶束比较慢,并且形成胶束的时候TX-100的聚氧乙烯链可能会变得卷曲或弯曲,并沿着表面排列[27],这样进一步降低了TX-100分子进出胶束的速率,因此TX-100的平均停留时间比CTAB长.
3 结论本文应用1D NMR线型分析方法实现了对表面活性剂快交换体系平均停留时间的定量测量.实验测量了TX-100和CTAB胶束溶液中表面活性剂分子在不同温度下的平均停留时间,在计算过程中根据溶剂HDO线宽的变化,扣除了浓度和磁场不均匀性等非交换因素的对线宽的影响.通过变温实验,利用阿伦尼乌斯公式,拟合获得了TX-100和CTAB的表观交换活化能.对TX-100和CTAB交换速率和活化能进行分析得出交换速率和活化能与分子结构的关系:活化能反映的是疏水相互作用的大小;平均停留时间不仅受活化能的影响,还与分子结构分子链的长短相关.
| [1] | Shchekin A K, Rusanov A I, Kuni F M. Kinetic theory of molecular mechanism of micellar relaxation[J]. Chem Lett , 2012, 41 (10) : 1081-1083 DOI:10.1246/cl.2012.1081 |
| [2] | Grinin A P, Grebenkov D S. Study of relaxation in micellar solution by the numerical experiment[J]. Colloid , 2003, 65 (5) : 552-561 DOI:10.1023/A:1026111504241 |
| [3] | Aniansson E A G, Wall S N, Almgren M, et al. Theory of kinetics of micellar equilibria and quantitative interpretation of chemical relaxation studies of micellar solutions of ionic surfactants[J]. Phy Chem , 1976, 80 (9) : 905-922 DOI:10.1021/j100550a001 |
| [4] | Lang J, Zana R, Bauer R, et al. Chemical relaxation studies of micellar equilibria[J]. Phy Chem , 1975, 79 (3) : 276-283 DOI:10.1021/j100570a017 |
| [5] | Aniansso E, Wall S N. Kinetics of step-wise micelle association[J]. Phy Chem , 1974, 78 (10) : 1024-1030 DOI:10.1021/j100603a016 |
| [6] | Patist A, Kanicky J R, Shukla P K, et al. Importance of micellar kinetics in relation to technological processes[J]. Colloid Interface Sci , 2002, 245 (1) : 1-15 DOI:10.1006/jcis.2001.7955 |
| [7] | Patist A, Oh S G, Leung R, et al. Kinetics of micellization: Its significance to technological processes[J]. Colloids Surf A , 2001, 176 (1) : 3-16 DOI:10.1016/S0927-7757(00)00610-5 |
| [8] | Mijnlief P, Ditmarsc R. Rate of micelle formation of sodium alkyl sulphates in water[J]. Nature , 1965, 208 (5013) : 889-891 |
| [9] | Frindi M, Michels B, Zana R. Ultrasonic-absorption studies of surfactant exchange between micelles and the bulk phase in aqueous micellar solutions of amphoteric surfactants[J]. Phy Chem , 1994, 98 (26) : 6607-6611 DOI:10.1021/j100077a029 |
| [10] | Muller N. Kinetics of micelle dissociation by temperature-jump techniques-reinterpretation[J]. Phy Chem , 1972, 76 (21) : 3017-3020 DOI:10.1021/j100665a017 |
| [11] | Yasunaga T, Takeda K, Harada S. Kinetic study of sodium dodecyl sulfate micelle dissociation by a stopped-flow method[J]. Colloid Interface Sci , 1973, 42 (2) : 457-463 DOI:10.1016/0021-9797(73)90312-3 |
| [12] | Bain A D, Rex D M, Smith R N. Fitting dynamic NMR lineshapes[J]. Magn Reson Chem , 2001, 39 (3) : 122-126 DOI:10.1002/(ISSN)1097-458X |
| [13] | Rao B D N. Nuclear magnetic resonance line-shape analysis and determination of exchange rates[J]. Methods Enzymol , 1989, 176 : 279-311 DOI:10.1016/0076-6879(89)76016-X |
| [14] | Sergeev N M. Dynamic nuclear magnetic resonance[J]. Russ Chem Rev , 1973, 42 (5) : 769-798 |
| [15] | 李楠, 孙鹏, 刘买利, 等. 磷脂酰胆碱SUV的NMR研究[J]. 波谱学杂志 , 2014, 31 (4) : 572-578 Li Nan, Sun Peng, Liu Mai-li, et al. An NMR study of phosphatidylcholine small unilamellar vesicles[J]. Chinese J Magn Reson , 2014, 31 (4) : 572-578 |
| [16] | 李春发, 朱雪荣. 聚醚改性有机硅表面活性剂的核磁共振及红外光谱表征[J]. 波谱学杂志 , 2014, 31 (2) : 222-231 Li Chun-fa, Zhu Xue-rong. An NMR and FT-IR study on polyether modified silicon surfactant[J]. Chinese J Magn Reson , 2014, 31 (2) : 222-231 |
| [17] | 杨春升, 崔晓红, 蒋艳, 等. 表面活性剂SDS/TX-100混合体系的NMR研究[J]. 波谱学杂志 , 2009, 26 (4) : 466-475 Yang Chun-sheng, Cui Xiao-hong, Jiang Yan, et al. Mixed micelles of sodium dodecyl sulfate and triton X-100 in aqueous solution studied by 1H NMR[J]. Chinese J Magn Reson , 2009, 26 (4) : 466-475 |
| [18] | Huc I, Oda R. Gemini surfactants: Studying micellisation by 1H and 19F NMR spectroscopy[J]. Chem Commun , 1999, 20 : 2025-2026 |
| [19] | Cui X H, Yang X Y, Chen H, et al. NMR investigation of the exchange kinetics of quaternary ammonium dimeric surfactants C-14-s-C-14·2Br[J]. Phy Chem B , 2008, 112 (10) : 2874-2879 DOI:10.1021/jp710784p |
| [20] | Liu J, Jiang Y, Chen H, et al. Probing dynamics and mechanism of exchange process of quaternary ammonium dimeric surfactants, 14-s-14, in the presence of conventional surfactants[J]. Phy Chem B , 2012, 116 (51) : 14859-14868 DOI:10.1021/jp3082694 |
| [21] | Jiang Y, Chen H, Mao S Z, et al. Dynamics of mixed surfactants in aqueous solutions[J]. Phy Chem B , 2011, 115 (9) : 1968-1990 |
| [22] | Ramey K C, Louick D J, Whitehur P, et al. A Line width method for determining chemical exchange rates from NMR spectra[J]. Omr-Organic Magn Reson , 1971, 3 (2) : 201-216 DOI:10.1002/(ISSN)1097-458X |
| [23] | Gutowsky H S, Holm C H. Rate processes and nuclear magnetic resonance spectra.2. Hindered internal rotation of amides[J]. Chem Phy , 1956, 25 (6) : 1228-1234 |
| [24] | Shinoda K, Hutchinson E. Pseudo-phase separation model for thermodynamic calculations on micellar solutions[J]. Phy Chem , 1962, 66 (4) : 577-582 DOI:10.1021/j100810a001 |
| [25] | Zhang S H, Gao Y N, Dong B, et al. Interaction between the added long-chain ionic liquid 1-dodecyl-3-methylimidazolium tetrafluoroborate and triton X-100 in aqueous solutions[J]. Colloids Surf A , 2010, 372 (1-3) : 182-189 DOI:10.1016/j.colsurfa.2010.10.011 |
| [26] | Ali A, Uzair S, Malik N A, et al. Study of interaction between cationic surfactants and cresol red dye by electrical conductivity and spectroscopy methods[J]. Mol Liq , 2014, 196 : 395-403 DOI:10.1016/j.molliq.2014.04.013 |
| [27] | Yuan H Z, Cheng G Z, Zhao S, et al. Conformational dependence of triton X-100 on environment studied by 2D NOESY and 1H NMR relaxation[J]. Langmuir , 2000, 16 (7) : 3030-3035 DOI:10.1021/la990568p |
 2016, Vol. 33
2016, Vol. 33



