文章信息
- 王丽敏, 仇汝臣, 黄少华
- WANG Li-min, QIU Ru-chen, HUANG Shao-hua
- 复方乙酰水杨酸片中有效成分的DOSY技术分析
- Quantitative Analysis of Active Ingredients in Compound Acetylsalicylic Acid Tablets by DOSY
- 波谱学杂志, 2016, 33(3): 415-421
- Chinese Journal of Magnetic Resonance, 2016, 33(3): 415-421
- http://dx.doi.org/10.11938/cjmr20160306
-
文章历史
收稿日期: 2015-10-08
收修改稿日期: 2016-07-10


DOI:10.11938/cjmr20160306
2. 中国科学院 青岛生物能源与过程研究所, 山东省合成生物学省级重点实验室, 山东 青岛 266101
2. Shandong Provincial Key Laboratory of Synthetic Biology, Qingdao Institute of Bioenergy and Bioprocess Technology, Chinese Academy of Sciences, Qingdao 266101, China
复方乙酰水杨酸片是临床常用的解热镇痛药物,具有镇痛、解热及消炎等作用,其有效成分为阿司匹林、咖啡因和非那西丁(图 1所示).阿司匹林和非那西丁均具有解热镇痛作用;咖啡因则是一种中枢神经兴奋药,能使大脑皮层兴奋从而提高对外界的感应性,并具有收缩脑血管、加强前两种药物缓解头痛的效果[1].对于复方乙酰水杨酸片中有效成分的分析,中华人民共和国药典规定:用氯仿对复方乙酰水杨酸片进行提取分离,然后再用重氮化法分析测定三种有效成分[2].其它用于分析测定上述三种有效成分的方法有高效液相色谱法(HPLC)、胶束薄层色谱法及分光光度法等[3, 4].以上方法均存在操作繁琐、分析速度慢等不足.
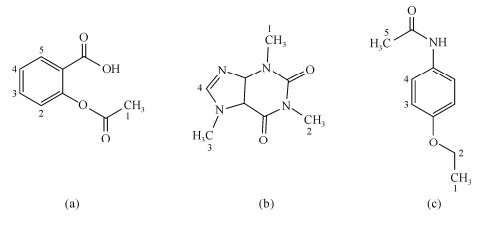
|
| 图 1 复方乙酰水杨酸片中有效成分的分子结构.(a)阿司匹林,(b)咖啡因,(c)非那西丁 Fig. 1 Molecular structures of the active ingredients of acetylsalicylic acid tablets. (a) aspirin, (b) caffeine, (c) phenacetin |
近年来,核磁共振(NMR)技术已越来越多地应用于化学、生物学及医学等领域中混合物的分析[5-9].在众多NMR技术中,二维扩散排序谱(DOSY)[10, 11]技术以其独特特点而成为国内外学者研究的热点.通过DOSY技术,可测得混合溶液中各组分分子的自扩散系数(D),依据自扩散系数的不同可实现不同组分NMR信号的分离.对自扩散系数相差不大的混合物的DOSY分析,则可以借助于虚拟固定相(VSP)来不同程度地改变各组分分子的自扩散系数,从而达到信号分离的目的[12-16].本实验室新发现的二甲基硅油(PDMS)是一种具有广泛适用性的VSP,它对烷烃、芳香烃、醇以及酸分析物等均具有较好的分离性能[17, 18].
本工作利用PDMS辅助的DOSY技术以及扩散排序-同核相关(DOSY-COSY)联用技术实现了复方乙酰水杨酸片中三种有效成分的快速定性分析,并进一步对其进行了相对定量分析.该研究结果为药物的质量评价提供了一个可借鉴参考的方法.
1 实验部分 1.1 仪器及试剂仪器:配有三共振反式超低温探头(TCI)的Bruker Avance Ⅲ 600型核磁NMR仪(瑞士Bruker公司);XS105D1型号电子分析天平(瑞士Mettler-toledo公司);KQ5200E型超声波清洗器(昆山市超声仪器有限公司).
试剂:复方乙酰水杨酸片购于山东新华制药股份有限公司,产品批号为1407232;PDMS购于国药集团化学试剂有限公司,产品批号为20150227,运动粘度(25℃)为(500±25)mm2/s;氘代氯仿(CDCl3)(纯度:99.8%,含0.03% v/v TMS)购于美国CIL公司.
1.2 样品制备取适量药品用研钵研碎,用电子分析天平称取13 mg置于离心管中,用移液枪移取0.6 mL CDCl3加入其中,混合均匀离心后,取上清液转移至NMR样品管中,用于DOSY实验;然后称取29.5 mg PDMS加入上述样品管中,再次混合均匀,用于DOSY实验.
1.3 NMR实验条件1HNMR的工作频率为600.13MHz,谱宽为6648.94 Hz.二维DOSY谱采用标准脉冲程序LEDBPGP2S采集.采样温度为298K,时域点数为4096,采样延迟时间为1.5s.扫描次数为8,空扫次数为4.梯度持续时间为1.6ms,线性梯度变化区间为2%~95%.三维DOSY-COSY谱图的采样参数与二维谱图相同.所有谱图均采用TopspinV3.1软件处理.
2 结果与讨论 2.1 1H NMR谱图分析由复方乙酰水杨酸片中的三种有效成分结构式可知:三者在1HNMR谱图(图 2)中的脂肪区和芳香区均会出现信号;且由于三者含量的不同,信号强度也会有所不同.阿司匹林在脂肪区只有一个单一信号(-CH3),而在芳香区会出现四组化学位移不同的信号(-Ph);咖啡因在脂肪区会有三个化学位移不同的单一的信号(-CH3),而在芳香区只有一个单一质子的信号峰(CH);非那西丁在脂肪区有一个单一质子的信号峰(-CH3)、一组三重峰信号(-CH2CH3)及一组四重峰信号(-CH2CH3),而在芳香区有两组化学位移不同的质子信号峰(-Ph).由于三种成分中不同质子的化学位移相差不大,在1HNMR谱图中,尤其在芳香区,出现了信号峰重叠的现象,因此只通过1HNMR谱图是很难对各成分质子进行归属.
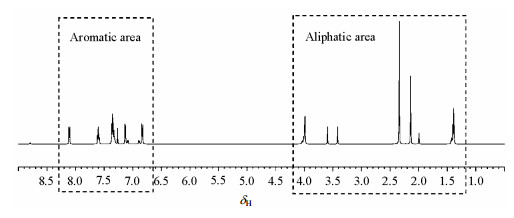
|
| 图 2 复方乙酰水杨酸片的1HNMR谱图(600 MHz) Fig. 2 1H NMR spectrum (600 MHz) of acetylsalicylic acid tablets |
在2D DOSY谱图中,横坐标表示化学位移,纵坐标表示自扩散系数,通过谱图可直观地得到各物质的D值,并且依据各组分的NMR信号分布可以进行结构定性.由于利用纯DOSY技术无法有效分离复方乙酰水杨酸片中的三种有效成分[图 3(a)],因此,本论文利用了PDMS辅助的DOSY技术[17, 18]对复方药物的NMR信号进行分离分析.结果发现,当溶液中加入PDMS后,复方乙酰水杨酸片中三种有效成分的D值均得到了不同程度的减小,从而实现了复方药物中有效成分NMR信号分离的目的[图 3(b)].依据谱图中各个组分的NMR信号分布以及相应的分子结构特征,可以推断图 3(b)中由上到下的组分依次为阿司匹林、咖啡因及非那西丁.
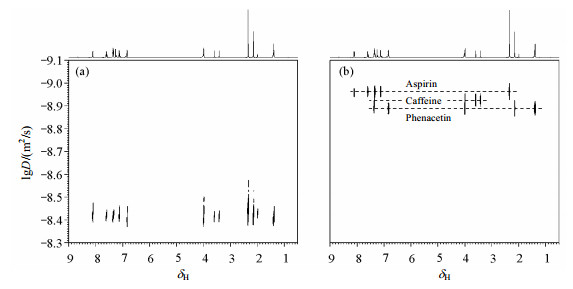
|
| 图 3 复方乙酰水杨酸片的2DDOSY谱(600MHz, CDCl3).(a)没有添加PDMS;(b)添加29.5mg PDMS. Fig. 3 3 2D DOSY spectra (600 MHz, CDCl3) of compound acetylsalicylic acid tablets before (a) and after (b) the addition of PDMS (29.5 mg) |
为进一步佐证2DDOSY 1H NMR谱图中三种组分的定性结果,本工作在上述实验基础上对复方乙酰水杨酸片进行了3DDOSY-COSY联用实验.通过每个组分信号的COSY谱图可精确推断出相应组分中不同质子之间的关联性(图 4),从而可最终准确确定复方药物中三种成分的分子结构.图 4左图为图 3(b)中自扩散系数最大的组分所对应的COSY谱图,由图中可以看出,对角峰的化学位移由左下到右上依次为δH7.37、6.83、4.00、2.14及1.39,并且该谱图中存在两组相关峰:δH4.00/δH1.39和δH7.37/δH6.83,说明此处所对应的组分应为非那西丁,且对角峰由左下到右上依次对应的质子分别为H-4、H-3、H-2、H-5及H-1.图 4右图为图 3(b)中自扩散系数最小的组分所对应的COSY谱图,同理,由图中可以看出,对角峰的化学位移由左下到右上依次为δH8.11、7.60、7.33、7.13及2.34,该谱图中存在三组相关峰:δH7.60/δH7.13、δH7.60/δH7.33和δH7.33/δH8.11,说明此处所对应的组分应为阿司匹林,且对角峰由左下到右上依次对应的质子为H-5、H-3、H-4、H-2及H-1.依据上述的分析结果,我们最终可以推断出,图 3(b)中自扩散系数处于中间的组分应为咖啡因.
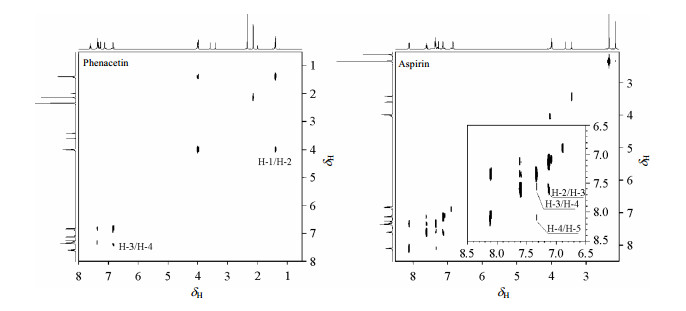
|
| 图 4 复方乙酰水杨酸片中有效成分的3DDOSY-COSY谱图的2DCOSY截面图(600MHz, CDCl3).左图:图 3(b)中自扩散系数最大的组分所对应的2DCOSY谱图;右图:图 3(b)中自扩散系数最小的组分所对应的2DCOSY谱图. Fig. 4 Fig. 4 Two-dimensional sectional view (600 MHz, CDCl3) of 3D DOSY-COSY of the active ingredients of compound acetylsalicylic acid tablets. 2D COSY spectra of the signals of component with the maximal (left) and minimum diffusion coefficient (right) in Fig. 3(b) |
由以上定性分析结果可知,1H NMR谱图中δ2.14、2.34以及3.42处的信号峰分别对应非那西丁中的H-5、阿司匹林中的H-1以及咖啡因中的H-2(图 1).对上述三处的信号峰分别进行三次积分并求平均值,可得出该批次复方乙酰水杨酸片中咖啡因、阿司匹林及非那西丁之间的摩尔比为1:8.0:4.6,根据质量与物质的量之间的换算关系,进而可计算出三者的质量比为:1:7.4:4.2.
3 结论本文利用PDMS辅助的DOSY技术对复方乙酰水杨酸片中有效成分的NMR信号进行了分离,结果发现,该技术能够有效地将复方乙酰水杨酸片中三种有效成分进行信号分离,并且利用3D DOSY-COSY联用技术,对各有效成分的结构进行了进一步确认,最后利用1H NMR技术对三种有效成分进行了相对定量分析.上述实验结果表明PDMS辅助的DOSY技术以及相应的DOSY-其它二维谱联用技术可为药物的质量评价提供一种新的可借鉴方法,该方法不仅能节省人力、物力,还具有简单、高效、快捷的优点.
| [1] | 沈蓉滨. 药物学[M]. 北京: 科学出版社, 2008 : 117 -121 Shen Rong-bin. Pharmacology[M]. Beijing: Science Press, 2008 : 117 -121 |
| [2] | 国家药典委员会. 中华人民共和国药典[M]. 北京: 化学工业出版社, 1997 : 386 China Pharmacopoeia Committee. Pharmacopoeia of the people's republic[M]. Beijing: Chemical Industry Press, 1997 : 386 |
| [3] | 王腾, 王晓敏, 张亚运, 等. 高效液相色谱法同时测定复方乙酰水杨酸片中各有效成分的含量[J]. 北京石油化工学院学报 , 2012, 20 (1) : 41-44 Wang Teng, Wang Xiao-min, Zhang Ya-yun, et al. Simultaneous determination of three components in compound aspirin tablets by HPLC[J]. Journal of Beijing Institute of Petro-chemical Technology , 2012, 20 (1) : 41-44 |
| [4] | 赵怀清, 王学娅, 杨丽, 等. 胶束薄层色谱法同时测定APC片中3组分含量[J]. 沈阳药科大学学报 , 2001, 18 (5) : 338-340 Zhao Huai-qing, Wang Xue-ya, Yang Li, et al. Simultaneous determination of the contents of the three components in the APC by micellar thin layer chromatography[J]. Journal of Shenyang Pharmaceutical University , 2001, 18 (5) : 338-340 |
| [5] | 孙增先, 张骞峰, 周金玉. 双波长比值光谱法测定复方乙酰水杨酸片中三组分含量[J]. 光谱学与光谱分析 , 2004, 24 (7) : 883-886 Sun Zeng-xian, Zhang Qian-feng, Zhou Jin-yu. Determination of three components in compound acetylsalicylic acid tablet by dual-wavelength ratio spectrometry[J]. Spectros Spect Anal , 2004, 24 (7) : 883-886 |
| [6] | 周秋菊, 向俊峰, 唐亚林. 核磁共振波谱在药物发现中的应用[J]. 波谱学杂志 , 2010, 27 (1) : 68-79 Zhou Qiu-ju, Xiang Jun-feng, Tang Ya-lin. Applications of nuclear magnetic resonance spectroscopy in drug discovery[J]. Chinese J Magn Reson , 2010, 27 (1) : 68-79 |
| [7] | Balayssac S, Trefi S, Gilard V, et al. 2D and 3D DOSY 1H NMR, a useful tool for analysis of complex mixtures: application to herbal drugs or dietary supplements for erectile dysfunction[J]. Pharm Biomed Anal , 2009, 50 (4) : 602-612 DOI:10.1016/j.jpba.2008.10.034 |
| [8] | Trefi S, Routaboul C, Hamieh S. Analysis of illegally manufactured formulations of tadalafil (Cialis) by 1H NMR, 2D DOSY 1H NMR and Raman spectroscopy[J]. Pharm Biomed Anal , 2008, 47 (1) : 103-113 DOI:10.1016/j.jpba.2007.12.033 |
| [9] | 李爽, 冯秀燕. NMR方法在煤炭分析中的应用进展[J]. 波谱学杂志 , 2013, 30 (1) : 148-155 Li Shuang, Feng Xiu-yan. A mini review on NMR approaches for coal analysis[J]. Chinese J Magn Reson , 2013, 30 (1) : 148-155 |
| [10] | Johnson C S. Diffusion ordered nuclear magnetic resonance spectroscopy: Principles and applications progress in nuclear magnetic resonance[J]. Prog Nucl Magn Reson Spectrosc , 1999, 34 (3, 4) : 203-256 |
| [11] | Cohen Y, Avram L, Frish L. Diffusion NMR spectroscopy in supramolecular and combinatorial chemistry: an old parameter—new insights[J]. Angew Chem Int Edit , 2005, 44 (4) : 520-554 DOI:10.1002/(ISSN)1521-3773 |
| [12] | Ito F, Hirabayashi S. Infrared spectra of the CF3I dimer: a concurrent application of matrix-isolation spectroscopy and cavity ring-down spectroscopy[J]. J Chem Phys , 2006, 124 (23) : 234509 DOI:10.1063/1.2206784 |
| [13] | Tormena C F, Evans R, Haiber S, et al. Matrix-assisted diffusion-ordered spectroscopy: mixture resolution by NMR using SDS micelles[J]. Magn Reson Chem , 2010, 48 (7) : 550-553 DOI:10.1002/mrc.v48:7 |
| [14] | Tormena C F, Evans R, Haiber S, et al. Matrix-assisted diffusion-ordered spectroscopy: application of surfactant solutions to the resolution of isomer spectra[J]. Magn Reson Chem , 2012, 50 (6) : 458-465 DOI:10.1002/mrc.v50.6 |
| [15] | Evans R, Haiber S, Nilsson M, et al. Isomer resolution by micelle-assisted diffusion-ordered spectroscopy[J]. Anal Chem , 2009, 81 (11) : 4548-4550 DOI:10.1021/ac9005777 |
| [16] | Chaudhari S R, Suryaprakash N. Diffusion ordered spectroscopy for resolution of double bonded cis, trans-isomers[J]. J Mol Struct , 2012, 1017 (23) : 106-108 |
| [17] | 吴瑞, 柏正武, 杨盈, 等. 基于PDMS的NMR中色谱技术的分离性能研究[J]. 波谱学杂志 , 2015, 27 (1) : 68-79 Wu Rui, Bai Zheng-wu, Yang Ying, et al. Study of the separation performance of PDMS matrixed chromatographic NMR technique[J]. Chinese J Magn Reson , 2015, 27 (1) : 68-79 |
| [18] | Huang S H, Gao J, Wu R, et al. Polydimethylsiloxane: a general matrix for high-performance chromatographic NMR spectroscopy[J]. Angew Chem Int Edit , 2014, 53 (43) : 11592-11595 DOI:10.1002/anie.201406967 |
 2016, Vol. 33
2016, Vol. 33



