文章信息
- 朱庆英, 何佩芝
- ZHU Qing-ying, HE Pei-zhi
- D-樟脑与β-环糊精包合物的结构表征
- Structural Elucidation of D-Camphor and β-Cyclodextrin Inclusion Complex
- 波谱学杂志, 2015, 32(1): 87-94
- Chinese Journal of Magnetic Resonance, 2015, 32(1): 87-94
- http://dx.doi.org/10.11938/cjmr20150110
-
文章历史
收稿日期: 2014-06-26
收修改稿日期: 2015-01-08


DOI:10.11938/cjmr20150110
樟脑是从植物樟树里提取挥发油,再经分离得到的一种饱和环状酮,分子式为C10H16O,化学名称为1, 7, 7-三甲基二环[2.2.1]庚烷-2-酮.天然樟脑是右旋体(D-樟脑),合成樟脑是消旋体.D-樟脑具有消炎、镇痛、兴奋、强心、止咳、驱蚊、抑菌等作用[1, 2],含樟脑的复方制剂[3, 4]在药物等领域得到广泛应用.但由于樟脑不溶于水,挥发性较强,采用β-环糊精(β-CD)包结后,保存D-樟脑在药物制剂中的有效浓度,提高其稳定性[5],并起到良好的控制释放.
β-CD是一种特殊的“内疏水,外亲水”的圆锥状空腔结构,由7个D-吡喃葡萄糖单元通过α-1, 4-糖苷键连接而成的环状低聚糖,根据其空间大小,可通过分子间非共价键力[6, 7](如疏水作用力,氢键和范德华力等)与不同客体分子形成稳定的主客体包合物.本实验利用NMR技术分析包合物结构,能够确定D-樟脑与用β-CD主客体之间的化学计量关系,通过ROESY[8, 9]考察主客体分子之间的空间结构信息,为该样品的生产实践应用提供了理论依据.
1 实验部分 1.1 仪器与试剂D/Max-IIIA型X射线衍射仪(日本理学电机);AvanceIII型核磁共振谱仪(Bruker公司);TENSOR37型傅立叶变换红外光谱仪(Bruker公司);β-CD(纯度99%以上,上海伯奥生物科技有限公司);D-樟脑(分析纯,阿拉丁公司).
1.2 包合物的制备与XRD和FTIR分析按照文献[10]方法制备D-樟脑与β-CD不同物质的量配比的包结物,对β-CD及最佳物质的量比的包合物进行X-射线粉末衍射(XRD)和红外光谱(FTIR)分析.XRD技术是判断是否生成固体包合物的有用方法,该方法简单,样品可以回收,对结果的分析比较直观.XRD分析条件:Cu耙,管电压36 kV、管电流40 mA、扫描范围5°~60°、步宽0.04°,扫描速率4°/min.
FTIR最突出的优点是可以表征包合物固相状态下包合物的结构,弥补其他光谱的不足.β-CD与客体分子形成包合物后,从包合物,客体分子,β-CD在峰形、峰位和强度的变化能够提供客体分子是否进入空腔及相互作用力性质的证据.FTIR测试(KBr压片法),扫描范围400~4 000 cm-1.
1.3 β-CD/D-樟脑包合物的1H NMR分析核磁共振(NMR)对于CD包合物结构的几何学,客体在空腔内的方位研究是一个重要手段.当客体分子进入β-CD空腔后,其空腔内氢原子(H-3,H-5)的周围环境发生改变,也会引起NMR参数变化.测试条件:样品溶于D2O,以TMS为内标,1H NMR的工作频率为400.13 MHz,谱宽为8 223.685 Hz.
1.4 β-CD/D-樟脑包合物的1H ROESY NMR分析测试条件:样品溶于D2O,以TMS为内标,1H ROESY NMR谱宽均为6 009.615 Hz,采样数据点阵t2×t1=2 048×256.
1.5 β-CD/D-樟脑包合物的量子化学计算研究所有量子化学计算均采用Gaussian 03程序包[11],在PM3,B3LYP/6-31G(d)和ONIOM(B3LYP/6-31G(d): PM3)水平上进行.β-CD初始结构来源于文献报道[12],β-CD与客体分子形成包结络合物的坐标体系,根据参考文献报道建立[13].β-CD母体葡萄糖苷键中氧原子所在平面定为XY平面,其中心定为坐标原点,C-6羟基指向Z轴的正方向,C-2和C-3羟基指向Z轴的负方向.在该坐标体系中,客体分子D-樟脑借助3个虚拟原子进行定位,一个虚拟原子位于Z轴上,两个位于XY平面上,同时客体分子定义为标记原子.客体分子与β-CD的相对位置由客体分子中的标记原子与3个虚拟原子之间的距离、角度和二面角来确定.为计算方便,这里将D-樟脑C-1原子定义为标记原子.先用PM3方法对包合物模型进行计算,得到能量最低的稳定包结物,然后在两层杂化方法ONIOM(B3LYP/6-31G(d): PM3)(PM3计算β-CD,B3LYP/6-31G计算客体D-樟脑)水平上进行再优化.包结物的结合能(BE)为: BE=Ecomplex-Eguest-Ehost;式中Ecomplex为包结物的总能量,Eguest为底物分子的总能量,Ehost为β-CD的总能量.
2 结果与讨论 2.1 β-CD与客体分子D-樟脑包合的化学计量比通过1H NMR实验可以确认D-樟脑与β-CD发生包合,从图 1中可以发现,逐渐提高D-樟脑/β-环糊精的包合摩尔比,β-环糊精的H-3和H-5(位于CD空腔内氢)发生明显的化学位移,说明D-樟脑与β-CD发生包合,因为H-3和H-5是构成β-CD空腔的内壁原子,当客体分子D-樟脑进入空腔后,由于二者之间的分子间相互作用力,氢键的形成,使得β-CD的H-3和H-5发生高场移动.[D-樟脑]/[β-CD]的比例从1.0提高到1.2时,H-3的化学位移几乎保持不变,因此β-CD和D-樟脑包合物的主客体化学计量比为1:1.
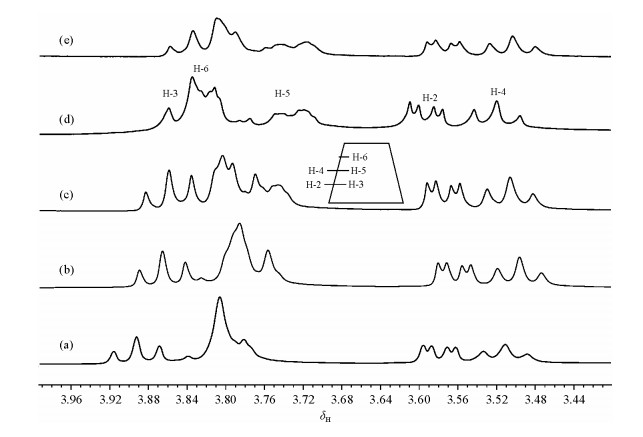
|
| 图 1 D-樟脑/β-CD包合物的部分1H NMR图.[D-樟脑]/[β-CD]的比例:(a) 0, (b) 0.5, (c) 0.7, (d) 1.0, (e) 1.2 Fig. 1 Partial 1H NMR spectra of solutions of D-camphor /β-CD complex. [D-camphor]/[β-CD] ratios: (a) 0, (b) 0.5, (c) 0.7, (d) 1.0, (e) 1.2 |
图 2为β-CD粉末、β-CD/D-樟脑包合物的XRD谱图,由图可知,β-CD包合物的晶型结构与初始β-CD粉末的晶型结构相差很大,由此说明加入D-樟脑后,β-CD发生聚集,并生成了物相不同聚集体.β-CD在12.6°处具有最强的衍射峰,然而,在包合物中,由于晶格间距的增大,该峰往更低的2q值移动到11.3°.此外,β-CD在9.0°和18.8°处的峰消失,β-CD包合物在9.2°,17.6°出现新的衍射峰.这些结果说明在固态下β-CD与客体分子D-樟脑产生了分子间弱相互作用力,从而导致粉末晶型的变化.

|
| 图 2 包合物的XRD谱图:(a) β-CD, (b) β-CD/D-樟脑包合物 Fig. 2 Power X-ray diffractograms of: (a) β-CD, (b)β-CD/ D-camphor inclusion complex |
对β-CD及其包合物进行FTIR分析.从图 3中可以看出,β-CD (a),β-CD/D-樟脑包合物(b),β-CD/D-樟脑混合物(d)的FTIR图结构相似,说明β-CD的骨架结构没有发生变化.但β-CD的-OH伸缩振动峰由3 407 cm-1蓝移到了3 383 cm-1 (b),可以说明β-CD环境发生了变化引起-OH伸缩振动峰的位移.D-樟脑的IR谱图(c)中3 471 cm-1处归属于D-樟脑羰基C=O伸缩振动的倍频峰;2 964 cm-1处归属于D-樟脑中甲基C-H的伸缩振动,2 872 cm-1处归属于D-樟脑亚甲基的C-H伸缩振动,这3个峰在β-CD/D-樟脑包合物(b)上消失,与包合物的形成有关,对比β-CD/D-樟脑混合物(d),这些峰仍存在.同时因为β-CD本身的特征吸收频率覆盖了400~3 800 cm-1区域,当客体小分子在包结物中所占的分量小于25% w/w时,其特征峰很容易被CDs的吸收峰掩盖.在曲线(b)上看到1 743 cm-1峰(D-樟脑羰基C=O伸缩振动峰)的减弱,极有可能是羰基与β-CD的羟基间形成氢键所致.

|
| 图 3 β-CD (a),β-CD/D-樟脑包合物(b),D-樟脑(c),β-CD/D-樟脑混合物(d)的FTIR图 Fig. 3 The FTIR spectra of β-CD (a), β-CD/ D-camphor inclusion complex (b), D-camphor (c), β-CD/ D-camphor mixture (d) |
β-CD/D-樟脑包结物的1H ROESY NMR如图 4所示,D-樟脑环己酮基上的H原子(d位,e位,f位,g位和h位)与β-CD空腔中的H-3和H-5具有明显的交叉峰,相互作用明显,而与β-CD空腔外氢(H-2和H-4)作用不明显,进一步证明包结络合物的形成.另外D-樟脑上3个甲基基团都不仅与β-CD空腔内氢(H-3和H-5)有明显的交叉峰,与β-CD空腔外氢(H-2和H-4)作用也存在,但相对较弱.说明包合物结构型式中,D-樟脑的二环[2.2.1]-2-庚酮位于β-CD空腔内的形式为主,其三甲基部分位于β-CD空腔外.
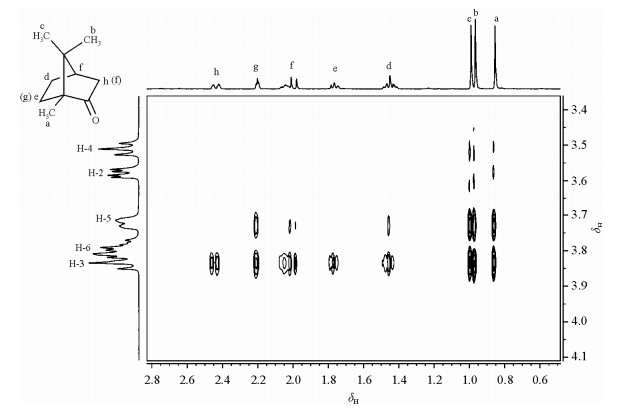
|
| 图 4 β-CD/D-樟脑(1:1摩尔比)包合物的2D ROESY图 Fig. 4 2D ROESY spectrum of the inclusion complex of D-camphor and β-cyclodextrin (1:1) in D2O at 20 ℃ |
通过量子化学计算β-CD与D-樟脑结合能,结合能越负,包结物越稳定.最稳定的包结物在ONIOM (B3LYP/6-31G(d): PM3)水平上优化得到的几何构型,如图 5所示,其最低的结合能为-76.95 kJ/mol,结合能为负值,说明二者的包结过程是自发的.从状态图中看出甲基部分处于β-CD空腔外[图 5(a)],与之前的分析结果是一致的;从图 5(b)和表 1中,可以观察到D-樟脑上H原子与β-CD空腔内H原子,形成的氢键数目和键长.原子序号信息见图 5(c),构成β-CD的7个糖苷单元分别以数字序号I~VII表示,每个糖苷单元中的不同位置的C,H,O原子分别被定义为C-1~C-6,H-1~H-6和O-2~O-6.表 1的结果表明,底物分子D-樟脑与β-CD之间的氢键是形成稳定包合物的主要作用力,影响包结过程结合能的大小.

|
| 图 5 ONIOM(B3LYP/6-31G(d): PM3)水平上优化的最稳定β-CD/D-樟脑包合物空间构型. (a)侧视图;(b)俯视图(氢键的成键位置);(c) D-樟脑原子序号 Fig. 5 Geometrical structures of the most stable inclusion complexes of β-CD/D-camphor optimized by ONIOM (B3LYP/6-31G(d): PM3) method (a) side view, (b) vertical view (the position of formed hydrogen bond), (c) molecular number of D-camphor |
| Number | Type | Bond length/(10-1 nm) | Bond angle/° |
| 1 | O-9…H-5~C-5(VII) | 1.8778 | 158.6 |
| 2 | C-10~H-23…O-6(IV) | 2.7311 | 109.8 |
综上所述,XRD和FTIR证实D-樟脑与β-CD存在着分子间的相互作用力,1H NMR实验表明D-樟脑和β-CD包合物的包合化学计量比为1:1.β-CD/D-樟脑包结物的1H ROESY NMR结果进一步揭示了D-樟脑与β-CD的结合位点,说明D-樟脑的二环[2.2.1]-2-庚酮位于β-CD空腔内,其三甲基部分位于β-CD空腔外.通过量子化学的B3LYP/6-31G(d): PM3水平优化计算得到的最优结构,表明形成β-CD/D-樟脑包合物的作用力主要是氢键.
| [1] | Xiong Ying(熊颖), Wu Xue-ru(吴雪茹), Tu Xing-ming(涂兴明) et al . Progress in pharmaceutical camphor(樟脑的药学研究进展)[J]. Lab Med Clin(检验医学与临床) , 2009, 6 (12) : 999-1001 |
| [2] | Xu H, Blair N T, Clapham D E . Camphor activates and str ongly desensitizes the transient receptor potential vanilloid subtype 1 channel in a vanilloid-independent mechanism[J]. J Neurosci , 2005, 25 (39) : 8924-8928 DOI:10.1523/JNEUROSCI.2574-05.2005 |
| [3] | Liu Peng(刘朋), Nie Hong-mei(聂红梅), Xiong Wei-zheng(熊维政) et al . Assay method of compound camphor cream(复方樟脑乳膏含量测试方法研究)[J]. China Journal of Chinese Medicine(中医学报) , 2014, 29 (188) : 71-75 |
| [4] | Huang Shao-hua(黄少华), Bai Zheng-wu(柏正武), Feng Ji-wen(冯继文) et al . Enantiomeric discrimination of D/ L-10-camphoric sulfonicAcid by β-cyclodextrins studied by NMR spectroscopy(β-环糊精手性识别D/L-樟脑磺酸的NMR研究)[J]. Chinese J Magn Reson(波谱学杂志) , 2009, 26 (4) : 457-465 |
| [5] | Qin Dong-yan(秦冬彦), Song Hong-tao(宋洪涛), Guo Tao(郭涛) et al . Studies on the stability of borneol-β-cyclodextrin inclusion complex(冰片-β-环糊精包合物的稳定性考察)[J]. Chinese Traditional and Herbal Drugs(中草药) , 2000, 31 (4) : 255-257 |
| [6] | Szejtli J . Introduction and general overview of cyclodextrin chemistry[J]. Chem Rev , 1998, 98 : 1743-1753 DOI:10.1021/cr970022c |
| [7] | Liu L, Guo Q X . Novel prediction for the driving force and guest orientation in the complexation of α and β-cyclodextrin with benzene derivatives[J]. J Phys Chem B , 1999, 103 : 3 461-3 467 DOI:10.1021/jp984545f |
| [8] | Schneider H J, Hacket F . NMR studies of cyclodextrins and cyclodextrin complexes[J]. Chem Rev , 1998, 98 : 1755-1785 DOI:10.1021/cr970019t |
| [9] | Zhao Bing(赵兵), Li Yi-lei(李艺蕾), Li Ming(李明) et al . An NMR study of capsaicin /β-cyclodextrin complex(辣椒碱与β-环糊精包合物的核磁共振研究)[J]. Chinese J Magn Reson(波谱学杂志) , 2013, 30 (4) : 576-584 |
| [10] | Li Jun-fen(李俊芬), Xu Zhi-cheng(许志成), Dong Chuan(董川) . Preparation and spectroscopic study on the inclusion complexes of cryptotanshinone with β-CD(隐丹参酮与环糊精包结物的制备与光谱研究)[J]. Journal of Analytical Science(分析科学学报) , 2004, 20 (3) : 229-232 |
| [11] | Frisch M J, Trucks G W, Schlegel H B, et al. Gaussian 03, Revision D.01, Gaussian, Inc[CP], Wallingford, CT, 2004. |
| [12] | Betzel C, Saenger W, Hingerty B E et al . Circular and flip-flop hydrogen bonding in. β-cyclodextrin undecahydrate: a neutron diffraction study[J]. J Am Chem Soc , 1984, 106 (24) : 7545-7557 DOI:10.1021/ja00336a039 |
| [13] | Yan C, Xiu Z, Li X et al . Theoretical study for quercetin/β-cyclodextrin complexes: quantum chemical calculations based on the PM3 and ONIOM2 method[J]. J Incl Phenom Macro Chem , 2007, 58 (3-4) : 337-344 DOI:10.1007/s10847-006-9280-1 |
 2015, Vol. 32
2015, Vol. 32



