随着核技术的发展,放射性废水造成的污染严重影响了人类健康,近年来已有大量相关研究(Das,2012;贾麟等,2015;Kim et al., 2016)。由于放射性核素物理化学性质复杂,污水厂的常规处理工艺很难对其去除(Reddad et al., 2002)。吸附是放射性污染水体处理中一种应用较多、较为成熟、行之有效的方法(Sheng et al., 2016)。目前最常用的吸附剂是活性炭、膨润土和沸石等,但由于成本较高,难以得到广泛应用(Kadirvelu and Namasivayam, 2003)。而凹土具有成本低(其价格仅为活性炭的1/10)、吸附效果好、再生简单等优点(Yang et al., 2016)。但受原状凹土固液难以分离的制约,如何应用于实际工程中仍需探索。
凹土对Pb、Cd、Cu、Zn、Mn等多种重金属具有良好的吸附作用。Chen和Wang(2007)开展了凹土吸附Pb2+的研究,其结果表明单位最大吸附量为104.28 mg/g;Álvarez-Ayuso和García-Sánchez(2003, 2007)研究了凹土对Pb、Cu、Zn、Cd等重金属污染的土壤的吸附作用,认为具有良好去除效果,且对于溶液中Cd2+的去除率可达85%;不同酸改条件下,凹土对Cu2+的去除率达93.85%(龚安华和孙岳玲,2013),对Cd2+的最佳去除率达到92.6%(叶鸣等,2013),吸附污水中P时,去除率可达95.0%(Gan et al., 2010);十六烷基三甲基溴化铵有机改性凹土,吸附Ni2+、Cr6+和Cu2+,去除率均在80%以上(杨佳静,2015)。Sr和Cs是放射性废物中典型组分,对其处置研究是当前的热点问题(Leboda et al., 2001;Sureda et al., 2010;Rahman et al., 2011)。王哲等(2015)进行了凹土吸附Sr和Cs的相关实验,其结果表明凹土能够有效去除溶液中的Sr和Cs,且对Cs的吸附效果优于Sr;Kaygun等(2017)的研究结果是天然粉状凹土对Sr和Cs的去除率可达65.0%和80.0%。可见,凹土在放射性污染水体处理中具有广阔的应用前景。
由于粉状凹土在吸附之后难以实现固液分离,不能应用到实际工程中,因此,研究凹土造粒后对核素的吸附作用对于将凹土应用于实际处置工程具有重要的意义。本文选用酸处理改性凹土,研究其对Sr和Cs的吸附性能的影响,同时开展了海藻酸钠-酸改性凹土造粒对溶液中核素Sr和Cs的吸附研究,以期为凹土在核素污染水体处理中的实际应用提供参考。
1 实验材料与方法 1.1 试剂与仪器实验所用试剂包括六偏磷酸钠[(NaPO3)6]、盐酸(HCl)、海藻酸钠、氯化锶、氯化铯,以上药品均为分析纯,购自(国药集团化学试剂有限公司);凹土购自江苏盱眙鑫磊矿物有限公司。
实验用仪器包括磁力搅拌器(90-2,上海振荣科学仪器有限公司)、离心机(Biofuge primo R,上海安亭科学仪器厂)、鼓风干燥箱(DHG-9 123 A,Thermo Sorvall)、恒温振荡器(ZHWY-100D/103D,上海智诚分析仪器有限公司)、pH计(PHS-3C,上海精科仪器有限公司)、蠕动泵(BT-100,上海沪西分析仪器厂)。
1.2 实验方法(1) 凹土的纯化:处理方法参见郭娜等(2015)。
(2) 凹土的改性:向5.0 g纯化凹土中加入10 mL 1 mol/L盐酸,使盐酸与凹土混合均匀,干燥过筛备用,制得酸改性凹土。
(3) 凹土吸附剂颗粒的制备:称取10.0 g酸改性凹土,加入质量分数为3%的海藻酸钠溶液中,室温下磁力搅拌2 h,滴入CaCl2溶液中,海藻酸钠遇CaCl2溶液凝结形成凝胶球,于4 ℃下静置12 h,确保其充分交联,过滤后置于鼓风干燥箱,105 ℃下干燥2 h,制得海藻酸钠-酸改性凹土颗粒(简称SAA颗粒),备用。
1.3 数据处理Sr和Cs在凹土吸附剂上的平衡吸附量qe(mg/g)和去除率Y(%)根据下式计算:
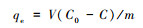
|
(1) |
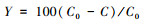
|
(2) |
式中:V是Sr和Cs溶液的体积(L);m是SAA颗粒的质量(g);C0是Sr和Cs溶液的初始质量浓度(mg/L);C是吸附平衡后质量浓度(mg/L)。
2 实验过程与结果分析 2.1 SAA颗粒的微观表征利用扫描电子显微镜(SEM)表征凹土与SAA颗粒,可以看出凹土含有棒状的黏土以及粒状杂质石英,呈团块状结构,晶束较粗,结构致密(图 1a)。通过海藻酸钠凝胶法制备出的SAA颗粒(图 1b、1c),粒径2~3 mm不等,呈球状或椭球状,表面粗糙,呈褶皱状,孔隙发育,利于溶液渗入颗粒内部;且具有一定比表面积,可供溶液与颗粒接触。但对比图 1a可见,造粒明显降低了凹土的比表面积。

|
图 1 凹土原土(a),SAA颗粒[b(X50),c(X2000)]SEM结构表征 Fig.1 SEM images of the original attapulgite (a) and the SAA Particle [(b(X50), c(X2000)] |
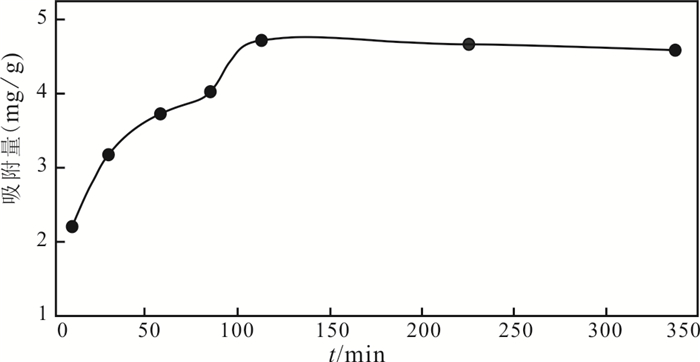
将0.1 g SAA颗粒置于锥形瓶中,加入10 mL浓度为100 mg/L的Sr溶液,封口膜密封瓶口,置于恒温振荡器内,于20 ℃下以200 r/min的速率振荡,分别在10 min、30 min、60 min、90 min、120 min、240 min、360 min取样,样品体积为10 mL,经0.45 μm纤维素膜过滤,采用电感耦合等离子发射光谱仪(ICP-AES)测试样品中Sr的浓度。不同时间下SAA颗粒对Sr溶液的吸附效果如图 2所示。
|
图 2 Sr在SAA颗粒上吸附的变化规律(100 mg/L) Fig.2 The variation of contents of adsorbed Sr on the SAA particles(100 mg/L) |
由图 2可得,0~120 min,SAA颗粒对Sr的吸附速率较快,此时主要为表面和孔隙吸附过程。在120 min时,吸附基本达到平衡,此时最大吸附量为4.6 mg/g,去除率为40.4%。同等条件下采用天然凹土粉末吸附Sr的实验中,去除率为49.3%,SAA颗粒的去除率较之降低8.9%。
2.2.2 初始浓度对SAA颗粒吸附Sr的影响将0.1 g SAA颗粒置于锥形瓶中,加入10 mL浓度分别为1 mg/L、5 mg/L、10 mg/L、20 mg/L、50 mg/L的Sr溶液,封口膜密封瓶口,置于恒温振荡器内20 ℃下以200 r/min的速率振荡,360 min后取出,测量方法同上。不同初始浓度下SAA颗粒对Sr溶液的吸附效果如表 1所示。
|
|
表 1 初始浓度对Sr、Cs在SAA颗粒上吸附的影响规律(360 min) Table 1 Effect of initial Sr and Cs concentrations in the solution to the Sr adsorption of the SAA particles (360 min) |
由表 1可以看出,对于Sr溶液,浓度由1 mg/L变为10 mg/L,吸附量由0.03 mg/g增至0.35 mg/g,增大11.6倍;由5 mg/L变为50 mg/L,吸附量由0.20 mg/g增至2.50 mg/g,增大12.5倍;由10 mg/L变为100 mg/L,吸附量由0.35 mg/g增至2.50 mg/g,增大7.1倍;由1 mg/L变为100 mg/L,吸附量由0.03 mg/g增至4.50 mg/g,增大150.0倍。说明随Sr初始浓度的增大,SAA颗粒对Sr的吸附量明显增加,这是由于随着初始浓度的增大,单位体积溶液中Sr离子密度增大,与吸附剂颗粒接触机会增多,宏观上表现出的吸附量越大。
2.3 SAA颗粒吸附Cs的结果与分析 2.3.1 吸附时间对SAA颗粒吸附Cs的影响实验过程与2.2.1中描述的方法相同,采用电感耦合等离子发射质谱仪(ICP-MS)测试样品中Cs的浓度。不同时间下SAA颗粒对Cs溶液的吸附效果如图 3所示。由图 3可得,SAA颗粒吸附Cs的过程与吸附Sr的过程相似,0~120 min,SAA颗粒对Cs的吸附速率较快,120 min时,吸附基本达到平衡,此时的最大吸附量4.5 mg/g,去除率为45.9%。同等条件下进行的采用天然凹土粉末吸附Cs的实验中,去除率为62.7%,SAA颗粒的去除率较之降低17.8%。

|
图 3 Cs在SAA颗粒上吸附的变化规律(100 mg/L) Fig.3 The variation of contents of adsorbed Cs on the SAA particles(100 mg/L) |
实验过程与2.2.2中描述的方法相同,不同初始浓度下SAA颗粒对Cs溶液的吸附效果如表 1所示。表 1反映出对于Cs溶液,浓度由1 mg/L变为10 mg/L,吸附量由0.08 mg/g增至0.59 mg/g,增大7.4倍;由5 mg/L变为50 mg/L,吸附量由0.33 mg/g增至2.71 mg/g,增大8.2倍;由10 mg/L变为100 mg/L,吸附量由0.59 mg/g增至3.85 mg/g,增大6.5倍;由1 mg/L变为100 mg/L,吸附量由0.08 mg/g增至3.85 mg/g,增大48.1倍。随着溶液初始浓度的增加,SAA颗粒对Cs的吸附量逐渐增加。对比Sr的吸附过程,初始浓度对SAA颗粒吸附Cs的影响要小于吸附Sr时的影响。
2.4 批试验结果分析Kaygun等(2017)的研究结果表明,天然粉状凹土对Sr的去除率可达65.0%,30 min达到平衡;对Cs的去除率可达80.0%,15 min达到平衡。本实验采用的天然凹土,对Sr和Cs去除率分别为49.3%和62.7%,较上述研究结果低,这是由于凹土产地不同、纯化方法及实验条件等因素的差异导致。SAA颗粒吸附Sr和Cs的平衡时间约为2 h,与Wang等(2007)研究不同浓度盐酸改性的凹土对Cd2+的吸附过程相似,其平衡时间约为1 h,可见溶液与SAA颗粒充分接触所需时间多于粉末状凹土所需时间。本实验中初始浓度对SAA颗粒吸附Sr和Cs的影响规律,与王金明和易发成(2006)的研究结果一致,即吸附量随溶液初始浓度的增大而增大。
利用海藻酸钠凝胶法制备的SAA颗粒,相比天然凹土粉末,对溶液中Sr和Cs的吸附效果有明显降低,对Sr的去除率降低8.9%,对Cs的去除率降低17.8%。这是因为SAA颗粒虽然表面粗糙,孔隙发育,利于溶液渗入颗粒内部,且具有一定比表面积,但远小于同等质量粉末状凹土与溶液的接触面积。
3 柱实验过程与结果分析 3.1 实验装置与过程柱实验装置图 4如下所示,吸附柱为直径2.5 cm、高20 cm的树脂吸附柱,通过管径为2 cm橡胶管与蠕动泵和水槽相连,溶液通过蠕动泵自下而上流经凹土柱。

|
图 4 柱实验装置图 Fig.4 The sketch of the column adsorption experiment |
流速对柱实验的影响:称取10.0 g SAA颗粒装入吸附柱,装入石英砂调节吸附剂颗粒使用量。配制浓度为1 mg/L的Sr和Cs溶液,调整蠕动泵流量为5 mL/min、10 mL/min、20 mL/min、50 mL/min、80 mL/min。取样时间为20 min、40 min、60 min、80 min、100 min、120 min、150 min、180 min、240 min、300 min,每次取样10 mL,经0.45 μm纤维素膜过滤后备测,测试方法同上。
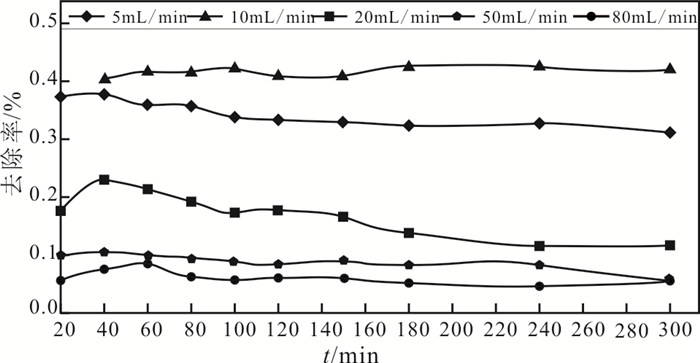
3.2 流速对Sr迁移的影响不同流速条件下初始浓度为1 mg/L的Sr溶液在SAA颗粒中去除率变化情况如图 5所示:
|
图 5 Sr溶液在吸附柱中不同流速下的去除率变化规律(1 mg/L) Fig.5 The variation of Sr removal rates at various flow rates of the Sr-bearing solution passing through the adsorption column (1 mg/L) |
由图 5可以看出,流速为10 mL/min时SAA颗粒对Sr的吸附效果最好,去除率为41.8%,流速减小为5 mL/min时,去除率降低为36.6%,流速增加到20 mL/min时,去除率降低为22.2%,流速增加到50 mL/min和80 mL/min时,去除率低至10.0%,吸附效果不明显。可以判定SAA颗粒吸附Sr的最佳流速为10 mL/min。
3.3 流速对Cs迁移的影响不同流速下初始浓度为1 mg/L的Cs溶液在吸附剂颗粒中的去除率变化情况如图 6所示:

|
图 6 Cs溶液在吸附柱中不同流速下的去除率变化曲线(1 mg/L) Fig.6 The variation of Cs removal rates at different flow rates of the Cs-bearing solution passing through the adsorption column (1 mg/L) |
由图 6可得,流速为10 mL/min时SAA颗粒对Cs的吸附效果最好,去除率为61.6%,流速减小为5 mL/min时,去除率降低为61.5%,流速增加到20 mL/min时,去除率降低为36.6%,流速增加到50 mL/min和80 mL/min时,去除率低至10%左右,吸附效果很差。在上述柱实验中,SAA颗粒吸附Cs表现的规律与吸附Sr的规律一致,最佳流速为10 mL/min,随流速的减小和增大,SAA颗粒对Cs的去除率均降低。
3.4 柱实验结果分析由上述柱实验可得,SAA颗粒吸附Sr和Cs的最佳流速为10 mL/min,去除率分别为41.8%和61.5%,但随流速的增加或降低,SAA颗粒对Sr和Cs的去除率均降低,且不同流速下SAA颗粒对Sr和Cs的去除效果差异突出,去除效果较差。本结果与胡显峰等(2011)研究凹土对Ni2+的动态吸附结果类似,即随着溶液流速的加快,凹土对Ni2+的去除率降低。
由于流速增加,Sr和Cs溶液在吸附柱中停留时间缩短,溶液中离子与SAA颗粒接触时间减少,降低离子吸附在颗粒上的机率,导致相同时间间隔内,大流速吸附柱去除效果明显低于小流速吸附柱去除效果。而对于流速降低至5 mL/min去除率却低于流速为10 mL/min去除率,可能是该颗粒对流速变化敏感,差异较大。实验结果表明,将凹土造粒明显降低了其吸附性能,同时,将颗粒应用到柱实验中,对核素Sr和Cs的去除效果更差。
4 结论(1) 电镜对海藻酸钠-凹土颗粒的微观表征显示颗粒表面呈褶皱状,存在孔隙发育,具有较大的比表面积,但较与其原土比表面积有明显的减小。
(2) 批试验结果显示,SAA颗粒投加量为10 g/L、初始浓度100 m/L时,20 ℃下以200 r/min的速率振荡,0~120 min内主要为表面和孔隙吸附过程,120 min时,吸附剂颗粒对Sr和Cs的吸附基本达到平衡,Cs的去除率45.9%,Sr的去除率40.4%,低于同等条件下天然凹土粉末对Sr和Cs的去除率,49.3%和62.7%。表明将凹土造粒,其对吸附Sr和Cs有明显负效应,但应用到实际工程中,对污水处理仍具有一定去除效果。
(3) 柱实验结果显示,吸附柱中吸附剂质量为10.0 g SAA颗粒,浓度1 mg/L的Sr和Cs溶液在流速为10 mL/min时,Sr和Cs的去除率达到41.8%和61.6%,随流速的增加或降低,去除率均减小,不同流速下海藻酸钠-凹土颗粒对Sr和Cs的去除效果差异较大,去除效果较差。
Álvarez-Ayuso E, García-Sánchez A. 2003. Palygorskite as a feasible amendment to stabilize heavy metal polluted soils. Environmental Pollution, 125(3): 337-344. DOI:10.1016/S0269-7491(03)00121-0 |
Álvarez-Ayuso E, García-Sánchez A. 2007. Removal of cadmium from aqueous solutions by palygorskite. Journal of Hazardous Materials, 47(1-2): 594-600. |
Chen H, Wang A Q. 2007. Kinetic and isothermal studies of lead ion adsorption onto palygorskite clay. Journal of Colloid and Interface Science, 307(2): 309-316. DOI:10.1016/j.jcis.2006.10.054 |
Das N. 2012. Remediation of radionuclide pollutants through biosorption-an overview. Clean-Soil, Air, Water, 40(1): 16-23. DOI:10.1002/clen.v40.1 |
Gan F Q, Zhou J M, Wang H Y, Ma Y J, Dong Y H, Liu Y. 2010. Effect of Acid Concentration on Phosphate Adsorption Capacity of Acid Modified Palygorskites. Acta Pedologica Sinica, 47(2): 319-324. |
Kadirvelu K, Namasivayam C. 2003. Activated carbon from coconut coirpith as metal adsorbent:adsorption of Cd(Ⅱ) from aqueous solution. Advances in Environmental Research, 7(2): 471-478. DOI:10.1016/S1093-0191(02)00018-7 |
Kaygun A K, Eral M, Erenturk S A. 2017. Removal of cesium and strontium using natural attapulgite:evaluation of adsorption isotherm and thermodynamic data. Journal of Radioanalytical and Nuclear Chemistry, 311(2): 1459-1464. DOI:10.1007/s10967-016-4989-9 |
Kim K W, Baek Y J, Lee K Y, Chung D Y, Moon J K. 2016. Treatment of radioactive waste seawater by coagulation-flocculation method using ferric hydroxide and poly acrylamide. Journal of Nuclear Science and Technology, 53(3): 439-450. DOI:10.1080/00223131.2015.1055313 |
Leboda R, Chodorowski S, Skubiszewska-Zięba J, Tarasevich Y I. 2001. Effect of the carbonaceous matter deposition on the textural and surface properties of complex carbon-mineral adsorbents prepared on the basis of palygorskite. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 178(1-3): 113-128. |
Rahman R O A, Ibrahium H A, Hung Y T. 2011. Liquid radioactive wastes treatment:a review. Water, 3(2): 551-565. DOI:10.3390/w3020551 |
Reddad Z, Gerente C, Andres Y, Le Cloirec P. 2002. Adsorption of several metal ions onto a low-cost biosorbent:kinetic and equilibrium studies. Environmental Science & Technology, 36(9): 2067-2073. |
Sheng G D, Yang P J, Tang Y N, Hu Q Y, Li H, Ren X M, Hu B W, Wang X K, Huang Y Y. 2016. New insights into the primary roles of diatomite in the enhanced sequestration of UO22+ by zerovalent iron nanoparticles:an advanced approach utilizing XPS and EXAFS. Applied Catalysis B Environmental, 193: 189-197. DOI:10.1016/j.apcatb.2016.04.035 |
Sureda R, Martínez-Lladó X, Rovira M, De Pablo J, Casas I, Giménez J. 2010. Sorption of strontium on uranyl peroxide:Implications for a high-level nuclear waste repository. Journal of Hazardous Materials, 181(1-3): 881-885. DOI:10.1016/j.jhazmat.2010.05.095 |
Wang W J, Chen H, Wang A Q. 2007. Adsorption characteristics of Cd(Ⅱ) from aqueous solution onto activated palygorskite. Separation and Purification Technology, 55(2): 157-164. DOI:10.1016/j.seppur.2006.11.015 |
Yang F C, Sun S Q, Chen X Q, Chang Y, Zha F, Lei Z Q. 2016. Mg-Al layered double hydroxides modified clay adsorbents for efficient removal of Pb2+, Cu2+ and Ni2+ from water. Applied Clay Science, 123: 134-140. DOI:10.1016/j.clay.2016.01.026 |
龚安华, 孙岳玲. 2013. 盐酸改性凹凸棒土对铜离子的吸附性能. 湖北农业科学, 52(2): 313-315. DOI:10.3969/j.issn.0439-8114.2013.02.018 |
郭娜, 王金生, 李剑, 滕彦国. 2015. 2种四环素类抗生素在凹凸棒石黏土中的吸附研究. 环境科学与技术, 38(3): 81-85. |
胡显峰, 赵旭涛, 张庆芳, 周丹丹. 2011. 凹凸棒石粘土对Ni(Ⅱ)的动态吸附研究. 化学与生物工程, 28(6): 56-60. DOI:10.3969/j.issn.1672-5425.2011.06.016 |
贾麟, 刘阳, 张光辉, 顾平. 2015. 去除水体中放射性碘核素的研究进展. 工业水处理, 35(7): 10-18. |
王金明, 易发成. 2006. 改性凹凸棒石对模拟核素Sr2+的吸附性能的研究. 水处理技术, 32(10): 25-28. DOI:10.3969/j.issn.1000-3770.2006.10.007 |
王哲, 易发成, 刘艳. 2015. 安徽明光凹凸棒石黏土对锶、铯、钴的吸附特性研究. 科学技术与工程, 15(31): 234-238. DOI:10.3969/j.issn.1671-1815.2015.31.044 |
杨佳静. 2015.有机改性凹凸棒石黏土的制备及其吸附性能研究.硕士学位论文.兰州: 兰州交通大学
|
叶鸣, 李丽, 张先斌. 2013. 盐酸改性凹凸棒石条件对去除Cd2+效果的影响. 工业用水与废水, 44(6): 49-52. DOI:10.3969/j.issn.1009-2455.2013.06.014 |
 2018, Vol. 37
2018, Vol. 37


