2. 首都师范大学,北京 100048;
3. 山西师范大学,山西临汾 041004;
4. 河北地质大学,河北石家庄 050031
2. Capital Normal University, Beijing 100048, China;
3. Shanxi Normal University, Linfen, Shanxi 041004, China;
4. Hebei GEO University, Shijiazhuang, Hebei 050031, China
土壤酶作为土壤生态系统的重要组分之一,参与催化土壤中的各类生化反应,在土壤营养物质循环与转化、有机质的分解和固存等方面起着非常重要的作用,由于其敏感且易于测定的优势,可以作为土壤质量和生态系统健康的重要指标[1–3]。与碳和氮转化相关的酶是细胞生长和能量过程的核心,因此土壤酶活性的高低可以表征土壤碳氮循环转化的强弱与方向[4–5]。不同的长期耕作措施通过改变土壤中生境和营养元素的供应来影响土壤微生物的活动,从而对碳氮循环酶产生反馈,改变土壤酶的活性[6–8]。
根际区域作为植物、微生物和土壤相互交汇的重要场所,是土壤中生物化学性质最活跃的微域。耕作通过改变土壤的物理性状和有机质的输入,影响作物根系的生长发育,进而改变作物对营养元素的吸收利用效率,而根际土壤酶的种类和活性是影响土壤养分有效性的主要因素[9]。因此,研究不同长期耕作措施对作物根际和非根际土壤碳氮元素含量和土壤酶活性的影响,以及土壤碳氮元素与碳氮转化相关酶之间的相互联系,对认识土壤酶对土壤碳氮变化的响应机制和选择合理有效的耕作技术具有重要的理论和实践意义。
研究表明,土壤有机碳会随着耕作措施和土地利用方式的改变相应降低与升高[10–11]。相比于长期以来的传统耕作方式,保护性耕作是近些年被广泛推广的一种耕作方式,以减少土壤扰动和增加秸秆覆盖为主要特点。王晓凌等[12]通过比较几种不同耕作方式对土壤微生物量和土壤酶活性的影响,发现免耕条件下的土壤蔗糖酶、脲酶、蛋白酶、过氧化氢酶的活性和土壤微生物量碳氮都显著高于传统耕作,而没有秸秆还田的耕作处理则显著降低了土壤碳氮含量和土壤酶活性。戴志刚等[13]的研究同样认为,秸秆还田能够显著提高土壤有机质,但由于秸秆中含氮量较少,存在的形态为有机态,不利于转化为土壤全氮,所以耕作措施对总氮的影响较小。高秀君等[14]结合中长期田间定位试验,对春小麦生长期内土壤酶活性在不同耕作措施下的动态变化趋势进行了研究,发现在春小麦的各生育期,免耕、免耕结合秸秆覆盖和秸秆还田等保护性耕作处理的土壤酶活性均高于传统耕作处理。然而孙露莹[1]的研究表明,土壤β-葡萄糖苷酶的活性和总氮具有明显的季节性波动和垂直分布特征,但对耕作措施的响应并不显著。崔雯雯等[15]研究发现,长期的耕作措施通过改变土壤酶活性及土壤养分含量,进而导致土壤腐殖化过程和熟化程度减慢,最终会造成连作障碍和连作减产。
以往研究中,关于耕作措施对土壤酶的研究,大多局限于蔗糖酶、脲酶、过氧化氢酶和磷酸酶上,而对直接参与碳氮转化的β-葡萄糖苷酶 (BG)、β-纤维二糖苷酶 (CBH)、β-木糖苷酶 (BXYL)、乙酰氨基葡萄糖苷酶 (NAG) 和亮氨酸氨基肽酶 (LAP) 研究较少。本研究依托河南豫西地区 17 年的长期耕作试验基地,选择从无人管理的草地到长期以来的传统耕作方式,再到近年来提倡的免耕和深松四种长期耕作措施,探讨不同长期耕作措施下作物根际土壤和非根际土壤中碳氮含量与相应转化酶的变化特征,阐明碳氮转化酶对土壤碳氮元素含量变化的响应机制,量化耕作措施对农田土壤生态系统功能的影响。
1 材料与方法 1.1 研究区概况试验地位于农业部旱地农业野外科学观测实验站保护性耕作田间试验场内 (34.80 °N,112.56 °E),地处豫西黄土丘陵区河南孟津县送庄,属于黄土高原东部边缘,土层深厚 (50—100 m),土壤类型是壤质黄绵土。气候类型属于亚热带向温带过渡地带。年平均气温13.7℃,l月最冷,平均为–0.5℃,7月最热,平均为26.2℃。多年平均降水量为650 mm,保证率80%的降水量为600 mm。平均全年日照时数为2270 h,全年平均日照率为51%。在作物生长的4~10月份,日温差5月份最大为12.7℃,8月份最小为8.6℃,积温平均为5046℃,平均无霜期为235 d。
1.2 试验设计本试验为长期定位试验,开始于1999年10月份。供试小麦品种选用当地优势品种洛旱7号,每年10月初播种,6月中旬收获,夏季休闲。基本苗270万株/hm2,小区面积90 m2 (3 m × 30 m),20 cm行距,3叶期定苗。小麦全生育期不浇水。各处理肥料施用量相同,分别为N 150 kg/hm2、P2O5 105 kg/hm2、K2O 45 kg/hm2。试验前耕层 (0—20 cm) 土壤的养分含量如下:有机质11.5 g/kg、无机碳11.3 g/kg、全氮1.1 g/kg、全磷0.69 g/kg、全钾18 g/kg、有效氮82.5 mg/kg、有效磷6.1 mg/kg、速效钾139.5 mg/kg、pH 7.28。土壤颗粒组成如下:粘粒15.2%、粉粒24.3%、细砂58.2%、粗砂2.3%。
试验设4种不同耕作处理,分别是草地 (GL)、传统耕作 (CT)、免耕覆盖 (NT)、深松覆盖 (SM),各耕作处理具体方法见表1。
| 表1 试验处理方法 Table 1 Treatments of different tillage |
 |
土壤样品采集时间为小麦灌浆期2016年5月。根际土壤的采集方法为在各处理小区随机选取适量的小麦植株,挖取根系,采用抖根分离法取粘着在根系1 cm的土壤,非根际土壤样品的采集采用直径为5 cm的土钻取相应植株行间土壤,其中非根际表层土的采样深度为0—20 cm,非根际底层土的采样深度为20—40 cm。根际和非根际土各自混匀,装入聚乙烯样袋中,迅速放入保鲜箱中带回实验室。将土壤样品分为两部分,一部分过2 mm筛,放入–20℃冰箱中保存,用于测定土壤酶活性;另一部分放于阴凉处风干,过0.15 mm筛,用于测定土壤总碳、总氮和有机碳含量。
1.3.2 土壤碳氮元素含量测定土壤总碳、总氮和有机碳含量采用元素分析仪 (ElementarAnalysensysteme GmbH,德国Elementary公司) 进行测定。其中,总碳测定的是土壤中所有含碳成分的含量,包括无机碳和有机碳,有机碳是将土壤酸化处理去除无机碳后的碳含量。
1.3.3 土壤酶活性测定称取相当于1.0 g烘干土的新鲜土样,放入500 mL的玻璃烧杯中,加入50 mM灭菌后冷却的醋酸缓冲液125 mL,在磁力搅拌器上搅拌10 min充分混匀,用多通道移液器将缓冲液、土壤样品悬浊液、10 μM标准品和200 μM相应底物严格按照相应的体积和顺序加入到黑底的96孔酶标板中,采用多功能酶标仪 (Scientific Fluoroskan Ascent FL,美国Thermo公司) 测定土壤β-葡萄糖苷酶 (BG)、β-纤维二糖苷酶 (CBH)、β-木糖苷酶 (BXYL)、乙酰氨基葡萄糖苷酶 (NAG) 和亮氨酸氨基肽酶 (LAP) 活性 (相应底物及酶代码编号见表2)。具体测定参照Saiya-Cork等[16]的方法并略作修改。试剂购于Sigma-Aldrich Co. Ltd公司,用无菌水配置后于4℃冰箱短暂保存待用。
| 表2 测试酶及所用底物 Table 2 Enzymes and corresponding substrates used for measurements |
 |
土壤酶活性值计算参照Deforest[17]的方法。
| $\begin{aligned}&{\text{酶活性}}[{\rm{mmol}}/({\rm{h}} \cdot {\rm{g}})] =\\ &\quad\frac{{{{\text{净荧光值}} \times {\rm{125}}\;{\rm{mL}}}}}{{{{\text{激发系数}} \times 0.2\;{\rm{mL}} \times {\text{时间}}\left( {\rm{h}} \right) \times {\text{土样}}\left( {\rm{g}} \right)}}}\\&{\text{净荧光值}} = \left( {\frac{{{\text{样品荧光}} - {\text{样品对照}}}}{{{\text{淬灭系数}}}}} \right) - {\text{底物对照}}\\&{\text{激发系数}}\left( {{\rm{nmol}}{{\rm{e}}^{ - 1}}} \right) = \frac{{{\text{标准荧光}}}}{{0.5\;{\rm{nmol}}}}\\&{\text{淬灭系数}} = \frac{{{\text{淬灭标准}} - {\text{样品对照}}}}{{{\text{标准荧光}}}}\end{aligned}$ |
采用Microsoft Excel进行数据、图表处理,利用SPSS16.0软件进行方差分析 (ANOVA),用最小显著差数法 (LSD) 进行差异显著性检验。
2 结果与分析 2.1 土壤碳氮含量与传统耕作相比,免耕和深松显著提高了小麦根际以及非根际0—20 cm土壤的总碳含量 (P < 0.05)( 图1),其中深松处理对土壤总碳含量的提升更为明显。然而,在非根际20—40 cm土壤中,免耕和深松处理反而显著降低了土壤总碳含量。草地根际土壤总碳含量显著高于免耕和传统耕作,而草地非根际土壤总碳含量显著低于其他三个耕作处理。
 |
| 图1 长期不同耕作措施下根际和非根际土壤总碳和有机碳含量 Fig. 1 Soil total carbon and organic carbon content in rhizosphere and non-rhizosphere under different long-term tillage treatments |
与传统耕作相比,草地、免耕和深松处理显著提高了作物根际以及非根际0—20 cm的土壤有机碳含量 (P < 0.05),显著降低了非根际20—40 cm土壤有机碳含量,分别较传统耕作处理降低了18.69%、31.42%和32.49%。
总体来看,草地、免耕和深松处理土壤的总碳和有机碳含量沿根际、非根际0—20 cm、非根际20—40 cm逐渐降低,而传统耕作这三个层次土壤的总碳和有机碳含量则基本一致。可见,草地、免耕和深松处理的土壤具有明显的分层现象,其土壤总碳和有机碳富集在作物根际土壤中。由于草地、免耕和深松三个处理均有大量凋落物或秸秆还田,说明秸秆还田造成了有机碳的再分配,特别是0—20 cm土壤碳的积累。
与传统耕作相比,草地、免耕和深松处理显著提高了作物根际土壤的总氮含量 (P < 0.05)( 图2),深松耕作处理显著提高了非根际0—20 cm土壤的总氮含量,但降低了非根际20—40 cm土壤总氮含量。
土壤C/N可以调节微生物的活性并反映相关元素的有效性,是评价农田土壤质量水平的一个重要指标。不同的长期耕作措施对土壤C/N有显著影响 (图2),与传统耕作相比,深松处理显著降低了作物非根际土壤C/N,免耕显著降低了作物非根际20—40 cm土壤中的C/N。免耕处理降低了作物根际土壤中的C/N,并提高了作物非根际0—20 cm土壤中的C/N,但相比于传统耕作差异并不显著。草地处理的非根际0—20 cm土壤中的C/N显著高于传统耕作,而非根际20—40 cm土壤的C/N显著低于传统耕作。
 |
| 图2 长期不同耕作措施下根际和非根际土壤总氮含量和碳氮比 Fig. 2 Soil total N content and C/N ratio in rhizosphere and non-rhizosphere under different long-term tillage treatments |
根际土壤中深松处理的β-葡萄糖苷酶活性最高,而传统耕作最低,草地、免耕和深松处理相比于传统耕作分别提高了56.7%、54.7% 和105.9% (图3)。深松处理的β-葡萄糖苷酶活性显著高于免耕和草地处理 (P < 0.05),而免耕和草地之间无显著性差异。
与根际土壤不同,非根际土壤中传统耕作的β-葡萄糖苷酶活性最高。在非根际0—20 cm土壤中,传统耕作和草地的β-葡萄糖苷酶活性显著高于免耕和深松处理,免耕和深松处理土壤的β-葡萄糖苷酶活性之间没有显著性差异。相比于传统耕作,草地、免耕和深松处理的非根际0—20 cm土壤的β-葡萄糖苷酶活性分别降低了5.8%、36%和32.2%。
在非根际20—40 cm土壤中,传统耕作土壤的β-葡萄糖苷酶活性显著高于其他三种处理,而免耕和深松处理土壤的β-葡萄糖苷酶活性之间同样没有显著性差异。相比于传统耕作,草地、免耕和深松处理的非根际20—40 cm土壤的β-葡萄糖苷酶活性比0—20 cm土壤的降幅更大,分别降低了17.6%、50.6%和46.5%。
2.2.2 β-纤维二糖苷酶活性四个处理的根际土壤中,免耕处理的β-纤维二糖苷酶酶活性最高,传统耕作的β-纤维二糖苷酶活性最低 (图3)。深松处理的β-纤维二糖苷酶活性显著高于传统耕作和草地处理,免耕处理作物根际土壤的β-纤维二糖苷酶活性显著高于其他三个处理,而传统耕作和草地之间无显著性差异。草地、免耕和深松处理的β-纤维二糖苷酶活性相比于传统耕作分别提高了24.2%、259.6%和166.4%。
在非根际土壤中,传统耕作土壤的β-纤维二糖苷酶活性最高,显著高于其他三个处理。其中,草地、传统耕作和深松处理的非根际0—20 cm土壤的β—纤维二糖苷酶活性之间无显著差异,而免耕和深松处理的非根际20—40 cm土壤的β—纤维二糖苷酶活性则显著高于草地。与耕作处理对β—葡萄糖苷酶活性的影响一致,相比于传统耕作,草地、免耕和深松处理的非根际20—40 cm土壤的β—纤维二糖苷酶活性比0—20 cm土壤的降幅更大,分别降低了93.4%、80.3%和77.6%。
2.2.3 β-木糖苷酶活性根际土壤中深松处理的β-木糖苷酶活性最高,而传统耕作的β-木糖苷酶活性在四个处理中最低,草地、免耕和深松处理的β-木糖苷酶活性相比于传统耕作显著提高了144.7%、117.4%和290.1% (图3)。深松处理的β-木糖苷酶活性显著高于免耕和草地处理,而免耕和草地之间无显著性差异。
非根际0—20 cm土壤中,深松处理的β-木糖苷酶活性显著高于其他三个处理。免耕处理的β-木糖苷酶活性在四个处理中最低,显著低于草地、传统耕作和深松处理。而在非根际20—40 cm土壤中,传统耕作的β-木糖苷酶活性显著高于其他三个处理。草地、免耕和深松处理的β-木糖苷酶活性基本一致。
2.2.4 乙酰氨基葡萄糖苷酶和亮氨酸氨基肽酶活性由图3可以看出,根际土壤中草地处理的乙酰氨基葡萄糖苷酶活性显著高于其他三个处理。草地、免耕和深松处理的乙酰氨基葡萄糖苷酶活性显著高于传统耕作,分别提高了531.0%、131.7%和306.0%。
 |
| 图3 不同长期耕作措施下根际和非根际土壤酶活性 Fig. 3 Soil enzyme activity in rhizosphere and non-rhizosphere under different long-term tillage treatments |
在非根际土壤中 (0—20 cm和20—40 cm),草地土壤的乙酰氨基葡萄糖苷酶活性最高,免耕处理最低,草地、传统耕作和深松处理的乙酰氨基葡萄糖苷酶活性均显著高于免耕处理。
亮氨酸氨基肽酶,在根际土壤和非根际土壤中,亮氨酸氨基肽酶的活性均表现为GL > CT > NT > SM,且各处理之间差异显著。
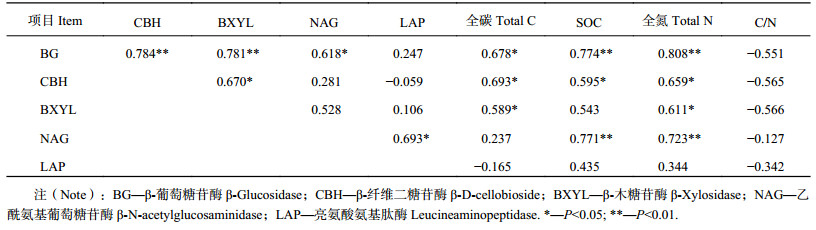
2.3 长期不同耕作措施下土壤碳氮元素与碳氮转化相关酶的相关分析长期不同耕作措施下,碳氮转化相关酶彼此之间存在联系 (表3)。其中,β-葡萄糖苷酶与β-纤维二糖苷酶和β-木糖苷酶之间呈极显著正相关,β-纤维二糖苷酶与β-木糖苷酶之间呈显著正相关。β-葡萄糖苷酶与乙酰氨基葡萄糖苷酶之间呈显著正相关。乙酰氨基葡萄糖苷酶与亮氨酸氨基肽酶之间呈显著正相关。除β-纤维二糖苷酶与亮氨酸氨基肽酶外,本研究中碳氮转化相关酶彼此之间均存在正相关关系。同时,土壤中碳氮元素含量的变化与碳、氮转化相关酶也密切相关。β-葡萄糖苷酶与有机碳和总氮之间均呈极显著正相关,与总碳之间呈显著正相关。β-纤维二糖苷酶与总碳、有机碳和总氮之间均呈显著正相关。β-木糖苷酶与总碳和总氮之间均呈显著正相关。乙酰氨基葡萄糖苷酶与有机碳和总氮之间均呈极显著正相关。亮氨酸氨基肽酶与有机碳和总氮之间均呈正相关关系,与总碳和C/N之间均呈负相关关系,但均不显著。碳氮转化相关酶与土壤总碳、总氮和有机碳之间均存在正相关关系 (除亮氨酸氨基肽酶与总碳之间),与C/N之间均存在负相关关系。
| 表3 土壤碳、氮元素含量与碳、氮转化相关酶的相关分析 Table 3 Correlation of soil C and N contents with the activities of enzymes related to C and N transformation |
 |
保护性耕作可不同程度地改变土壤中的总碳和有机碳含量。陈娟等[18]研究认为,在0—40 cm土壤中,长期保护性耕作的土壤有机碳含量显著高于传统耕作。而姜学兵等[19]依托冬小麦夏玉米轮作免耕长期定位试验点,研究了不同耕作措施对土壤水稳性团聚体和有机碳储量变化的影响发现,与传统耕作相比,免耕和免耕秸秆不还田可提高表层土壤有机碳含量和储量,与表层不同,深层土壤有机碳的含量和储量表现为免耕 < 免耕秸秆不还田 < 传统耕作。
本研究表明,与传统耕作相比,保护性耕作显著提高了作物根际以及非根际0—20 cm的土壤总碳含量;相比于免耕,深松对土壤总碳含量的提升更为明显。然而,在非根际20—40 cm土壤中,保护性耕作并没有显著改变土壤总碳含量。与草地相比,传统耕作造成了作物根际土壤碳的流失,而保护性耕作则损失较少,其中深松处理作物根际土壤总碳含量与草地处理基本一致,这主要是由于耕作处理土壤中的无机碳含量显著高于草地,其原因可能是人为活动和耕作扰动携带更多的二氧化碳和风积灰尘进入土壤。而在非根际土壤中,耕作处理土壤的总碳含量高于草地,说明相比于完全没有植物生长的撂荒地,耕作提高了土壤中的总碳含量,提升了土壤的固碳容量。
保护性耕作提升了土壤0—20 cm的有机碳含量,但与传统耕作相比,保护性耕作非根际20—40 cm土壤的有机碳含量反而降低,这也与李景等[20]在2011年依托该长期试验点的研究结果一致。这说明保护性耕作仅仅是改变了土壤有机碳在垂直剖面上的分布,提升土壤表层碳的积累和固存,降低了非根际20—40 cm土壤中的有机碳含量。同时Six等[21]关于耕作对土壤有机碳影响的研究也表明与传统耕作相比,免耕并不利于深层土壤有机碳的积累。
保护性耕作被认为是提升农田土壤全氮含量的有效措施。丁晋利[22]结合长期定位试验和 RZWQM2模型模拟方法,研究传统耕作转变为免耕和深松等保护性耕作措施后土壤水氮平衡、氮素迁移转化及土壤有机质的变化特征发现,长期不同耕作措施下土壤全氮和有机碳含量均表现出了明显的表层富集效应。其中,与传统耕作相比,免耕和双季秸秆还田处理显著提高耕层 (0—40 cm) 土壤有机碳和全氮含量。同时许菁等[23]在收集整理连续10年的长期定位保护性耕作试验结果后认为,土壤碳氮储量密切相关,变化趋势也基本一致,各保护性耕作措施的土壤碳氮储量均显著高于常规翻耕无秸秆还田。而López-Fando等[24]的研究则表明,免耕显著提高表层0—5 cm的全氮含量,但对5—30 cm土壤全氮含量影响较小。
本研究表明,与传统耕作相比,草地、免耕和深松处理显著提高了作物根际土壤的总氮含量,免耕和深松耕作处理显著提高了非根际0—20 cm土壤的总氮含量,但显著降低了非根际20—40 cm土壤总氮含量。同时,深松显著降低了作物根际和非根际土壤C/N,免耕显著降低了作物非根际20—40 cm土壤中的C/N,但对作物根际和非根际0—20 cm土壤C/N的影响并不显著。草地处理显著提高了作物非根际0—20 cm土壤C/N,却显著降低了作物非根际20—40 cm土壤的C/N。
3.2 保护性耕作对土壤碳氮转化相关酶的影响及其原理土壤中的β-葡萄糖苷酶、β-纤维二糖苷酶、β-木糖苷酶、乙酰氨基葡萄糖苷酶和亮氨酸氨基肽酶都在有机质分解中起重要作用[6]。其中,β-葡萄糖苷酶、β-纤维二糖苷酶和β-木糖苷酶是促进纤维素和其他β-1,4-葡聚糖降解的酶[25]。β-纤维二糖苷酶负责从纤维素分子的非还原端水解出纤维二糖二聚体,β-葡萄糖苷酶则负责将产生的纤维二糖水解成葡萄糖。β-木糖苷酶在水解纤维组织中的木聚糖过程中起着重要的作用,其水解产物木糖是微生物的能源之一[26]。乙酰氨基葡萄糖苷酶和亮氨酸氨基肽酶是参与氮循环的重要物质,乙酰氨基葡萄糖苷酶主要降解的是土壤中的几丁质、甲壳素和具备β-1,4键的氨基葡萄糖聚合物,其作用与β-葡萄糖苷酶水解纤维素相似。亮氨酸氨基肽酶可水解蛋白质,能够从多肽的N端水解亮氨酸和其他疏水氨基酸[27]。
黄召存[28]通过研究不同耕作方式对蚕豆根际土壤微生物和酶活性的影响发现,垄作和秸秆覆盖为微生物提供了适宜温度,使得土壤微生物活动增强,数量增多。因此土壤酶的活性在垄作和秸秆覆盖条件下最高,秸秆覆盖量越多,活性越强。同时黄召存[28]和孙敬克等[29]认为,作物根际土壤酶活性显著高于非根际土壤的酶活性。孙萌等[30]的研究同样表明有机物覆盖处理提高了土壤的纤维素酶活性、中性蛋白酶活性和脲酶活性。Zuber等[8]通过对全球范围内关于耕作对土壤微生物生物量和酶活性影响的研究进行了Meta分析后发现,相比于传统的耕作方式,免耕均显著提高了土壤的酶活性。
本研究表明,在与碳转化相关酶中,β-葡萄糖苷酶活性最高,β-纤维二糖苷酶活性最低。β-葡萄糖苷酶是β-葡萄糖苷酶、β-纤维二糖苷酶、β-木糖苷酶3种土壤中与碳转化相关的酶中活性最高的,说明相比于其他两种酶,其在参与土壤碳转化,特别是纤维素的分解过程中起到更大的作用。在作物根际土壤中,草地、免耕和深松处理相比于传统耕作均显著提高了β-葡萄糖苷酶、β-纤维二糖苷酶、β-木糖苷酶和乙酰氨基葡萄糖苷酶的活性。而相比于传统耕作,草地根际土壤的亮氨酸氨基肽酶活性显著提高,免耕和深松处理的亮氨酸氨基肽酶活性则显著降低。在作物非根际0—20 cm和20—40 cm土壤中,传统耕作的β-葡萄糖苷酶活性显著高于其他三种处理。说明秸秆还田后,提高了根际土壤中与碳转化相关酶的活性,降低了非根际土壤中与碳转化相关酶的活性。主要原因是作物根系生境对秸秆的降解起关键作用,说明秸秆还田会抑制非根际土壤中的β-葡萄糖苷酶活性,影响到非根际土壤中秸秆的降解,从秸秆降解的角度来看,建议可以将耕作行和走道进行轮换,促进还田秸秆的降解。
土壤酶既是土壤有机物转化的执行者,又是植物营养元素的活性库。土壤中养分的循环和转化等过程都离不开土壤酶的参与。土壤中的碳氮元素含量与土壤酶活性之间存在紧密关系。本研究表明,碳转化相关酶 (β-葡萄糖苷酶、β-纤维二糖苷酶和β-木糖苷酶) 相互之间均呈极显著或显著正相关。与氮转化相关酶,乙酰氨基葡萄糖苷酶与β-葡萄糖苷酶和亮氨酸氨基肽酶之间均呈显著正相关。亮氨酸氨基肽酶与β-葡萄糖苷酶、β-纤维二糖苷酶和β-木糖苷酶之间相关性均不显著。除β-纤维二糖苷酶与亮氨酸氨基肽酶外,本研究中与碳氮转化相关酶彼此之间均存在正相关关系,说明在土壤有机质分解转化的过程中,碳氮转化相关酶酶活性之间彼此相互促进,而Ekenler等[31]的研究也证实了这一点,他认为β-葡萄糖苷酶是纤维素降解过程中限制步骤的关键,同时β-葡萄糖苷酶还参与土壤中几丁质转化为氨基糖的生化反应过程。碳氮转化相关酶与C/N之间均呈负相关关系,其中β-葡萄糖苷酶和乙酰氨基葡萄糖苷酶与C/N呈极显著负相关,β-纤维二糖苷酶和β-木糖苷酶与C/N之间均呈显著负相关,亮氨酸氨基肽酶与C/N之间相关性不显著。这主要是因为土壤中C/N的改变,影响了土壤中的微生物活动,进而改变了碳氮转化相关酶的分泌。亮氨酸氨基肽酶与总碳、有机碳、总氮和C/N之间相关性均不显著。碳氮转化相关酶除β-木糖苷酶与有机碳以及乙酰氨基葡萄糖苷酶与总碳之间外,β-葡萄糖苷酶、β-纤维二糖苷酶、β-木糖苷酶和乙酰氨基葡萄糖苷酶与土壤碳氮元素含量之间均呈极显著或显著正相关。说明β-葡萄糖苷酶、β-纤维二糖苷酶、β-木糖苷酶和乙酰氨基葡萄糖苷酶在土壤碳氮元素的转化过程中起着十分重要的作用,是土壤碳氮循环的重要组成部分,可作为衡量土壤肥力理想的生物化学指标之一。
4 结论1) 保护性耕作措施下土壤总碳、总氮和有机碳含量均表现出明显的表层富集效应。采用不同耕作措施17年后,作物根际土壤总碳、有机碳和总氮含量表现为草地 > 深松地 > 免耕地 > 传统耕作地。与传统耕作相比,深松显著降低了作物根际和非根际土壤C/N,免耕和草地显著降低了作物非根际20—40 cm土壤中的C/N,但草地处理显著提高了作物非根际0—20 cm土壤C/N。
2) 四种耕作措施下,各土层中碳氮转化相关酶活性的变化趋势基本一致,表现为亮氨酸氨基肽酶 > β-葡萄糖苷酶 > β-木糖苷酶 > 乙酰氨基葡萄糖苷酶 > β-纤维二糖苷酶。在作物根际土壤中,草地、免耕和深松处理相比于传统耕作均显著提高了β-葡萄糖苷酶、β-纤维二糖苷酶、β-木糖苷酶和乙酰氨基葡萄糖苷酶的活性。耕作处理对各土层亮氨酸氨基肽酶活性的影响一致,表现为GL > CT > NT > SM,且各处理之间差异显著。秸秆还田提高了根际土壤中与碳转化相关酶的活性,降低了非根际土壤中与碳转化相关酶的活性。β-葡萄糖苷酶和乙酰氨基葡萄糖苷酶在参与土壤碳氮转化过程中起着更大的作用。
3) 在土壤有机质分解转化的过程中,碳氮转化相关酶活性之间彼此相互促进。碳氮转化相关酶与土壤总碳、总氮和有机碳之间均存在正相关关系 (除亮氨酸氨基肽酶与总碳之间),与C/N之间均存在负相关关系,且基本上显著相关。β-葡萄糖苷酶、β-纤维二糖苷酶、β-木糖苷酶和乙酰氨基葡萄糖苷酶在土壤碳氮元素的转化过程中起着十分重要的作用,是土壤碳氮循环的重要组成部分,可作为衡量土壤肥力理想的生物化学指标之一。
| [1] |
孙露莹. 玉米不同种植模式对土壤酶活性及微生物量碳氮的影响[D]. 北京: 中国科学院研究生院(东北地理与农业生态研究所)硕士学位论文, 2015.
Sun L Y. Effect of different planting patterns of maize on soil enzyme activities and microbial biomass carbon and nitrogen [D]. Beijing: MS Thesis of Chinese Academy of Sciences(Northeast Institute of Geography and Agroecology), 2015. |
| [2] | Bandick A K, Dick R P. Field management effects on soil enzyme activities[J]. Soil Biology & Biochemistry, 1999, 31(11): 1471–1479. DOI:10.1016/S0038-0717(99)00051-6 |
| [3] | Acosta-Martinez V, Harmel R D. Soil microbial communities and enzyme activities under various poultry litter application rates[J]. Journal of Environmental Quality, 2006, 35(4): 1309–1318. DOI:10.2134/jeq2005.0470 |
| [4] |
黄巧云, 林启美, 徐建明. 土壤生物化学[M]. 北京: 高等教育出版社, 2015.
Huang Q Y, Lin Q M, Xu J M. Soil biochemistry [M]. Beijing: Higher Education Press, 2015. |
| [5] | Burns R G, Dick R P. Enzymes in the environment: activity, ecology and applications[M]. New York: Marcel Dekker Inc, 2002. |
| [6] | Gispert M, Emran M, Pardini G, et al. The impact of land management and abandonment on soil enzymatic activity, glomalin content and aggregate stability[J]. Geoderma, 2013, 202: 51–61. DOI:10.1016/j.geoderma.2013.03.012 |
| [7] | Abdalla K, Chivenge P, Ciais P, et al. Notillage lessens soil CO2 emissions the most under arid and sandy soil conditions: results from a meta-analysis [J]. Biogeosciences, 2017, 12: 15495–15535. |
| [8] | Zuber S M, Villamil M B. Meta-analysis approach to assess effect of tillage on microbial biomass and enzyme activities[J]. Soil Biology & Biochemistry, 2016, 97: 176–187. |
| [9] |
梁国鹏, Albert A H, 吴会军, 等. 施氮量对夏玉米根际和非根际土壤酶活性及氮含量的影响[J].
应用生态学报, 2016, 27(6): 1917–1924.
Liang G P, Albert A H, Wu H J, et al. Soil nitrogen content and enzyme activities in rhizosphere and non-rhizosphere of summer maize under different nitrogen application rates[J]. Chinese Journal of Applied Ecology, 2016, 27(6): 1917–1924. |
| [10] | Christensen B T. Physical fractionation of soil and structural and functional complexity in organic matter turnover[J]. European Journal of Soil Science, 2001, 52(3): 345–353. DOI:10.1046/j.1365-2389.2001.00417.x |
| [11] |
谢泽宇, 罗珠珠, 李玲玲, 等. 黄土高原不同粮草种植模式土壤碳氮及土壤酶活性[J].
草业科学, 2017, 34(11): 2191–2199.
Xie Z Y, Luo Z Z, Li L L, et al. Soil carbon and nitrogen and soil enzyme activities of different forage planting model on the Loess Plateau[J]. Pratacultural Science, 2017, 34(11): 2191–2199. |
| [12] |
王晓凌, 陈明灿, 张雷. 不同耕作方式对土壤微生物量和土壤酶活性的影响[J].
安徽农学通报, 2007, 13(12): 28–30.
Wang X L, Chen M C, Zhang L. Effects of different tillage methods on soil microbial biomass and soil enzyme activities[J]. Anhui Agricultural Science Bulletin, 2007, 13(12): 28–30. DOI:10.3969/j.issn.1007-7731.2007.12.014 |
| [13] |
戴志刚, 鲁剑巍, 周先竹, 等. 不同耕作模式下秸秆还田对土壤理化性质的影响[J].
中国农技推广, 2012, 28(3): 46–48.
Dai Z G, Lu J W, Zhou X Z, et al. Effects of straw returning on soil physical and chemical properties under different tillage patterns[J]. China Agricultural Technology Extension, 2012, 28(3): 46–48. DOI:10.3969/j.issn.1002-381X.2012.03.029 |
| [14] |
高秀君, 张仁陟, 杨招弟. 不同耕作方式对旱地土壤酶活性动态的影响[J].
土壤通报, 2008, 39(5): 1012–1016.
Gao X J, Zhang R Z, Yang Z D. Effects of different tillage practices on the dynamics of soil enzyme activities in dryland[J]. Chinese Journal of Soil Science, 2008, 39(5): 1012–1016. DOI:10.3321/j.issn:0564-3945.2008.05.009 |
| [15] |
崔雯雯, 宋全昊, 高小丽, 等. 糜子不同种植方式对土壤酶活性及养分的影响[J].
植物营养与肥料学报, 2015, 21(1): 234–240.
Cui W W, Song Q H, Gao X L, et al. Influence of different cropping patterns on soil enzyme activities and yield of broomcorn millet[J]. Journal of Plant Nutrition and Fertilizer, 2015, 21(1): 234–240. |
| [16] | Saiya-Cork K R, Sinsabaugh R L, Zak D R. The effects of long term nitrogen deposition on extracellular enzyme activity in an Acer saccharum, forest soil[J]. Soil Biology & Biochemistry, 2002, 34(9): 1309–1315. |
| [17] | Deforest J L. The influence of time, storage temperature, and substrate age on potential soil enzyme activity in acidic forest soils using MUB-linked substrates and L-DOPA[J]. Soil Biology & Biochemistry, 2009, 41(6): 1180–1186. |
| [18] |
陈娟, 马忠明, 刘莉莉, 等. 不同耕作方式对土壤有机碳、微生物量及酶活性的影响[J].
植物营养与肥料学报, 2016, 22(3): 667–675.
Chen J, Ma Z M, Liu L L, et al. Effect of tillage system on soil organic carbon, microbial biomass and enzyme activities[J]. Journal of Plant Nutrition and Fertilizer, 2016, 22(3): 667–675. |
| [19] |
姜学兵, 李运生, 欧阳竹, 等. 免耕对土壤团聚体特征以及有机碳储量的影响[J].
中国生态农业学报, 2012, 20(3): 270–279.
Jiang X B, Li Y S, Ouyang Z, et al. Effect of no-tillage on soil aggregate and organic carbon storage[J]. Chinese Journal of Eco-Agriculture, 2012, 20(3): 270–279. |
| [20] |
李景, 吴会军, 武雪萍, 等. 长期保护性耕作提高土壤大团聚体含量及团聚体有机碳的作用[J].
植物营养与肥料学报, 2015, 21(2): 378–386.
Li J, Wu H J, Wu X P, et al. Impact of long-term conservation tillage on soil aggregate formation and aggregate organic carbon contents[J]. Journal of Plant Nutrition and Fertilizer, 2015, 21(2): 378–386. |
| [21] | Six J, Bossuyt H, Degryze S, Denef K. A history of research on the link between (micro) aggregates, soil biota and soil organic matter dynamics[J]. Soil and Tillage Research, 2004, 79(1): 7–31. DOI:10.1016/j.still.2004.03.008 |
| [22] |
丁晋利. 保护性耕作农田土壤水碳氮演变特征及模型模拟[D]. 陕西杨凌: 西北农林科技大学博士学位论文, 2017.
Ding J L. Change characteristics of conservation tillage on soil water, carbon and nitrogen in farmland[D]. Yangling, Shaanxi: PhD Dissertation of Northwest A&F University, 2017. |
| [23] |
许菁, 李晓莎, 许姣姣, 等. 长期保护性耕作对麦-玉两熟农田土壤碳氮储量及固碳固氮潜力的影响[J].
水土保持学报, 2015, 29(6): 191–196.
Xu J, Li X S, Xu J J, et al. Effects of long-term conservation tillage on soil organic carbon and nitrogen storages, soil carbon sequestration potential and nitrogen fixation potential in wheat maize crop system[J]. Journal of Soil and Water Conservation, 2015, 29(6): 191–196. |
| [24] | López-Fando C, Pardo M T. Use of a partial-width tillage system maintains benefits of no-tillage in increasing total soil nitrogen[J]. Soil & Tillage Research, 2012, 118(5): 32–39. |
| [25] | Sinsabaugh R. Fungal enzymes at the community scale [J]. Fungal Community, 2004, doi: 10.1201/9781420027891.ch17. |
| [26] | Sinsabaugh R, Lauber C, Weintraub M, et al. Stoichiometry of soil enzyme activity at global scale[J]. Ecology Letters, 2008, 11(11): 1252–1264. DOI:10.1111/ele.2008.11.issue-11 |
| [27] |
何翠翠. 长期不同施肥措施对黑土土壤碳库及其酶活性的影响研究[D]. 北京: 中国农业科学院硕士学位论文, 2014.
He C C. Effects of long-term fertilization on soil carbon pools and enzymes activity of black soil in cropland of northeast China[D]. Beijing: MS Thesis of Chinese Academy of Agricultural Sciences, 2014. |
| [28] |
黄召存. 不同耕作方式对蚕豆根际土壤微生物和酶活性的影响[D]. 重庆: 西南大学硕士学位论文, 2015.
Huang Z C. Effects of tillage modes on soil microbes and enzyme activity in rhizosphere of broad bean [D]. Chongqing: MS Thesis of Southwest University, 2015. |
| [29] |
孙敬克, 李友军, 黄明, 等. 不同耕作方式对冬小麦生育期根际土及非根际土土壤酶活性的影响[J].
河南科技大学学报(自然科学版), 2007, 28(2): 59–62.
Sun J K, Li Y J, Huang M, et al. Effects of different tillage on rhizosphere and non-rhizosphere soil enzyme activity of winter wheat at different developing stages[J]. Journal of Henan University of Science and Technology (Natural Science Edition), 2007, 28(2): 59–62. DOI:10.3969/j.issn.1672-6871.2007.02.017 |
| [30] |
孙萌, 刘洋, 李寒, 等. 有机物覆盖对核桃园土壤有机碳库及酶活性的影响[J].
植物营养与肥料学报, 2018, 24(1): 270–278.
Sun M, Liu Y, LI H, et al. Effects of organic mulching on soil organic carbon pool and soil enzyme activity in walnut orchard[J]. Journal of Plant Nutrition and Fertilizers, 2018, 24(1): 270–278. |
| [31] | Ekenler M, Tabatabai M A. Beta-Glucosaminidase activity of soils: effect of cropping systems and its relationship to nitrogen mineralization[J]. Biology & Fertility of Soils, 2002, 36(5): 367–376. |
 2018, Vol. 24
2018, Vol. 24  doi:
doi: 

