磷肥是世界上最早应用的化学肥料,自1843年世界上第一种化学肥料—过磷酸钙问世以来[1],磷肥应用于农业生产已有170多年的历史[2]。迄今,农业生产所施用的磷肥主要以正磷酸为主[3]。土壤中Ca2+、Mg2+、Al3+、Fe3+ 等离子易与肥料中的磷酸根发生化学沉淀反应,致使大部分施入土壤的磷转化为无效磷 (难溶态) 积累在土壤中[4],从而导致磷肥当季利用率一般只有7.3%~20.1% [5]。大量积累在土壤中的磷还可引发水体污染等环境问题[6–7]。晚近研究表明聚磷酸类磷肥可显著促进作物生长,提高磷肥利用率[8–9]。因此,聚磷酸类磷肥作为新的替代磷源在国内外广受关注[10]。
聚磷酸 (Poly-P) 是磷分子间通过共价缩合 (P-P) 而成的直链或支链型结构聚合物[11]。当聚合度小于20时 (n < 20),其可作为磷肥单独施用,也可作为基础肥源与其他NPK复合形成复混肥施用。通常聚磷酸磷肥多以不同聚合度和聚合率的无机磷混合物形式存在。如澳大利亚聚磷酸铵肥料中25%以正磷酸盐存在,50%~55%以焦磷酸形式存在,其余20%~25%以三聚及三聚以上的形式存在 [12]。研究发现,液体聚磷酸铵肥料较磷酸一铵可显著提高小麦产量[13],其增产幅度可达36%[14]。Jain等[15]通过两年大田试验研究发现,聚磷酸铵肥料显著提高了大豆产量。Torres-Dorante等[16]通过盆栽试验表明,聚磷酸磷肥可显著提高土壤有效磷含量与植株吸磷量。其原因主要是由于聚磷酸磷肥中的磷是以聚合态 (Poly-P) 为主,故而减少了土壤固相对磷的吸附与固定,提高了土壤无机磷库中高活性磷 (如Resin-P、NaHCO3-P) 含量[17–18]。而另外一些研究则表明聚磷酸磷肥与正磷酸磷肥相比并无明显优势[19–20]。其可能的原因为:聚磷酸磷效应的发挥既受土壤结构、温度、pH、粘粒矿物、金属离子活度及土壤生物活性等土壤学性状的影响,也受聚磷酸类肥料表征指标聚合度 (衡量聚合物分子大小的指标) 与聚合率 (聚合态磷占总磷的百分含量) 的影响[16, 21]。聚磷酸类磷肥施入土壤后在土壤水解酶的作用下发生水解断链[22–23],聚合度越高 (链越长),水解断链速率越缓慢[24]。Busman等[25]研究发现环状三聚偏磷酸盐经水解首先转变为三聚磷酸盐 (n = 3),再水解为焦磷酸盐 (n = 2),最后水解为正磷酸盐。在水环境中,焦磷酸盐完全水解为正磷酸盐需要15天,而三聚偏磷酸盐90天时只能水解30%[16]。土壤质地也可显著影响聚磷酸盐水解,如聚磷酸在壤土中的水解速率要快于沙土[16]。Dick等[20]发现磷酸酶在中性土壤中有更大的活性,且聚磷酸处理显著提高了土壤有效磷及中微量元素含量[26]。此外,研究发现水溶性聚磷酸铵对微量元素Mg2+、Cu2+与Fe3+均有显著的螯合活化作用[27],较常规正磷酸肥料 (DAP),聚磷酸铵处理显著增加了土壤有效态Mn、Zn及植株对Mn与Zn的吸收量[28]。
石灰性土壤作为分布于干旱区主要的土壤类型,磷的固定发生强烈。本文以新疆灌耕灰漠土为供试土壤,通过盆栽试验初步探讨了不同聚合度与聚合率的聚磷酸类磷肥对土壤磷及微量元素有效性、土壤无机磷分级转化及肥料效应的影响。旨在揭示聚磷酸类磷肥有效磷的转化及其肥料效应机理,为提出适宜聚合度或聚合率参数的聚磷酸类磷肥及田间施用提供参考。
1 材料与方法 1.1 试验区概况试验于2017年6月中旬在新疆石河子市石河子大学试验站 (44˚18′N, 86˚02′E) 进行。该区属温带大陆性气候区,年平均气温7.5~8.2℃,≥ 10℃的活动积温为3729℃,无霜期为171天,年降水量与蒸发量分别为207.7和1500 mm,年日照时数为2818 h。
1.2 试验材料 1.2.1 供试土壤供试土壤为灌耕灰漠土 (Calcaric fluvisals),采自石河子大学试验站,土壤质地为壤土、土壤pH 8.0、电导率1.2 ms/cm、有机质15.8 g/kg、全磷0.8 g/kg、有效磷17.2 mg/kg、水溶性磷3.5 mg/kg、NaOH-P 11.2 mg/kg、HCl-P 481.9 mg/kg、Residue-P 252.2 mg/kg、有效态Fe 7.6 mg/kg、有效态Mn 7.1 mg/kg、有效态Zn 1.4 mg/kg、CaCO3 16.1%、无定型Fe2O3 285.8 mg/kg、无定型Al2O3 1519 mg/kg。
1.2.2 供试肥料供试磷肥分别为磷酸二氢铵 (MAP,N 12.1%,P2O5 61.8%,分析纯,白色晶体) 与聚磷酸铵 (APP,N 20%~30%,P2O5 45%~60%,白色粉末);供试氮肥为尿素 (Urea,N 46.7%,分析纯,白色晶体);供试钾肥为硫酸钾 (K2SO4,K2O 53.5%,分析纯,白色粉末)。
1.3 试验设计试验用规格为上端内径35 cm、下端内径 20 cm、高25 cm的陶瓷盆钵。待土壤风干后,过0.5 cm筛,除去植物根系及残膜等备用。试验共设5个处理:1) 不施磷肥 (CK);2) 磷酸二氢铵 (MAP);3) 聚磷酸铵,平均聚合度3,聚合率40% (APP-3-40%);4) 聚磷酸铵,平均聚合度3,聚合率90% (APP-3-90%);5) 聚磷酸铵,平均聚合度2.7,聚合率90% (APP-2.7-90%)。每个处理4次重复。按大田施肥量的3倍,所有处理保持施氮磷钾的总量一致,每钵施N 2.4 g,P2O5 1.1 g,K2O 0.7 g (其中MAP与APP所带的N,用Urea-N补充)。所有肥料的施肥方式均采用基施加追施,33%基施,67%追施 (分别于播种后的第30与60 d各随水施入33.5%)。每钵装土7.0 kg。种植作物为玉米,品种为先玉335 (Zea mays Lcv Xianyu 335)。选取大小均匀饱满的玉米种子于 2017年6月中旬播种,播种深度为2 cm左右,出苗后通过称重量法,保持全生育期土壤含水量为最大田间持水量的60%~65%,待幼苗5~6片可见叶时,每钵定苗4株,10月中旬试验结束,试验共计90 d。
1.4 测定项目与方法 1.4.1 土壤样品采集与测定采用微型打孔器,每钵6个取样点,取样深度为20 cm,于播种后第10、20、30、40、50、60、70、80、90 d取土样并混合均匀 (追肥当天土壤为追施前取样),风干后过2 mm筛,测定土壤水溶性磷与有效磷,水溶性磷 (Water-P) 采用孔雀绿比色法,有效磷 (Olsen-P) 采用0.5 mol/L NaHCO3浸提法。第90 d土样测定土壤全磷、磷分级及土壤有效态Fe、Mn与Zn含量,全磷采用HClO4–H2SO4法,磷分级采用Guppy法[18],有效态微量元素采用M3浸提法,浸提液用ICP进行测定[29] (ICAP6300, Inc., USA)。
1.4.2 植株样品采集与测定玉米植株样品分别于播种后第45和90 d每钵各取两株 (本试验选取第90 d样品数据)。植株样品采集后用自来水洗净,于105℃下杀青半小时,75℃烘干至恒重,测定干物质,粉碎,过0.25 mm筛,备用。植株样品测定含磷量与微量元素Fe、Mn与Zn含量。植株含磷量测定采用H2SO4–H2O2消煮,钒钼黄比色法。微量元素测定采用HNO3–H2O2–HF (3∶1∶1) 消解法,消解液用ICP测定 (ICAP6300, Inc. USA)。
1.4.3 磷肥利用率计算磷肥利用率 (PUE,%) = (U–U0)/F×100,其中U为施磷肥处理作物收获时地上部的吸磷总量,U0为未施磷处理作物收获时地上部的吸磷总量,F代表外施磷源总量。
本试验磷肥利用率为第90 d时每株玉米的磷肥利用率。
1.5 数据分析采用Excel和多元统计分析软件Graph Pad Prism5.0 software (Graphpad software, Inc., USA) 进行图表制作。使用SPSS 17.0 software统计分析软件 (SPSS Inc., Chicago) 进行方差分析 (ANOVA),处理间的差异显著性采用Duncan法进行多重比较。
2 结果与分析 2.1 不同聚合度和聚合率聚磷酸磷肥对土壤有效态磷的影响由图1可知,三个APP处理土壤水溶性磷与有效磷含量的平均值较MAP处理分别显著增加了21.8%与25.3%。三个APP肥料相比,在相同聚合度条件下 (n = 3),聚合率为90%处理的土壤水溶性磷与有效磷比聚合率为40%处理的分别提高了15.7%与7.9%;在相同聚合率条件下 (90%),聚合度为3处理的土壤有效磷比聚合度为2.7处理的提高了5.0% (图2)。播种后60~90 d时,土壤水溶性磷与有效磷含量随聚合度与聚合率的增大呈上升趋势。在播种0~50 d时,由于水解效应,高聚合度与聚合率处理的土壤水溶性磷、有效磷含量明显低于低聚合度与聚合率处理的;在70 d时,则表现出相反趋势,如APP-3-90% 处理的土壤有效磷较APP-3-40% 与APP-2.7-90%处理的分别增加了32.2%与25.1%。在整个生长期,APP处理显著提高了土壤水溶性磷与有效磷含量,且土壤有效磷含量随聚合度与聚合率的增加而显著提高;土壤水溶性磷含量随聚合率的提高而显著提高,但不同聚合度处理差异不显著。
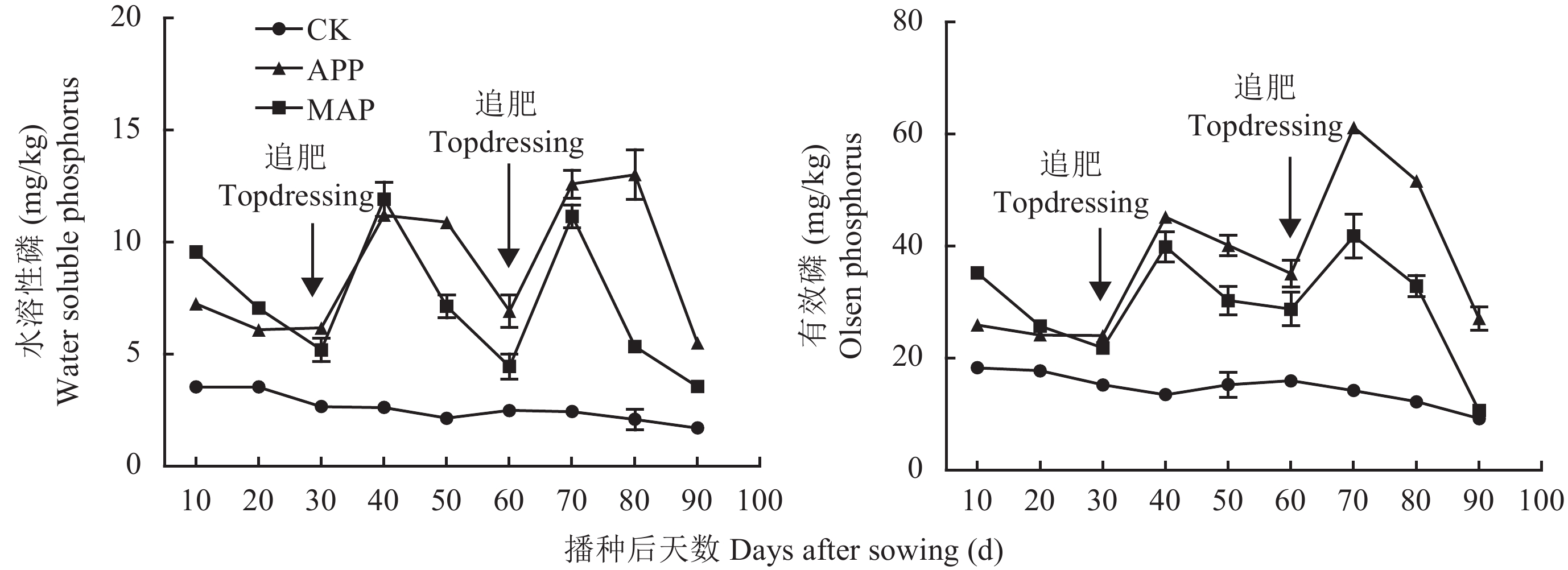 |
| 图1 不同磷肥处理对土壤水溶性磷与有效磷含量的影响 Fig. 1 Influences of different P sources treatments on water-P and Olsen-P concentrations [注(Note):APP—所有聚磷酸处理的均值 Average of all polyphosphate treatments.] |
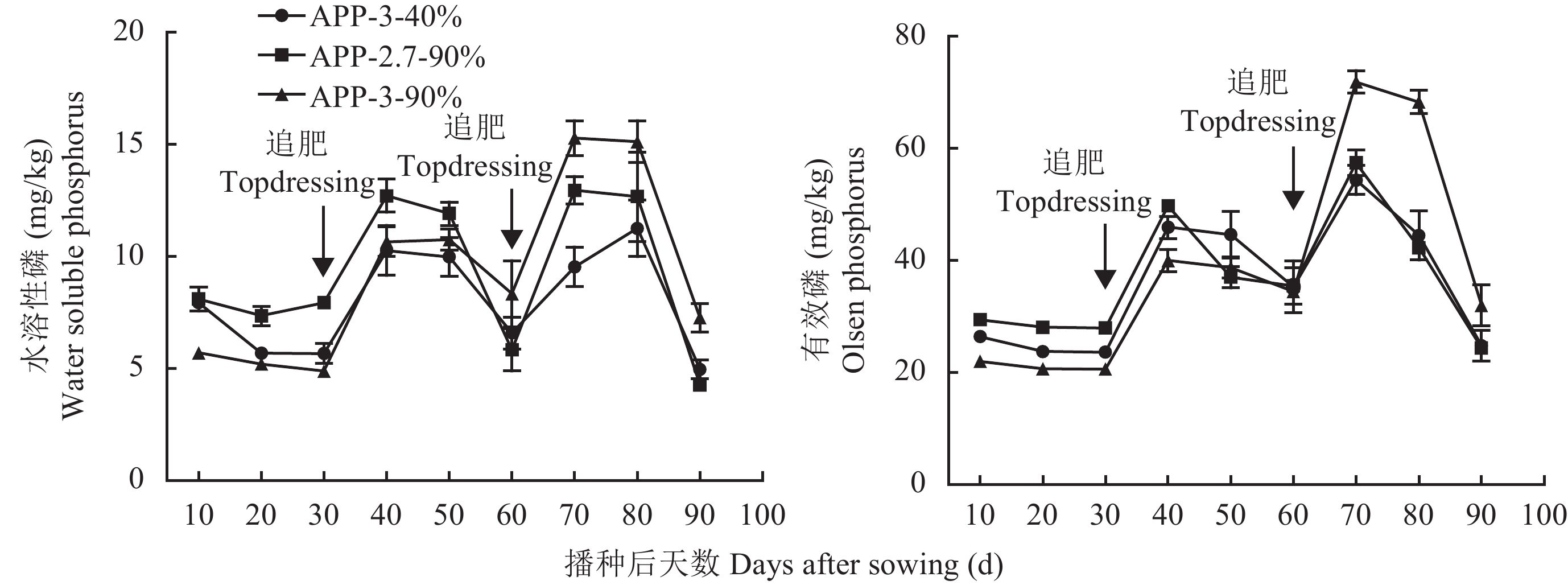 |
| 图2 不同聚磷酸铵处理对土壤水溶性磷与有效磷含量的影响 Fig. 2 Influences of different APP treatments on water-P and Olsen-P concentrations |
不同聚合度与聚合率的聚磷酸类磷肥对土壤中各级磷转化有显著影响。不同聚合度和聚合率聚磷酸磷肥处理的Resin-P和NaHCO3-P明显高于对照 (图3)。在相同聚合度条件下 (n = 3),聚合率为90%处理的土壤Resin-P与NaHCO3-P比聚合率为40%处理的分别提高了38.0%和22.8% (图3c);在相同聚合率条件下 (90%),聚合度为3处理的土壤Resin-P与NaHCO3-P比聚合度为2.7处理的分别提高了75.1%与34.2%,且土壤NaOH-P、HCl-P与Residue-P随聚合度与聚合率的增大呈现降低趋势,其中HCl-P含量差异达到显著水平 (图2c)。对于APP与MAP处理,APP处理可显著提高土壤Resin-P和NaHCO3-P含量,降低土壤HCl-P含量 (图3a)。APP较MAP处理,土壤Resin-P和NaHCO3-P含量分别提高了1.6和6.4 mg/kg,HCl-P含量降低了38.1 mg/kg。由图3 (b, d) 可知,APP处理的土壤高活性磷及中活性磷 (Resin-P+NaHCO3-P+ NaOH-P) 较MAP处理提高了21%,不同聚合度处理中,APP-3-90%处理较APP-2.7-90%处理提高了26.5%,而不同聚合率处理没有显著差异。表明聚磷酸磷肥聚合度的提高可显著提高土壤高活性磷含量,减少土壤对P的固定作用。
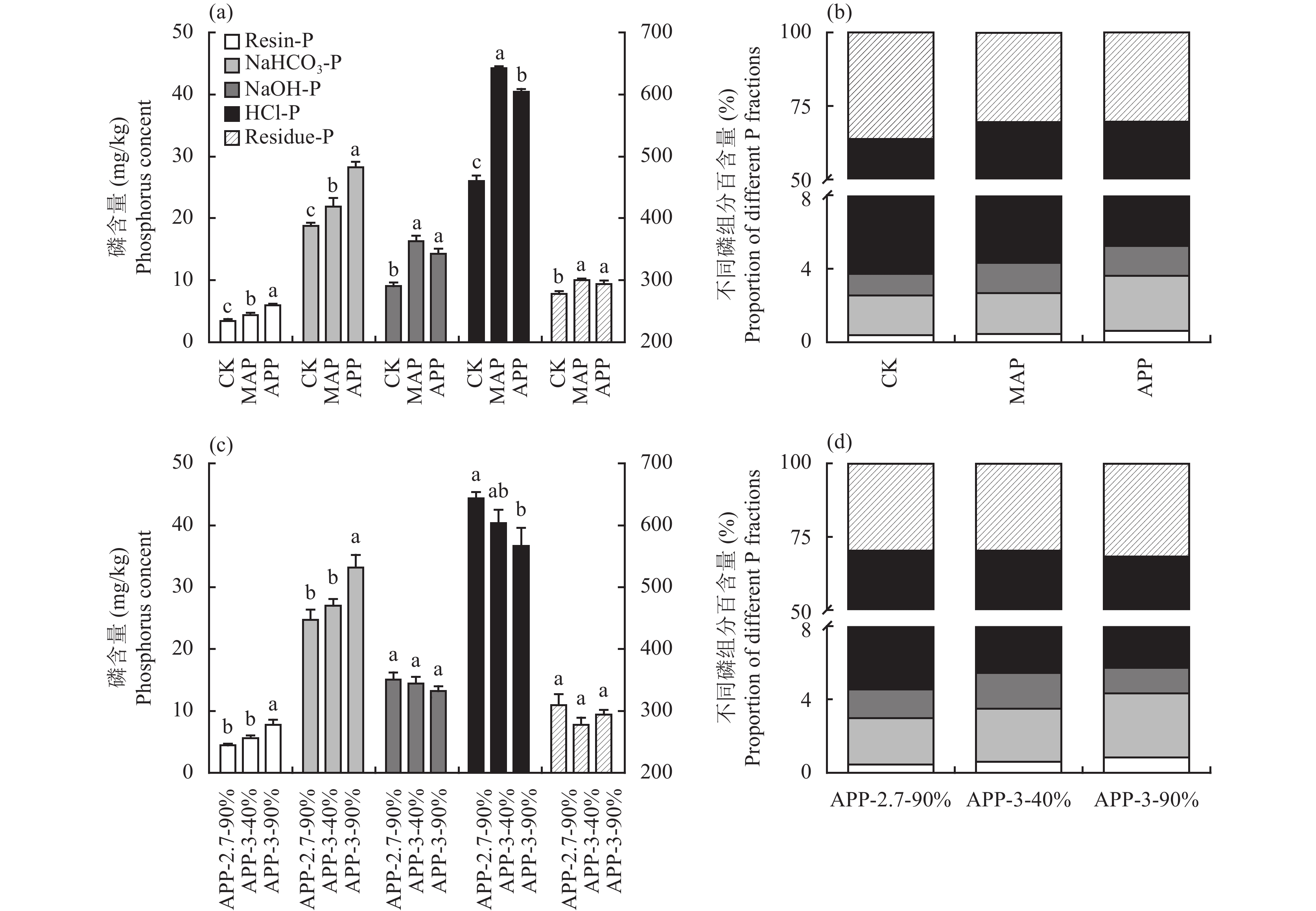 |
| 图3 不同磷肥处理对土壤各形态无机磷组分的影响 Fig. 3 Effects of different P sources on the variation of soil inorganic P fractionations [注(Note):APP—所有聚磷酸处理的均值The averaged value of all polyphosphate treatments;柱上不同字母表示处理间差异达到显著水平Values followed by different letters mean significant difference among the treatments (P < 0.05).] |
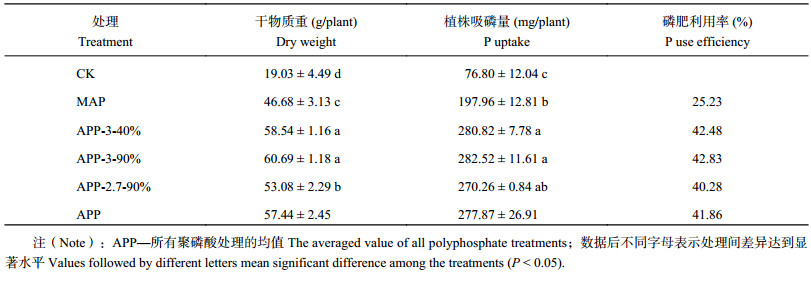
聚磷酸磷肥可显著提高玉米干物质重、吸磷量及肥料利用率 (表1)。3种聚磷酸磷肥处理的玉米干物质重、植株吸磷量及肥料利用率均值分别比MAP处理的提高了23.1%、40.4%与65.9%。在相同聚合率条件下 (90%),聚合度为3的聚磷酸铵处理的玉米干物质重、植株吸磷量及肥料利用率分别较聚合度为2.7处理的提高了14.3%、4.5%与6.3%;然而在相同聚合度条件下 (n = 3),不同聚合率处理对玉米干物质重、植株吸磷量与肥料利用率并没有显著性影响。表明,聚磷酸类磷肥聚合度的提高较聚合率更好地促进了作物的生长与磷素营养水平。
| 表1 不同磷源对玉米植株干物质重、吸磷量及磷肥利用率的影响 Table 1 Effects of different P sources on maize dry weight, P uptake of plant and P use efficiency |
 |
由表2可知,APP处理显著提高了土壤中有效态Fe、Mn和Zn含量。3个APP处理土壤有效态Fe、Mn和Zn含量的平均值分别较MAP处理的提高了22.4%、13.0%和29.4%。在不同聚合度处理条件下 (90%),土壤有效态Fe、Mn和Zn含量均表现为:APP-3-90% > APP-2.7-90%。在不同聚合率条件下 ( n = 3),聚合率为90%处理的土壤有效态Zn含量比聚合率为40%处理的提高了11.9%。同时,APP处理显著提高了玉米植株对Fe、Mn和Zn吸收量。与MAP处理相比,APP-3-40%处理植株的Fe、Mn和Zn吸收量提高了99.0%、55.3%和75.7%。不同聚合度处理对玉米Fe和Zn的吸收表现为:APP-3-90% > APP-2.7-90%,APP-3-90%处理的玉米对Zn的吸收量较APP-2.7-90%处理的增加了19.5%,而不同聚合率处理植株对Fe、Mn和Zn的吸收量无显著性差异。表明高聚合度 ( n = 3) 与高聚合率 (90%) 聚磷酸磷肥对土壤微量元素Fe、Mn和Zn的活化有显著效应。
| 表2 不同磷源对土壤有效态Fe、Mn和Zn水平与植株Fe、Mn和Zn吸收量的影响 Table 2 Effects of different P sources on soil available Fe, Mn, Zn and maize plant Fe, Mn, Zn uptake |
 |
本试验结果表明,虽然聚磷酸磷肥施入初期土壤溶液中有效磷含量 (图1) 显著低于磷酸一铵处理的,但尔后则逐渐升高,后期明显高于MAP处理。研究发现,聚磷酸盐更容易被土壤粘粒吸附,与磷酸根离子竞争吸附位点,从而导致土壤磷含量增加[16]。McBeath等[21]和Mnkenie等[30]研究发现,土壤粘粒对焦磷酸比正磷酸具有更强的吸附亲和力。Philen等[31]认为焦磷酸与土壤金属离子发生沉淀反应的速率要显著低于正磷酸肥料。不同聚合度/聚合率聚磷酸肥料在土壤生物学/化学的水解作用下逐渐水解为正磷酸根被作物吸收,降低了发生沉淀反应的机率。因此,聚磷酸提高土壤磷的有效性可能归因于聚磷酸磷肥的逐渐水解作用,而正磷酸磷肥则在土壤中被快速沉淀固定[25]。本试验表明,聚磷酸类磷肥处理较MAP处理降低了土壤低活性磷 (HCl-P,Residue-P) 与中活性磷 (NaOH-P) 含量,增加了土壤高活性磷 (Resin-P,NaHCO3-P) 含量[17]。
影响聚磷酸盐水解的因素包括土壤酶活性[32]、土壤固相对聚磷酸盐的吸附、沉淀强度及聚磷酸类磷肥的聚合特性 (聚合度、聚合率) 等[20]。其中,聚合度是显著影响聚磷酸盐水解的主要因素,如线性四聚磷酸较正磷酸肥料可显著提高土壤磷的有效性[20]。本研究发现,在相同聚合率条件下 (90%),聚合度为3的处理土壤有效磷含量明显高于聚合度为2.7的处理。说明聚合程度越高其提高土壤有效磷含量的效果越好。此外,土壤有效磷的提高同时也显著影响着作物地上部的生长[33],聚磷酸磷肥的肥效最终应在作物的响应上得到印证。研究发现其增产效果在水稻、鹰嘴豆、大豆[15, 34–35]等不同作物上均有体现。如EL-Sayed[28]研究发现,聚磷酸肥料处理显著增加了向日葵的吸磷量且在施肥后的第三年,177.5 kg/hm2 磷处理时,APP较DAP处理向日葵产量增加了750 kg/hm2。本试验结果也显示,植株吸磷量与土壤有效磷含量呈现显著线性相关,植株干物质重与含磷量也呈显著线性相关 (图4)。
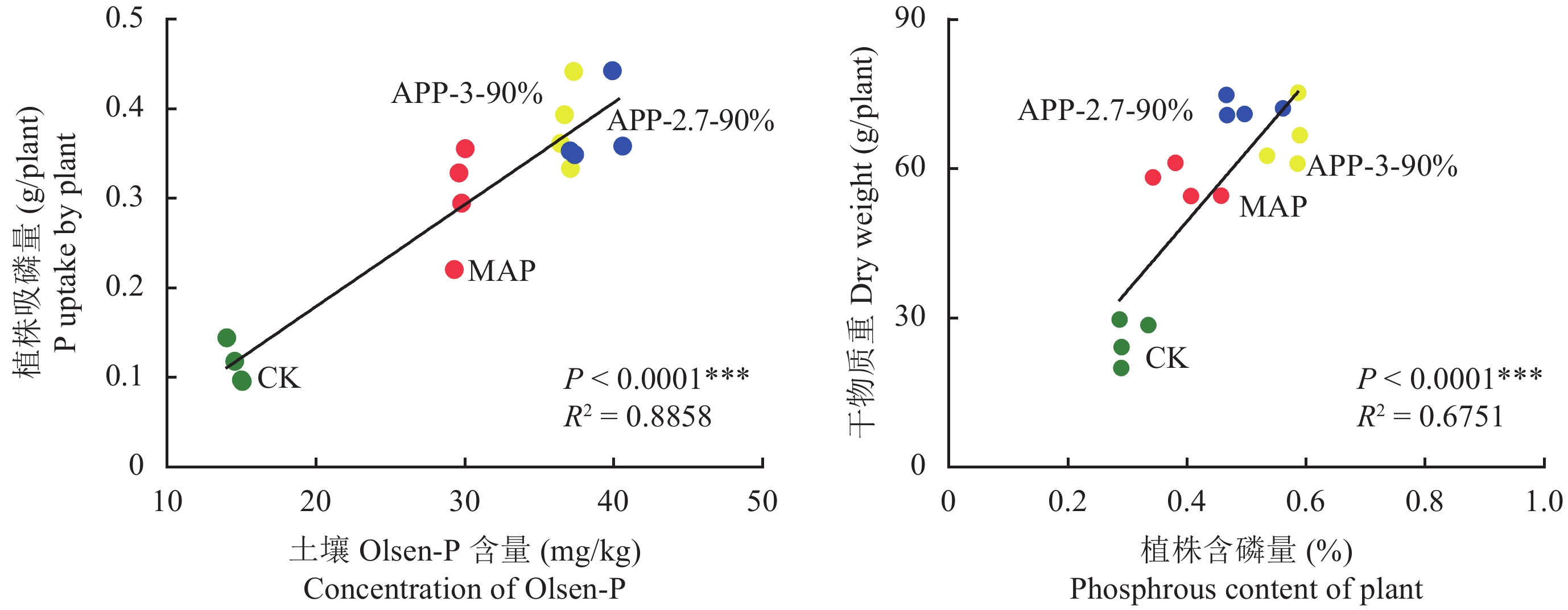 |
| 图4 玉米吸磷量与土壤有效态磷及植株干物质重与植株含磷量的相关性 Fig. 4 Correlations between maize P uptake and soil Olsen-P concentration, plant dry weight and plant P concentration |
螯合是螯合物形成体 (中心离子) 与特定螯合剂 (配位体) 配合而形成具有环状结构配合物的过程。其形成的条件首先是螯合剂必须有两个或两个以上都能给出电子对的配位原子 (主要是N、O、S等原子)。其次,每两个能给出电子对的配位原子,必须隔着两个或三个其他原子,唯有此才可形成稳定的原子环[36]。聚磷酸铵 (NH4)n+2PnO3n+1分子中能给出电子的羟基氧与铵根离子之间隔着n个P与O,故聚磷酸铵能很好地螯合土壤中的微量元素。研究表明,聚磷酸磷可通过螯合反应提高土壤有效Zn、Mn及Fe的含量[21, 35, 37]。因此,在石灰性土壤中聚磷酸盐与微量元素金属离子螯合反应可能是其提高土壤微量元素有效性的作用机理。El-Sayed[28]研究发现聚磷酸铵处理可显著提高向日葵植株对Mn与Zn的吸收。本研究证实了APP处理不但可提高土壤有效态Fe、Mn和Zn含量,也提高了植株对其Fe、Mn与Zn的吸收 (表2, 图5);同时,植株对Fe、Mn和Zn的吸收量与土壤有效态Fe、Mn和Zn含量呈显著的正相关 (图5)。另一方面,本研究发现聚合度为 (APP-3-90%) 处理的土壤有效态Zn含量较聚合度为 (APP-2.7-90%) 处理的提高了29.9%,说明聚合度与聚合率对土壤微量元素有效性也有一定影响。聚磷酸磷与石灰性土壤中的钙八磷 (Ca8-P)、铁磷 (Fe-P)、铝磷 (Al-P) 的磷竞争络合位点也是其释放和活化微量元素的原因之一[26]。本试验结果也表明,MAP处理较不施肥 (CK) 处理提高了土壤有效Fe、Mn和Zn含量。在缺磷土壤,植物通过分泌低分子有机酸 (如柠檬酸、草酸、苹果酸和酒石酸钾等) 可导致根际土壤微酸化并与磷酸根竞争土壤溶液中的微量元素,从而与土壤铁铝氧化物及无效态微量元素发生络合反应,提高微量元素的有效性[38]。这一结论也被Dinkelaker等[39]的研究结果所证实。
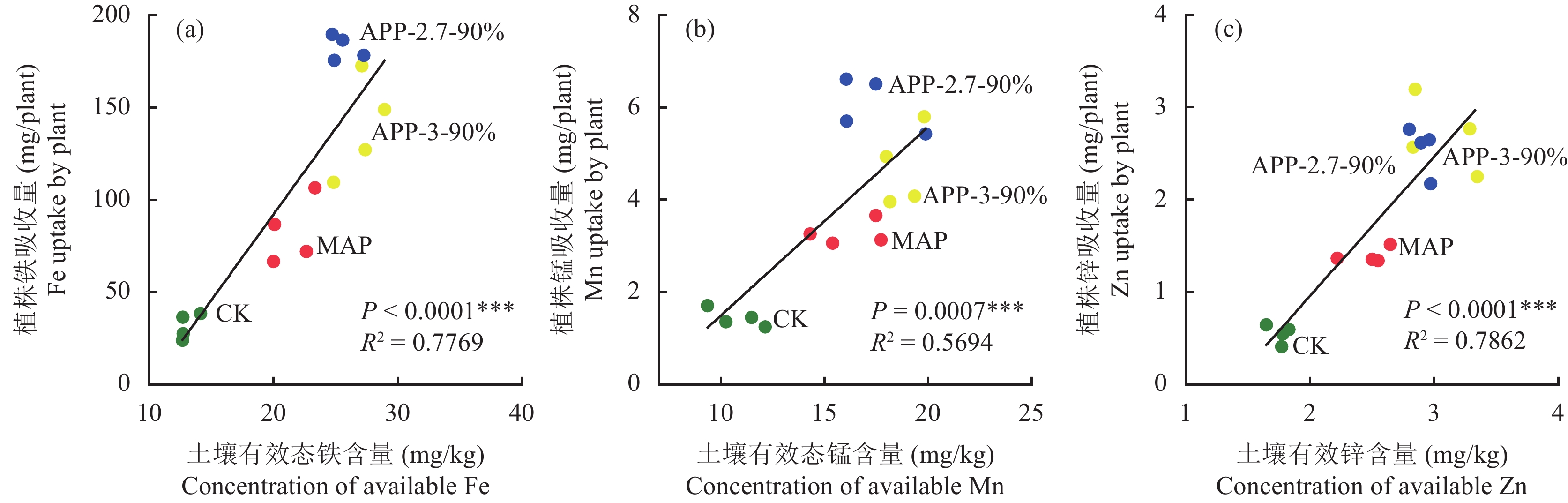 |
| 图5 玉米植株Fe、Mn和Zn营养与土壤有效Fe、Mn和Zn的相关性 Fig. 5 Correlations between maize plant Fe, Mn, Zn nutritional status and soil available Fe, Mn, Zn |
1) 聚磷酸类磷肥 (APP) 较正磷酸磷肥 (MAP) 显著提高了石灰性土壤磷的有效性与磷肥肥效。聚合度对土壤有效磷及磷肥肥效的影响大于聚合率,不同聚合率间差异不明显。
2) 聚磷酸类磷肥 (APP) 较正磷酸磷肥 (MAP) 显著增加了土壤高活性Resin-P与NaHCO3-P,降低了中活性NaOH-P及低活性HCl-P与Residue-P含量,且聚合度与聚合率越高土壤活性磷 (Resin-P,NaHCO3-P) 含量越高,说明聚磷酸磷肥可显著减少土壤对磷的固定作用。
3)聚磷酸类磷肥 (APP) 可显著提高土壤有效态Fe、Mn与Zn含量。增加聚磷酸磷肥的聚合度可显著增加微量元素的有效性,但聚合率对微量元素有效性的影响不显著。
| [1] |
闫湘. 我国化肥利用现状与养分资源高效利用研究[D]. 北京: 中国农业科学院博士论文, 2008.
Yan X. Study on present status of chemical fertilizer application and high efficient utilization of nutrition in China[D]. Beijing: PhD Dissertation of Chinese Academy of Agricultural Sciences, 2008. |
| [2] | Mardamootoo T, Kwong K, Preez C. History of phosphorus fertilizer usage and its impact on the agronomic phosphorus status of sugarcane soils in Mauritius[J]. Sugar Technology, 2010, 12(2): 91–97. DOI:10.1007/s12355-010-0019-3 |
| [3] | Havlin J L, Tisdale S L, Nelson W L, et al. Soil fertility and fertilizers: An introduction to nutrient management[M]. Upper Saddle River, NJ: Pearson Prentice Hall, 2014. |
| [4] | Hedley M, McLaughlin M. Reactions of phosphate fertilizers and by-products in soils[M]. Phosphorus: Agriculture and the Environment, 2005, 181–252. |
| [5] |
鲁如坤, 时正元, 顾益初. 土壤积累态磷研究Ⅱ.磷肥的表观积累利用率[J].
土壤, 1995, (6): 286–289.
Lu R K, Shi Z Y, Gu Y C. Research on accumulative phosphorus in soilsⅡ. The apparent accumulation of phosphate fertilizer utilization[J]. Soils, 1995, (6): 286–289. |
| [6] | Saleque M A, Abedin M J, Bhuiyan N I, et al. Long-term effects of inorganic and organic fertilizer sources on yield and nutrient accumulation of lowland rice[J]. Field Crops Research, 2004, 86(1): 53–65. DOI:10.1016/S0378-4290(03)00119-9 |
| [7] | Kuo S, Huang B, Bembenek R. Effects of long-term phosphorus fertilization and winter cover cropping on soil phosphorus transformations in less weathered soil[J]. Biology and Fertility of Soils, 2005, 41(2): 116–123. DOI:10.1007/s00374-004-0807-6 |
| [8] |
王方进. 低聚磷酸铵肥料的合成及其在土壤中的转化研究[D]. 泰安: 山东农业大学硕士论文, 2014.
Wang F J. Synthesis of ammonium low-polyphosphate fertilizer and its transformation in soil[D]. Tai'an: MS Thesis of Shandong Agricultural University, 2014. |
| [9] |
王连祥. 农用肥料聚磷酸铵的制备与应用[J].
磷肥与复肥, 2008, 23(2): 49–50.
Wang L X. The preparation and application of agricultural ammonium polyphosphate system[J]. Phosphate and Compound Fertilizer, 2008, 23(2): 49–50. DOI:10.3969/j.issn.1007-6220.2008.02.019 |
| [10] |
徐保明, 徐思思, 唐强, 等. 水溶性聚磷酸铵的合成工艺进展[J].
无机盐工业, 2017, 49(4): 5–8.
Xu B M, Xu S S, Tang Q, et al. Progress in synthesis of water-soluble ammonium polyphosphate[J]. Inorganic Chemicals Industry, 2017, 49(4): 5–8. |
| [11] | Niemeyer R. Cyclic condensed metaphosphates in plants and the possible correlations between inorganic polyphosphates and other compounds[J]. Progress in Molecular and Subcellular Biology, 1999, 23(1): 83–100. |
| [12] | Mcbeath T M, Smernik R J, Lombi E, et al. Hydrolysis of pyrophosphate in a highly calcareous soil: A solid-state phosphorus31 NMR study[J]. Soil Science Society of America Journal, 2006, 70(3): 856–862. DOI:10.2136/sssaj2005.0184 |
| [13] | Venugopalan M V, Prasad R. Relative efficiency of ammonium polyphosphate and orthophosphates for wheat and their residual effects on succeeding cowpea fodder[J]. Nutrient Cycling in Agro-ecosystems, 1989, 20(2): 109–114. |
| [14] | Holloway R E, Frischke A J, Dot Brace. "How much fluid P fertilizer is enough?" Eyre peninsula farming systems summary[M]. Pt. Lincoln, Australia: South Australian Research and Development Institute, 2002, 84–89. |
| [15] | Jain S C, Kushwaha S S. Effect of ammonium polyphosphate on the yield of soybean (Glycine max L.) [J]. Indian Journal of Agronomy, 1993, 38: 33–36. |
| [16] | Torres-Dorante L O, Claassen N, Steingrobe B, et al. Fertilizer use efficiency of different inorganic polyphosphate sources: effects on soil P availability and plant P acquisition during early growth of corn[J]. Journal of Plant Nutrition and Soil Science, 2006, 169(4): 509–515. DOI:10.1002/(ISSN)1522-2624 |
| [17] |
王静. 不同施磷策略对磷在土壤中移动、转化及磷肥利用率的影响[D]. 石河子: 石河子大学硕士学位论文, 2016.
Wang J. Effects of phosphate fertilizer application strategies on soil P mobility, transformation and P use efficiency on calcareous soil[D]. Shihezi: MS Thesis of Shihezi University, 2016. |
| [18] | Guppy C N, Menzies N W, Moody P W, et al. A simplified sequential phosphorus fractionation method[J]. Communications in Soil Science and Plant Analysis, 2000, 31(11-14): 1981–1991. DOI:10.1080/00103620009370556 |
| [19] | Engelstad O P, Terman G L. Agronomic effectiveness of phosphate fertilizers[A]. Khasawneh F E, Sample E C, Kamprath E J. The role of phosphorus in agriculture[M]. Madison: ASA, 1980. 311–322. |
| [20] | Dick R P, Tabatabai M A. Polyphosphates as P sources for plants[J]. Nutrient Cycling in Agro-ecosystems, 1987, 12(2): 107–118. |
| [21] | McBeath T M, Lombi E, McLaughlin M J, et al. Pyrophosphate and orthophosphate addition to soils: sorption, cation concentrations, and dissolved organic carbon[J]. Soil Research, 2007, 45(45): 237–245. |
| [22] |
王蕾, 龚林, 邓兰生, 等. 不同温度和pH对聚磷酸铵水解的影响[J].
磷肥与复肥, 2015, 30(12): 8–11.
Wang L, Gong L, Deng L S, et al. Effects of temperature and pH on hydrolysis of ammonium polyphosphate[J]. Phosphate and Compound Fertilizer, 2015, 30(12): 8–11. DOI:10.3969/j.issn.1007-6220.2015.12.003 |
| [23] |
王蕾, 邓兰生, 涂攀峰, 等. 聚磷酸铵水解因素研究进展及在肥料中的应用[J].
磷肥与复肥, 2015, 30(4): 25–27.
Wang L, Deng L S, Tu P F, et al. Research progresses of hydrolysis factors of ammonium polyphosphate and its application in fertilizer[J]. Phosphate and Compound Fertilizer, 2015, 30(4): 25–27. DOI:10.3969/j.issn.1007-6220.2015.04.011 |
| [24] |
杨荣杰, 仪德启. 聚磷酸铵[M]. 北京: 科学出版社, 2015.
Yang R J, Yi D Q. Polyphosphate[M]. Beijing: Science Press, 2015. |
| [25] | Busman L M, Tabatabai M A. Hydrolysis of trimetaphosphate in soil[J]. Soil Science Society of America Journal, 1985, 49(3): 630–636. DOI:10.2136/sssaj1985.03615995004900030021x |
| [26] | McLaughlin M J, Bertrand I, Lombi E, et al. New fertilizer formulations for highly calcareous soils of South Australia: Final report to South Australian Grain Industry Trust Fund[R]. Adelaide, Australia: CSIRO Land and Water and SA Grain Industry Trust Fund, 2003. |
| [27] |
兰国志. 水溶性聚磷酸铵与金属离子螯合制取螯合物实验研究[D]. 昆明: 昆明理工大学硕士学位论文, 2016.
Lan G Z. Experimental study on preparation of chelate by chelation of water-soluble ammonium polyphosphate with metal ions[D]. Kunming: MS Thesis of Kunming University of Technology, 2016. |
| [28] | El-Sayed SAM. Ammonium polyphosphate and ammonium orthophosphate as sources of phosphorus for Jerusalem artichoke[J]. Alexandria Science Exchange Journal, 2015, 36(1): 47–57. |
| [29] |
马立锋, 杨亦扬, 石元值, 等. Mehlich 3浸提剂在茶园土壤养分分析中的应用[J].
土壤通报, 2007, (4): 745–748.
Ma L F, Yang Y Y, Shi Y Z, et al. Applications of an universal soil extractant of Mehlich 3 to nutrient analysis of tea garden soil[J]. Chinese Journal of Soil Science, 2007, (4): 745–748. DOI:10.3321/j.issn:0564-3945.2007.04.027 |
| [30] | Mnkenie P N S, MacKenzie A F. Retention of ortho- and polyphosphates in some Quebec soils as affected by added organic residues and calcium carbonate[J]. Canadian Journal of Soil Science, 1985, 65(3): 575–585.. DOI:10.4141/cjss85-061 |
| [31] | Philen O D, Lehr J R. Reactions of ammonium polyphosphates with soil minerals[J]. Soil Science Society of America Journal, 1967, 31(2): 196–199. DOI:10.2136/sssaj1967.03615995003100020017x |
| [32] | Shand C, Smith S. Enzymatic release of phosphate from model substrates and P compounds in soil solution from a peaty podzol[J]. Biology and Fertility of Soils, 1997, 24(2): 183–187.. DOI:10.1007/s003740050229 |
| [33] | Föhse D, Claassen N, Jungk A. Phosphorus efficiency of plants. I. External and internal P requirement and P uptake efficiency of different plant species[J]. Plant and Soil, 1988, 110(1): 101–109. DOI:10.1007/BF02143545 |
| [34] | Rao P, Raghavulu P, Reddy S R, et al. Relative efficiency of superphosphate and polyphosphate sources on growth and yield of rice[J]. Indian Journal of Agronomy, 1991, 36(2): 165–168. |
| [35] | Billore S D, Bargale M. Influence of ammonium polyphosphate and orthophosphate on growth and yield attributes in chick pea (Cicer arietinum) at different fertility levels [J]. Indian Journal of Agricultural Sciences, 1991, 61(9): 643–645. |
| [36] |
林邦. 分析化学中的络合作用[M]. 长沙: 中南工业大学出版社, 1987.
Lin B. Complexation in analytical chemistry[M]. Changsha: Zhongnan University of Technology Press, 1987. |
| [37] | Coetzee P E, Ceronio G M, Preez C C D. Effect of phosphorus and nitrogen sources on essential nutrient concentration and uptake by maize (Zea mays L.) during early growth and development [J]. South African Journal of Plant and Soil, 2017, 34(1): 55–64. DOI:10.1080/02571862.2016.1180714 |
| [38] |
陆文龙, 曹一平, 张福锁. 根分泌的有机酸对土壤磷和微量元素的活化作用[J].
应用生态学报, 1999, 10(3): 124–127.
Lu W L, Cao Y P, Zhang F S. Role of root-exuded organic acids in mobilization of soil phosphorus and micronutrients[J]. Chinese Journal of Applied Ecology, 1999, 10(3): 124–127. |
| [39] | Dinkelaker B, Romheld V, Marschner H. Citric acid excretion and precipitation of calcium citrate in the rhizosphere of white lupin (Lupinus albus L) [J]. Plant Cell and Environment, 1989, 12(3): 285–292. DOI:10.1111/pce.1989.12.issue-3 |
 2018, Vol. 24
2018, Vol. 24  doi:
doi: 

