2. 河南中烟工业公司技术中心,郑州 450002;
3. 河南省洛阳市烟草公司,洛阳 471000
2. Technology Center, China Tobacco Henan Industrial Corporation, Zhengzhou, 450002, China;
3. Luoyang Municipal Tobacco Company in Henan Province, Luoyang, 471000, China
烟草叶面腺毛丰富且具有较强的分泌能力[1],其分泌物与烟草的香味有密切的关系,是烟草香味和香气组分的重要前体物,某些品种叶面分泌物可占烟叶干重的10% [2]。西柏三烯二醇是烤烟叶面腺毛分泌物的主要成分,占到腺毛分泌物总量的40%~80%[3]。已有研究表明,西柏三烯二醇是烤烟香味成分的重要前提物质,经一定的降解过程可形成以茄酮为主要代表物的多种致香成分[4],而茄酮作为烤烟中含量最丰富的的中性香味物质之一,本身具有很好的香气,对改善烟草的香味也有很重要的作用[5]。诸多因素对烤烟西柏三烯二醇的代谢都有影响,赵华新等[6]研究了不同海拔高度对烤烟西柏三烯二醇含量的影响,指出较低的海拔高度更易于积累西柏三烯二醇;翁梦玲等[7]对遮阴条件下及正常光照条件下烟草叶面腺毛密度及西柏三烯二醇含量进行了比较,结果表明遮阴处理的烟叶腺毛密度和西柏三烯二醇含量明显低于正常光照处理,说明光照对叶面腺毛的分泌活动有着显著的影响;孔光辉等[8]的研究表明施用有机肥料能显著提高叶片腺毛密度,西柏三烯二醇含量显著高于施用无机肥料。
黄腐酸是腐殖酸中分子量较小的高分子有机化合物,含有多种活性官能团,易被植物吸收,具有较强的生物活性[9],已在多种作物上应用并取得了很好的效果。陈玉玲等[10]在含有黄腐酸的营养液中培养小麦幼苗并测定其IAA和ABA两种激素的水平,发现黄腐酸能显著提升IAA和ABA的水平,并指出这与黄腐酸能刺激植物生长、抑制气孔开启是一致的,说明黄腐酸既能直接对植物起作用,也能通过改变内源激素水平间接起作用。回振龙等[11]研究了黄腐酸对连作马铃薯幼苗生长发育、块茎营养和抗性生理的影响,结果表明黄腐酸能显著促进连作马铃薯的生长发育,提高马铃薯块茎的淀粉含量、Vc含量和可溶性蛋白含量,增强连作马铃薯的抗逆能力。张亚飞等[12]研究指出化肥和黄腐酸配施能显著减少氨挥发,增加土壤氮肥残留,提高根系活力并增加根系生物量,从而提高氮肥利用率,有利于桃树新梢生长和树势健壮。黄腐酸类物质 (黄腐酸钾) 在烟草种植方面的应用已有研究,刘国顺等[13]研究了在基肥中配施黄腐酸钾对烤烟质体色素和碳氮代谢及品质的影响,发现该施用方法能提高烟叶生育前期质体色素含量和碳氮代谢水平,而且能够促进烟叶质体色素适时降解和碳氮代谢的协调,有利于优质烟叶的形成。赵永长等[14]采用水培的方法研究了叶面喷施黄腐酸钾对烤烟幼苗生长和光合荧光特性的影响,结果表明喷施黄腐酸钾能改善渗透胁迫下烤烟幼苗的生长,减缓净光合速率 (Pn) 和蒸腾速率 (Tr) 的下降,同时减轻胁迫对烤烟叶片光系统II (PSII) 的伤害,提高光化学效率。
目前,关于西柏三烯二醇代谢的研究多注重对现象的分析,深入到分子水平对叶面分泌物代谢过程中的关键基因进行分析的研究还不多见,至于黄腐酸对烟草次生代谢的影响更是鲜有报道。本研究从利用水肥一体化技术改良烤烟叶面分泌物入手,通过对比各处理烤烟西柏三烯二醇代谢关键基因CYC-1、CYP71D16以及DXS和DXR的表达情况,并结合对叶面腺毛密度及感官评价结果的分析,初步阐明了新型含黄腐酸烟草专用液体肥料提高烤烟叶面分泌物含量 (尤其是西柏三烯二醇含量) 的原因,以期为在烟叶生产中推广使用水肥一体化技术和含黄腐酸新型烟草专用液体套餐肥来改良烤烟叶面分泌物提供科学依据。
1 材料与方法 1.1 试验区概况试验于2015—2016年进行了2年的田间试验和1年的盆栽试验,供试品种均为豫烟6号。2年田间试验均安排在洛阳市宜阳县盐镇乡张村 (34°38′N,111°58′E) 进行;盆栽试验于2016年安排在郑州市河南农业大学毛庄科教园区 (34°51′N,113°35′E) 进行。两个区域均位于华北平原南部,属北温带大陆性季风气候。田间试验所在地洛阳市宜阳县2015年和2016年平均气温分别为15.2℃和14.9℃,年降水量分别为702.3 mm和670.5 mm。前茬作物为烤烟。土壤的基础肥力指标分别为:pH值为7.91、有机质含量12.2 g/kg、碱解氮82.03 mg/kg、有效磷 (P2O5) 含量13.62 mg/kg、有效钾 (K2O) 含量185.8 mg/kg。盆栽试验所在地郑州市2016年平均气温为15.5℃,年降水量为640.7 mm。盆栽试验供试土壤由田间试验所在地提供。
1.2 试验设计田间试验和盆栽试验均设置3个处理,即常规栽培处理 (用FP表示)、水肥一体化施用普通烟草专用液体肥 (用DF1表示) 和水肥一体化施用含黄腐酸烟草专用液体肥 (用DF2表示)。田间试验采用小区对比试验设计,各处理小区面积均为667 m2,行株距为1.1 m × 0.55 m,另设保护行,每个小区种植1000株,每个处理重复3次;盆栽试验用土风干后过40目筛子,盆高30 cm,直径35 cm,每盆装土20 kg,每个处理种10盆,周围摆放保护盆,以消除边行优势。田间试验和盆栽试验各处理除施肥方案不同外,其他栽培措施按优质烟生产技术规范进行。
田间试验3个处理具体施肥方案如下:FP处理在大田起垄时条施芝麻饼肥 (含氮量4%) 225 kg/hm2、过磷酸钙 [Ca(H2PO4)2·H2O] 150 kg/hm2、烟草专用复合肥 (15–15–15) 225 kg/hm2作基肥,硝酸钾 (KNO3) 用量75 kg/hm2,作为追肥在团棵期一次穴施,硫酸钾 (K2SO4) 用量300 kg/hm2,在烟株圆顶后分3次穴施,烟株全生育期总施氮量为52.5 kg/hm2;DF1处理在大田起垄时仅条施芝麻饼肥 (含氮量4%) 375 kg/hm2作基肥,追肥采用本课题组研制的烟草专用液体套餐肥 (不含黄腐酸),其中包括烟草专用还苗生根肥 (肥料品级 20–10–10) 75 kg/hm2,旺长肥 (肥料品级 15–5–10) 150 kg/hm2,成熟落黄肥 (肥料品级 0–0–40) 150 kg/hm2,通过水肥一体化滴灌系统根据烟株需肥需水规律分6次施入,烟株全生育期总施氮量与常规栽培处理保持一致。DF2处理基肥同DF1处理,追肥采用本课题组研制的新型含黄腐酸烟草专用液体套餐肥,该套餐肥各类型肥料基础配方与DF1处理相同,但均添加黄腐酸,黄腐酸含量≥20.0%,其余与DF1处理保持一致。盆栽试验施肥方案与田间试验基本相同,所施肥料用量和灌水量均按照田间试验用量进行换算,保持一致。
田间试验水源由当地烟水配套工程修建的500 m3蓄水池提供,盆栽试验水源由河南农业大学科教园区水井提供,施肥灌溉首部系统均采用移动式施肥灌溉一体机 (由汽油机水泵、过滤器、施肥桶、空气阀等部件构成),管网系统由主管道 (PE材质,直径63 mm) 连接贴片式滴管带 (PE材质,直径16 mm,滴头间距30 cm,滴头流量2.5~3 L/h) 组成。
1.3 样品的采集与测定 1.3.1 样品的采集盆栽试验选定各处理具有代表性的烟株,自下而上挂牌标记1~22位可收叶,并记录各处理第13、14叶位叶片的叶龄 (叶片生长至2~3 cm长度时开始计算叶龄)。在叶龄60 d时取样2 片,样品遮光干冰保存运送到实验室进行叶面腺毛密度观察、RNA提取和叶面分泌物的提取;田间试验取各处理叶龄60 d的中部鲜烟叶进行调制并测其茄酮含量,待烟叶成熟采烤后取各处理具代表性等级 (C3F) 烤后烟叶,测定茄酮含量和进行感官质量评价。
1.3.2 叶片腺毛密度观察于各处理烟株中部叶片 (第14叶位) 叶龄60 d时采取新鲜叶片,沿其主脉两侧切取约10 mm × 10 mm的平整小块叶片,使用捷克TESCAN公司的VEGA 3 LM扫描电子显微镜进行观察和拍照,连续拍摄并统计3个视野中的腺毛数,这3个观察值平均数代表每个样品的腺毛密度值。该电镜采用气体二次电子成像,工作电压15 KV,工作距离11 mm,样品室和镜筒状态选用高真空 (10–3 Pa)。
1.3.3 叶面腺毛分泌物的提取与测定 1.3.3.1 叶面分泌物的提取与浓缩在叶龄60 d时取各处理烟株第14叶位叶片,将1000 mL二氯甲烷倒入金属托盘 (清洁无水残留) 中,用镊子夹住叶柄基部将叶片整片浸入二氯甲烷溶液中2秒钟,将叶片提出溶液2秒,使叶片上的二氯甲烷滴回到盘中,这样为完成浸提一次,每片叶片反复浸提4次,最后1次浸提后需要将叶片上的二氯甲烷完全滴回盘中。
将托盘中所有的二氯甲烷转移到2000 mL的烧杯中,向烧杯中加入1 mL的内标 (内标为1.01 g蔗糖八乙酸酯和1.271 g正–17–烷醇,定容500 mL),充分混匀,加入10 g左右无水硫酸钠,充分搅拌吸去水分,用定量滤纸过滤至1000 mL圆底烧瓶中,滤液减压旋转蒸发至20 mL左右,最后定容至50 mL容量瓶。用移液管取5 mL上述浸提液于色谱瓶中,在氮气保护下将溶剂吹干。加入500 μL 1∶1 (v∶v) DMF∶BSTFA,在75℃水浴中进行衍生化反应60 min,加入0.5 mL的二氯甲烷溶解不溶物,即为GC/MS分析样品液。
1.3.3.2 叶面分泌物的测定采用美国Thermo Fisher Scientific公司的TRAVE GC ULTRA-DSQ ⅡMS型气相色谱–质谱 (GC–MS) 联用仪进行定性定量测定。
气相色谱–质谱联用仪反应条件:GC条件,色谱柱DB-5MSUI石英毛细管柱 (30 m × 0.25 mm,0.25 μm);进样口温度 250℃;程序升温,40℃保持2 min,然后以6℃/min升温至180℃保持2 min,以2℃/min升温至280℃保持 20 min;载气为高纯氦气,载气流速为恒流0.8 mL/min;进样量 1.0 μL,分流比15∶1;MS条件为传输线温度 250℃;EI离子源温度 280℃;电离能量 70 eV;质量数范围50~650 amu;检索谱库 NIST11。
1.3.4 叶片腺毛相关基因表达分析 1.3.4.1 叶片总RNA的提取使用TaKaRa公司生产的RNAiso Reagent试剂盒,并按照说明书提供的方法提取参试材料叶片的总RNA。
将提取的RNA溶于适量的DEPC水中,采用紫外分光光度计分别测定260 nm和280 nm分光率并计算二者比值,以判断提取RNA的纯度和浓度;然后进行2%甲醛变性琼脂糖凝胶电泳检测RNA的完整性;RNA样品–80℃保存备用。
1.3.4.2 荧光定量PCR以烟草Actin基因 (Genebank Accession No. AB158612) 为内参,引物序列为Actin-F: 5′-GCTGTTTTTCCTAGTATTGTTGGTC-3′,Actin-R: 5′-AATACCTGTTGTACGGCCACTG-3′;CYC-1 (Genebank Accession No. AY049090) 引物为F: 5′-CGAGGGTGGGATCAAGGAAATACA-3 ′,R: 5′-ATCGCATCCGTGAAAAGCATAAG-3′;CYP17D16 (GenBank Accession No. AF166332) 引物为F: 5′-ATGGACCAATTATGCACCTTCAACT-3′,R: 5′-GGCACTGAGCAATTCCAAGAGACA-3′;DXS (GenBank Accession No. EU650419) 引物为F: 5′-GCCGAGAGAGCTGCAGACAAGTAT-3′,R: 5′-TTGGGAAGCGACGGTGGAATA-3′;DXR (GenBank Accession No. DQ839130) 引物为F: 5′-TCGCTGAGAATCCGGACAAGTTTA-3′,R: 5′-TGCGCAACCAACTATTCCTGTAAC-3′。
荧光定量PCR反应体系为20 μL:10 μL SYBR Green qPCR Mix,0.4 μL Forward Primer (10 μmol/L),0.4 μL Reverse Primer (10 μmol/L),0.4 μL ROX,cDNA 1 μL,水7.8 μL。PCR扩增程序为:95℃预变性10 min;95℃模板变性15 s,55℃引物和模板充分退火15 s,72℃延伸45 s,共循环40次,分离后4℃保存。
1.3.5 烤后烟叶茄酮含量的测定使用同时蒸馏萃取装置,以二氯甲烷作为萃取剂,装置的一端接1000 mL平底烧瓶,内盛20.0 g烟样及350 mL蒸馏水,加热。装置的另一端接100 mL烧瓶内盛40 mL二氯甲烷,此处在水浴锅内加热,水浴温度为60℃,蒸馏萃取同时进行2 h,完成之后,向二氯甲烷萃取液中加入10 g左右无水硫酸钠吸取水分,然后冷却干燥,最后直至把二氯甲烷萃取液浓缩至1 mL,并以乙酸苯乙酯为内标,做定量分析。
采用美国HP5890Ⅱ-5972气质联用仪对烟叶样品进行定性定量分析。GC/MS分析条件:色谱柱,hp-5 (60 m × 0.25 mm.i.d. × 0.25 μm d.f.);载气及流速为He 0.8 mL/min;进样口温度250℃;传输线温度280℃;离子源温度177℃;升温程序为初温50℃,恒温5 min后以5℃/min升至120℃,保持5 min,再以5℃/min升至180℃,保持5 min,再以6℃/min升至250℃,保持15 min;分流比为1∶15;进样量2 μL;电离电压70 ev;电离方式EI;质量数范围 50~500 amu。MS谱库:NIST11。
1.3.6 单料烟感官质量评价将样品烟叶进行切丝卷制单料烟,卷烟感官评吸鉴定聘请河南中烟有限责任公司5位评吸专家按香气质、香气量、浓度、柔细度、余味、杂气、刺激性等方面进行评价。
1.4 数据处理所有试验数据采用Excel2013进行整理,采用Sigmaplot12.5软件进行图表绘制。采用Prizm4统计分析软件进行荧光定量PCR数据统计分析,使用2T–ΔΔC的方法对基因的相对表达量进行检测。
2 结果与分析 2.1 烟株叶片叶面腺毛密度差异分析烟草的腺毛根据腺毛柄情况可分为长柄、短柄和分枝腺毛[15]。一般认为,长柄腺毛数量较多,具有较强的分泌能力,短柄腺毛数量较少,分泌能力较弱,分枝腺毛一般出现在叶脉和烟茎上,数量最少[16]。通过盆栽试验,对各处理中部叶龄60 d叶片的腺毛密度进行电镜扫描观察并进行统计发现,腺毛在各处理烤烟叶片上的分布密度存在明显的差异 (图1)。从图1-Ⅳ可以看出,DF2处理腺毛总密度最高,达到10.7根/mm2,且具有较强分泌能力的长柄腺毛数量也最多,达到8.6根/mm2,体型也较大 (图1-Ⅲ),而FP和DF1处理腺毛总密度较低,分别为8.5根/mm2和7.6根/mm2,尤其是长柄腺毛的数量明显低于DF2处理,分别为5.8根/mm2和6.2根/mm2,体型也较小 (图1-Ⅰ和图1-Ⅱ)。可见,施用含黄腐酸液体肥料可以提高烟叶的腺毛密度,明显增加长柄腺毛的数量。
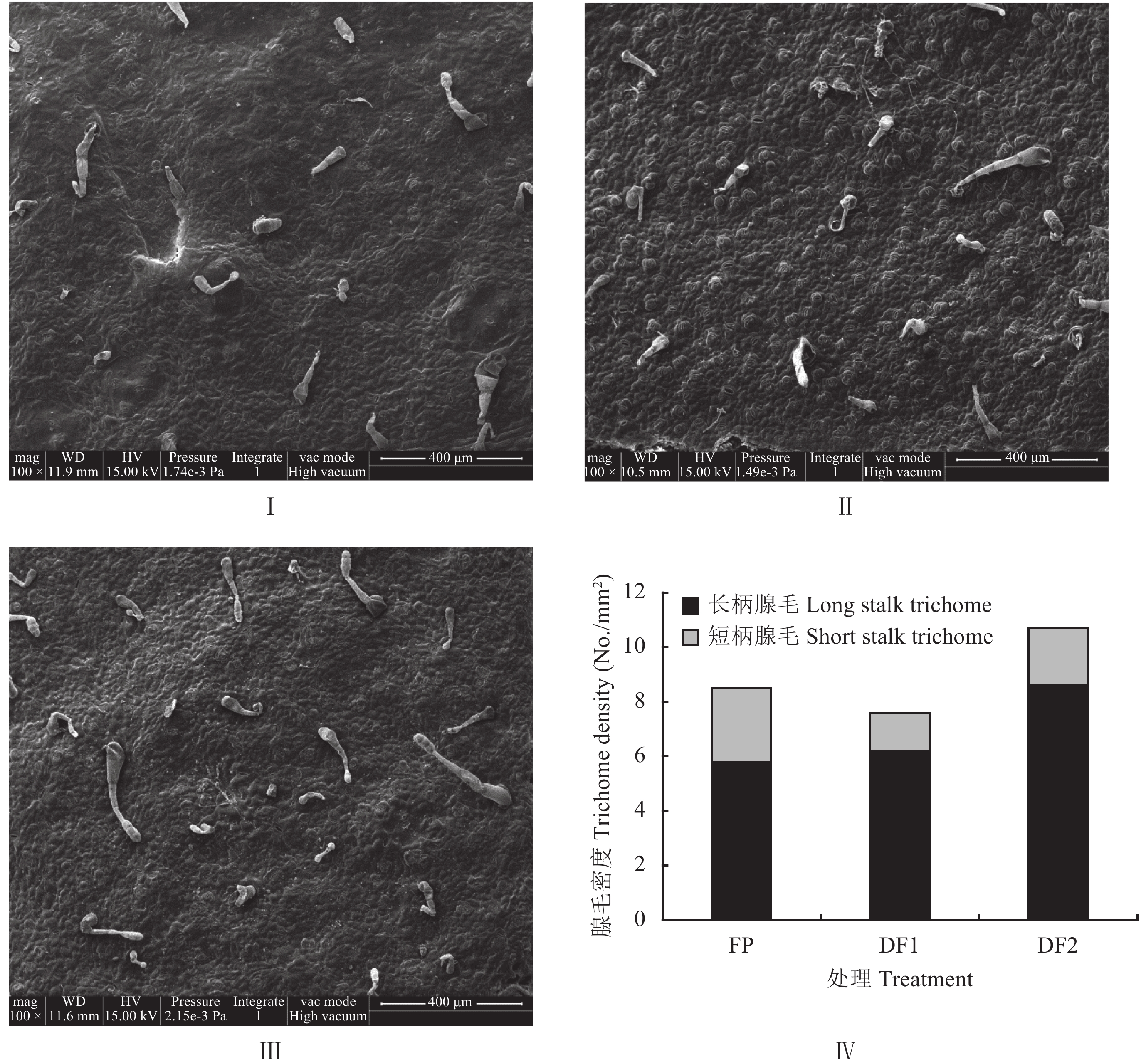 |
| 图1 叶龄60 d时各处理叶片的腺毛形态及密度 (盆栽试验) Fig. 1 Trichome morphology and density at the leaf age of 60 d (Pot experiment) [注(Note):Ⅰ,FP处理叶面腺毛形态Leaf trichome morphology of FP treatment;Ⅱ,DF1处理叶面腺毛形态Leaf trichome morphology of DF1 treatment;Ⅲ,DF2处理叶面腺毛形态Leaf trichome morphology of DF2 treatment;Ⅳ,各处理叶面腺毛密度差异统计Statistical analysis of leaf trichome density.] |
烟叶叶片分泌物在叶龄60 d时各组分含量差异最明显[17],对叶龄60 d时中部叶的叶面分泌物进行分析 (表1) 可以看出,在3个处理中,DF2处理西柏三烯二醇含量占总含量的75.61%,为各处理中最高,FP处理次之,为70.56%,DF1处理最低,为67.13%。可见,西柏三烯二醇为各处理叶片叶面腺毛分泌物的主要成分,这也决定了其在烟叶香味形成的过程中起着决定性的作用。就叶面腺毛分泌物总量而言,DF2处理具有最高的分泌量,FP处理次之,DF1处理最低,西柏三烯二醇的含量也具有相同规律,DF2处理西柏三烯二醇达到65.43 μg/cm2,为各处理最高,明显高于FP处理 (46.84 μg/cm2) 和DF1处理 (39.8 μg/cm2),这说明施用含黄腐酸液体肥料能明显提高烟草叶面分泌物的含量,尤其是西柏三烯二醇的含量。
| 表1 各处理烤烟中部叶叶龄60 d叶面分泌物组分含量 (μg/cm2,盆栽试验) Table 1 GC-MS analysis of the trichome exudates components at the leaf age of 60 days (Pot experiment) |
 |
已有研究表明,烟叶的西柏三烯二醇代谢受CYC-1、CYP71D16、DXR、DXS等基因的调控[18]。对各处理叶龄60 d的中部叶进行荧光定量PCR测定 (图2) 可以看出,黄腐酸能显著提高烟叶CYC-1、CYP71D16、DXR、DXS基因的表达量。DF2处理上述4个基因的相对表达量均显著高于FP和DF1处理,其中,CYC-1的相对表达量分别是FP和DF1处理的12.45倍和4.11倍,CYP71D16的相对表达量分别是FP和DF1处理的3.54倍和5.71倍,DXR的相对表达量分别是FP和DF1处理的3.22倍和2.44倍,DXS的相对表达量分别是FP和DF1处理的3.44倍和2.28倍。前面的分析已经揭示含黄腐酸液体肥料能使烟叶的腺毛密度和叶面分泌物的主要成分西柏三烯二醇的含量得到大幅提升,与烟叶西柏三烯二醇代谢密切相关的基因显著地上调表达则可以很好地解释这一现象,这也再一次证明西柏三烯二醇的代谢与CYC-1、CYP71D16、DXR、DXS基因密切相关,同时,也证实了黄腐酸可以通过使相关基因的上调表达显著增加烟叶西柏三烯二醇的含量。
2.4 西柏三烯二醇主要降解产物茄酮含量差异分析茄酮是目前学界公认的西柏三烯二醇主要降解产物[19],是烟草中含量最丰富的的中性香味物质之一,本身具有很好的香气,对改善烟草的香味也有很重要的作用[5]。对2015—2016年连续2年田间试验各处理叶龄60 d和调制后的中部烟叶茄酮含量进行测定,取2年数据的均值(图3),可以看出不同处理西柏三烯二醇的降解存在明显的差异,叶龄60 d时各处理茄酮含量差异不明显,而调制后DF2处理的初烤烟叶茄酮含量明显高于其他处理,可达到112.27 μg/g,分别是FP和DF1处理的2.93倍和1.99倍,这进一步验证了前述的结果,说明施用含黄腐酸的液体肥料能明显提高西柏三烯二醇的降解能力,其烟叶中较高含量的西柏三烯二醇经调制过程降解为对烟叶香气有巨大贡献的茄酮,从而使初烤烟叶茄酮含量明显提升。
 |
| 图2 盆栽试验叶龄60 d时各处理CYC1、CYP71D16、DXR和DXS基因的相对表达量 Fig. 2 Relative expressions of CYC-1, CYP71D16, DXR and DXS at the leaf age of 60 days in pot experiment [注(Note):FP—常规栽培处理Conventional fertilizer, basal applied in soil; DF1—烟草专用液体肥, 随水灌溉Liquid fertilizer for tobacco, applied with irrigation; DF2—含黄腐酸烟草专用液体肥Liquid fertilizer containing fulvic acid for tobacco, applied with irrigation.] |
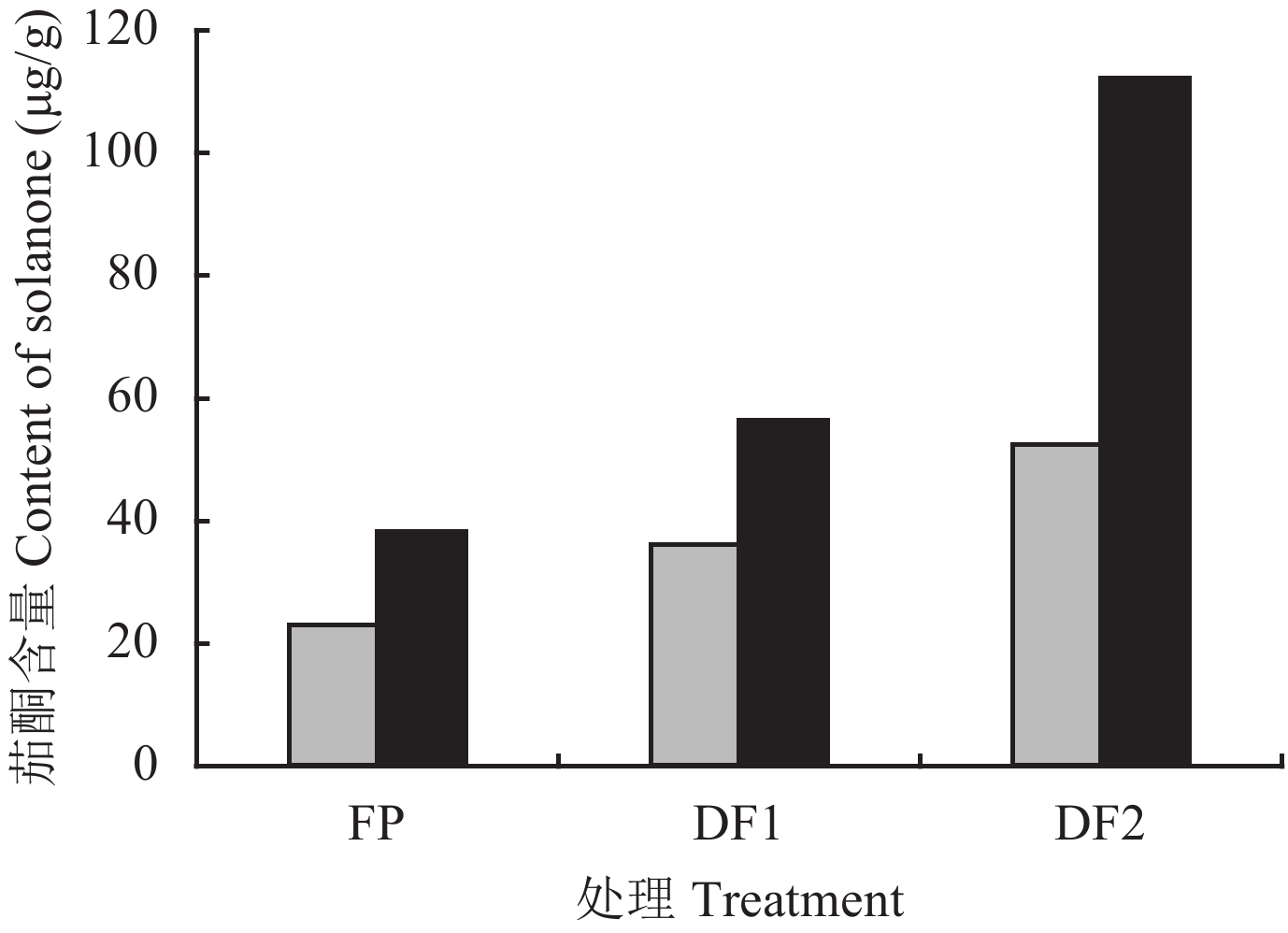 |
| 图3 各处理中部烟叶叶龄60 d和调制后茄酮的含量 (2年田间试验均值) Fig. 3 The content of solanone at leaf age of 60 days and after flue-cured (Mean of two years for field experiment) [注(Note):FP—常规栽培处理Conventional fertilizer, basal applied in soil; DF1—烟草专用液体肥, 随水灌溉Liquid fertilizer for tobacco, applied with irrigation; DF2—含黄腐酸烟草专用液体肥Liquid fertilizer containing fulvic acid for tobacco, applied with irrigation.] |
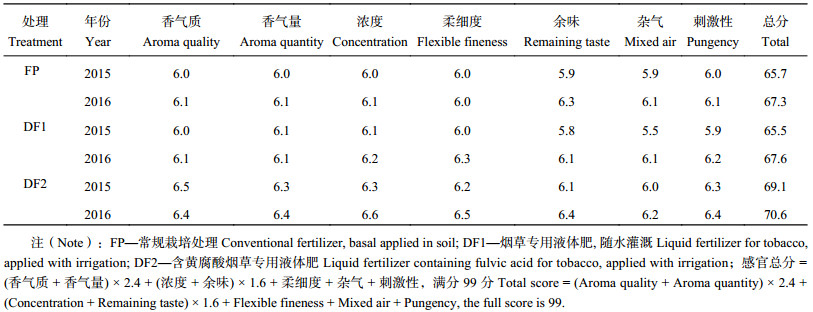
烟叶的感官质量是卷烟产品质量的重要组成部分,是烟叶质量的核心和基础[20]。委托河南中烟工业有限公司评吸专家连续2年对田间试验中部初烤样品烟进行感官质量评价 (表2)。由表2可以看出,DF2处理连续2年中部叶感官质量评价得分均为各处理最高,DF1处理2015年感官评价结果略低于FP处理,2016年则要高于FP处理。其中DF2处理香气质较好,香气量较足,浓度较足,烟气细腻且余味较舒适,杂气和刺激性较小,无明显缺点。相比之下,FP和DF1处理稍显逊色,主要表现在香气质略显平淡,香气量较少,烟气浓度不足,杂气和刺激性较重。这说明茄酮对烟叶香气的改善有着重要贡献,施用含黄腐酸的液体肥料能显著增加烟叶中的茄酮含量,提升烟叶的抽吸品质。
| 表2 田间试验各处理中部初烤烟叶感官质量评分 (n = 9) Table 2 Scores of sensory quality of modulated flue-cured tobacco leaves in field experiment |
 |
大量研究表明,烟草腺毛的发育过程和代谢活动是同步进行的[21]。杨铁钊等[22]研究指出烟叶生长过程中单位面积叶面的分泌物量呈双峰曲线变化态势,中部位叶面分泌物量在叶龄60 d时达到最大值,之后直至烟叶成熟,腺毛分泌物含量呈逐渐下降趋势。因此,本研究选取中部叶叶龄60 d进行叶面腺毛密度和分泌物的测定,这是最佳的时期。烟草的腺毛根据腺毛柄情况可分为长柄、短柄和分枝腺毛。就数量而言,长柄腺毛是烟叶腺毛的主要类型,这与本研究结果相一致;就分泌能力而言,分枝腺毛的分泌能力最强,但数量较少。关于作物叶片腺毛密度与其分泌物含量的关系,目前的研究尚未能形成一致意见,陈淑珍等[23]认为腺毛密度与整叶分泌物量正相关,时向东等[24]研究认为对烟叶香气品质作用最大的为长柄腺毛,长柄腺毛越多,叶面腺毛分泌物量越大,与腺毛密度的关系不大,而Nielsen等[25]综合分析了多个品系烟草腺毛密度与其分泌量的关系,认为在烟草中一些腺毛密度很小的品系,其腺毛分泌物的含量与腺毛密度呈正相关,而腺毛密度大的品系,其腺毛分泌物的含量可能更多地取决于腺毛的分泌能力,而与腺毛密度关系不大。根据本研究结果可以看出DF1处理单位面积叶片的长柄腺毛数量高于FP处理,但是叶面腺毛的分泌量却低于FP处理;本研究结果还表明叶面腺毛的分泌量与叶面腺毛密度呈正相关,腺毛密度越大腺毛的分泌量越大,因此作者认为腺毛分泌量受多种因素的影响,而腺毛密度很可能是主要的影响因素。本试验中DF1和DF2处理均在水肥一体化条件下滴施液体肥料,但是DF1处理腺毛密度低、分泌量少,这很可能是因为DF1处理在水肥一体化条件下施用液体肥料,肥料利用率高,烟株田间长势较旺,叶片开片较好,叶面积较大。DF2处理同样在水肥一体化条件下施用液体肥料,却因为黄腐酸具有较强的生物活性,能够刺激植物表皮毛的形成[26],从而使叶片在叶面积增加的情况下依然保持较高的腺毛密度。
3.2 对西柏三烯二醇合成代谢相关基因表达的影响关于西柏三烯二醇代谢的基因调控过程前人已有研究,目前已经明确CYC-1和CYP71D16这2个基因直接参与了西柏三烯二醇的合成[27]。其中,CYC-1是编码西柏三烯醇合成酶的基因,西柏三烯醇合成酶以香叶基香叶基焦磷酸为底物催化合成西柏三烯一醇[28],而作为编码细胞色素P450加氧酶的基因,CYP71D16主要参与调控了西柏三烯一醇向西柏三烯二醇转变的过程[29],可见,CYC-1和CYP71D16直接决定着植物腺毛分泌物中西柏三烯一醇和西柏三烯二醇的含量,在类西柏烷二萜合成中发挥着重要的作用。本试验除了对上述2个基因进行了研究,还对与西柏三烯二醇合成密切相关的另外2个基因DXS和DXR进行了研究。DXS是编码脱氧木酮糖磷酸代谢途径第一个限速酶脱氧木酮糖–5–磷酸合成酶的基因,该酶的作用是催化糖酵解产物丙酮酸和3–磷酸甘油醛形成脱氧木酮糖–5–磷酸[30],由于脱氧木酮糖–5–磷酸也是维生素B1和B6的前体物[31],所以催化脱氧木酮糖–5–磷酸形成甲基赤鲜糖醇–4–磷酸的脱氧磷酸木酮糖还原异构酶 (DXR),被认为是脱氧木酮糖磷酸代谢途径中的另一个更为重要的关键酶。一般认为,香叶基香叶基焦磷酸是合成西柏三烯二醇的底物,在植物中以香叶基香叶基焦磷酸为底物发生环化作用形成的二萜还有顺–冷杉醇和赖百当二萜,但香叶基香叶基焦磷酸环化作用的具体走向以及所占比例如何,一方面取决于CYC-1和CYP71D16基因的调控作用,另一方面则由底物香叶基香叶基焦磷酸的丰富程度决定[32],DXR和DXS基因的过表达为下游限速酶提供了充足的底物,保障GGPP环化作用向合成西柏三烯二醇的方向发生,因此,本研究认为黄腐酸促进DXR和DXS基因上调表达可能对西柏三烯二醇的合成具有更大贡献。为了探究不同处理对西柏三烯二醇代谢在分子水平上的差异,本试验测定了不同处理上述4个基因的表达量,结果表明DF2处理CYC-1、CYP71D16、DXR和DXS的基因相对表达量均明显高于其余处理,究其原因DF1处理和DF2处理均采用水肥一体化滴施液体肥料,且二者肥料配方基本相同,区别仅在于DF2处理施用的液体肥料含有黄腐酸,可见黄腐酸是西柏三烯二醇代谢相关基因上调表达的主要原因。前人的研究已经证实黄腐酸能调控某些基因的表达量,于学建[33]研究了黄腐酸调控甜菊糖苷合成的机理,结果发现黄腐酸可以显著提高甜叶菊叶片中UGT基因的表达并使其在甜叶菊生长过程中维持较高的表达水平。许原原[34]研究了黄腐酸对苜蓿根瘤固氮菌S.meliloti群体感应系统的调控机理,结果表明黄腐酸可以显著抑制S.meliloti8530群体感应相关基因expR、sinI、sinR的表达。Schmidt等研究发现黄腐酸显著下调了控制根毛生长的负调控基因WEREWOLF和GLABRA2的表达,从而提高了拟南芥根毛的长度及密度。本研究结果也表明施用含黄腐酸的液体肥料能够明显使CYC-1、CYP71D16、DXR和DXS基因上调表达,使烟叶腺毛大量分泌西柏三烯二醇,进而提高初烤烟叶的茄酮含量,改善烟叶的抽吸品质。关于黄腐酸调控基因表达的原因可能是多样的,Fialova[35]对比了小麦培养在水中和含有黄腐酸营养液中时根中RNA的含量,发现当培养在含有黄腐酸营养液中时根中RNA含量 (60 μg/株) 明显高于在水中培养 (25 μg/株),且下降十分缓慢,通过进一步研究发现,黄腐酸对RNA合成的影响是不均衡的,核糖体RNA受影响最大。Wang等[36]用14C标记的黄腐酸进行实验,结果表明水稻细胞能利用黄腐酸的降解物来合成蛋白质和DNA。还有人研究发现黄腐酸能使洋葱分生组织间期细胞核体积增大,3H标记的胸苷实验证明DNA合成增加,3H标记的尿苷实验证明相应的mRNA增加[37]。以上研究可以为解释黄腐酸参与基因调控提供一些思路,黄腐酸很可能是参与了DNA的合成、转录以及翻译的过程,从而完成其调控过程,影响蛋白质的合成。
3.3 对西柏三烯二醇生物降解的影响业已证明,大多数西柏烯类物质都来源于西柏三烯二醇的生物降解[5],而关于其生物降解途径国内外的研究鲜有报道,一般认为西柏三烯二醇的降解主要有两种模式[38],一种是在氧化剂的作用下进行,另一种是在酶的催化作用下进行,如在脂肪氧化酶的作用下完成。起始氧化完成之后经过脱水、酸碱重排和消除反应后,西柏三烯二醇可转化为C8~C18不同碳原子数的香味物质,其中主要以C13的茄酮为主。本研究连续2年对比了3个处理叶龄60 d和调制后初烤烟叶茄酮含量的差异,在叶龄60 d时3个处理茄酮含量差异不明显,而调制后的初烤烟叶DF2处理的茄酮含量却显著高于FP和DF1处理,这很可能是因为在烟叶成熟和调制的过程中黄腐酸及其降解物质参与了西柏三烯二醇的降解并促进了该过程。黄腐酸调节植物生长代谢的作用机理比较复杂,根据已有研究可以明确的是[39],在酚–醌氧化还原体系中黄腐酸既是氧的活化剂,又是氢的载体,直接参与了和呼吸作用有关的电子传递,提高了植物体内的氧化还原能力,影响植物的呼吸作用、细胞膜透性和渗透压,以及多种与氧化还原反应有关的酶的活性,从而完成对植物生长代谢的调控,其对西柏三烯二醇降解的影响很可能就是通过增强氧化剂的氧化能力或者提高酶的活性来完成的。目前公认的西柏三烯二醇主要降解产物是茄酮,是烟草中含量最丰富的中性香味物质之一,本身具有很好的香气,对改善烟草的香味也有很重要的作用[5]。茄酮的转化产物如茄醇、茄尼呋喃、降茄二酮也是重要的烟草香味物质,茄酮的氧杂双环化合物具有特别的香味,对于改善烟草的香味和提升抽吸品质也有重要的贡献[40],本研究的感官质量评价结果也证实了这一点。
4 结论本研究初步阐明了黄腐酸调控烤烟西柏三烯二醇代谢的机理,试验所用的新型黄腐酸烟草专用液体套餐肥含有的有机和无机养分,在合理组配的条件下能够充分发挥黄腐酸的生物活性,通过促进西柏三烯二醇代谢相关基因CYC-1、CYP71D16、DXR和DXS的表达,尤其是DXR和DXS的表达,进而提升叶面腺毛密度和分泌量,提高叶面分泌物中西柏三烯二醇的含量,并通过增强相关氧化剂的氧化能力和提高酶的活性参与了西柏三烯二醇的生物降解,促进了西柏三烯二醇向茄酮转化的过程,进而提高初烤烟叶的茄酮含量,改善烟叶的抽吸品质。
| [1] |
高致明, 刘国顺, 段增强. 烟草叶发育的组织细胞学研究[J].
河南农业大学学报, 1991, 25(1): 24–28.
Gao Z M, Liu G S, Duan Z Q. Histo-cytological study on development of the leaf of nicotinia tabacum[J]. Journal of Henan Agricultural University, 1991, 25(1): 24–28. |
| [2] | Wagner G J. Secreting glandular trichomes: more than just hairs[J]. Plant Physiology, 1991, 96: 675–679. DOI:10.1104/pp.96.3.675 |
| [3] | Johnson A W. Tobacco leaf trichomes and their exudetas[J]. Tobacco Science, 1985, 29: 67–72. |
| [4] |
钱晓波. 烤烟中西柏三烯醇、糖苷类物质的检测及其与烟叶油 润性的关系[D]. 合肥: 中国科学技术大学硕士学位论文, 2014.
Qian X B. Study on quantification of cembranoids and glycosides in tobacco and their impacts on oil wetability property of tobacco leaves [D]. Hefei: MS Thesis of University of Science and Technology of China, 2014. |
| [5] |
史宏志, 刘国顺, 杨惠娟, 等. 烟草香味学[M]. 北京: 中国农业出版社, 2011: 133–135.
Shi H Z, Liu G S, Yang H J, et al. Tobacco flavor [M]. Beijing: China Agriculture Press, 2011: 133–135. |
| [6] |
赵华新, 武丹风, 姬小明, 等. 海拔对不同基因型烤烟西柏三烯 二醇含量的影响[J].
河南农业科学, 2014, 43(5): 56–61.
Zhao H X, Wu D F, Ji X M, et al. Effects of altitude on duvatrienediol content in different genotypes of flue-cured tobacco[J]. Journal of Henan Agricultural Sciences, 2014, 43(5): 56–61. |
| [7] |
翁梦苓, 梁志敏, 崔红, 等. 遮荫对烟草叶片腺毛形态结构及分 泌物含量的影响[J].
河南农业大学学报, 2008, 42(6): 613–616, 631.
Weng M L, Liang Z M, Cui H, et al. Effects of shading on leaf trichome morphology and structure and secretions content of flue-cured tobacco[J]. Journal of Henan Agricultural University, 2008, 42(6): 613–616, 631. |
| [8] |
孔光辉, 徐照丽, 王伟, 等. 不同肥料对红花大金元中部叶片腺 毛及分泌物积累的影响[J].
中国烟草学报, 2007, 13(4): 41–44.
Kong G H, Xu Z L, Wang W, et al. Effect of fertilizer on glandular trichome density and exudates accumulation in middle leaf of " Honhuadajinyuan”[J]. Acta Tabacaria Sinica, 2007, 13(4): 41–44. |
| [9] |
李捷, 杨小鹏, 冯建军. 不同条件下黄腐酸对春小麦生长和水 分利用的影响[J].
干旱地区农业研究, 2002, 20(2): 52–55.
Li J, Yang X P, Feng J J. Effects of fulvic acid on spring wheat growth and water use in different conditions[J]. Agricultural Research in the Arid Areas, 2002, 20(2): 52–55. |
| [10] |
陈玉玲, 曹敏, 周燮, 等. 黄腐酸对冬小麦幼苗IAA、ABA水平 的影响及作用机理的探讨[J].
植物学通报, 1999, 16(5): 587.
Chen Y L, Cao M, Zhou X, et al. Effects of FA on IAA and ABA levels of winter wheat seedlings and the discussion of Its mechanism[J]. Chinese Bulletin of Botany, 1999, 16(5): 587. |
| [11] |
回振龙, 李朝周, 史文煊, 等. 黄腐酸改善连作马铃薯生长发育及抗性生理的研究[J].
草业学报, 2013, 22(4): 130–136.
Hui Z L, Li C Z, Shi W X, et al. A study on the use of fulvic acid to improve growth and resistance in continuous cropping of potato[J]. Acta Prataculturae Sinica, 2013, 22(4): 130–136. DOI:10.11686/cyxb20130416 |
| [12] |
张亚飞, 罗静静, 彭福田, 等. 黄腐酸钾与化肥控释袋促进桃树生长及氮肥吸收利用[J].
植物营养与肥料学报, 2017, 23(4): 998–1005.
Zhang Y F, Luo J J, Peng F T, et al. Fulvic acid potassium and nutrient-controlled release paper bag enhance peach tree growth, nitrogen absorption and utilization[J]. Journal of Plant Nutrition and Fertilizer, 2017, 23(4): 998–1005. DOI:10.11674/zwyf.16473 |
| [13] |
刘国顺, 何永秋, 杨永锋, 等. 不同钾肥配施对烤烟质体色素和碳氮代谢及品质的影响[J].
中国烟草科学, 2013, 34(6): 49–55.
Liu G S, He Y Q, Yang Y F, et al. Effects of combining application of various potassium fertilizers on plastid pigment, carbon- nitrogen metabolism and quality in flue-cured tobacco[J]. Chinese Tobacco Science, 2013, 34(6): 49–55. |
| [14] |
赵永长, 宋文静, 邱春丽, 等. 黄腐酸钾对渗透胁迫下烤烟幼苗生长和光合荧光特性的影响[J].
中国烟草学报, 2016, 22(4): 98–106.
Zhao Y C, Song W J, Qiu C L, et al. Effects of fulvic acid potassium on growth and photosynthetic fluorescence characteristics of flue-cured tobacco seedlings under osmotic stress[J]. Acta Tabacaria Sinica, 2016, 22(4): 98–106. |
| [15] |
张华, 赵百东, 冀浩, 等. 烟草腺毛发育的形态学研究[J].
中国烟草学报, 2009, 15(1): 22–24.
Zhang H, Zhao B D, Ji H, et al. Morphology research on tobacco trichome during growth[J]. Acta Tabacaria Sinica, 2009, 15(1): 22–24. |
| [16] | Barrera R, Wrensman E A. Trichome type, density and distribution on the leaves of certain tobacco varieties and hybrids[J]. Tobacco Science, 1966, 10: 157–161. |
| [17] |
王冬, 孙九哲, 彭玉富, 等. 不同品种(系)烤烟西柏三烯二醇代谢差异研究[J]. 中国烟草学报, 2014, 20(6): 63–69.
Wang D, Sun J Z, Peng Y F, et al. Metabolism differences of cembratrien-diols in different tobacco cultivars [J]. Acta Tabacaria Sinica, 2014, 20(6): 63–69. |
| [18] |
王冬. 烟草西柏三烯二醇积累的遗传及生态响应研究[D]. 郑州: 河南农业大学博士学位论文, 2014.
Wang D. Research of genetic basis and ecological response of cembratrien-diol synthesis in tobacco [D]. Zhengzhou: PhD Dissertation of Henan Agricultural University, 2014. |
| [19] |
王瑞新. 烟草化学[M]. 北京: 中国农业出版社, 2003. 202–203.
Wang R X. Tobacco chemistry [M]. Beijing: China Agriculture Press, 2003. 202–203. |
| [20] |
朱尊权. 烟叶的可用性与卷烟的安全性[J].
烟草科技, 2000, (8): 3–6.
Zhu Z Q. Availability of tobacco leaves and safety of cigarettes[J]. Tobacco Science & Technology, 2000, (8): 3–6. |
| [21] |
冯琦. 烟草腺毛发育及类萜代谢研究[D]. 郑州: 河南农业大学硕士学位论文, 2013.
Feng Q. Studies on development and terpenoid metabolism of tobacco trichome [D]. Zhengzhou: MS Thesis of Henan Agricultural University, 2013. |
| [22] |
杨铁钊, 李伟, 李钦奎, 等. 烤烟叶面腺毛密度及其分泌物变化动态的相关分析[J].
中国烟草科学, 2005, 26(1): 43–46.
Yang T Z, Li W, Li Q K, et al. Analysis of the varying trends and correlation of the density of glandular trichome and leaf surface exudates of flue-cured tobacco[J]. Chinese Tobacco Science, 2005, 26(1): 43–46. |
| [23] |
陈淑珍, 马长力, 高致明, 等. 烟草叶片腺毛发育及其分泌活动对烟叶品质的影响[J].
烟草科技, 1993, 101(4): 32–36.
Chen S Z, Ma C L, Gao Z M, et al. Effects of glandular trichome development and secretary activity on leaf quality in tobacco leaves[J]. Tobacco Science & Technology, 1993, 101(4): 32–36. |
| [24] |
时向东, 刘国顺, 韩锦峰, 等. 不同类型肥料对烤烟叶片腺毛密度、种类及分布规律的影响[J].
中国烟草学报, 1999, 5(2): 22–25.
Shi X D, Liu G S, Han J F, et al. Effect of various fertilizers on the type and distribution of trichome in flue-cured tobacco[J]. Acta Tabacaria Sinica, 1999, 5(2): 22–25. |
| [25] | Nielsen M T, Severson R F. Variation of flavor components on leaf surfaces of tobacco genotypes differing in trichome density[J]. Journal of Agricultural and Food Chemistry, 1990, 38(2): 467–471. DOI:10.1021/jf00092a030 |
| [26] |
张水勤, 袁亮, 林治安, 等. 腐植酸促进植物生长的机理研究进展[J].
植物营养与肥料学报, 2017, 23(4): 1065–1076.
Zhang S Q, Yuan L, Lin Z A, et al. Advances in humic acid for promoting plant growth and its mechanism[J]. Journal of Plant Nutrition and Fertilizer, 2017, 23(4): 1065–1076. DOI:10.11674/zwyf.16255 |
| [27] |
王冬, 张小全, 彭玉富, 等. 昼夜温差和光照强度对烟草西柏三烯二醇的合成及CYC-1、CYP71D16基因表达的影响
[J].
华北农学报, 2014, 29(5): 150–155.
Wang D, Zhang X Q, Peng Y F, et al. Effects of temperature range and light intensity on content of CBT-diols and expression of CYC-1 and CYP71D16 in tobacco [J]. Acta Agriculturae Boreali-Sinica, 2014, 29(5): 150–155. DOI:10.7668/hbnxb.2014.05.026 |
| [28] | Guo Z, Wagner G J. Biosynthesis of cembratrienols in cell-free extracts from trichomes of Nicotiana tabacum [J]. Plant Science, 1995, 110: 1–10. DOI:10.1016/0168-9452(95)04174-S |
| [29] | Wang E, Wang R, DeParasis J, et al. Suppression of a P450 hydroxylase gene in plant trichome glands enhances natural-product-based aphid resistance[J]. Nature Biotechnology, 2001, 19: 371–374. DOI:10.1038/86770 |
| [30] | Lichtenthaler H K. The 1-deoxy-D-xylose-5-phosphate pathway of isoprenoid biosynthesis in plants[J]. Annual Review of Plant Physiology and Plant Molecular Biology, 1999, 50: 47–55. DOI:10.1146/annurev.arplant.50.1.47 |
| [31] | Watanabe H, Takahashi S, Kuzuyama T, et al. A 1-deoxy-d-xylulose 5-phosphate reductoisomerase catalyzing the formation of 2-C-methyl-derythritol 4-phosphate in an alternative nonmevalonate pathway for terpenoid biosynthesis[J]. Proceedings of National Academy of Sciences USA, 1998, 95: 9879–9884. DOI:10.1073/pnas.95.17.9879 |
| [32] | Wang E, Wagner G J. Elucidation of the functions of genes central to diterpene metabolism in tobacco trichomes using posttranscriptional gene silencing[J]. Planta, 2003, 216: 686–691. |
| [33] |
于学健. 黄腐酸调控甜菊糖苷合成的机理及甜菊糖苷的酶法转化[D]. 北京: 中国农业大学博士学位论文, 2016.
Yu X J. Mechanism of stevioside synthesis regulation by fulvic acid and its enzymatic modification [D]. Beijing: PhD Dissertation of China Agricultural University, 2016. |
| [34] |
许原原. 黄腐酸提高苜蓿产量及促进Sinorhizobium meliloti与苜蓿结瘤固氮的作用机理[D]. 北京: 中国农业大学博士学位论文, 2016.
Xu Y Y. The effect of water-soluble humic material on Medicago sativa yield and its mechanism on inducing nodulation and nitrogen fixation of Sinorhizobium meliloti with M. sativa[D]. Beijing: PhD Dissertation of China Agricultural University, 2016. |
| [35] | Fialova S. Metabolism of nucleic acid in wheat roots independent of nutritive conditions[J]. Biologia Plantarum, 1969, 11: 424–431. DOI:10.1007/BF02920706 |
| [36] | Wang W H, Bray C M, Jones M N. The fate of C-labeled humic substance in rice cells in culture[J]. Journal of Plant Physiology, 1999, 154(2): 203–211. DOI:10.1016/S0176-1617(99)80211-9 |
| [37] |
李丁丁. 蔗糖、腐殖酸对平邑甜茶氮素吸收利用和分配影响研究[D]. 山东农业大学硕士学位论文, 2008.
Li D D. Effect of sugar and HA on nitrogen absorption and distribution of Malus hupenensis Rehd [D]. MS Thesis of Shandong Agricultural University, 2008. |
| [38] |
何峰. 西柏三烯-4,6-二醇的分离纯化及热裂解和烟草中HPLC分析方法研究[D]. 郑州: 郑州轻工业学院硕士学位论文, 2015.
He F. Isolation & purification and pyrolysis analysis of cembratriene-4,6-diols and their determination in tobacco with HPLC [D]. Zhengzhou: MS Thesis of Zhengzhou University of Light Industry, 2015. |
| [39] | Canellas L R, Olivares F L, et al. Humic and folvic acids as biostimulants in horticulture[J]. Scientia Horticulturae, 2015, 196: 15–27. DOI:10.1016/j.scienta.2015.09.013 |
| [40] | Arnarp J, Chu W L A, Enzell C R, et al. Tobacco chemistry.77: Biotransformations of a major tobacco cembratrienediol using plant cell cultures of Nicotiana sylvestris [J]. Acta Chemica Scandinavica, 1993, 47(7): 689–694. |
 2018, Vol. 24
2018, Vol. 24  doi:
doi: 

