2. 中国农业科学院研究生院,北京 100081
2. Graduate School of Chinese Academy of Agricultural Sciences, Beijing 100081, China
土壤磷素分为无机磷和有机磷两大类。无机磷主要有矿物态、吸附态和水溶态。矿物态磷包括含磷的原生矿物磷灰石、次生矿物磷铝石和粉红磷铁矿及其他含磷化合物。植物吸收的磷主要是土壤溶液中的磷酸盐。一定条件下土壤中不同形态磷发生相互转化[1–2]。同位素示踪技术是研究生态系统中元素循环与形态转化的重要工具。磷元素有23种同位素,分别从24P到 46P。31P是唯一的稳定同位素,所以无法直接利用稳定性磷同位素开展磷示踪研究[3]。自然界中氧原子存在18O、17O和16O三种稳定性同位素,丰度分别为0.204%、0.037%和99.76%。氧同位素自然丰度组成用δ18O表示,定义为:
| ${{\rm{\delta }}^{{\rm{18}}}}{\rm O} = \left( {\frac{{{R_{sample}}}}{{{R_{VSMOW}}}} - 1} \right) \times 1000$ |
式中:Rsample 为样品18O/16O原子丰度比值;RVSMOW是维也纳标准平均海洋水 (Vienna standard mean ocean water) 的18O/16O原子丰度比值。
磷酸盐中磷原子通过共价键与四个氧原子相连,P—O键能较高,自然条件下稳定,沉淀溶解、吸附解吸等过程中不易导致P—O键断裂[4],利用磷酸盐中氧稳定性同位素可以示踪表征生态系统中磷的转化。
微生物、磷酸酶催化等生物反应,可使磷酸盐与周围水中氧发生交换,导致磷酸盐中氧同位素 (δ18O-P) 出现分馏[5–7]。Longinelli等[8]发表了磷酸盐和周围水体间氧同位素交换平衡分馏系数与温度的关系式T = 111.4 – 4.3 (δ18O-P–δ18O-H2O),式中,T代表海水温度,δ18O-P和δ18O-H2O分别代表磷灰石中磷酸盐和周围水中氧同位素组成。根据实测温度和δ18O-H2O,计算出磷酸盐δ18O-P平衡值。若δ18O-P实测值与计算值接近,说明磷酸盐和周围水分子间氧同位素越接近平衡分馏,即生物对磷利用转化率越高。McLaughlin等[9–12]采用Mg(OH)2-PO4共沉淀法 (MAGIC共沉淀法) 富集提取水体中磷酸盐,再利用CePO4沉淀分离纯化,最终得到磷酸银沉淀,利用元素分析仪—稳定性同位素比例质谱仪测试磷酸盐中氧同位素。
磷素化学连续浸提分级方法研究土壤中磷素的形态和有效性,对揭示和评价土壤磷库大小和土壤磷供应状况具有重要意义[1–2]。Zohar等[13]利用H2O、NaHCO3、NaOH和HCl提取土壤中不同形态无机磷,采用MAGIC共沉淀法分离磷酸盐,每级无机磷分别沉淀为Ag3PO4,结果发现不同形态磷酸盐δ18O-P值存在差异。盐酸提取的磷酸盐主要是石灰性土壤中磷灰石和部分闭蓄态磷,难以直接被作物吸收利用,但在根系分泌物和土壤微生物的作用下,可以被转化利用[1–2]。Tamburini等[14]采用以磷酸钼铵和磷酸铵镁先后沉淀–溶解–沉淀的方法 (APM-MAP多步沉淀法) 得到纯净Ag3PO4,对HCl提取的土壤磷酸盐氧同位素进行分析,该方法有效排除了有机磷酸盐水解的干扰,并采用DAX-8树脂进一步吸附溶解液中可能残余的有机质。采用MAGIC共沉淀法富集HCl浸提液中磷酸盐,强酸溶解后,磷酸铈沉淀分离净化,最终得到磷酸银沉淀上机测试,但该法导致土壤中有机磷酸盐或焦磷酸盐发生水解,δ18O-P值明显偏高。土壤成分复杂,利用HCl提取土壤磷酸盐,浸提液中含酸溶性的有机质以及非磷酸盐含氧化合物如硫酸盐、硝酸盐,氧同位素来源复杂,易造成土壤δ18O-P值失真;浸提液含有丰富的Cl– 离子,pH较低,干扰磷酸盐分离纯化形成Ag3PO4沉淀过程[15–16],因此有关HCl提取的土壤磷酸盐δ18O-P研究报道还较为有限。
本文选择黑土和潮土的长期定位试验中NK (不施磷肥)、NPK (施用无机磷肥)、NPKM (施用无机磷肥 + 有机粪肥)、NPKS (NPK + 秸秆还田) 4个施肥处理土样,按照Guppy土壤磷分级方法逐级浸提,通过对盐酸提取磷酸盐 (HCl-Pi) 进行富集、纯化,获得Ag3PO4沉淀,采用元素分析仪—稳定性同位素比例质谱仪 (elemental analyzer-stable isotope ratio mass spectrometers,EA-IRMS) 测定其中δ18O-P值,建立盐酸提取的土壤磷酸盐中氧同位素分析技术,拟为农田土壤中磷的循环转化及其溯源研究提供技术支撑。
1 材料方法 1.1 供试土壤黑土采自“国家土壤肥力和肥料效益长期监测基地”吉林省公主岭市试验点,作物种植模式为一年一熟玉米连作。潮土采自河南省郑州市,作物种植模式为玉米–小麦轮作。两处土壤样品均采集于2015年玉米收获期。供试土壤样品来自4个施肥处理,分别为:1) 不施磷肥 (NK);2) 施用无机氮磷钾肥 (NPK);3) NPK常量,加有机粪肥 (NPKM);4) NPK常量,加粉碎秸秆 (NPKS)。
1.2 仪器与试剂仪器:X射线衍射仪 (型号为Empyrean,PANalytical公司);元素分析仪—稳定性同位素比例质谱仪 (型号:vario PYRO cube-IsoPrime100,Elementar Analysensysteme GmbH公司)。
试剂:硝酸银、硝酸铵、钼酸铵、柠檬酸、氯化镁、氯化铵、氨水 (分析纯,国药集团化学试剂有限公司);DAX-8大孔树脂 (40~60目,Sigma-Aldrich公司);Ag3PO4标准参考品 (标准参考值δ18O = 21.7 ± 0.3‰,Elemental Microanalysis Ltd公司)。
1.3 HCl-Pi提取、富集与纯化步骤1,磷酸盐提取:准确秤取一定量过2 mm筛土壤样品于塑料瓶中,按照Guppy等[17]土壤磷分级方法,分别经过H2O、0.5 mol/L NaHCO3、0.1 mol/L NaOH、1 mol/L HCl逐级浸提,收集1 mol/L HCl的浸提液,离心,收集上清液。NK和NPK处理黑土样品测试时,每个处理3次重复,其他处理的样品,每个处理4次重复。
步骤2,磷钼酸铵沉淀与溶解:参照Tamburini等[14]和Jaisi等[18]方法,向上清液中加入DAX-8大孔树脂,振荡过夜,分离树脂后向溶液中加入4.2 mol/L NH4NO3溶液,50℃水浴条件下加入100 g/L钼酸铵溶液,振荡过夜。离心弃去上清液,沉淀用0.6 mol/L NH4NO3淋洗数次,加入柠檬酸溶液至沉淀完全溶解。
步骤3,磷酸铵镁沉淀与溶解:向溶液中加入10 mL pH 1.0镁溶液 (20 g NH4Cl和10 g MgCl2溶解于100 mL超纯水中,用HCl调节) 至白色沉淀析出。离心,沉淀用氨水 (氨水∶超纯水体积比为1∶1) 淋洗数次,沉淀用0.5 mol/L HNO3溶解,加入H+型阳离子交换树脂,振荡10 h,过滤。
步骤4,形成Ag3PO4沉淀:在滤液中加入2滴溴百里酚蓝指示剂,用氨水和3 mol/L HNO3调节溶液pH 8.0,加入AgNO3溶液,得到黄色Ag3PO4沉淀,沉淀用超纯水洗涤离心数次。
步骤5,Ag3PO4纯化:加入15% H2O2 浸泡过夜,离心,沉淀用超纯水洗涤数次,加入5 mL氨水溶解沉淀,离心收集上清液,置于50℃水浴中,使NH3在高温下缓慢挥发,至黄色Ag3PO4沉淀析出,冷却至室温,离心收集,超纯水清洗数次,50℃下烘干。
1.4 Ag3PO4中氧同位素测定称取0.5 mg左右Ag3PO4样品,包入银舟中,放入元素分析仪 (EA) 自动进样器,样品在1450℃高温条件下裂解,释放O原子被玻璃碳和石墨转化为CO,CO在流速80 mL/min的He气吹扫下进入色谱柱,在85℃条件下与N2分离,进入稳定性同位素比例质谱仪 (IRMS) 测定。质谱CO参考气校准采用国际原子能机构提供的IAEA-601标准参照品Benzoic Acid (δ18O = 23.3‰ ± 0.3‰)。仪器EA工作条件:He载气压力0.2 MPa,CO解吸温度110℃。IRMS工作条件:电压3.117 V,电流1.5 mA,CO参考气信号12.6 nA。利用EA-IRMS对Ag3PO4标准品进行了6次测量,测定结果为δ18O = 21.7‰ ± 0.2‰,与标准参考值δ18O = 21.7‰ ± 0.3‰ 接近,EA-IRMS实验条件满足样品δ18O测定要求。
1.5 实验获得的Ag3PO4纯度测定参照Tamburini等[14]方法,利用EA-IRMS分别测量实验获得的Ag3PO4样品和标准品中氧元素含量,比较两者氧元素含量是否存在差异,从而验证分离得到Ag3PO4样品纯度。
采用X射线衍射仪 (XRD) 测定实验获得Ag3PO4样品的矿物结构特征,与标准图谱比较,进一步检验Ag3PO4样品纯度。XRD工作条件:电压40 kV,电流40 mA,粉末多晶衍射方式为连续扫描模式,测量角度5.000°~65.0054°。
1.6 全流程氧同位素分馏检测按照McLaughlin等[9]和陈志刚等[19]方法,吸取10 mL 100 mg/L的KH2PO4溶液,加入AgNO3直接形成Ag3PO4沉淀。同时吸取10 mL上述KH2PO4溶液,按照HCl-Pi提取、富集与纯化等步骤获得Ag3PO4沉淀,测定此Ag3PO4沉淀的δ18O值,与直接形成Ag3PO4沉淀的δ18O值比较,检验磷酸盐分离流程中氧同位素是否出现分馏。
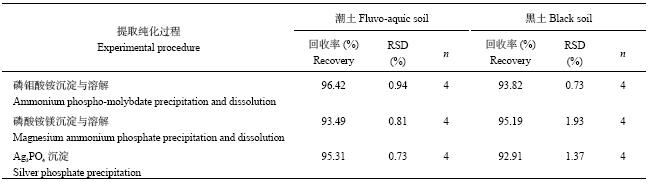
2 结果与分析 2.1 土壤磷酸盐的磷回收率HCl提取土壤磷酸盐富集、分离与纯化流程包括磷钼酸铵沉淀与溶解、磷酸铵镁沉淀与溶解、Ag3PO4沉淀3个重要步骤。表1结果表明,这3个实验步骤中磷回收率均在92%以上,回收率较高,说明实验步骤中磷分离转化较完全,降低了实验流程造成磷酸盐氧同位素分馏的可能。
| 表1 HCl提取土壤磷酸盐的富集、分离与纯化实验室过程中磷回收率 Table 1 Recovery rate and relative standard deviation (RSD) of inorganic phosphate during the process of HCl-Pi extraction and purification, Ag3PO4 precipitation |
 |
本实验获得的Ag3PO4测定XRD谱图,与Ag3PO4标准谱图 (谱库中编号02-070-0702) 比较,十分吻合,说明本实验得到的Ag3PO4样品纯度较高 (图1)。
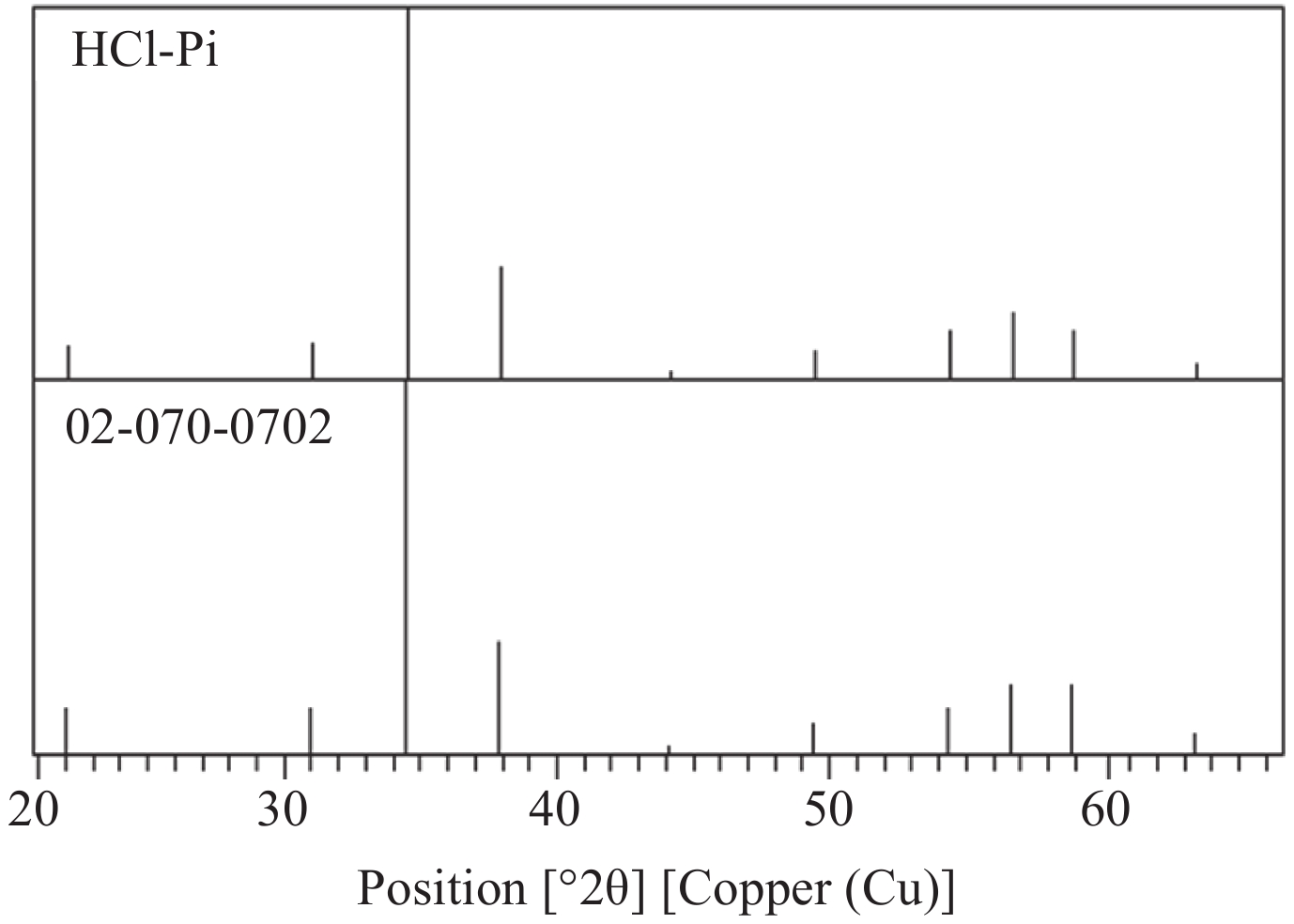 |
| 图1 磷酸银沉淀样品的X射线衍射谱图 Fig. 1 X-ray diffraction diagrams of Ag3PO4 obtained from HCl-Pi |
称取不同量的经过分离纯化获得的Ag3PO4样品,利用EA-IRMS测定,以裂解产生的氧元素含量 (以CO峰高计) 与样品量之间作图,并与Ag3PO4标准品做比较 (图2)。结果发现,Ag3PO4标准品和实验提取的Ag3PO4样品裂解产生的氧元素含量与样品测定量间呈较好的线性关系 (R2 = 0.999,n = 36),表明本实验提取的Ag3PO4样品中氧元含量组成比例和Ag3PO4标准品吻合,进一步验证了本实验步骤获取的Ag3PO4纯度较高。
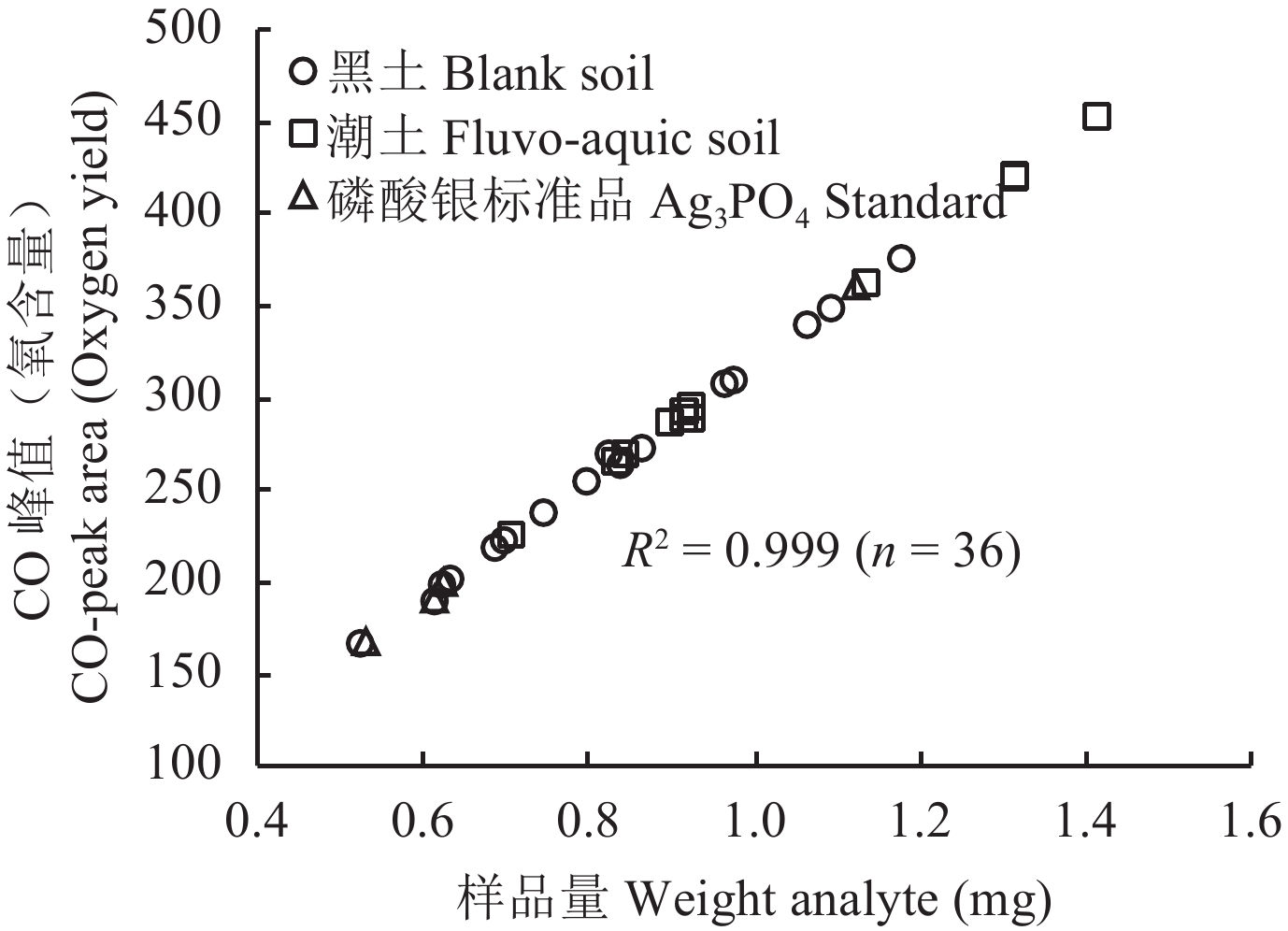 |
| 图2 利用元素分析仪测定HCl-Pi分离纯化获得Ag3PO4样品与Ag3PO4标准品产生的CO量与样品量之间的线性相关图 Fig. 2 Weight of analyte plotted against the CO peak area for Ag3PO4 standard and samples obtained from HCl-Pi |
利用KH2PO4溶液直接与AgNO3反应形成Ag3PO4沉淀,测定其δ18O-P值为 (6.82 ± 0.26)‰ (n = 4)。KH2PO4溶液通过磷钼酸铵沉淀与溶解、磷酸铵镁沉淀与溶解及Ag3PO4沉淀纯化等实验流程形成Ag3PO4沉淀,δ18O-P值为 (6.73 ± 0.11)‰ (n = 4),两者绝对相差0.09‰,无显著性差异,表明HCl-Pi在分离纯化全流程中没有产生氧同位素分馏。
Tamburini等[14]向HCl提取土壤样品磷酸盐中加入18O标记水,示踪磷酸盐通过APM-MAP多步沉淀法得到纯净磷酸银过程中是否发生氧同位素分馏,结果证明实验过程未出现同位素分馏。
2.4 黑土和潮土HCl-Pi的δ18O-P结果从图3结果可知,黑土与潮土各施肥处理中HCl-Pi的δ18O-P依次为16.91‰和17.90‰ (NK)、17.25‰和17.61‰ (NPK)、17.62‰和17.87‰ (NPKM)、17.90‰和17.70‰ (NPKS),各个处理间δ18O-P均无显著差异。瑞士与以色列两地不同施肥处理的HCl提取土壤磷酸盐δ18O-P值为13.5‰~17.6‰,农田土壤中磷酸盐δ18O-P相对富集,为19‰左右[14]。采用APM-MAP多步沉淀法富集纯化HCl提取的土壤磷酸盐,通过H2O2漂洗去除有机质,辅以氨水重结晶去除Ag3PO4 中夹杂的Ag2O和Ag等杂质,测定厦门集美地区森林、公园和农田HCl提取土壤磷酸盐δ18O-P值在15.2‰~19.5‰之间[20]。Amelung等[21]采用APM-MAP多步沉淀法,富集提取德国施用矿质磷肥和有机肥的土壤HCl浸提磷酸盐。发现有机粪肥δ18O-P值较化学磷肥低,可能导致长期施用有机粪肥土壤δ18O-P值 (17.2‰ ± 2.23‰) 低于化学磷肥施用的土壤 (19.8‰ ± 0.56‰),长期施肥条件下,土壤磷酸盐供给主要来源于肥料。
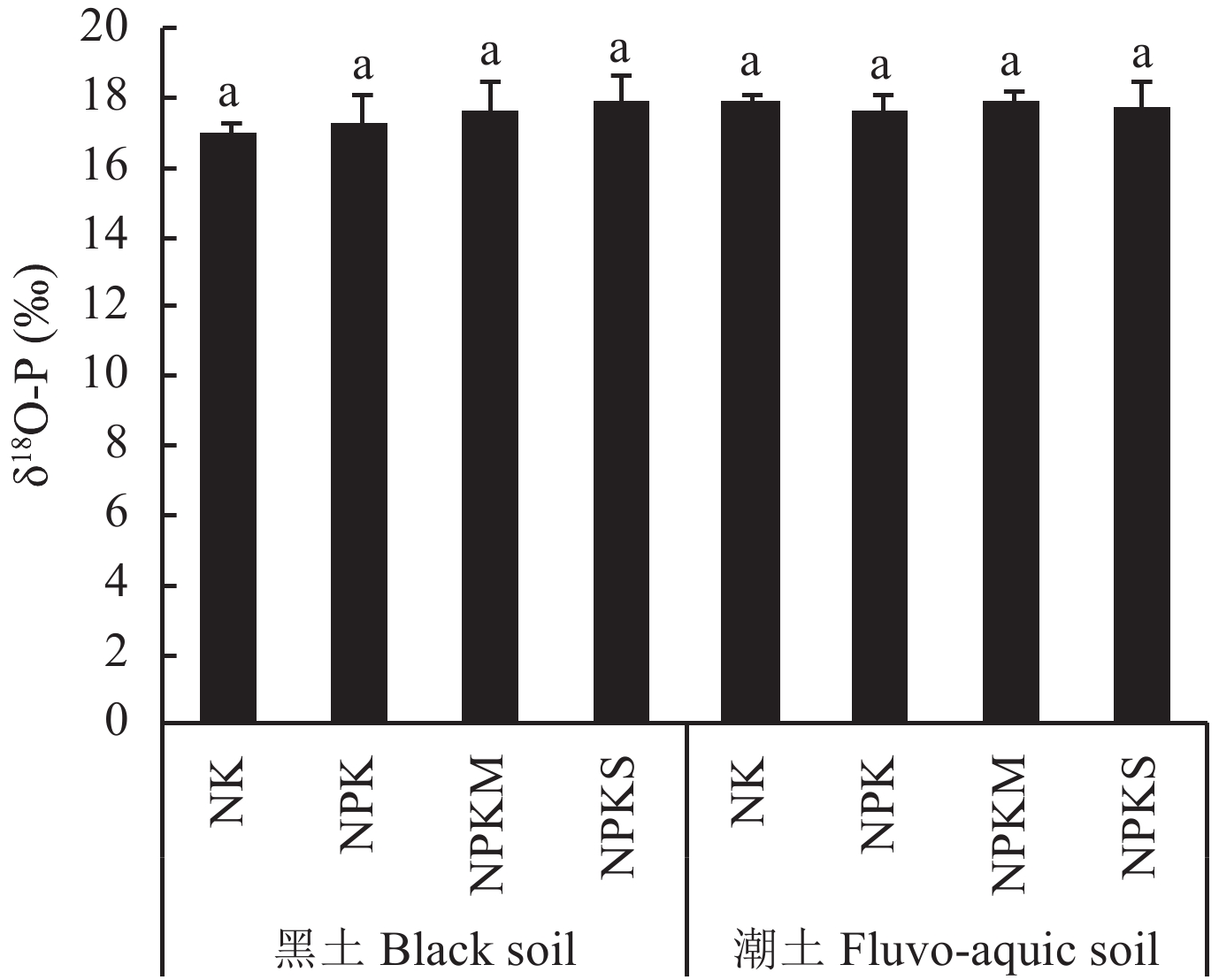 |
| 图3 长期施肥处理黑土和潮土HCl浸提土壤磷酸盐δ18O-P Fig. 3 Isotopic oxygen composition (δ18O-P) of inorganic phosphate extracted by HCl from the soils under long-term fertilization [注(Note):柱上相同字母表示不同处理之间数据差异不显著 (P < 0.05, Ducan检验)The same letters above the bars indicate no significant difference among different treatments (P < 0.05, Ducan test).] |
连续浸提土壤后,利用1 mol/L HCl土壤浸提液,对浸提液中磷酸盐采用磷酸钼铵和磷酸铵镁先后沉淀–溶解–沉淀方法进行提取纯化,获得磷酸银沉淀,关键过程中磷回收率均在92%以上,磷酸盐损失较少;XRD和氧含量测定表明,磷酸银沉淀纯化效果较好。分离纯化过程中未出现氧同位素分馏。测定供试黑土与潮土HCl-Pi的δ18O-P分别为16.91‰和17.90‰ (NK)、17.25‰和17.61‰ (NPK)、17.62‰和17.87‰ (NPKM)、17.90‰和17.70‰ (NPKS)。本研究建立了盐酸提取的土壤磷酸盐中氧同位素分析测定方法,为农田土壤中磷的循环转化及其溯源研究提供技术支撑。
| [1] | Condron L M, Turner B L, Cademenun B J, et al. Chemistry and dynamics of soil organic phosphorus [A]. Sims J T, Sharpley A N, Pierzynski G M, et al. Phosphorus: Agriculture and the environment[M]. Madison: American Society of Agronomy, 2005. 87–121. |
| [2] | Condron L M, Newman S. Revisiting the fundamentals of phosphorus fractionation of sediments and soils[J]. Journal of Soils and Sediments, 2011, 11(5): 830–840. DOI:10.1007/s11368-011-0363-2 |
| [3] | Bünemann E K, Steinebrunner F, Smithson P C, et al. Phosphorus dynamics in a highly weathered soil as revealed by isotopic labeling techniques[J]. Soil Science Society of America Journal, 2004, 68(5): 1645–1655. DOI:10.2136/sssaj2004.1645 |
| [4] | Liang Y, Blake R E. Oxygen isotope fractionation between apatite and aqueous-phase phosphate: 20–45℃[J]. Chemical Geology, 2007, 238(1–2): 121–133. |
| [5] | Longinelli A, Bartelloni M, Cortecci G. The isotopic cycle of oceanic phosphate[J]. Earth and Planetary Science Letters, 1976, 32(2): 389–392. DOI:10.1016/0012-821X(76)90079-0 |
| [6] | Blake R E, O'Neil J R, Surkov A V. Biogeochemical cycling of phosphorus: Insights from oxygen isotope effects of phosphoenzymes[J]. American Journal of Science, 2005, 305(6–8): 596–620. |
| [7] | Li X, Wang Y, Stern J. Isotopic evidence for the source and fate of phosphorus in Everglades wetland ecosystems[J]. Applied Geochemistry, 2011, 26(5): 688–695. DOI:10.1016/j.apgeochem.2011.01.027 |
| [8] | Longinelli A. Revised phosphate–water isotopic temperature scale[J]. Earth and Planetary Science Letters, 1973, 19: 373–376. DOI:10.1016/0012-821X(73)90088-5 |
| [9] | McLaughlin K, Silva S, Kendall C, et al. A precise method for the analysis of δ18O of dissolved inorganic phosphate in seawater [J]. Limnology and Oceanography Methods, 2004, 2: 202–212. DOI:10.4319/lom.2004.2.202 |
| [10] | McLaughlin K, Cade-Menun B J, Paytan A. The oxygen isotopic composition of phosphate in Elkhorn Slough, California: A tracer for phosphate sources[J]. Estuarine Coastal and Shelf Science, 2006, 70(3): 499–506. DOI:10.1016/j.ecss.2006.06.030 |
| [11] | McLaughlin K, Kendall C, Silva S R, et al. Phosphate oxygen isotope ratios as a tracer for sources and cycling of phosphate in North San Francisco Bay, California[J]. Journal of Geophysical Research: Biogeosciences, 2006, 111: 2156–2202. |
| [12] | McLaughlin K, Paytan A, Kendall C, et al. Oxygen isotopes of phosphatic compounds–Application for marine particulate matter, sediments and soils[J]. Marine Chemistry, 2006, 98(2): 148–155. |
| [13] | Zohar I, Shaviv A, Klass T, et al. Method for the analysis of oxygen isotopic composition of soil phosphate fractions[J]. Environmental Science and Technology, 2010, 44(19): 7583–7588. DOI:10.1021/es100707f |
| [14] | Tamburini F, Bernasconi S M, Angert A, et al. A method for the analysis of the δ18O of inorganic phosphate extracted from soils with HCl [J]. European Journal of Soil Science, 2010, 61(6): 1025–1032. DOI:10.1111/ejs.2010.61.issue-6 |
| [15] |
张晗, 王佳妮, 郭庆军, 等. 土壤磷酸盐氧同位素分析方法和应用研究进展[J].
土壤学报, 2015, 52(1): 19–27.
Zhang H, Wang J N, Guo Q J, et al. Advance in study on method for oxygen isotopic analysis of phosphate in soil and its application[J]. Acta Pedologica Sinica, 2015, 52(1): 19–27. DOI:10.11766/trxb201401150028 |
| [16] | Tamburini F, Pfahler V, Sperber C. Oxygen isotopes for unraveling phosphorus transformations in the soil–plant system: A review[J]. Soil Science Society of America Journal, 2014, 78(1): 47–53. DOI:10.2136/sssaj2013.05.0159 |
| [17] | Guppy C N, Menzies N W, Moody P W, et al. A simplified, sequential, phosphorus fractionation method[J]. Communications in Soil Science and Plant Analysis, 2000, 31(11): 1981–1991. |
| [18] | Jaisi D P, Blake R E. Tracing sources and cycling of phosphorus in Peru Margin sediments using oxygen isotopes in authigenic and detrital phosphates[J]. Geochimica et Cosmochimica Acta, 2010, 74: 3199–3212. DOI:10.1016/j.gca.2010.02.030 |
| [19] |
陈志刚, 黄奕普, 刘广山, 等. 磷酸盐氧同位素组成的测定方法及分馏机理研究进展[J].
地球科学进展, 2010, 25(10): 1040–1050.
Chen Z G, Huang Y P, Liu G S, et al. Advances in the measurement methods and fractionation mechanism of the oxygen isotope composition of phosphate[J]. Advances in Earth Science, 2010, 25(10): 1040–1050. |
| [20] |
张晗, 王佳妮, 朱永官, 等. 土壤无机磷酸盐中氧同位素分析方法的研究及应用[J].
分析化学, 2015, 43(2): 187–192.
Zhang H, Wang J N, Zhu Y G, et al. Research and application of analytical technique on δ18OP of inorganic phosphate in soil [J]. Chinese Journal of Analytical Chemistry, 2015, 43(2): 187–192. |
| [21] | Amelung W, Antar P, Kleeberg I, et al. The δ18O signatures of HCl-extractable soil phosphates: methodological challenges and evidence of the cycling of biological P in arable soil [J]. European Journal of Soil Science, 2015, 66(6): 965–972. DOI:10.1111/ejss.2015.66.issue-6 |
 2018, Vol. 24
2018, Vol. 24  doi:
doi: 

