文章信息
- 两样本孟德尔随机化研究肢端肥大症与结肠癌的因果关系
- Causal Relationship Between Acromegaly and Colon Cancer: A Two-sample Mendelian Randomization Study
- 肿瘤防治研究, 2023, 50(12): 1209-1213
- Cancer Research on Prevention and Treatment, 2023, 50(12): 1209-1213
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2023.23.0507
- 收稿日期: 2023-05-11
- 修回日期: 2023-06-20
2. 730000 兰州,兰州市第一人民医院药剂科;
3. 730000 兰州,兰州大学第一临床医学院
2. Department of Pharmacy, The First People's Hospital of Lanzhou, Lanzhou 730000, China;
3. The First Clinical Medical College of Lanzhou University, Lanzhou 730000, China
结肠癌是严重威胁人类生命健康的常见恶性肿瘤之一,其发病率和死亡率都很高[1]。中华医学会内分泌学分会发布的《肢端肥大症诊治规范(草案)》指出,肢端肥大症可能导致结肠癌等恶性肿瘤的发生率增加[2]。肢端肥大症是由分泌生长激素的垂体腺瘤引起的一种骨骼、组织和器官生长不成比例的疾病,临床上多表现为肢端和面部变化、多汗症、头痛、感觉异常、性功能障碍、高血压、甲状腺肿和罕见的视野缺损等[3-4]。相关研究指出,肢端肥大症致死的主要原因并不是垂体腺瘤,而多是由其引起的多系统并发症所致,其中最主要的是心血管系统疾病及呼吸系统疾病[5],另有相关研究显示,肢端肥大症还可能增加部分恶性肿瘤的发生率[6-7],而且Rokkas等的一项研究[8]结果显示肢端肥大症可能导致结肠癌的发病风险增加,类似的研究也显示,相对于健康群体,肢端肥大症患者的结肠癌发病率和死亡率均更高[9-10],但是也有研究表明,肢端肥大症患者的较高结肠癌发病率并不是一个普遍的研究结果[11]。本研究引入孟德尔随机化的方法来明确肢端肥大症与结肠癌发病的因果关系及关联强度。
近年来,孟德尔随机化在医学研究和实践中逐渐兴起,相关研究发现孟德尔随机化研究近年的发文量正快速增长,这表明孟德尔随机化研究已成为流行病学的研究热点[11]。相关研究也完善了孟德尔随机化研究的报告要点[12]。孟德尔随机化研究是一种以孟德尔独立分配定理为基础的流行病学研究工具,采用遗传变异,即单核苷酸多态性(SNP)作为工具变量来评估复杂疾病的危险因素的因果关系,根据孟德尔定律:配子在形成时遵循等位基因随机分配的原则,潜在的混杂因素也会被平均分布于两组,使基因表型的遗传效应不会受到常见混杂因素的干扰,因此,孟德尔随机化研究可以克服观察性研究中存在的混杂因素和反向因果关系等局限性因素,可以作为研究暴露因素与结局因果关系的有效手段。
1 资料与方法 1.1 研究设计本研究采用两样本孟德尔随机化分析研究肢端肥大症与结肠癌风险之间的因果关系。其中将肢端肥大症作为暴露因素,选择与肢端肥大症显著相关的单核苷酸多态性作为工具变量,以结肠癌作为结局变量。随后采用Cochran Q检验进行异质性检验,最后采用“留一法(leave-one-out)”对所获得的结果进行敏感性分析以验证其可靠性。
1.2 数据来源肢端肥大症的遗传数据来自于芬兰数据库(The FinnGen Biobank),遗传数据的人群来源为欧洲,男女不限。结肠癌的遗传数据来自于UK Biobank数据库(https://www.ukbiobank.ac.uk/),数据ID为:ukb-b-20145,遗传数据的人群来源为欧洲,男女不限。数据下载时间为2022年10月2日。数据详情见表 1。
孟德尔随机化工具变量应满足如下要求:(1)工具变量应与暴露高度相关,P < 5×10-8。(2)工具变量与结局不直接相关,仅通过暴露影响结局,即不存在基因多效性。此次研究以MR-Egger检验的截距不为0(即P < 0.05)表明不存在基因多效性。从肢端肥大症的全基因组关联分析(GWAS)汇总数据中筛选出有意义的SNP(P < 5×10-8),设定连锁不平衡系数r2 < 0.001,连锁不平衡区域宽度为10 000 kb,从而保证各个SNP相互独立。从结肠癌的GWAS数据中提取出按照上述标准筛选出的与肢端肥大症相关的SNP。汇总上述两个数据集的信息,剔除暴露因素中与结肠癌直接相关的SNP(P < 5×10-8)[10]。最后计算所纳入SNP的F统计量来评估工具变量的强度[13],F统计量 < 10表明可能为弱工具变量。计算公式如下:
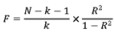 |
(1) |
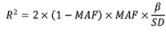 |
(2) |
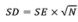 |
(3) |
公式1中:N:GWAS研究的样本数;K:工具变量的个数;R2:工具变量解释暴露的程度。公式2中:MAF:最小等位基因频率;β:SNP对暴露的效应量;SD:标准差。公式3中:SE:式2中β的标准误;N:GWAS研究的样本数。
1.4 研究方法本研究采用R4.2.1进行统计分析,软件包TwoSampleMR可在GitHub网站上下载。根据孟德尔随机化分析的要求,遗传变异作为工具变量时需要满足以下三个假设;(1)关联性假设:工具变量与暴露因素(肢端肥大症)应显著相关;(2)独立性假设:工具变量应与混杂因素无关;(3)排他性假设:工具变量只能通过暴露因素去影响结局变量,而不能通过其他途径。
本研究采用逆方差加权法(IVW),MR-Egger法,加权中位数法(Weight Median)进行统计分析,IVW是一种加权线性回归模型,在多种工具变量的MR研究中使用,其首先计算出每个SNP的因果效应估计值,随后利用Meta分析的随机效应模型结合每个工具变量的因果效应估计值,在此基础上获得一个总因果效应估计值[14]。MR-Egger回归多用于Meta分析研究,以检查发表偏倚、检测基因多效性,其截距是定向多重性的指标[15]。Weight Median是采用加权中位数方法来补充MR-Egger回归,与MR-Egger回归相比,加权中位数的显著优势在于即使在50%的SNPs都具有多效性的情况下,仍然可以得出比较准确的因果估计[16]。在进行孟德尔随机化研究之前,需要对基因遗传变异进行多效性评估,本研究采用MR-Egger回归的方法对工具变量进行基因多效性检验,P > 0.05为差异无统计学意义。即工具变量不存在基因多效性的影响。另外,进行孟德尔随机化后因采用“leave-one-out”法进行敏感性分析,用以评价非特异SNP对因果估计结果的影响大小。
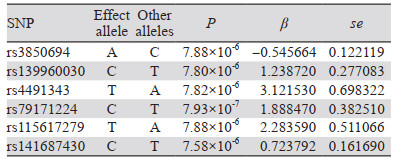
2 结果 2.1 工具变量SNP的筛选与验证根据全基因组关联研究中的检验水准,以P < 5×10-8为标准筛选SNP,经筛选,在本研究中所应用肢端肥大症GWAS数据中未筛选出可用的SNP,因此调整P值为1×10-5再次筛选[17],筛选出65个SNP,设定连锁不平衡系数r2为0.001,连锁不平衡区域宽度为10 000 kb,最终得到6个SNP作为工具变量,见表 2。
|
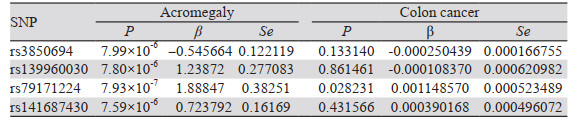
随后,找到初步筛选的6个工具变量在两个数据库结肠癌遗传数据中对应的信息。在UK Biobank数据库结肠癌遗传数据中有5个工具变量,5个工具变量在结肠癌GWAS数据中均满足P > 1×10-5,见表 3。
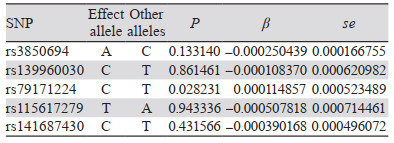
对以上数据进行整合,结肠癌遗传数据在整合过程中剔除了一个具有中间等位基因频率的回文SNP,为rs115617279。整合后见表 4。可见最终所筛选得到的4个工具变量满足两样本孟德尔随机化分析的第一假设和第二假设:工具变量必须与肢端肥大症相关联,工具变量只通过肢端肥大症对结肠癌风险产生效应。根据前述公式计算最终获得的工具变量的F统计量,rs3850694的F值为261.32,rs139960030的F值为20.66,rs79171224的F值为6.99,rs141687430的F值为92.44。
本研究采用MR-Egger回归的方法对工具变量进行基因多效性检验。分析结果显示:截距=0.0005(P=0.42)。两组数据均无统计学意义,说明本研究筛选出的工具变量未受到基因多效性的过大影响。
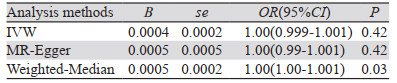
2.3 因果效应估计的结果在两样本孟德尔随机化的研究过程中,为了保证研究结果的准确性,本研究采用了IVW、MR-Egger、MR-Weighted-Median三种分析方法对肢端肥大症和结肠癌风险的因果效应进行评估,对比分析结果如下,IVW法:OR=1.00, 95%CI=0.999~1.001, P=0.42;MR-Egger法:OR=1.00, 95%CI=0.99~1.001, P=0.42;Weighted-Median法:OR=1.00, 95%CI=1.00~1.001, P=0.03。三种分析方法的研究结果一致,表明肢端肥大症不是结肠癌的独立危险因素,见表 5、图 1。

|
| 图 1 三种模型散点图比较 Figure 1 Comparison of scatter plots among three models |
由于数据来源于不同的GWAS队列研究,工具变量之间可能存在异质性,本研究采用IVW模型和MR-Egger模型估算异质性,研究结果表明MR-Egger: Q=3.30, P=0.19, IVW: Q=3.41, P=0.33。两个不同数据库的结肠癌GWAS采用不同方法的异质性检验结果均显示P > 0.05,表明筛选出的工具变量之间不存在异质性。
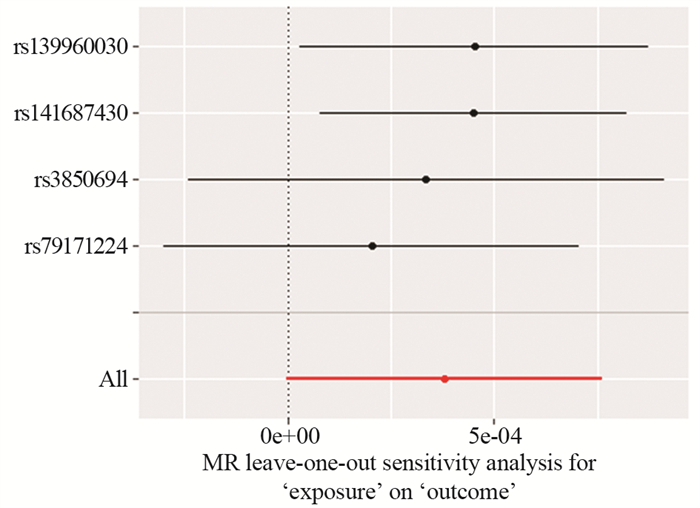
2.5 敏感度分析本研究采用逐一剔除工具变量SNP的方法对研究结果进行敏感度分析。研究结果见图 2,可见所有工具变量SNP的置信区间基本均在原点右侧(其中rs3850694、rs79171224的置信区间经过原点),说明本孟德尔随机化研究的结果比较稳健。
|
| 图 2 “留一法”敏感性分析 Figure 2 Sensitivity analysis of "leave-one-out" |
既往研究显示,结肠癌具有多种危险因素[18],而相关研究表明肢端肥大症可能引起结肠癌的发病率升高[8],其最终纳入了3项病例对照研究进行Meta分析,结果显示,相对于对照组,肢端肥大症患者的结肠癌发病率是对照组的4.35倍(OR=4.35(1.433~12.354)),该研究所纳入的样本量较少(肢端肥大症组14/304,对照组8/627),虽然是无异质性检验且无发表偏倚,但研究结果并不是决定性的。另外由于病例对照研究及Meta分析固有的缺陷[19-20],本研究结论也不一定是可靠的,此外本研究的前期研究也表明该研究质量可信度极低[21],因此采用两样本孟德尔随机化对肢端肥大症与结肠癌发病的相关性进行研究。
Ochiai等研究发现肢端肥大症患者结直肠息肉的发生率明显增加,尤其在直肠乙状结肠区域。然而,尚未发现肢端肥大症患者比一般人群更容易患结直肠癌的病理学证据。肢端肥大症由GH和IGF-I水平过高的不适当分泌所引起,导致许多全身并发症,包括心血管、呼吸和代谢疾病,以及一些肿瘤的潜在风险增加。尽管关于肢端肥大症和癌症的研究结果存在不确定性,但大多数数据表明结直肠癌在研究人群中发病率增加。GH-IGF-I轴在结直肠癌中的确切作用机制尚未完全解释清楚,但它与GH和IGF-I对结肠的局部和循环作用有关,促进血管生成、细胞增殖、突变风险、抑制肿瘤抑制基因表达和凋亡,从而促进肿瘤微环境的形成[22]。
然而,基于人群的研究结果对于CRC的发病率和死亡率存在争议。孟德尔随机化分析的有效性依赖于所研究人群的代表性和多样性。遗传数据的人群来源于欧洲以及结果的普适性问题,是重要的考虑因素。如果遗传数据仅限于欧洲人,那么该研究的结果可能在其他人群中的适用性有限。对于肢端肥大症与结肠癌的因果关系,未来的研究可以考虑拓展研究样本,包括不同人种和地理区域的人群,以更好地了解这种关系的普适性。
尽管在肢端肥大症中进行结肠镜筛查和监测是所有国际指南和专家共识的共识,但关于最佳筛查时机尚无一致意见。综合现有数据,包括病理生理学、流行病学研究及其局限性、结肠息肉特征、总体癌症和结直肠癌发病率和死亡率、结肠癌病理生理学的风险因素和指南建议,可以得出结论认为肢端肥大症和结直肠癌的发病关系尚不明确[23-24]。为了全面评估这种关联,需要更大样本量和跨地区、跨人种的研究。
孟德尔随机化的一个基本假设是:遗传变异不会通过其他生物途径影响结局(即SNP不具有基因多效性)。本研究中对与肢端肥大症相关的4个SNP进行多效性检验,以评估多效性对因果估计的影响,根据这些不同的测试发现本研究的结果是稳健的。最终结论与之前的Meta分析及相关对照试验研究结果不一致,主要考虑原因如下:(1)既往研究多采用小样本的队列研究和病例对照试验,检验效能不强;(2)既往多采用观察性研究来对暴露因素与结局的相关性进行研究,而观察性研究无法完全控制或者消除潜在的混杂因素,这使得既往的研究结果未必可靠;(3)已发表的Meta分析和相关研究与本研究进行孟德尔随机化分析的人群来源不同。
总之,采用孟德尔随机化研究结果显示,肢端肥大症与结肠癌的发病并无相关性,与既往的队列研究及Meta分析结论不一致,这就要求研究人员进行进一步的研究,以明确肢端肥大症是否是结肠癌发病的危险因素。
利益冲突声明:
所有作者均声明不存在利益冲突。
作者贡献:
魏巍:研究方法和数据分析,论文撰写
刘明:研究方法的完善和指导
许建国、高亚:数据检索和下载
申采奕:数据分析
田金徽:论文审阅和修改
| [1] |
罗玉政, 李铁军, 王佾. 腺病毒介导miR-99a过表达抑制人结肠癌HCT-8细胞的生长抑制及其作用机制[J]. 兰州大学学报(医学版), 2016, 42(3): 22-28. [Luo YZ, Li TJ, Wang J. Adenovirus-mediated miR-99a overexpression inhibits the growth inhibition of human colon cancer HCT-8 cells and its mechanism[J]. Lanzhou Da Xue Xue Bao(Yi Xue Ban), 2016, 42(3): 22-28.] |
| [2] |
中华医学会内分泌学分会, 中华医学会神经外科学分会. 肢端肥大症诊治规范(草案)[J]. 中华神经外科杂志, 2007, 23(6): 8. [Chinese Society of Endocrinology. Criteria for diagnosis and treatment of acromegaly (draft)[J]. Zhonghua Shen Jing Wai Ke Za Zhi, 2007, 23(6): 8.] |
| [3] |
Fleseriu M, Langlois F, Lim DST, et al. Acromegaly: pathogenesis, diagnosis, and management[J]. Lancet Diabetes Endocrinol, 2022, 10(11): 804-826. DOI:10.1016/S2213-8587(22)00244-3 |
| [4] |
Melmed S. Acromegaly pathogenesis and treatment[J]. J Clin Invest, 2009, 119(11): 3189-3202. DOI:10.1172/JCI39375 |
| [5] |
Gadelha MR, Kasuki L, Lim DST, et al. Systemic Complications of Acromegaly and the Impact of the Current Treatment Landscape: An Update[J]. Endocr Rev, 2019, 40(1): 268-332. |
| [6] |
Alexander L, Appleton D, Hall R, et al. Epidemiology of acromegaly in the Newcastle region[J]. Clin Endocrinol(Oxf), 1980, 12(1): 71-79. DOI:10.1111/j.1365-2265.1980.tb03135.x |
| [7] |
Ritchie CM, Atkinson AB, Kennedy AL, et al. Ascertainment and natural history of treated acromegaly in Northern Ireland[J]. Ulst Med J, 1990, 59(1): 55-62. |
| [8] |
Rokkas T, Pistiolas D, Sechopoulos P, et al. Risk of colorectal neoplasm in patients with acromegaly: a meta-analysis[J]. World J Gastroenterol, 2008, 14(22): 3484-3489. DOI:10.3748/wjg.14.3484 |
| [9] |
Bengtsson BA, Edén S, Ernest I, et al. Epidemiology and long-term survival in acromegaly. A study of 166 cases diagnosed between 1955 and 1984[J]. Acta Medica Scand, 1988, 223(4): 327-335. DOI:10.1111/j.0954-6820.1988.tb15881.x |
| [10] |
Pines A, Rozen P, Ron E, et al. Gastrointestinal tumors in acromegalic patients[J]. Am J Gastroenterol, 1985, 80(4): 266-269. |
| [11] |
Xu J, Li M, Gao Y, et al. Using Mendelian randomization as the cornerstone for causal inference in epidemiology[J]. Environ Sci Pollut Res Int, 2022, 29(4): 5827-5839. DOI:10.1007/s11356-021-15939-3 |
| [12] |
刘明, 高亚, 杨珂璐, 等. 孟德尔随机化研究的报告规范(STROBE-MR)解读[J]. 中国循证医学杂志, 2022, 22(8): 978-987. [Liu M, Gao Y, Yang KL, et al. STROBE-MR Interpretation of Mendel's Randomized Research[J]. Zhongguo Xun Zheng Yi Xue Za Zhi, 2022, 22(8): 978-987.] |
| [13] |
Bowden J, Del Greco MF, Minelli C, et al. Assessing the suitability of summary data for two-sample Mendelian randomization analyses using MR-Egger regression: the role of the I2 statistic[J]. Int J Eepidemiol, 2016, 45(6): 1961-1974. |
| [14] |
Ortego J, Vega B, Sampedro J, et al. Neoplastic colonic polyps in acromegaly[J]. Horm Metab Res, 1994, 26(12): 609-610. DOI:10.1055/s-2007-1001769 |
| [15] |
Moghetti P. Insulin Resistance and Polycystic Ovary Syndrome[J]. Curr Pharm Des, 2016, 22(36): 5526-5534. DOI:10.2174/1381612822666160720155855 |
| [16] |
Macut D, Bjekić-Macut J, Rahelić D, et al. Insulin and the polycystic ovary syndrome[J]. Diabetes Res Clin Pract, 2017, 130: 163-170. |
| [17] |
Cai J, He L, Wang H, et al. Genetic liability for prescription opioid use and risk of cardiovascular diseases: a multivariable Mendelian randomization study[J]. Addiction, 2022, 117(5): 1382-1391. DOI:10.1111/add.15767 |
| [18] |
Orme SM, McNally RJ, Cartwright RA, et al. Mortality and cancer incidence in acromegaly: a retrospective cohort study. United Kingdom Acromegaly Study Group[J]. J Clin Endocrinol Metab, 1998, 83(8): 2730-2734. |
| [19] |
Bowden J, Davey Smith G, Haycock PC, et al. Consistent Estimation in Mendelian Randomization with Some Invalid Instruments Using a Weighted Median Estimator[J]. Genet Epidemiol, 2016, 40(4): 304-314. DOI:10.1002/gepi.21965 |
| [20] |
Dupépé EB, Kicielinski KP, Gordon AS, et al. What is a Case-Control Study?[J]. Neurosurgery, 2019, 84(4): 819-826. |
| [21] |
魏巍. 基于伞形评价和孟德尔随机化的结肠癌危险因素证据研究[D]. 兰州: 兰州大学, 2022. [Wei W. Evidence study on risk factors of colon cancer based on umbrella evaluation and Mendelian randomization[D]. Lanzhou: Lanzhou University, 2022.]
|
| [22] |
Ochiai Y, Inoshita N, Iizuka T, et al. Clinicopathological features of colorectal polyps and risk of colorectal cancer in acromegaly[J]. Eur J Endocrinol, 2020, 182(3): 313-318. |
 2023, Vol. 50
2023, Vol. 50