文章信息
- 胃癌术后胃排空延迟的肠-胃抑制负反馈发病机制
- Negative Feedback Mechanism of Entero-gastric Inhibitory in Delayed Gastric Emptying Following Surgery for Stomach Cancer
- 肿瘤防治研究, 2022, 49(8): 760-763
- Cancer Research on Prevention and Treatment, 2022, 49(8): 760-763
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2022.21.1243
- 收稿日期: 2021-11-03
- 修回日期: 2021-11-29
在我国,胃癌是一种常见恶性肿瘤。术后胃排空延迟(delayed gastric emptying, DGE)又称胃排空障碍或胃轻瘫(gastroparesis),是远端胃大部分切除术后的一种常见并发症。文献中对术后胃排空延迟的原因和机制众说纷纭[1],本文重点介绍肠-胃抑制反射这一负反馈机制。
1 胃排空的生理机制胃排空的调节机制错综复杂,此外,人们对各种调节机制之间的相互关系尚未完全了解。食物进入胃和十二指肠后,其容量、渗透压、pH和营养成分(如:脂肪、蛋白质)等特性激活十二指肠的黏膜受体,通过神经和体液因素抑制胃排空,既有外部神经(来自大脑和脊髓)控制,又有位于胃肠管壁内的复杂神经丛和Cajal间质细胞通路协调(所谓“肠脑”理念),还有近段小肠释放的递质(胃动素、缩胆囊素和胰多肽等)等因素参与,最终使胃肠平滑肌的兴奋性改变。很显然,调控的目的是为食糜的渗透压平衡、酸中和以及脂质的溶解和消化争取时间。这些调控机制中的某一项出现异常都会使得胃肠肌肉的正常工作受到影响,出现DGE。DGE的临床表现通常为上胃肠道症状,包括恶心、呕吐、餐后饱胀、早饱或易饱感、腹部胀满感和体重减轻,甚至腹痛。在这些胃肠运动调控机制中,最重要的是十二指肠的机械性扩张对胃排空的负反馈抑制作用[2-3]。
2 胃排空延迟的分类DGE是一种重要的临床疾病,其特征是在没有机械性出口阻塞情况下,胃内容的移动排出减缓或停止。从病因学角度,DGE可以分为特发性、糖尿病性和外科手术相关性三大类[4]。前两种DGE通常系患者自身疾病所致,后一种DGE属于手术后并发症。术后DGE不仅给患者身心带来负面影响、延长住院时间、陡增相关医疗费用,严重者还会因为营养不良或呕吐误吸导致死亡,甚至可能成为医疗纠纷的“导火索”。这就要求外科医生掌握DGE的发病机制,采取有针对性的预防措施,能早期识别和处理这一外科并发症。
术后DGE又可以进一步分为原发性和继发性。术后继发性DGE是指与胰漏、胆漏、腹腔积液、脓毒症和肺部并发症等术后并发症相关的DGE。术后原发性DGE的发病机制迄今不明,主要见于上消化道手术后,外科医生很难采取针对性预防措施。胰十二指肠切除(Whipple手术)后DGE发生率为14%~30%[1],远端胃切除术后为5%~25%[5]。2007年国际胰腺外科学组(International Study Group of Pancreatic Surgery, ISGPS)对术后DGE颁布了行业定义,统一了术后DGE的诊断和分级标准[6],便于研究报告之间相互比较。然而,依旧有文献未参照ISGPS的标准[7],甚至有研究者试图修改诊断标准[8],这是术后DGE发生率各家报道差异大的原因之一,也妨碍了人们对这一并发症的进一步探究。
3 术后原发性胃排空延迟的发生机制人们对术后原发性DGE发病原因的关注已经超过半个世纪。研究表明与原发性DGE发病的相关的因素繁多,除了公认的术前胃潴留、营养不良(肌少症)、糖尿病和病毒感染等因素外,涉及外科操作细节的因素包括:十二指肠切除后或缺血后循环中胃动素、缩胆囊素、胰多肽等水平下降,迷走神经的胃窦和幽门支损伤,结肠前或结肠后胃肠吻合法; BillrothⅡ式、Roux-en-Y或BillrothⅠ式胃肠吻合法,以及是否采用Braun肠肠吻合等[1]。在胰十二指肠切除术后还有胰胃吻合抑或胰空肠吻合[9]以及是否做幽门环肌切开[10]等。很显然,全胃切除患者不会存在DGE问题; 因食管胃交界区恶性肿瘤行近侧胃次全切除后的DGE可以归咎于迷走神经切断; 胰十二指肠切除(Whipple手术)后的DGE可以用十二指肠切除后多种胃肠调节机制丧失以及幽门环肌张力来解释,例如:十二指肠受体功能丧失和局部递质(胺类、肽类等)释放功能丧失。除此之外,大多数远端胃大部分切除术后的DGE都难以用上述因素或机制解释。
4 术后原发性胃排空延迟的负反馈机制 4.1 临床所见多年前我们在临床上观察到[11],在远端胃癌根治性胃大部分切除后,采用管形吻合器做BillrothⅡ式结肠前胃空肠侧侧吻合、Roux-en-Y结肠前胃空肠侧侧吻合和Roux-en-Y结肠前胃空肠侧端吻合这三种吻合方法中,第三种吻合方法术后DGE的发生率高于前两种吻合方法。由于这些DGE患者都不存在前述术后继发性DGE的相关因素,这提示Roux-en-Y胃空肠侧端吻合与DGE存在关联性。认识到这一问题后,我们把消化道重建方式改为Roux-en-Y结肠前胃空肠侧侧吻合加手工法空肠空肠吻合,依据Wente[6]的定义和分级,DGE的发生率有所减少。
4.2 发病机制众所周知,肠襻梗阻或扩张后通常会通过反馈信号使梗阻点近侧肠襻的运动或蠕动增强[12],与此相反,研究发现十二指肠的扩张会导致胃排空延迟,此称“肠-胃抑制反射”[3]。Treacy等[13-15]实验研究都表明随着十二指肠内的球囊膨胀,胃的排空会显著受抑。只要十二指肠处于扩张状态,这种抑制反应就持续存在。然而,迄今尚未见到近段空肠扩张对胃排空是否具有类似的负反馈效应。我们推测,这种肠壁扩张或“胀满”的负反馈效应在近段空肠很可能依旧存在,从而导致DGE。其机制有多个:
4.2.1在管形吻合器直径大于肠腔直径、但能够勉强插入空肠肠腔的情况下,近段空肠黏膜会被吻合器蹭擦损伤,导致肠黏膜炎性反应水肿,甚至血肿形成,结果空肠盲襻处于“胀满”状态,导致DGE。这类患者在做胃镜检查时会观察到空肠黏膜存在水肿或血肿,但是胃镜很容易通过,并没有机械性梗阻。
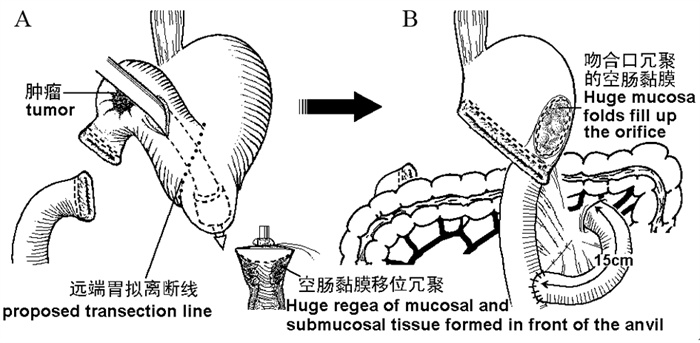
4.2.2在管形吻合器抵钉座直径大于肠腔直径、但能够勉强塞入肠腔的情况下,近段空肠的黏膜和黏膜下组织会被抵钉座向前推挤离开其原来位置,在抵钉座头端冗聚,见图 1A[16]。吻合完毕后,冗聚的黏膜和黏膜下组织会“胀满”在胃空肠吻合口,见图 1B。这类患者在胃镜检查中会观察到花瓣样空肠黏膜“挡”在吻合口,但是胃镜很容易通过,不存在机械性梗阻。
|
| A: mucosa1 and submucosal tissue is pushed forward and glides outof place when the diameter of the circular stapling device is slightlygreater in relation to the luminal diameter of the bowel and huge rugaeof mucosal and submucosal tissue formed in front of the anvil; B: aftercompleting anastomosis, the huge rugae of mucosal and submucosa1tissue wil1 fil1 up the jejuna1 lumen. Postoperative gastroscopyinvestigation will find giant mucosal folds "blocking"the entrance ofthe anastomotic orifice, but endoscope tip can pass through it withoutany difficulty. 图 1 管形吻合器所致空肠“胀满”机制示意图[16] Figure 1 Mechanism of the "fullness" of jejunum created by a circular stapler[16] |
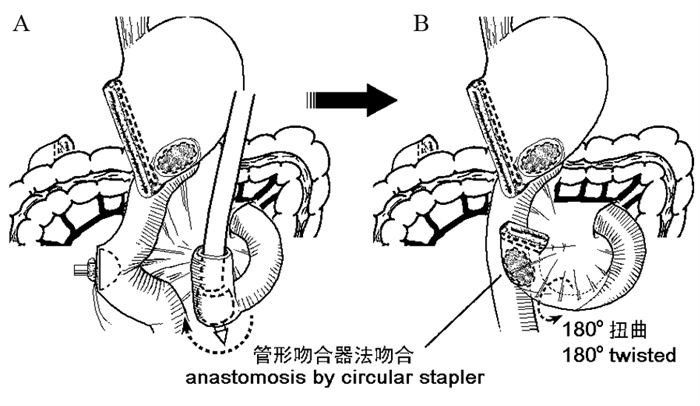
空肠空肠侧侧吻合通常都采用对系膜缘肠壁与对系膜缘肠壁做吻合。在用管形吻合器做空肠空肠侧侧吻合时,需要将输入襻肠段扭转180度,这会影响肠襻的通畅性,见图 2。理论上讲,输入襻越短,肠襻的扭转越严重,肠襻会出现“梗阻”扩张,属于输入襻不全性梗阻。不过,从手术中的实际情况看来,180度的扭转似乎并不至于影响肠内容的通过。Braun肠肠吻合之所以能降低DGE发生率[1],其机制可能就是解除了输入襻扭转造成的通畅性问题。这类患者在做胃镜检查时输出襻没有机械性梗阻表现。
|
| A: when the circular stapling technique is used for side-to-sidejejuno-jejunal anastomosis, both anvil insertion point and central rodperforation point are usually on the antimesenteric wall of the jejunum; B: the afferent loop might be twisted about 180 degrees to completeanastomosis. 图 2 管形吻合器所致空肠扭转机制示意图 Figure 2 Mechanism of twisting of the afferent loop caused by circular stapler |
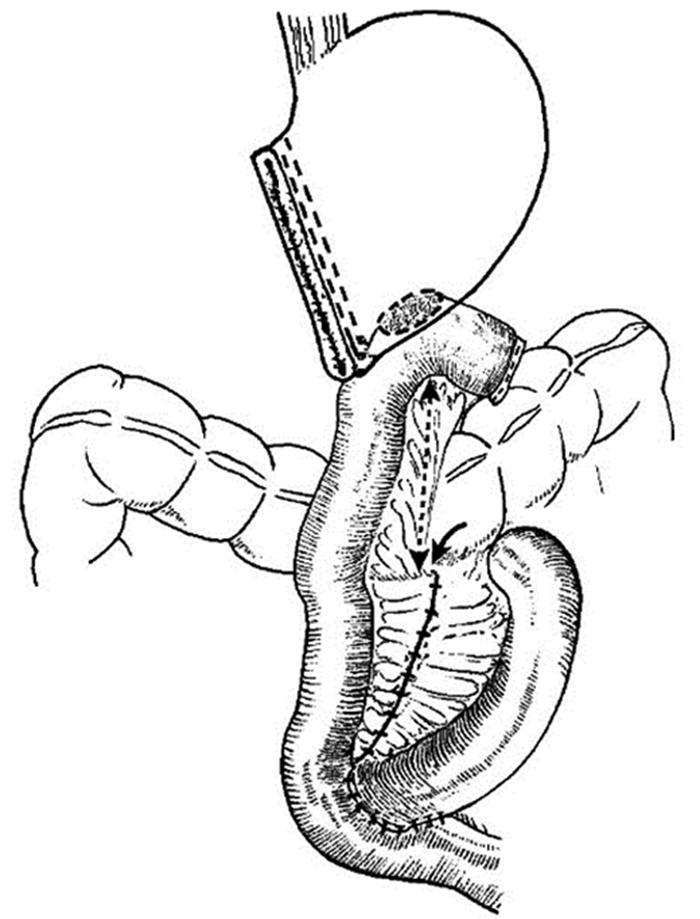
在胃空肠吻合空肠系膜不够长时,尤其在结肠前胃空肠吻合时,横结肠因重力下坠会牵扯吻合口的系膜侧,使空肠襻因牵拉出现“扩张”效应,导致DGE,见图 3。这类患者输入和输出襻都没有机械性梗阻情况。
|
| The solid arrow representsgravity of transverse colon, and the dotted arrow expressestension or stretching effecton the mesenteric side of thegastrojejuostomy. 图 3 胃空肠吻合空肠系膜有张力时对吻合口外牵“扩张”效应示意图 Figure 3 Tension orstretching effect onthe mesenteric side ofgastrojejuostomy |
导致DGE发病的外科因素错综复杂,本文仅就原发性术后DGE的负反馈假说提出个人的观点和4种相关的外科因素,其中前3种都涉及管形吻合器使用问题,最后一种涉及吻合口张力问题。其实,导致原发性术后DGE的、与肠-胃抑制反射相关的外科因素远远不止这4种,例如:Whipple手术后DGE可能的机制之一就是胰肠吻合口内翻过多(尤其在套入式胰肠端端吻合时)造成近段空肠腔出现“胀满”效应。
| [1] |
Macutkiewicz C. Delayed gastric emptying after pancreatic surgery[M]//Søreide K, Stättner S. Textbook of Pancreatic Cancer, Switzerland: Springer Nature. 2021: 1069-1078.
|
| [2] |
Johnson LR. Gastrointestinal Physiology[M]. 9th Edition. Philadelphia: Elsevier, 2019: 31-35.
|
| [3] |
Trowers E, Tischler M. Brain-gut axis and regional gastrointestinal tract motility[M]//Trowers E, Tischler M. Gastrointestinal physiology: a clinical approach. Switzerland: Springer International Publishing, 2014: 41-42.
|
| [4] |
Hasler W. Gastroparesis: Pathogenesis, Diagnosis, and Management[J]. Nat Rev Gastroenterol, 2011, 8(8): 438-453. DOI:10.1038/nrgastro.2011.116 |
| [5] |
Bar-Natan M, Larson GM, Stephens G, et al. Delayed gastric emptying after gastric surgery[J]. Am J Surg, 1996, 172(1): 24-28. DOI:10.1016/S0002-9610(96)00048-7 |
| [6] |
Wente MN, Bassi C, Dervenis C, et al. Delayed gastric emptying (DGE) after pancreatic surgery: a suggested definition by the International Study Group of Pancreatic Surgery (ISGPS)[J]. Surgery, 2007, 142(5): 761-768. DOI:10.1016/j.surg.2007.05.005 |
| [7] |
Kim SH, Keum B, Choi HS, et al. Self-expandable metal stents in patients with postoperative delayed gastric emptying after distal gastrectomy[J]. World J Gastroenterol, 2018, 24(40): 4578-4585. DOI:10.3748/wjg.v24.i40.4578 |
| [8] |
Cakir M, Akinci M, Akturk OM. Delayed gastric emptying as a complication of Whipple's procedure: could it be much less frequent than anticipated? could the definition be revised? Asingle center experience[J]. Medeni Med J, 2020, 35(3): 181-187. |
| [9] |
Hayama S, Senmaru N, Hirano S. Delayed gastric emptying after pancreatoduodenectomy: comparison between invaginated pancreatogastrostomy and pancreatojejunostomy[J]. BMC Surg, 2020, 20(1): 60-65. DOI:10.1186/s12893-020-00707-w |
| [10] |
Schrempf MC, Pinto DRM, Gutschon J, et al. Intraoperative endoluminal pyloromyotomy as a novel approach to reduce delayed gastric emptying after pylorus-preserving pancreaticoduodenectomy-a retrospective study[J]. Langenbecks Arch Surg, 2020, 406(4): 1103-1110. |
| [11] |
Tang WH, Shi X, Fan X, et al. Fullness or distension of proximal jejunum: A risk factor contributing to the delayed gastric emptying[J]. Am Surg, 2018, 84(6): e185-e187. DOI:10.1177/000313481808400604 |
| [12] |
Gan T, Evers BM. Small Intestine[M]//Townsend CM, Beauchamp RD, Evers BM, et al. Sabiston textbook of surgery: the biological basis of modern surgical practice. 21th ed. St. Louis: Elsevier Inc, 2022: 1252-1253.
|
| [13] |
Treacy PJ, Jamieson GG, Dent J. The effect of duodenal distension upon antropyloric motility and liquid gastric emptying in pigs[J]. Aust N Z J Surg, 1996, 66(1): 37-40. DOI:10.1111/j.1445-2197.1996.tb00698.x |
| [14] |
Hirayama N, Gunji Y, Miyazaki S, et al. Inhibitory remnant stomach motility by duodenal distention after B-I gastrectomy[J]. Hepatogastroenterology, 2005, 52(62): 633-638. |
| [15] |
Xu J, Chen JDZ. Intestinal electrical stimulation improves delayed gastric emptying and vomiting induced by duodenal distension in dogs[J]. Neurogastroenterol Motil, 2008, 20(3): 236-342. |
| [16] |
Tang WH, Fan X, Rui ZD, et al. Intestinal obstruction from end-to-side or side-to-side anastomosis made by a circular stapling device[J]. Am Surg, 2011, 77(5): 651-653. DOI:10.1177/000313481107700531 |
 2022, Vol. 49
2022, Vol. 49

