文章信息
- 腹腔热灌注化疗在腹膜癌中的应用现状
- Current Situation of Hyperthermic Intraperitoneal Chemotherapy in Peritoneal Carcinoma
- 肿瘤防治研究, 2021, 48(4): 327-332
- Cancer Research on Prevention and Treatment, 2021, 48(4): 327-332
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2021.20.1280
- 收稿日期: 2020-11-01
- 修回日期: 2021-01-11
腹腔热灌注化疗(hyperthermic intraperitoneal chemotherapy, HIPEC)是一种应用腹腔灌注技术,利用温热效应以及化疗药物治疗腹膜癌(peritoneal carcinoma, PC)的综合疗法[1]。自1980年Spratt等首次报道HIPEC技术以来[2],近40年的临床应用表明HIPEC对PC具有很好的疗效。随着对PC生物学机制研究的不断深入和HIPEC医疗设备的逐步革新,HIPEC在治疗PC中得到了广泛的临床应用[3-9]。2020年初出版的《中国腹腔热灌注化疗技术临床应用专家共识(2019版)》对我国HIPEC在PC治疗中的临床应用、作用机制和疗效评价等问题进行了详细阐述[10]。本文就PC热灌注化疗领域的现状、存在的问题及未来的发展方向进行综述。
1 腹膜癌热灌注化疗领域的现状 1.1 PC的发生机制腹膜是腹腔中由间皮细胞构成、结缔组织支持的膜状结构,包覆大部分腹腔内器官,能够分泌黏液润湿脏器表面,减少摩擦并对冲击起到保护作用。此外,腹膜上含有的血管和淋巴,为腹腔内脏器提供营养支持的同时,也成为肿瘤细胞生长的沃土。胃癌、结直肠癌、卵巢癌、腹膜假黏液瘤、恶性腹膜间皮瘤、胰腺癌、胆管癌和肝癌等腹腔恶性肿瘤是继发性PC的重要来源,肿瘤细胞作为“种子”在腹膜上着生定植,在腹膜的“土壤”上迅速发展,最终导致PC的发生[1, 11]。原发性PC主要发生在女性卵巢外腹膜处,其临床特点与卵巢癌类似,病因有两个主要观点,一是女性腹膜与苗勒氏管上皮有共同的胚胎来源,因此与卵巢有相似的癌变机制; 二是由于胚胎使其性腺迁移途径中遗留下的卵巢组织发生恶变[12]。早期对PC的认识是它被定义为是一种癌细胞广泛转移的表现,常诊断为癌症晚期或终末期,通常的治疗方案以保守治疗为主,外科干预也仅仅采取姑息性的减瘤手术。目前,肿瘤学界认为PC是一种区域性癌转移,经过HIPEC结合其他治疗方法能够进行有效的治疗。
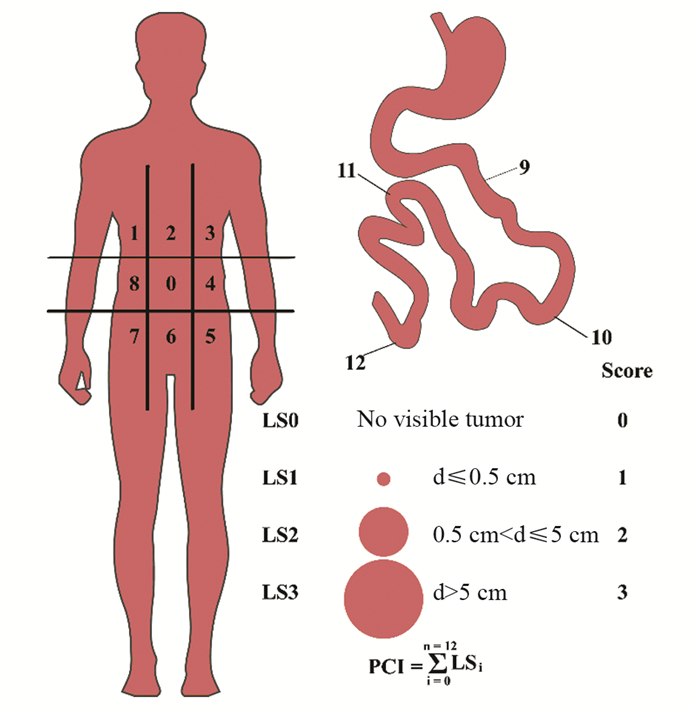
1.2 PC的评价标准目前HIPEC术前需要对PC的严重程度进行评价,其主要的依据是病灶大小和位置,规范是根据Harmon和Sugarbaker提出的腹膜癌指数(peritoneal carcinomatosis index, PCI)而系统量化PC的累计范围[13]。通过PCI的计算方法,将患者腹部划分为13部分,根据每部分内病灶的大小(1esion size, LS)分别打分,以肉眼可见最大结节直径为主要评分对象,最终求和得到PCI,见图 1。
|
| 图 1 腹膜癌指数计算模式图 Figure 1 Calculation model of peritoneal carcinoma index |
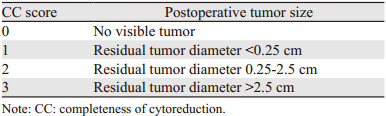
HIPEC术后减瘤的满意程度常用Jacquet和Sugarbaker制定的CC评分标准,见表 1,对术后肿瘤大小进行评估,CC-0和CC-1被认为术后减瘤手术达到满意结果[14]。
PC病灶位于“血液-腹膜屏障”的保护下,常规的亲水性药物难以到达肿瘤组织,而在未达到有效药物浓度情况下,PC的治疗效果往往表现不佳。单纯增加药物剂量的全身治疗会对患者造成严重的健康威胁,因此PC的治疗一直是医学界的重大难题。
HIPEC通过腹腔灌注的方法使得腹膜充分地与化疗药物接触,在肿瘤组织附近的药物浓度超出常规用药血液中的药物浓度20~1000倍[15]。持续的高浓度化疗药物增加了肿瘤细胞与药物接触的机会,最大程度地消灭肿瘤细胞,提高了化疗药物的疗效,减少全身治疗的毒性反应。热疗是杀死肿瘤细胞的另一重要手段[16-17],43℃持续1 h能够有效地抑制肿瘤细胞的生长,造成肿瘤细胞不可逆的损伤,而正常细胞能够耐受47℃持续1 h,HIPEC利用合适的温度和处理时间可以对肿瘤细胞进行消减[18]。在细胞水平和小鼠移植瘤模型中研究发现,热疗主要通过上调细胞黏附因子和凋亡相关基因的表达从而促进肿瘤细胞的死亡[19-20]。此外,较高的温度可以抑制血管形成,提高肿瘤细胞对化疗药物的敏感度,增强药物的渗透深度[21],导致热休克蛋白变性,诱发机体自身的免疫系统产生免疫反应对抗肿瘤细胞[22]。另外,HIPEC灌注液循环对腹膜组织不断冲刷,机械性地剪切力也能够导致肿瘤细胞的直接死亡[23]。
HIPEC除了对治疗PC疗效显著外,对脏器肿瘤的转移复发也具有一定的预防转移作用。在肝、脾、胃、肠等器官的肿瘤进行治疗后,采用HIPEC对腹膜的热化疗处理能有效抑制肿瘤经腹膜转移的发生,我们之前的研究发现HIPEC在治疗胃癌过程中表现出较好的预后[24-26],同时正在开展胃癌D2根治术后的HIPEC疗效的三期临床研究(NCT02356276),现已取得了满意的结果。随着理论和技术的不断进步,HIPEC已经成为预防和治疗PC的最优选择,结合其他多种治疗方法能够有效地控制病情,达到令人满意的疗效。
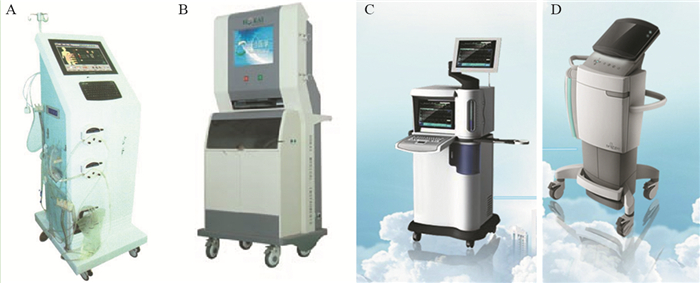
1.4 HIPEC治疗技术的发展自1980年首次使用HIPEC技术至今,HIPEC已经有了近四十年的发展历程,其应用方法经历了4个主要时期[27-28]。(1)温热灌注液直接灌注。早期的HIPEC在开腹或者腹腔穿刺后将混合化疗药物的温热灌注液直接导入患者腹腔中,保留一定时间吸出。虽然该方法简单易行,但是由于体温调节作用,灌注液的热温持续时间很短,疗效一般。(2)内生场温热灌注。热疗机的使用可以对患者腹腔内的灌注液进行加温,从而将灌注液维持在一定的温度,解决了直接灌注造成的温热持续时间短的问题。但是由于不能精准控温,腹腔内热量分布不均以及电极加热部位温度过高等问题阻碍了临床上的推广使用。(3)恒温水浴箱、微波加热灌注。通过恒温水浴箱或者微波持续加温灌注液,将恒定有效温度的灌注液通过动力泵注入患者腹腔内,可以借助引流管形成循环灌注,是一种较为成熟稳定的HIPEC技术,但是其温度控制的精确度不高。(4)高精度持续虚化热灌注。此类方法利用HIPEC方法专门制作的高精度温控循环医疗设备实现,是对恒温水浴箱、微波加热法的升级改进,一般具有内外双循环系统,内循环管路为含有化疗药物的灌注液,在腹腔和灌注袋之间循环,外循环则为密闭的热传导系统。内外循环通过热交换器进行热量传递,通过计算机进行精准控制,从而保证腹腔内温度维持在较为恒定的温度[29-30]。目前临床常用的腹腔热灌注化疗设备有RHL-2000A型腹腔热灌注机,HGGZ-102体腔热灌注治疗系统,体腔热灌注治疗系统BR-TRG-Ⅰ型和Ⅱ型,见图 2。
|
| A: RHL-2000A intraperitoneal hyperthermic perfusion machine; B: HGGZ-102 body cavity hyperthermic perfusion therapy system; C: BR-TRG-Ⅰ body cavity hyperthermic perfusion therapy system; D: BR-TRG-Ⅱ body cavity hyperthermic perfusion therapy system. 图 2 常用腹腔热灌注化疗设备 Figure 2 Common hyperthermic intraperitoneal chemotherapy (HIPEC) equipment |
虽然HIPEC的技术不断进步,但是一直缺乏统一的治疗标准。目前欧美国家所使用的HIPEC技术存在着很大的差别,用药类型和剂量、循环方式、有效治疗温度都不尽相同,因此不能科学准确地评价HIPEC的临床疗效。我国于2016年由临床专家共同发表的《腹腔热灌注化疗技术临床应用专家共识(2016版)》对HIPEC技术进行了规范化描述,制定了中国HIPEC标准[31],特别是对于灌注温度(43±0.1)℃、灌注时间(60~90 min)、灌注间隔(24 h)、灌注容量(4~6 L)和灌注速率(400~600 ml/min)有了明确的规定,建立了高精度、大容量、持续循环、恒温灌注的HIPEC技术方法,从而更好地评价和推广HIPEC,推动技术方法的不断进步和革新。
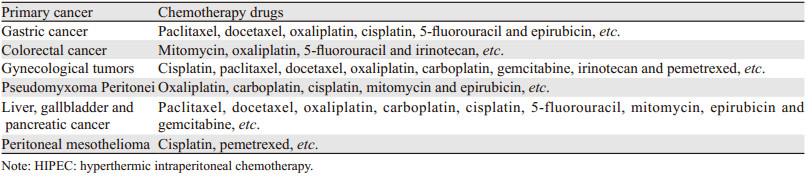
1.5 HIPEC的常用化疗药物化疗药物的选择对于HIPEC的疗效起到了至关重要的作用,选择腹腔穿透力强、腹膜吸收率高、热疗提高敏感度的药物能取得较为理想的预后[32],常见的HIPEC化疗药物,见表 2[10]。此外,对于继发性PC患者,除了考虑原发癌种类型外,还要结合以往的化疗治疗史,避免敏感度药物的使用。化疗药物剂量的选择上主要遵循系统化疗的用量标准,但在临床应用上还需要考虑患者的个体差异,如年龄、身体状况、药物耐受性等,进行适当调整。HIPEC的灌注液主要以0.9%氯化钠溶液为主,但是对于奥沙利铂和卡铂等药物,由于其在0.9%氯化钠溶液中的药效不稳定,常采用5%葡萄糖液作为灌注液。
HIPEC作为治疗PC的主要技术方法,常与其他治疗方法相结合,以提高PC患者的生存期和生活质量。目前比较常见的联合治疗方案主要有三种:肿瘤根治术(cancer radical resection, CRR)联合HIPEC(CRR+HIPEC)、肿瘤细胞减灭术(cytoreductive surgery, CRS)联合HIPEC(CRS +HIPEC)和CRR+CRS+HIPEC。
目前,CRS+HIPEC是临床上治疗腹膜癌最常用的方法,CRS手术通过清除腹腔内肉眼可见的病灶,将残余的肿瘤直径控制在0.25 cm以下,从而大幅降低肿瘤负荷,增强HIPEC的治疗效果,提高PC患者的预后[33]。但值得注意的是,CRS+HIPEC治疗后伴随的不良事件发生率较高,常见的不良事件有腹腔脓肿、吻合口瘘、胆瘘、肠瘘、肠梗阻、切口裂开、肺部感染等,其发生率主要与PCI评分、手术的时间、吻合口数量等有关[10]。
1.7 HIPEC治疗的注意事项在HIPEC治疗过程中,PC患者常伴有发热发汗、心率增加以及消化道反应等症状,这些临床表现可以提示术中患者的身体状态。血容量不足会引起患者发汗,心率过快,当心率超过120次/分钟时,应该考虑加强补液。当麻醉药物和灌注液体用量过高时,患者会出现呼吸抑制和血氧饱和度降低等症状,应降低药物浓度、减少灌注液体,严重时应立即停止治疗。HIPEC术中患者体温会略有升高,在38.5℃以下都属于正常范围; 体温如果超出范围应考虑是否存在合并感染,及时进行有效处理。胃肠道反应需要给予抑酸剂、止吐药和解痉挛处理。此外,HIPEC手术后部分患者会伴有一些并发症,应当进行预防性检查,提供有效治疗方案。如通过对外周血白细胞的变化判断患者是否出现骨髓抑制,通过对胃肠功能的检查判断患者是否出现胃排空障碍和肠麻痹等症状,检查是否有吻合口漏的发生等[10]。因此,在HIPEC治疗过程中,需要术前提前做好准备工作,对于术中和术后可能出现的问题做到及时应对,从而降低患者的手术风险,改善患者的预后。
2 HIPEC存在的问题尽管HIPEC技术已经有近四十年的临床发展历史,但是在治疗PC过程中目前仍然存在一些需要说明和解决的问题。现在认为热疗、化疗和机械性冲刷是HIPEC能够有效清除PC肿瘤细胞的三个主要机制,但是三者间如何协同合作以及其背后的分子调控机制还需要进一步研究。目前,先进的HIPEC设备能够达到精准温控,拥有完善的腹腔灌注系统,技术层面上已经达到理论要求,进一步提升的空间不大。只有阐明HIPEC治疗PC的分子机制,才能从根本上改善HIPEC的方法,提高治疗PC的疗效,为HIPEC的进一步发展提供理论基础。HIPEC技术在预防和治疗PC方面虽然已经得到广泛认可和临床应用,但是不同医疗机构采用的HIPEC治疗方案不同,很难进行多中心大样本的HIPEC的临床研究,并且由于缺乏规范标准,前瞻性的临床研究报道也很少,导致目前对HIPEC治疗PC的总体疗效不能进行准确评估。针对PC患者原发癌种和身体状况的不同,如何制定个性化的HIPEC治疗方案,选择合适的温度、灌注液和化疗药物,仍需要进一步开展临床研究对治疗方案进行优化。此外,对于HIPEC和术后并发症的关系研究还不清楚,虽然目前整体疗效令人满意,但是术后并发症严重地影响了PC患者的预后和生活质量。
3 HIPEC临床应用的未来展望为规范HIPEC操作标准,提高HIPEC在临床上的疗效,2016年和2020年我国腹腔热灌注化疗技术临床应用专家协作组和中国抗癌协会腹膜肿瘤专业委员会先后制定了《腹腔热灌注化疗技术临床应用专家共识(2016版)》和《中国腹腔热灌注化疗技术临床应用专家共识(2019版)》,提出了较为详细的国内HIPEC规范标准。在此规范标准基础上,进行前瞻性、多中心、大样本的临床研究成为可能。利用生物信息学和大数据挖掘技术,解析HIPEC治疗PC的作用机制,挖掘HIPEC疗效相关的关键因素,包括基因突变、临床指标以及身体状况等,对HIPEC术前进行全面评估,从而制定合理治疗方案,对于提高PC患者的预后具有重要的临床意义。同时,对HIPEC并发症发生的相关因素进行全面分析,规范手术治疗操作,减少PC手术的副作用也将成为未来重点研究方向。此外,探讨HIPEC与其他药物结合的治疗方案,发挥HIPEC灌注与肿瘤直接接触的优势,提高微环境药物浓度,能够为增强药物疗效提供新的思路。相信随着临床医学以及交叉学科的不断发展,未来HIPEC技术将得到不断完善和升级,将会显著提高PC的治疗水平,改善患者的生存情况。
作者贡献:
詹宏杰: 资料的收集、整理及论文撰写
梁寒: 技术指导,论文撰写及审核
| [1] |
梁寒. 腹腔热灌注化疗技术临床应用专家共识(2016版)解读——胃癌腹膜转移的防治[J]. 临床外科杂志, 2017, 25(1): 20-23. [Liang H. Clinical application of intraperitoneal hyperthermic perfusion chemotherapy: An expert consensus (2016 edition): Interpretation of prevention and treatment of peritoneal metastasis of gastric cancer[J]. Lin Chuang Wai Ke Za Zhi, 2017, 25(1): 20-23. DOI:10.3969/j.issn.1005-6483.2017.01.004] |
| [2] |
Spratt JS, Adcock RA, Muskovin M, et al. Clinical delivery system for intraperitoneal hyperthermic chemotherapy[J]. Cancer Res, 1980, 40(2): 256-260. |
| [3] |
中国抗癌协会妇科肿瘤专业委员会, 中国妇科腹腔热灌注化疗技术临床应用专家协作组. 妇科恶性肿瘤腹腔热灌注化疗临床应用专家共识(2019)[J]. 中国实用妇科与产科杂志, 2019, 35(2): 194-201. [Committee of Gynecological Oncology, China Anti-cancer Association, Expert Cooperative Group on clinical application of intraperitoneal hyperthermic perfusion chemotherapy in gynecology in China. Expert Consensus on clinical application of intraperitoneal hyperthermic perfusion chemotherapy for gynecological malignant tumors (2019)[J]. Zhongguo Shi Yong Fu Ke Yu Chan Ke Za Zhi, 2019, 35(2): 194-201.] |
| [4] |
李雁, 周云峰, 梁寒, 等. 细胞减灭术加腹腔热灌注化疗治疗腹膜表面肿瘤的专家共识[J]. 中国肿瘤临床, 2015, 42(4): 198-206. [Li Y, Zhou YF, Liang H, et al. Expert Consensus on Cytoreductive Surgery Plus intraperitoneal hyperthermic perfusion chemotherapy in the treatment of superficial peritoneal tumors[J]. zhongguo zhong liu lin chuang, 2015, 42(4): 198-206. DOI:10.3969/j.issn.1000-8179.20150013] |
| [5] |
肖绍文. 中国肿瘤热疗临床应用指南(2017.V1.1)[J]. 中华放射肿瘤学杂志, 2017, 26(4): 369-375. [Xiao SW. Chinese application guide of clinical application of tumor hyperthermia(2017.V1.1)[J]. Zhonghua Fang She Zhong Liu Xue Za Zhi, 2017, 26(4): 369-375. DOI:10.3760/cma.j.issn.1004-4221.2017.04.001] |
| [6] |
李雁, 许洪斌, 彭正, 等. 肿瘤细胞减灭术加腹腔热灌注化疗治疗腹膜假黏液瘤专家共识[J]. 中华医学杂志, 2019, 99(20): 1527-1535. [Li Y, Xu HB, Peng Z, et al. Expert Consensus on the treatment of Pseudomyxoma Peritonei by cytoreductive surgery and intraperitoneal hyperthermic perfusion chemotherapy[J]. Zhonghua Yi Xue Za Zhi, 2019, 99(20): 1527-1535. DOI:10.3760/cma.j.issn.0376-2491.2019.20.003] |
| [7] |
李鑫宝, 姬忠贺, 于洋, 等. 肿瘤细胞减灭术加腹腔热灌注化疗治疗阑尾腺癌腹膜癌的临床研究[J]. 实用肿瘤杂志, 2019, 34(1): 66-71. [Li XB, Ji ZH, Yu Y, et al. Clinical study on cytoreductive surgery plus hyperthermic intraperitoneal chemotherapy on patients with peritoneal carcinomatosis from appendiceal adenocarcinoma[J]. shi yong zhong liu za zhi, 2019, 34(1): 66-71.] |
| [8] |
崔书中, 王佳泓, 张相良. 肿瘤细胞减灭术联合腹腔热灌注化疗治疗结直肠癌腹膜转移癌[J]. 中国肿瘤临床, 2012, 39(22): 1691-1695. [Cui SZ, Wang JH, Zhang XL. Cytoreductive surgery combined with intraperitoneal hyperthermic perfusion chemotherapy for peritoneal metastasis of colorectal cancer[J]. Zhongguo Zhong Liu Lin Chuang, 2012, 39(22): 1691-1695. DOI:10.3969/j.issn.1000-8179.2012.22.003] |
| [9] |
中国医师协会结直肠肿瘤专委会腹膜肿瘤专业委员会. 结直肠癌腹膜转移诊治中国专家意见(2017)[J]. 中华结直肠疾病电子杂志, 2017, 6(5): 360-366. [Professional Committee of Peritoneal Metastasis, Colorectal Cancer Committee of Chinese Medical Doctor Association. Chinese expert opinion for diagnosis and treatment of colorectal cancer peritoneal metastasis. (2017 edition)[J]. Zhonghua Jie Zhi Chang Ji Bing Dian Zi Za Zhi, 2017, 6(5): 360-366. DOI:10.3877/cma.j.issn.2095-3224.2017.05.002] |
| [10] |
中国抗癌协会腹膜肿瘤专业委员会, 广东省抗癌协会肿瘤热疗专业委员会. 中国腹腔热灌注化疗技术临床应用专家共识(2019版)[J]. 中华医学杂志, 2020, 100(2): 89-96. [Peritoneal Tumor Committee of China Anti-cancer Association, Cancer Thermotherapy Committee of Guangdong Anti-cancer Association. Chinese expert consensus on clinical application of intraperitoneal hyperthermic perfusion chemotherapy (2019 edition)[J]. Zhonghua Yi Xue Za Zhi, 2020, 100(2): 89-96. DOI:10.3760/cma.j.issn.0376-2491.2020.02.003] |
| [11] |
Fidler IJ. The pathogenesis of cancer metastasis: the 'seed and soil' hypothesis revisited[J]. Nat Rev Cancer, 2003, 3(6): 453-458. DOI:10.1038/nrc1098 |
| [12] |
法洪文, 孙倩. 原发性腹膜癌的研究进展[J]. 长治医学院学报, 2015, 29(4): 311-314. [Fa HW, Sun Q. Research progress of primary peritoneal carcinoma[J]. Changzhi Yi Xue Yuan Xue Bao, 2015, 29(4): 311-314. DOI:10.3969/j.issn.1006-0588.2015.04.028] |
| [13] |
Harmon RL, Sugarbaker PH. Prognostic indicators in peritoneal carcinomatosis from gastrointestinal cancer[J]. Int Semin Surg Oncol, 2005, 2(1): 3. DOI:10.1186/1477-7800-2-3 |
| [14] |
Jacquet P, Sugarbaker PH. Clinical research methodologies in diagnosis and staging of patients with peritoneal carcinomatosis[J]. Cancer Treat Res, 1996, 82: 359-374. |
| [15] |
Lu Z, Wang J, Wientjes MG, et al. Intraperitoneal therapy for peritoneal cancer[J]. Future Oncol, 2010, 6(10): 1625-1641. DOI:10.2217/fon.10.100 |
| [16] |
詹宏杰, 梁寒. 肿瘤热疗的研究[J]. 国外医学肿瘤学分册, 2005, 32(1): 35-38. [Zhan HJ, Liang H. Study on Tumor Hyperthermia[J]. Guo Wai Yi Xue Zhong Liu Xue Fen Ce, 2005, 32(1): 35-38.] |
| [17] |
梁寒, 郝希山. 热疗的生物学机制[J]. 国外医学肿瘤学分册, 2001, 28(6): 438-441. [Liang H, Hao XS. Biological Mechanism of Hyperthermia[J]. Guo Wai Yi Xue Zhong Liu Xue Fen Ce, 2001, 28(6): 438-441.] |
| [18] |
Garofalo A, Valle M, Garcia J, et al. Laparoscopic intraperitoneal hyperthermic chemotherapy for palliation of debilitating malignant ascites[J]. Eur J Surg Oncol, 2006, 32(6): 682-685. DOI:10.1016/j.ejso.2006.03.014 |
| [19] |
梁寒, 李景武, 史玉荣, 等. 热疗对人类结肠癌细胞株细胞黏附因子表达的影响[J]. 中华医学杂志, 2004, 84(15): 1299-1303. [Liang H, Li JW, Shi YR, et al. Change in E-cadhrin, α-, β- and γ-catenin expression after hyperthermia of a human colon carcinoma cell line in vitro[J]. Zhonghua Yi Xue Za Zhi, 2004, 84(15): 1299-1303. DOI:10.3760/j:issn:0376-2491.2004.15.017] |
| [20] |
梁寒, 詹宏杰, 王宝贵, 等. 人结肠癌裸鼠移植瘤热疗和化疗及放疗后凋亡相关基因的变化[J]. 中华胃肠外科杂志, 2008, 11(3): 270-275. [Liang H, Zhan HJ, Wang BG, et al. Expression change of apoptosis-associated genes after hyperthermia, chemotherapy and radiotherapy in human colon cancer-transplanted nude mice[J]. Zhonghua Wei Chang Wai Ke Za Zhi, 2008, 11(3): 270-275. DOI:10.3760/cma.j.issn.1671-0274.2008.03.018] |
| [21] |
Chiva LM, Gonzalez-Martin A. A critical appraisal of hyperthermic intraperitoneal chemotherapy (HIPEC) in the treatment of advanced and recurrent ovarian cancer[J]. Gynecol Oncol, 2015, 136(1): 130-135. DOI:10.1016/j.ygyno.2014.11.072 |
| [22] |
Zunino B, Rubio-Patiño C, Villa E, et al. Hyperthermic intraperitoneal chemotherapy leads to an anticancer immune response via exposure of cell surface heat shock protein 90[J]. Oncogene, 2016, 35(2): 261-268. DOI:10.1038/onc.2015.82 |
| [23] |
Sugarbaker PH, Stuart OA, Yoo D. Strategies for management of the peritoneal surface component of cancer: cytoreductive surgery plus perioperative intraperitoneal chemotherapy[J]. J Oncol Pharm Pract, 2005, 11(3): 111-119. DOI:10.1191/1078155205jp157oa |
| [24] |
詹宏杰, 梁寒, 王宝贵, 等. 60例进展期胃癌术中腹腔热灌注化疗的临床观察[J]. 中国肿瘤临床, 2010, 37(4): 229-231. [Zhan HJ, Liang H, Wang BG, et al. Efficacy of intraoperative hyperthermic peritoneal perfusion on 60 patients with advanced gastric carcinoma[J]. Zhongguo Zhong Liu Lin Chuang, 2010, 37(4): 229-231. DOI:10.3969/j.issn.1000-8179.2010.04.015] |
| [25] |
詹宏杰, 梁寒, 王宝贵, 等. 进展期胃癌术中腹腔热灌注化疗的预后分析[J]. 中国肿瘤临床, 2012, 39(22): 1730-1733. [Zhan HJ, Liang H, Wang BG, et al. Prognostic anaiysis of patients with advanced gastric cancer undergoing intraoperative chemohyperthermic peritoneal perfusion[J]. Zhongguo Zhong Liu Lin Chuang, 2012, 39(22): 1730-1733. DOI:10.3969/j.issn.1000-8179.2012.22.011] |
| [26] |
詹宏杰, 梁寒, 刘洪敏, 等. 腹腔热灌注化疗对不同病理类型和Borrmann分型进展期胃癌患者的预后分析[J]. 中国肿瘤临床, 2020, 47(3): 135-139. [Zhan HJ, Liang H, Liu HM, et al. Prognostic analysis of intraoperative chemohyperthermic peritoneal perfusion in patients with advanced gastric cancer of different pathological types and Borrmann's classifications[J]. Zhongguo Zhong Liu Lin Chuang, 2020, 47(3): 135-139. DOI:10.3969/j.issn.1000-8179.2020.2020.03.631] |
| [27] |
潘子豪, 陈双. 腹腔热灌注化疗的研究进展[J]. 岭南现代临床外科, 2015, 15(1): 107-110. [Pan ZH, Chen S. Research progress of intraperitoneal hyperthermia perfusion chemotherapy[J]. Lingnan Xian Dai Lin Chuang Wai Ke, 2015, 15(1): 107-110. DOI:10.3969/j.issn.1009-976X.2015.01.029] |
| [28] |
崔书中, 巴明臣, 唐鸿生. 腹腔热灌注化疗技术方法变迁及展望[J]. 中华临床医师杂志, 2011, 5(7): 2039-2042. [Cui SZ, Ba MC, Tang HS. Changes and prospects of intraperitoneal hyperthermic perfusion chemotherapy[J]. Zhonghua Lin Chuang Yi Shi Za Zhi, 2011, 5(7): 2039-2042. DOI:10.3877/cma.j.issn.1674-0785.2011.07.034] |
| [29] |
崔书中, 巴明臣, 黄迪文, 等. BR-TRG-I型体腔热灌注治疗系统的研制与开发[J]. 中国医疗设备, 2009, 24(9): 7-9. [Cui SZ, Ba MC, Huang DW, et al. study and development of BR-TRG-I hyperthermic perfusion intraperitoneal treatment system[J]. Zhongguo Yi Liao She Bei, 2009, 24(9): 7-9. DOI:10.3969/j.issn.1674-1633.2009.09.003] |
| [30] |
崔书中, 黄狄文, 巴明臣. 高精度腹腔热灌注治疗系统设备的开发研究[J]. 中华生物医学工程杂志, 2009, 15(6): 471-474. [Cui SZ, Huang DW, Ba MC. Development of a high precision hyperthermic perfusion intraperitoneal treatment system[J]. Zhonghua Sheng Wu Yi Xue Gong Cheng Za Zhi, 2009, 15(6): 471-474. DOI:10.3760/cma.j.issn.1674-1927.2009.06.014] |
| [31] |
腹腔热灌注化疗技术临床应用专家协作组. 腹腔热灌注化疗技术临床应用专家共识(2016版)[J]. 中华胃肠外科杂志, 2016, 19(2): 121-125. [Cooperative Group of experts on clinical application of intraperitoneal hyperthermic perfusion chemotherapy. Expert Consensus on clinical application of intraperitoneal hyperthermic perfusion chemotherapy (2016 edition)[J]. Zhonghua Wei Chang Wai Ke Za Zhi, 2016, 19(2): 121-125. DOI:10.3760/cma.j.issn.1671-0274.2016.02.001] |
| [32] |
Yan TD, Cao CQ, Munkholm-Larsen S. A pharmacological review on intraperitoneal chemotherapy for peritoneal malignancy[J]. World J Gastrointest Oncol, 2010, 2(2): 109-116. DOI:10.4251/wjgo.v2.i2.109 |
| [33] |
Sugarbaker PH. Cytoreductive surgery and perioperative intraperitoneal chemotherapy as a curative approach to pseudomyxoma peritonei syndrome[J]. Tumori, 2001, 87(4): S3-5. DOI:10.1177/030089160108700415 |
 2021, Vol. 48
2021, Vol. 48