文章信息
- 伊马替尼致慢性粒细胞白血病患者玻璃体及眼底出血1例分析
- Chronic Myeloid Leukemia with Vitreous Body and Fundus Hemorrhage Caused by Imatinib: A Case Report
- 肿瘤防治研究, 2021, 48(4): 436-438
- Cancer Research on Prevention and Treatment, 2021, 48(4): 436-438
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2021.20.1096
- 收稿日期: 2020-09-15
- 修回日期: 2020-12-23
2. 067000 承德,承德医学院研究生院;
3. 071000 保定,保定市第一医院 血液内科
2. Graduate School of Chengde Medical University, Chengde 067000, China;
3. Department of Hematology, The No.1 Hospital of Baoding, Baoding 071000, China
慢性粒细胞白血病(chronic myelogenous leukemia, CML)为造血干细胞恶性克隆性疾病,其发病及进展缓慢,据病程分为三期:慢性期、加速期和急变期。CML的特征改变是染色体形成9,22号染色体易位,形成BCR-ABL融合基因,其蛋白产物具有酪氨酸激酶活性,从而导致CML的发生[1]。伊马替尼(imatinib)为酪氨酸激酶抑制剂,能够特异性的抑制BCR-ABL蛋白活性,为治疗CML的首选靶向药物[2]。伊马替尼的应用极大改善了CML患者的生存及预后。
伊马替尼对其常见不良反应有恶心、呕吐、肌痛及肌肉痉挛、水肿、骨髓抑制,心脏毒性,肝脏毒性等。尤其是水肿最为常见,严重水肿时可导致胸水、腹水及肺水肿[3],但绝大多数不良反应为轻至中度,经过对症支持治疗后可耐受或减轻不良反应,并不影响患者继续应用伊马替尼。部分患者可能因严重药物相关性不良事件导致治疗中断或更换其他药物。定州市人民医院收治一例CML患者口服伊马替尼后先后出现眼底出血及玻璃体出血等严重不良反应病例,而国内未见相关报道,现报道如下。
1 病例资料患者男,52岁,农民,主因确诊为慢性粒细胞性白血病8月,视物不清进行性加重4月于2020年6月5日入院。既往8年前出现血压升高,最高160/100 mmHg,未口服降压药物,后血压持续恢复正常。2型糖尿病病史8年,未口服降糖药物,空腹血糖在7~8 mmol/L之间,餐后血糖在10 mmol/L以内。患者8个月前因左上腹饱胀不适伴有腹痛就诊于当地医院,查血常规WBC 86×109/L,Hb 86g/L,PLT 156×109/L;腹部彩超示:脾大,肋下5 cm;骨髓象示:骨髓增生极度活跃,以粒系细胞为主,粒细胞与红系细胞比例明显增高,其中中性中幼粒、晚幼粒和杆状核粒细胞明显增多,原始粒细胞7%,嗜酸性和嗜碱性粒细胞增多,红系细胞减少,巨核细胞不少,考虑慢性粒细胞白血病-慢性期。染色体核型分析:46, XY, t(9; 22)(q34; q11.2)[6]/46, XY[11],BCR-ABL1融合基因P210:125.0857%,P190及P230阴性,流式细胞:髓系原始细胞比例不高,占1.16%,部分细胞CD117表达减弱或缺失,部分表达CD7表型异常;余表达未见异常,请结合BCR-ABL1融合基因查除外CML等骨髓增殖性肿瘤。给予口服甲磺酸伊马替尼片每日0.4 g,后患者复查血常规WBC 3.2×109/L,Hb 89 g/L,PLT 96×109/L,患者曾自行短期停药1周左右,后改为每日0.3 g,半月后患者外周血逐渐恢复基本正常,再次恢复伊马替尼用量为每日0.4 g,4月前出现双眼视物模糊,曾于我院眼科就诊。眼科检查:视力:OD: 0.15 OS: 眼前手动双眼球结膜水肿(+),余外眼(-),晶状体轻度混浊,玻璃体内可见较多血性物漂浮,左眼底无法看清,右眼底朦胧:视乳头界清,呈桔红色,网膜可见散在片状黄白色渗出及较多片状出血,A: V=1:2,黄斑区中心光反射未见,见图 1。3月前复查BCR-ABL1融合基因3.1861%,期间多次复查血常规WBC 2.5~4.2×109/L,Hb 90~110 g/L,PLT 80~130×109/L,20天前患者双眼视物不清加重,就诊眼科考虑眼底出血加重,建议手术治疗,但考虑到复发率极高,未手术。后患者视物不清进行性加重,仅余光感,同时伴有轻度头晕、胸闷、恶心、乏力及双下肢麻木,再次就诊我院,门诊以慢性粒细胞性白血病、眼底出血入院。T:36.4℃、BP:144/90 mmHg,神清,轻度贫血貌。全身皮肤黏膜无黄染及出血点,周身浅表淋巴结未触及肿大。眼睑轻度水肿,双眼视物模糊,仅有光感,双肺呼吸音粗,未闻及干湿性啰音,心率92次/分,律齐,无病理性杂音。腹软,无压痛、反跳痛,肝脾肋下未触及。双下肢无浮肿。神经系统查体未见异常。查胸部CT:(1)双肺钙化结节;(2)心包少量积液;(3)符合贫血改变;(4)主动脉及冠状动脉硬化。血常规(我院2020-06-05):WBC:2.77×109/L;Hg:109 g/L;PLT:110×109/L;免疫球蛋白A:3.88 g/L,免疫球蛋白G:12.59 g/L;免疫球蛋白M:1.03 g/L,肝功能:ALT:154 U/L;AST:113 U/L;TP:61.2 g/L;ALB:39.2 g/L;TBIL:19.6 μmol/L,DBIL:10 μmol/L,GLU:7.7 mmol/L,糖化血红蛋白5.8 mmol/L,餐后2 h血糖7.5 mmol/L,肾功能正常,心肌酶及LDH正常。甲状腺功能正常,凝血功能:纤维蛋白原1.64 g/L,凝血酶原时间、部分凝血酶原时间、D-二聚体及纤维蛋白降解产物均正常。肿瘤标志物未见异常,抗核抗体谱未见异常,叶酸及维生素B12正常。尿常规:红细胞(+),尿蛋白(2+),24 h尿蛋白定量0.96 g。头颅MRI:考虑左侧额叶、右侧放射冠、左侧基底节缺血灶。颅脑MRA:轻度动脉硬化表现。心脏彩超:二、三尖瓣少量返流,左室舒张功能减低,EF 72%。腹部彩超:脾厚4.6 cm,脾大,双肾大。再次骨髓象检测考虑CML慢性期。骨髓流式:可见髓系原始细胞约占有核细胞0.35%,表型未见明显异常。BCR-ABL1融合基因定量:0.0203%。ABL激酶区突变阴性、染色体核型46,XY[20]。脑脊液压力正常,脑脊液常规:无色、透明、无凝块、潘氏试验阴性,白细胞计数:4×106/L,脑脊液生化:葡萄糖:3.30 mmol/L,脑脊液,氯化物:126 mmol/L,脑脊液蛋白:0.7 g/L脑脊液,细胞分类:未找见幼稚细胞,脑脊液流式未发现异常原始细胞。眼科会诊并双眼B型超声检查提示玻璃体的液性暗区内可见团状和条索状强回声,球后壁欠光滑,考虑玻璃体出血,见图 2,未能看到眼底,考虑:(1)双眼虹膜新生血管;(2)双眼玻璃体积血。建议若全身情况允许,应尽快行双眼玻璃体切除术,但考虑到患者患有慢性粒细胞白血病,术后再次出血的可能性很大。综上诊断:(1)慢性粒细胞性白血病慢性期;(2)药物性肝损害;(3)周围神经病;(4)玻璃体积血;(5)虹膜新生血管;(6)高血压2级;(7)2型糖尿病。给予还原型谷胱甘肽保肝,利可君片提升白细胞、血小板。考虑患者眼底出血及玻璃体出血为伊马替尼不良反应,给予更换氟马替尼每日600 mg治疗,同时应用维生素B1及B12治疗后,患者自觉双眼光感增强,能看到模糊影子,治疗半月后复查血常规WBC 3.57×109/L、Hg98 g/L,血小板110×109/L。肝功能:ALT: 87U/L; AST: 44U/L; TP: 50.7 g/L; ALB: 33.1 g/L, TBIL: 14.3 μmol/L, DBIL: 3.3 μmol/L, GLU: 6.1 mmol/L,病情平稳出院。
|
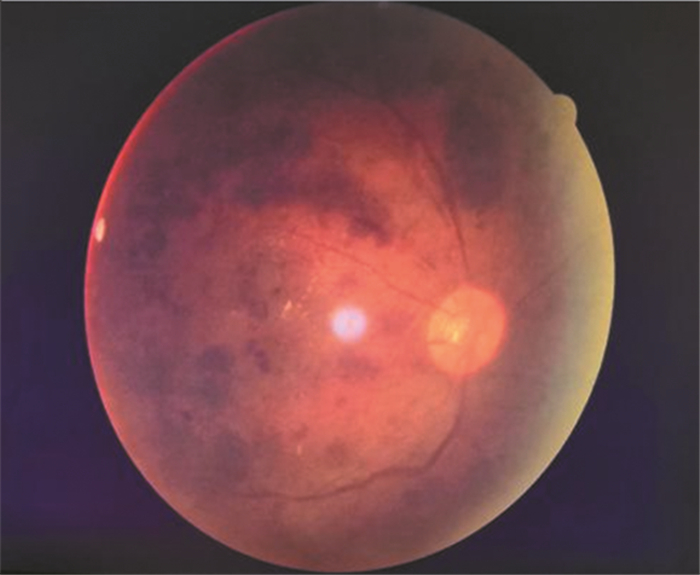
| 图 1 患者眼底视网膜出血图像 Figure 1 Image of retinal hemorrhage in fundus |

|
| 图 2 患者双眼B型超声玻璃体出血图像 Figure 2 B-ultrasound images of vitreous hemorrhage in both eyes |
慢性骨髓增殖性肿瘤包括BCR-ABL1阴性骨髓增殖性肿瘤,JAK2抑制剂芦可替尼为特异性靶向药物[4],而BCR-ABL1阳性慢性粒细胞白血病患者首选靶向药物为伊马替尼。
大多数患者在应用伊马替尼后会出现一些不良反应,各个系统均可出现,如消化系统:恶心、呕吐、腹泻及肝脏毒性;血液系统:可见一系或多系血细胞减少;皮肤:常见全身浮肿、各类皮炎及皮疹;肌肉骨骼系统:可有肌肉痉挛、关节肿胀及疼痛等。绝大多数不良反应较轻,经过对症支持治疗后可耐受或减轻,并可继续应用[5]。少部分患者需要减量或停用。其对眼部常见不良反应包括结膜炎、流泪增多、视力模糊。不常见不良反应包括眼刺激症状、结膜下出血、眼干、眶周浮肿。其中罕见不良反应包括黄斑水肿、视神经乳头水肿、视网膜出血、玻璃体出血、青光眼[6]。本例患者应用伊马替尼治疗后出现多种不良反应,包括水肿、恶心、心包积液、全血细胞减少,同时在应用伊马替尼4月时出现玻璃体及眼底视网膜出血,8月时再次加重,但患者同时存在高血压及糖尿病,而高血压眼底出血,一般伴有眼底小动脉硬化,出血顺小动脉呈火焰状。糖尿病眼底出血一般血管闭塞后出血,以点片状为主,同时易反复发作,常引起增殖性视网膜病变、新生血管性青光眼等[7]。该患者平素血糖及血压控制平稳,同时眼底不符合高血压、糖尿病眼底出血表现。患者头颅MRI及脑脊液检查,排除了患者白血病髓外浸润导致中枢神经系统白血病。该患者应用伊马替尼4月时双眼底可见的片状出血以周边为重,而血管迂曲硬化不明显。结合患者存在其他多种伊马替尼不良反应,眼底出血及玻璃体出血出现在应用伊马替尼过程中,在停用伊马替尼同时给予对症支持治疗后有所改善,后换用氟马替尼后患者视力出现不同程度恢复,均支持伊马替尼不良反应导致,而伊马替尼导致眼底出血机制可能包括:(1)血细胞减少,尤其是血小板减少;(2)肝功能损伤,凝血因子分泌减少,纤维蛋白原减低;(3)药物导致过敏或免疫反应介导的无菌性炎症所引起的血管损伤[8]。氟马替尼是国内第二代Bcr-Abl1酪氨酸激酶抑制剂药物。其安全性、耐受性良好,对野生型和伊马替尼耐药的患者疗效都强于伊马替尼[9],其不良反应中水肿显著轻于伊马替尼,未发生心脏和心血管系统不良反应,同时说明书中未提示存在眼部不良反应,故给予患者换用氟马替尼,目前观察治疗中。通过本例患者诊治,对于充分了解伊马替尼常见及罕见不良反应提供了新的依据。
作者贡献:
吴娜:病例资料整理、收集及文章撰写
齐林:影像及超声资料收集
成志勇:提供论文写作思路并修改论文
丁月玲、周小代、谢阳阳、赵亚玲:部分病理资料收集、整理及校对
| [1] |
Bennour A, Saad A, Sennana H. Chronic myeloid leukemia: Relevance of cytogenetic and molecular assays[J]. Crit Rev Oncol Hematol, 2016, 97: 263-274. DOI:10.1016/j.critrevonc.2015.08.020 |
| [2] |
Hantel A, Larson RA. Imatinib Is Still Recommended for Frontline Therapy for CML[J]. Blood Adv, 2018, 2(24): 3648-3652. DOI:10.1182/bloodadvances.2018018614 |
| [3] |
SobhiEA, Zahrani Z, Zevallos E, et al. Imatinib-induced immune hepatitis: Case report and literature review[J]. Hematology, 2007, 12(1): 49-53. DOI:10.1080/10245330600937929 |
| [4] |
刘贵敏, 张丽军, 付建珠, 等. Ruxolitinib对JAK2V617F阳性骨髓增殖性肿瘤细胞基质金属蛋白酶调控的研究[J]. 中华血液学杂志, 2017, 38(2): 140-145. [Liu GM, Zhang LJ, Fu JZ, et al. Regulation of Ruxolitinib on matrix metalloproteinase in JAK2V617F positive myeloroliferative neoplasms cells[J]. Zhonghua Xue Ye Xue Za Zhi, 2017, 38(2): 140-145.] |
| [5] |
谢周涛, 李德秀. 甲磺酸伊马替尼不良反应的文献分析[J]. 医药导报, 2011, 30(7): 963-964. [Xie ZT, Li DX. Literature analysis of adverse reactions of imatinib mesylate[J]. Yi Yao Dao Bao, 2011, 30(7): 963-964.] |
| [6] |
Fraunfelder FW, Solomon J, Druker BJ, et al. Ocular Side-Effects Associated With Imatinib Mesylate (Gleevec)[J]. J Ocul Pharmacol Ther, 2003, 19(4): 371-375. DOI:10.1089/108076803322279426 |
| [7] |
Chen YH, Kuo HK, Kao ML, et al. Malignant hypertensive retinopathy-clinical and fundus manifestations in patients with new onset or acute exacerbation of chronic hypertension[J]. Chang Gung Med J, 2003, 26(9): 669-677. |
| [8] |
Nair RR, Chauhan R, Harankhedkar S, et al. Imatinib-induced platelet dysfunction and hypofibrinogenemia in chronic myeloid leukemia[J]. Blood Coagul Fibrinolysis, 2019, 30(5): 246-248. DOI:10.1097/MBC.0000000000000817 |
| [9] |
刘佳, 谢晓宝, 顾伟英, 等. 氟马替尼与伊马替尼治疗初诊慢性粒细胞白血病的有效性和安全性比较[J]. 白血病·淋巴瘤, 2016, 25(9): 526-530. [Liu J, Xie XB, Gu WY, et al. Comparison of the efficacy and safety between flumatinib and imatinib in newly diagnosed chronic myeloid leukemia[J]. Bai Xue Bing·Lin Ba Liu, 2016, 25(9): 526-530.] |
 2021, Vol. 48
2021, Vol. 48


