文章信息
- 伴中危风险因素ⅠB~ⅡA期宫颈鳞癌辅助化疗与同步放化疗预后的前瞻随机对照研究
- Prognosis of Stage ⅠB-ⅡA Cervical Squamous Cell Carcinoma Patients with Intermediate Risk Factors Treated with Adjuvant Chemotherapy Versus Concurrent Chemoradiotherapy: A Prospective Randomized Controlled Trial
- 肿瘤防治研究, 2021, 48(7): 714-718
- Cancer Research on Prevention and Treatment, 2021, 48(7): 714-718
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2021.20.0905
- 收稿日期: 2020-11-27
- 修回日期: 2021-04-19
早期宫颈癌的治疗模式以手术治疗为主,放疗、化疗等综合治疗为辅。宫颈癌术后经病理证实为肿瘤最大直径(largest tumor diameter, LTD) > 4 cm、淋巴脉管间隙浸润(lymphatic vascular space infiltration,LVSI)阳性和宫颈间质深层受侵(DI≥2/3)[1]是影响术后复发或转移的中危风险因素。根据NCCN指南,术后伴中危风险因素的ⅠB~ⅡA期宫颈癌患者,建议行辅助盆腔放疗±顺铂同期化疗。研究表明,同步放化疗在复发率、PFS、OS等结局指标上均优于单纯放疗[2]。
但有部分学者不赞同把同步放化疗作为中危患者的常规治疗方案,这部分学者的研究显示中危患者术后采用单纯辅助化疗也能达到同步放化疗的效果[3],且并发症少,治疗相关不良反应可耐受,有利于改善中危患者的生活质量,符合生物-心理-社会医学模式,更高层次上实现了对患者健康的医疗保障。然而,中危患者单纯辅助化疗的预后,未获得广泛认可。因此, 我们开展了早期宫颈癌中危患者辅助化疗与同步放化疗预后的前瞻性随机对照研究,以了解中危患者采取术后化疗是否安全有效。
1 资料与方法 1.1 病例资料2009年1月—2015年10月共有190例ⅠB1~ⅡA期宫颈鳞癌患者入组本研究。
入选标准:(1)临床分期ⅠB~ⅡA期(FIGO2009); (2)无生育要求,且在我院行宫颈鳞癌广泛根治性切除术(QM-C1或C2),术后恢复好;(3)术后病理满足:宫颈鳞状细胞癌,且术后病理提示含有一种或一种以上中危因素,无高危因素者;(4)术后美国东部肿瘤协作组(ECOG)体能评分0~2分;(5)术后肿瘤标志物在正常范围内;(6)肝、肾、骨髓功能正常。
排除标准如下: (1)临床分期是ⅠA、ⅡB、Ⅲ及Ⅳ期(FIGO2009);(2)二重癌,或既往有放疗、化疗史;(3)有骨髓贮备不足、肝肾功能异常、一般情况衰竭、严重感染等放疗、化疗禁忌证;(4)术后病理:宫颈非鳞状细胞癌或有复发高危因素;(5)合并妊娠、冠心病、先天性心脏病、中重度贫血等合并症;(6)精神障碍,不能配合者;(7)术后患者恢复差,或未能按时返院继续治疗者。
所有患者均签署知情同意书。本研究经广西医科大学附属肿瘤医院伦理委员会批准。
1.2 随机分组及治疗方案满足入组标准的患者按1:1比例被随机分为二个治疗组:(1)同步放化疗组(concurrent chemoradiotherapy, CCRT):术后4~6周开始盆腔外放射,界限:上界在L4椎体下缘,下界在闭孔下缘,两侧为真骨盆外2 cm,前界在耻骨结节后1 cm,后界在骶骨前平面。采用医学直线加速器6 MV常规分割法外照射:2 Gy/次,每天1野1次,5次/周,共23次,盆腔剂量为46 Gy。化疗采用铂类单药,在放疗第l天开始,间隔7天,共4个疗程,顺铂35 mg/m2; (2)单纯化疗组(chemotherapy group, CT):术后4~6周开始行TP(紫杉醇135 mg/m2 d1+顺铂75 mg/m2)方案全身化疗,间隔21天,共4个疗程。
1.3 评估及随访主要研究终点为3年无进展生存率(progression-free survival, PFS),次要研究终点包括总生存率(overall survival, OS)、局部复发率/远处复发率、辅助治疗的相关不良反应。PFS定义为从入组至最初出现影像学和(或)病理学疾病进展证据、因其他原因所致死亡或末次联系的时间间隔。OS定义为从入组至死亡或末次联系的时间间隔。盆腔及阴道复发/进展为局部复发/进展,局部之外的其他部位复发/进展均为远处复发/进展。术后1年内出现肿瘤为未控,1年后出现肿瘤为复发。根据美国国立癌症研究所常见毒性反应标准(National Cancer Institute Common Toxicity Criteria, NCI-CTC)评估辅助治疗的不良反应,即0~4分评价。患者于治疗结束后2年内,每3~6月进行一次随访,2年后每6~12月进行一次随访。
1.4 统计学方法生存数据均根据意向性治疗原则进行分析。患者对术后辅助治疗的临床反应及不良反应则根据实际接受的治疗及检验结果进行分析。统计分析采用SPSS16.0软件,χ2检验分析计数资料。成组t检验分析连续性数据(年龄、肿瘤大小)。Mann-Whitney U检验分析不满足正态分布的计量资料(肿瘤大小)。生存率计算和生存曲线比较采用Kaplan-Meier生存分析法,生存率差异比较采用Log rank检验。采用Cox回归分析评估影响生存的独立预后因素。本研究中所有P值均为双侧,P < 0.05为差异有统计学意义。死亡病例均标记为完全数据,对随访期间失访病例、末次随访时仍存活病例,统计分析时均按截尾数据处理。
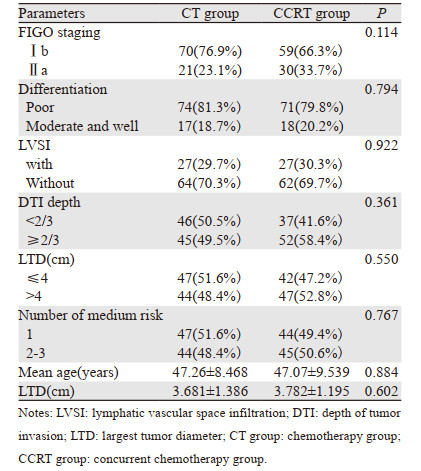
2 结果 2.1 基线评估两组患者的基线数据分布均衡,见表 1。两组临床参数、病理参数均有可比性。患者年龄31~70岁,平均年龄47岁。
|
主要的近期不良反应为血液学毒性及胃肠道不良反应。CCRT组易出现G3/4期的不良反应,其中CCRT组发生率为10.11%,CT组为3.30%,经对症治疗后可逐渐恢复,总体而言血液学不良反应可以接受,但胃肠道反应较重,患者生活质量差,5例因反应剧烈暂停放疗1周,CCRT组出现严重胃肠道反应的发生率为17.98%,CT组为4.4%。两组血液学及胃肠道不良反应差异有统计学意义(P=0.019, P=0.000),见表 2。化疗相关的恶心、呕吐及神经毒性较轻微且易于处理,未出现化疗相关的肾毒性、肝损害及过敏反应。CCRT组出现放疗相关反应,包括直肠炎、皮炎、膀胱炎、下肢水肿,发生率分别为11.24%、5.62%、3.37%、2.25%。
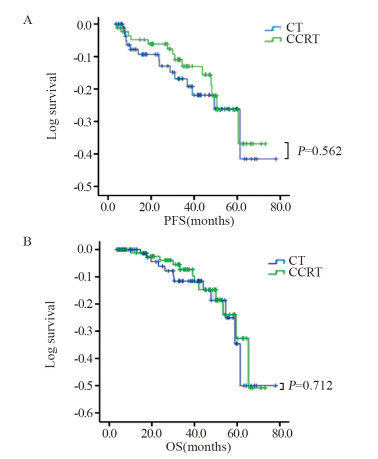
随访4~83月,中位随访36.7月,失访10例,共180例(随访率94.7%)患者可评估疗效。29例复发,24例死亡。两组间局部复发率(P=0.317)及远处复发率(P=0.224)差异无统计学意义,见表 3。CCRT组及CT组的3年PFS分别为89.6%及84.5%;5年PFS分别为80.2%及77.0%(P=0.562),见图 1A。3年OS分别为92.9%、89.1%,5年OS分别为83.1%、77.8%(P=0.712),见图 1B。PFS及OS在两组间亦无显著的统计学差异,见表 4。
|
| 图 1 两组无进展生存期(A)和总生存时间(B)的对数曲线 Figure 1 Logarithmic curves of PFS(A) and OS(B) of CT and CCRT groups |
早期宫颈癌经根治术后可达到手术完全缓解,但仍有10%~20%患者术后未控或复发,因此有必要对宫颈鳞癌中危患者进行术后辅助治疗[4]。唐秋等回顾性分析了行广泛性子宫切除术+盆腔淋巴结清扫术的早期(ⅠB~ⅡA期)宫颈癌患者临床资料,从中筛选出术后病理为鳞状细胞癌,伴有以下2~3个中危因素(淋巴脉管间隙浸润、肿瘤浸润深度 > 1/2或肿瘤大小 > 4 cm)的患者,其中单纯放疗组80例,同步放化疗组137例。分析结果认为同步放化疗能够改善术后伴有2~3个中危因素的早期宫颈癌患者预后,且急性骨髓抑制可耐受[5]。吉维等比较不同治疗方式对伴中危因素的Ⅰ~ⅡA期宫颈癌患者的生存差异,回顾性分析伴中危因素的323例宫颈癌术后患者,比较观察(NT)、单纯化疗(CT)、放疗(RT)及同步放化疗(CCRT)方式对生存的影响,认为仅有1个中危因素时,RT也能改善预后;伴有≥2个中危因素时,CCRT更能改善患者的预后[6]。
根据多项随机Ⅲ期临床试验结果,NCCN临床实践指南提倡对子宫颈癌根治术后具有中危因素患者行辅助放疗或者含铂类药物的同步放化疗。Sittidilokratna等[7]认为早期宫颈癌术后存在两个中危因素时需同步放化疗。同步放化疗的疗效已被大多数学者认可,并长期应用于临床,然而目前已有少量报道显示,术后单纯化疗对早期宫颈癌伴中危因素患者亦安全有效[8]。研究早期宫颈癌中危患者合理的综合治疗模式是进行规范化、个体化治疗的基础,对提高早期宫颈癌疗效、降低复发概率及改善患者生活质量有重要意义。本研究通过随机对照比较180例早期中危患者术后单纯化疗与同步放化疗的预后,在临床参数、病理参数、治疗相关不良反应、预后危险因素及治疗模式等方面进行分析,认为宫颈癌手术及术后化疗对于有复发中危因素的ⅠB~ⅡA期患者是一种可行的治疗选择,患者可耐受手术联合单纯化疗的并发症和不良反应。
化疗不但可缩小瘤体,有利于肿瘤的完整切除,而且能降低癌细胞活力、消灭微转移灶、减少术中播散及术后转移,有利于改善中危患者的术后生存质量、降低复发概率;术后同步放化疗可改善局部控制率及提高无瘤生存率和总的生存趋势[2-3]。本研究中,同步放化疗组的生存率与辅助化疗组无明显差异(P > 0.05)。Hosaka等[9]独立开展的临床研究也发现中危患者单纯化疗与放化疗的预后差异无统计学意义。Song等[2]研究指出宫颈癌患者术后行同步放化疗后Ⅲ、Ⅳ级的血液毒性明显增加。Ryu等[10]认为早期中危患者行术后同步放化疗可能导致过度治疗,影响患者生活质量。以上结论与本研究的统计分析结果一致。针对中危患者行根治术后辅助治疗的方案,在保证疗效的前提下,也需考虑到并发症、不良反应及患者意愿[11]。随着患者对生活质量要求的提高,选择化疗作为辅助治疗越来越多,术后单纯化疗可以避免术后放疗带来的不良反应(特别是阴道变窄、弹性降低,放射性肠炎及淋巴水肿等),而且化疗后复发多为盆腔复发,盆腔复发可以通过放疗完全缓解。相反,因为放疗的积累作用,导致宫颈癌CCRT后的复发患者,再次治疗方案的选择空间受限。
本前瞻随机对照研究结果显示,ⅠB~ⅡA期宫颈鳞癌术后伴中危因素患者单纯化疗与同步放化疗的疗效无显著差别,但不良反应较同步放化疗显著减少。因此,术后单纯化疗可作为此类患者的一种辅助治疗方案。
作者贡献:
潘忠勉:课题设计、实施、资料收集、论文撰写及修改
陈琦:病例随访、论文撰写
李力:课题总设计、监督课题实施、临床技术指导及论文修改
| [1] |
Mabuchi S, Morishige K, Isohashi F, et al. Postoperative concurrent nedaplatin-based chemoradiotherapy improves survival in early-stage cervical cancer patients with adverse risk factors[J]. Gynecol Oncol, 2009, 115(3): 482-487. DOI:10.1016/j.ygyno.2009.09.002 |
| [2] |
Song S, Song C, Kim HJ, et al. 20 year experience of postoperative radiotherapy in ⅠB-ⅡA cervical cancer patients with intermediate risk factors: impact of treataient period and concurrent chemotherapy[J]. Gynecol Oncol, 2012, 124(1): 63-67. DOI:10.1016/j.ygyno.2011.09.033 |
| [3] |
温宏武, 黄卫平, 刘桐宇, 等. 不同辅助治疗方法对Ⅰb~Ⅱa期子宫颈癌术后有危险因素患者预后的影响[J]. 中华妇产科杂志, 2013, 48(12): 920-926. [Wen HW, Huang WP, Liu TY, et al. Results of different postoperative adjuvant therapies for stage Ⅰb-Ⅱa cervical carcinoma with risk factors[J]. Zhonghua Fu Chan Ke Za Zhi, 2013, 48(12): 920-926. DOI:10.3760/cma.j.issn.0529-567x.2013.12.010] |
| [4] |
Landoni F, ColomboA, Milani R, et al. Randomized study between radical surgery and radiotherapy for the treatment of stage ⅠB-ⅡA cervical cancer: 20-year update[J]. J Gynecol Oncol, 2017, 28(3): e34: 1-10. |
| [5] |
唐秋, 屠晔强, 陈建红, 等. 同步放化疗治疗早期宫颈癌术后中危患者的疗效分析[J]. 中华肿瘤杂志, 2018, 40(6): 462-466. [Tang Q, Tu YQ, Chen JH, et al. Curative effect analysis of postoperative concurrent chemoradiotherapy on early-stage cervical cancer patients withintermediate-risk factors[J]. Zhonghua Zhong Liu Za Zhi, 2018, 40(6): 462-466. DOI:10.3760/cma.j.issn.0253-3766.2018.06.012] |
| [6] |
吉维, 冉立, 常建英, 等. 不同治疗方式对术后伴中危因素Ⅰ-ⅡA期宫颈癌预后影响[J]. 中华放射肿瘤学杂志, 2019, 28(5): 358-363. [Ji W, Ran L, Chang JY, et al. Effect of different therapeutic methods on survival of stage Ⅰ-Ⅱ A cervical cancer patients complicated with postoperative intermediate risk factors[J]. Zhonghua Fang She Zhong Liu Xue Za Zhi, 2019, 28(5): 358-363. DOI:10.3760/cma.j.issn.1004-4221.2019.05.008] |
| [7] |
Sittidilokratna K, Cheewakriangkrai C, Khunamornpong S, et al. Recurrence patterns after radical hysterectomy in stageⅠB1-ⅡA cervical[J]. Asian Pac J Cancer Prev, 2010, 11(2): 499-502. |
| [8] |
Lee KB, Lee JM, Ki KD, et al. Comparison ofadjuvant chemotherapy and radiation in patients with intermediate risk factors after radical surgery in FIGO stageⅠB-ⅡA cervical cancer[J]. Int J Gynecol Cancer, 2008, 18(5): 1027-1031. DOI:10.1111/j.1525-1438.2007.01136.x |
| [9] |
Hosaka M, Watari H, Takeda M, et al. Treatment of cervical cancer with adjuvant chemotherapy versus adjuvant radiotherapy after radical hysterectomy and systematic lymphadenectomy[J]. J Obstet Gynaecol Res, 2008, 34(4): 552-556. DOI:10.1111/j.1447-0756.2008.00739.x |
| [10] |
Ryu SY, Park SI, Nam BH, et al. Is adjuvant chemoradiotherapy overtreatment in cervical cancer patients with intermediate risk factors?[J]. Int J Radia Oncol Biol Physics, 2011, 79(3): 794-799. DOI:10.1016/j.ijrobp.2009.11.019 |
| [11] |
Hosaka M, Watari H, Kato T, et al. Clinical efficacy of paclitaxel/cisplatin as an adjuvant chemotherapy for patients with cervical cancer who underwent radical hysterectomy and systematic lymphadenectomy[J]. J Surg Oncol, 2012, 105(6): 612-616. DOI:10.1002/jso.22136 |
 2021, Vol. 48
2021, Vol. 48





