文章信息
- 常规根治术、门静脉重建和肝动脉重建治疗肝门部胆管癌的安全性及近期疗效比较
- Comparison of Safety and Short-term Efficacy Among Conventional Radical Surgery, Portal Vein Reconstruction and Hepatic Artery Reconstruction on Hilar Cholangiocarcinoma
- 肿瘤防治研究, 2020, 47(8): 623-626
- Cancer Research on Prevention and Treatment, 2020, 47(8): 623-626
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2020.19.0858
- 收稿日期: 2019-07-01
- 修回日期: 2020-05-18
肝门部胆管癌(hilar cholangiocarcinoma, HCCA)是发生在胆囊管开口以上的胆管黏膜上皮癌,是影响人类健康的肿瘤之一[1]。目前,医学界认为手术是根治肝门部胆管癌的最有效手段,但是由于肝管解剖位置的特殊性,手术难度较大,导致根治率较低[2]。既往认为肝动脉受侵犯时,肝门部胆管癌即已到终末期,根治性手术治疗将无法实施,反而会增加术后感染、肝功衰竭等并发症的发生,因此认为肿瘤侵犯血管是根治性手术的禁忌证[3];近年来有研究发现,肝门部胆管癌对肝动脉并不是真正的侵犯,而是肿瘤的生长对周围的组织结构产生了压迫,所以若肝动脉受侵犯只行姑息性手术而未行根治性切除术,患者得到根治肿瘤的可能性降到零;而联合血管切除能否有效提高手术根治切除率,仍存在一定的争议[4-6]。因此,本研究分析了108例肝门部胆管癌患者的临床资料,拟探讨联合肝动脉切除重建是否会改善肝门部胆管癌患者的预后。
1 资料与方法 1.1 一般资料选取2016年10月—2018年2月在我院行根治性手术的108例肝门部胆管癌患者作为研究对象,手术适应证为:(1)肿瘤边缘均未超过近端胆管切除极限点;(2)能够保留预留肝脏血管结构的完整性;(3)预留的肝脏功能性体积不小于患者的必需功能性肝体积。根据手术方式的不同分为三组:常规根治术组(A组)28例、门静脉重建术组(B组)48例和肝动脉重建术组(C组)32例。纳入标准:(1)术前均行上腹部增强CT联合血管成像、磁共振检查、肝功能及肿瘤标志物检测等确诊为肝门部胆管癌;(2)上腹部CT血管成像均显示存在血管侵犯;(3)术前合并黄疸患者行减黄治疗;(4)患者均符合肝门部胆管癌根治性切除术的手术指征[7],均行根治性切除术。排除标准:(1)合并其他肿瘤;(2)配合度低,不能完成本次研究的患者;(3)术后随访资料不全;(4)合并其他胆道疾病。本研究经辽宁省鞍钢集团总医院医学伦理委员会同意,所有患者均签署知情同意书。
1.2 方法患者术前均行辅助检查,进行术前评估,并通过调节内环境、保肝治疗、输注激化液等提高肝功储备功能。根据患者病情提供减黄治疗(患者术前血清总胆红素超过50 μmol/L时认为具有黄疸,需行减黄治疗[8])、ERCP内架引流术、PTCD等疗法。所有患者均行根治性切除术,常规根治术采用半肝联合尾状叶切除,切除肝十二指肠韧带内的全部组织,但是门静脉及肝动脉内的组织不予以切除。清扫肝总动脉周围、胰头后及腹腔干周围的淋巴结和神经丛组织。门静脉重建术组根据门静脉受侵犯情况,同时行门静脉吻合重建。肝动脉重建术组根据肝动脉受侵犯情况,进行肝动脉血管切除重建,最后完成胆管重建。
1.3 统计学方法采用统计学软件包SPSS22.0处理数据,其中,围手术期各指标均为定量资料,数据使用均数±标准差(x±s)来表示,三组间的比较采用单因素方差分析,有统计学意义时进行两两比较,采用LSD-t检验;并发症发生率、淋巴结转移率及术后1年生存率均为定性资料,数据用百分率表示,三组样本间的分析采用3×2列联表卡方检验,两两比较时需对检验水准进行校正,P < 0.05为差异有统计学意义。
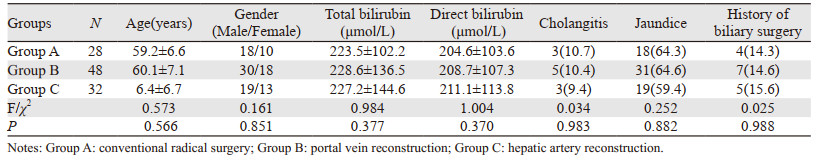
2 结果 2.1 患者一般资料的比较结果显示,三组间各指标的差异均无统计学意义(均P > 0.05),三组患者间存在可比性,见表 1。
|
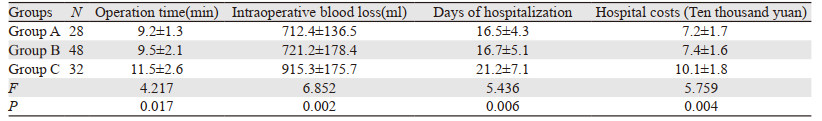
三组患者手术时间、术中出血量、住院时间及住院费用差异均有统计学意义(F=4.217, 6.852, 5.436, 5.759,均P < 0.05)。两两比较结果显示,C组上述指标值均高于A组和B组(均P < 0.05),见表 2。
|
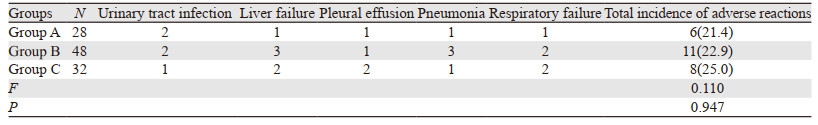
三组患者术后并发症发生率差异无统计学意义(χ2=0.110, P > 0.05),见表 3。
|
A、B、C三组患者淋巴结转移率分别为21.4%(6/28)、18.8%(9/48)、21.9%(7/32),差异无统计学意义(χ2=0.142, P=0.932);A、B、C三组患者术后1年生存率分别为85.7%、85.4%、81.3%,差异无统计学意义(χ2=0.312, P=0.856)。
3 讨论既往认为联合血管切除会增加术后并发症发生率,并不能改善患者预后,而成为了肝门部胆管癌根治术的禁忌证[9],而近些年随着血管外科技术的不断更新与发展,发现联合血管切除不仅可以减少术后并发症的发生,还能延长患者的生存期,提高其生活质量,已不再是根治术的禁忌证,并且该观点已被越来越多的研究组所认可[10]。传统根治术采用的是保留血管将肿瘤切除的观点,并不能将血管壁癌细胞清除干净,但相关研究认为,对粘连的血管进行切除可以达到根治的目的[11-12]。门静脉受侵袭时联合门静脉切除后重建可显著延长患者的生存时间,而肝动脉受侵时是否行肝动脉切除重建仍存在一定的争议[13-15]。部分研究者认为只需结扎肝动脉而无需重建,理由可能是肝脏同时具备门静脉及肝动脉双重血供,而门静脉可提供给肝脏70%的血供,结扎肝动脉对肝脏血供影响甚微[16-17];由于肝动脉口径细、重建难度大且易引发闭塞;切除肝动脉后不进行重建,不仅可以缩短手术时间,也不会增加术后并发症[18-19]。另一部分研究者认为需行肝动脉重建,理由是随着血管外科医疗技术的不断发展,肝动脉重建后再阻塞率明显下降[20];尽管肝动脉对肝脏的血供只有30%,但是肝动脉可为肝管提供全部的血供,且肝脏50%的氧供来源于肝动脉,直接对肝动脉进行结扎会造成肝组织缺血缺氧性损害,由此可见行肝动脉重建具有重要意义[21-22]。
本研究结果显示,肝动脉重建术组患者的术后并发症发生率、淋巴结转移率及术后1年生存率与常规根治术组、门静脉重建术组患者差异均无统计学意义,说明行肝动脉重建并未增加并发症发生率及淋巴结转移率,安全性较高;但是与行常规根治术、门静脉重建术相比,接受肝动脉重建的患者并未在生存时间上受益,且手术时间和住院时间均更长、术中出血量更多、住院费用更高,且肝动脉重建术的难度相对较高,要求医师具有较高的水准。陈志宇等[11]研究发现,与姑息性手术组相比,血管重建组患者的生存时间明显延长,如果由于血管受侵犯而放弃行根治性手术,这些患者从手术中的获益将大为降低,他们认为门静脉、肝动脉切除重建可以提高肝门部胆管癌的R0切除率,能够显著延长患者术后生存时间,且门静脉切除重建已被公认为有利于肝门胆管癌患者的预后;但是本研究并未得出门静脉重建术可提高患者生存时间的结论,这可能与本研究仅收集1年生存率且样本量有限存在一定关联。不同术式均具有其优势与劣势,故应视患者的具体情况,选取合适的手术方式。
综上所述,肝动脉重建与门静脉重建患者近期生存率无差异,并能提高根治性手术切除率,因此联合血管重建对患者预后具有积极意义;但是肝动脉重建也存在一定的缺陷,其手术时间与住院时间均较长、术中出血量较高、住院花费多,需根据患者情况选取合适的手术方式。
作者贡献
刘彬彬:论文撰写、研究实施、数据收集
富民:论文设计、立题
| [1] |
余安, 黄强, 刘臣海, 等. 联合门静脉切除及重建治疗肝门部胆管癌临床疗效的Meta分析[J]. 中华消化外科杂志, 2017, 16(1): 65-70. [Yu A, Huang Q, Liu CH, et al. Clinical efficacy of combined portal vein resection and construction in the treatment of hilar cholangiocarcinoma: A Meta-analysis[J]. Zhonghua Xiao Hua Wai Ke Za Zhi, 2017, 16(1): 65-70.] |
| [2] |
Sugiura T, Okamura Y, Ito T, et al. Left Hepatectomy with Combined Resection and Reconstruction of Right Hepatic Artery for Bismuth TypeⅠandⅡPerihilar Cholangiocarcinoma[J]. World J Surg, 2019, 43(3): 894-901. DOI:10.1007/s00268-018-4833-1 |
| [3] |
钟鼎文, 叶荣强, 廖永晖, 等. 联合血管切除重建在肝门部胆管癌外科手术中的应用[J]. 现代医院, 2018, 18(12): 1789-1791. [Zhong DW, Ye RQ, Liao YH, et al. Application of Combined Vascular Resection and Reconstruction in Surgical Treatment of Hilar Cholangiocarcinoma[J]. Xian Dai Yi Yuan, 2018, 18(12): 1789-1791.] |
| [4] |
Schmelzle M, Sucher R, Seehofer D, et al. Regarding: Impact of portal vein resection on oncologic long-term outcome in patients with hilar cholangiocarcinoma[J]. Surgery, 2016, 159(3): 986-987. |
| [5] |
Wiggers JK, Koerkamp BG, Cieslak KP, et al. Postoperative Mortality after Liver Resection for Perihilar Cholangiocarcinoma: Development of a Risk Score and Importance of Biliary Drainage of the Future Liver Remnant[J]. J Am Coll Surg, 2016, 223(2): 321-331.e1. DOI:10.1016/j.jamcollsurg.2016.03.035 |
| [6] |
Matsuyama R, Mori R, Ota Y, et al. Significance of Vascular Resection and Reconstruction in Surgery for Hilar Cholangiocarcinoma: With Special Reference to Hepatic Arterial Resection and Reconstruction[J]. Ann Surg Oncol, 2016, 23(Suppl 4): 475-484. |
| [7] |
Ethun CG, Lopez-Aguiar AG, Anderson DJ, et al. Transplantation Versus Resection for Hilar Cholangiocarcinoma: An Argument for Shifting Treatment Paradigms for Resectable Disease[J]. Ann Surg, 2018, 267(5): 797-805. DOI:10.1097/SLA.0000000000002574 |
| [8] |
孙文韬, 吴岚, 邓侠兴. 梗阻性黄疸术前减黄的必要性及依据[J]. 中华肝脏外科手术学电子杂志, 2018, 7(5): 357-359. [Sun WT, Wu L, Deng XX. The necessity and basis of preoperative jaundice reduction in obstructive jaundice[J]. Zhonghua Gan Zang Wai Ke Shou Shu Xue Dian Zi Za Zhi, 2018, 7(5): 357-359.] |
| [9] |
戴海粟, 别平, 王曙光, 等. 联合肝动脉切除重建在肝门部胆管癌根治术中的临床研究[J]. 中华外科杂志, 2018, 56(1): 41-46. [Dai HS, Bie P, Wang SG, et al. Clinical application of combined hepatic artery resection and reconstruction in surgical treatment for hilar cholangiocarcinoma[J]. Zhonghua Wai Ke Za Zhi, 2018, 56(1): 41-46.] |
| [10] |
Bhat M, Hathcock M, Kremers WK, et al. Portal vein encasement predicts neoadjuvant therapy response in liver transplantation for perihilar cholangiocarcinoma protocol[J]. Transpl Int, 2016, 28(12): 1383-1391. |
| [11] |
陈志宇, 别平. 联合血管切除与重建在肝门部胆管癌外科治疗中的应用[J]. 临床肝胆病杂志, 2016, 32(7): 1277-1279. [Chen ZY, Bie P. Clinical application of combined vascular resection and reconstruction in surgical treatment of hilar cholangiocarcinoma[J]. Lin Chuang Gan Dan Bing Za Zhi, 2016, 32(7): 1277-1279.] |
| [12] |
Olthof PB, Wiggers JK, Koerkamp BG, et al. Postoperative Liver Failure Risk Score: Identifying Patients with Resectable Perihilar Cholangiocarcinoma Who May Benefit from Portal Vein Embolization[J]. J Am Coll Surg, 2017, 225(3): 387-394. DOI:10.1016/j.jamcollsurg.2017.06.007 |
| [13] |
邱建国, 李明, 史政荣, 等. 门静脉动脉化在肝门部胆管癌根治术中的应用价值[J]. 中国普外基础与临床杂志, 2018, 25(2): 221-224. [Qiu JG, Li M, Shi ZR, et al. Application value of portal vein arterialization in radical operation of hilar cholangiocarcinoma[J]. Zhongguo Pu Wai Ji Chu Yu Lin Chuang Za Zhi, 2018, 25(2): 221-224.] |
| [14] |
Olthof PB, Wiggers JK, Koerkamp BG, et al. Postoperative Liver Failure Risk Score: Identifying Patients with Resectable Perihilar Cholangiocarcinoma Who May Benefit from Portal Vein Embolization[J]. J Am Coll Surg, 2017, 225(3): 387-394. DOI:10.1016/j.jamcollsurg.2017.06.007 |
| [15] |
Guiu B, Chevallier P, Denys A, et al. Simultaneous trans-hepatic portal and hepatic vein embolization before major hepatectomy: the liver venous deprivation technique[J]. Eur Radiol, 2016, 26(12): 4259-4267. DOI:10.1007/s00330-016-4291-9 |
| [16] |
洪德飞, 范小明, 罗祖炎, 等. 经皮微波或射频消融肝实质分隔联合门静脉栓塞计划性肝切除术治疗余肝体积不足肝癌及胆管癌3例报告[J]. 中国实用外科杂志, 2016, 36(1): 96-101. [Hong DF, Fang XM, Luo ZY, et al. Percutaneous microwave/ radiofrequency ablation liver partition and portal vein embolization for planned hepatectomy (PAPEP) for HCC and perihilar cholangiocarcinoma with insufficient future liver remnant:A report of 3 cases[J]. Zhongguo Shi Yong Wai Ke Za Zhi, 2016, 36(1): 96-101.] |
| [17] |
Miyata A, Sakamoto Y, Yamamoto S, et al. Aggressive Hemihepatectomy Combined with Resection and Reconstruction of Middle Hepatic Vein for Intrahepatic Cholangiocarcinoma[J]. Ann Surg Oncol, 2016, 23(Suppl 4): 494-500. |
| [18] |
张耀东, 李相成. 合并血管切除重建的肝门部胆管癌根治术[J]. 中华肝胆外科杂志, 2018, 24(2): 135-139. [Zhang YD, Li XC. Vascular resection and reconstruction for hilar cholangiocarcinoma[J]. Zhonghua Gan Dan Wai Ke Za Zhi, 2018, 24(2): 135-139.] |
| [19] |
Wang XD, Hu JG, Cao G, et al. Phase Ⅱ Study of Hepatic Arterial Infusion Chemotherapy with Oxaliplatin and 5-Fluorouracil for Advanced Perihilar Cholangiocarcinoma[J]. Radiology, 2017, 283(2): 580-589. DOI:10.1148/radiol.2016160572 |
| [20] |
Burt AD, Alves V, Bedossa P, et al. Data set for the reporting of intrahepatic cholangiocarcinoma, perihilar cholangiocarcinoma and hepatocellular carcinoma: recommendations from the International Collaboration On Cancer Reporting (ICCR)[J]. Histopathology, 2018, 73(3): 369-385. DOI:10.1111/his.13520 |
| [21] |
齐卫鹏, 王剑明, 张剑, 等. 联合血管切除重建在肝门部胆管癌根治术中的应用(附16例病例分析)[J]. 中国医师进修杂志, 2016, 39(7): 627-630. [Qi WP, Wang JM, Zhang J, et al. The application of vascular resection in the radical resection of hilar cholangiocarcinoma: an analysis of 16 cases[J]. Zhongguo Yi Shi Jin Xiu Za Zhi, 2016, 39(7): 627-630.] |
| [22] |
徐明月, 史宪杰, 梁雨荣, 等. 联合肝叶及肝门部血管切除治疗肝门部胆管癌[J]. 国际外科学杂志, 2012, 39(8): 535-538, 封3. [Xu MY, Shi XJ, Liang YR, et al. Combind liver and hilar vascular resection for hilar cholangiocarcinoma[J]. Guoji Wai Ke Xue Za Zhi, 2012, 39(8): 535-538, cover 3.] |
 2020, Vol. 47
2020, Vol. 47
