文章信息
- 甲状腺功能减退与子宫内膜癌的相关性分析
- Correlation of Hypothyroidism and Endometrial Carcinoma
- 肿瘤防治研究, 2019, 46(5): 452-455
- Cancer Research on Prevention and Treatment, 2019, 46(5): 452-455
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2019.18.1902
- 收稿日期: 2018-12-10
- 修回日期: 2019-01-17
子宫内膜癌(endometrial carcinoma, EC)是发生于子宫内膜的一组上皮恶性肿瘤,是最常见的妇科肿瘤之一,其发病率逐年上升。Ⅰ型EC的主要危险因素是长期暴露于缺乏孕激素拮抗的雌激素环境,临床上常见于肥胖、糖尿病、代谢综合征、月经初潮过早及绝经延迟、未生育、使用他莫昔芬[1]及饮食保健品的女性。而Ⅱ型EC的发病与雌激素无明确关系。年龄(> 55岁)、高血压、遗传因素、子宫内膜息肉、吸烟与饮酒等作用因素也与EC有关[2]。因此进一步发现EC的高危因素成为亟待解决的问题。探究EC的高危因素,有利于为EC的预防、筛查、诊断与治疗提供新的思路。
甲状腺分泌的甲状腺激素可通过下丘脑-垂体-卵巢轴的调节,对性腺的发育以及维持女性正常生殖内分泌功能起着重要的作用[3]。Ajmani等[4]的一项研究纳入了100例女性,其在对子宫内膜的病理分析中发现,在甲状腺功能减退患者中有21.42%表现为子宫内膜增生,甲状腺功能正常者仅有12%表现为子宫内膜增生。甲状腺功能减退往往起病隐匿,需要通过测定甲状腺功能来诊断,然而通过测定甲状腺功能来诊断甲状腺功能减退的EC与甲状腺功能减退的相关性研究,以及EC患者癌组织中雌激素受体(estrogen receptor, ER)、孕激素受体(progesterone receptor, PR)的表达与甲状腺功能之间关系,未见报道。本研究将测定EC患者术前及对照组的甲状腺功能,并分析EC患者癌组织分化程度及癌组织中雌激素受体、孕激素受体的表达与甲状腺功能之间相关性。
1 资料与方法 1.1 研究对象收集2015年1月—2018年7月桂林医学院附属医院妇科收治的EC患者113例,同时随机选取年龄与EC组相匹配的此段时间内我院体检中心进行健康体检的妇女156例作为对照组。EC组入选标准:女性,经分段诊刮或手术病理确诊为EC,排除其他恶性肿瘤和(或)因甲亢行甲状腺手术、碘131治疗及抗甲状腺药物治疗过量导致甲减者以及亚急性甲状腺炎、甲状腺结核患者。对照组入选标准:女性,排除恶性肿瘤相关疾病和(或)因甲亢行甲状腺手术、碘131治疗及抗甲状腺药物治疗过量导致甲减者以及亚急性甲状腺炎、甲状腺结核患者。本研究符合医院人体试验委员会制定的伦理学标准。
EC组年龄35~73岁,平均年龄52.97岁,中位年龄53岁;对照组年龄33~68岁,平均年龄51.26岁,中位年龄50.5岁,EC组与对照组的年龄等一般资料比较,差异无统计学意义(P > 0.05),具有可比性。
1.2 诊断标准原发性临床甲状腺功能减退:实验室检查血清促甲状腺激素(TSH)增高,游离甲状腺激素(FT4)降低。原发性亚临床甲状腺功能减退:实验室检查仅有血清TSH增高,FT4正常。中枢性甲状腺功能减退:实验室检查血清TSH减低或者正常,FT4减低[5]。本研究采用电化学发光法检测血清TSH、FT4,试剂盒为罗氏公司产品。TSH正常值为:0.27~4.2 uIU/ml,FT4正常值为12~22 pmol/L。
1.3 检测方法检测子宫内膜癌组术前及对照组的甲状腺功能:受检者空腹12 h后,于次日清晨抽取外周静脉血,采用电化学发光法检测血清TSH、FT4,试剂盒为罗氏公司产品。比较两组间甲状腺功能减退患病率,并利用免疫组织化学二步法检测EC患者手术切除标本石蜡切片的病变子宫内膜中ER、PR的表达。结果判断:以癌细胞核内是否有棕黄色颗粒判断,根据着色程度:标本无色为0分,浅黄色为1分,棕黄色2分,棕褐色3分。根据阳性细胞百分比:≤10%为1分;10%~50%为2分;≥50%~75%为3分;> 75%为4分。两项指标分数乘积,0~3分为阴性,≥4分为阳性,分析ER、PR与甲状腺功能之间的关联性。
1.4 统计学方法运用统计软件SPSS22.0对相关数据进行整理与分析,由于样本来自于非正态总体,本研究计量资料采用秩和检验,结果用中位数(四分位数间距)M(Q)表示。计数资料采用百分率(%)表示,进行χ2检验,P < 0.05为差异有统计学意义。
2 结果 2.1 EC组与对照组甲状腺功能减退的发病率比较EC组甲状腺功能减退(包括原发性临床甲状腺功能减退、原发性亚临床甲状腺功能减退和中枢性甲状腺功能减退)的患病率较对照组高(P < 0.000),见表 1。

|
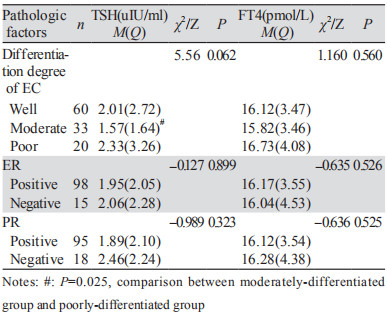
低分化EC患者的TSH高于中分化EC患者(P=0.025)。低分化EC患者的FT4与中分化EC患者的FT4比较差异无统计学意义(P=0.545)。高分化EC患者的TSH、FT4与中分化EC患者的TSH、FT4比较差异无统计学意义(P=0.073、P=0.785)。高分化EC患者的TSH、FT4与低分化EC患者的TSH、FT4比较差异无统计学意义(P=0.499、P=0.316)。EC患者手术切除标本的癌组织中ER、PR阳性与阴性患者的TSH、FT4差异无统计学意义(P > 0.05),见表 2。
本研究显示,EC组甲状腺功能减退(包括原发性临床甲状腺功能减退、原发性亚临床甲状腺功能减退和中枢性甲状腺功能减退)的患病率较对照组高(P < 0.000)。甲状腺功能减退可能导致外周雌激素代谢的改变,从而增加EC的发生风险。甲状腺功能减退症的女性严重者会有排卵障碍[6]。临床型甲状腺功能减退与不孕有关[7]。甲状腺功能减退患者血浆性激素结合球蛋白减少,导致血浆总睾酮和雌二醇浓度下降,但是游离的部分增加,游离雌激素可与相应的受体结合,发挥生物学效应。排卵障碍、不孕、游离雌激素增加可导致子宫内膜受到长期的雌激素作用而缺乏孕激素拮抗,增加EC发生的风险。
甲状腺相关激素有可能直接作用于子宫内膜。Aghajanova等[8]在子宫内膜上检测到促甲状腺激素受体(thyroid-stimulating hormone receptor, TSHR)和甲状腺素受体α1、α2、β1(thyroid hormone receptor α1、α2、β1,THRα1、α2、β1)mRNA及蛋白的表达,且在月经周期的不同时期表达量不同。与未刺激细胞相比,TSH能显著增加石川细胞(人EC细胞)分泌游离三碘甲状腺原氨酸和总甲状腺素。由此推测,甲状腺功能减退可能导致EC的作用机制可能与甲状腺相关激素直接作用于子宫内膜有关。但它们之间有怎样的相关性、具体作用机制如何,仍需要大量的临床观察和实验性研究。
甲状腺功能减退有可能通过瘦素途径促进EC的发生及发展。Kar等[9]发现甲状腺功能减退症患者血清TSH、瘦素显著高于对照组。冯宗昊等[10]发现高血浆瘦素水平是Ⅰ型EC发病的独立危险因素。由此推测甲状腺功能减退有可能导致体内瘦素的升高而增加EC的发生风险。
甲状腺功能减退有可能通过胰岛素抵抗等因素促进EC的发生及发展。Kar等[9]研究发现甲状腺功能减退症患者的胰岛素抵抗指数均显著高于对照组。Shan等[11]的一项纳入了314例的前瞻性横断面研究提示高胰岛素血症不仅增加Ⅰ型EC的风险,还增加了子宫内膜不典型性增生的风险。由此推测甲状腺功能减退有可能导致胰岛素抵抗进而促进EC的发生发展。
甲状腺功能减退可能导致血脂异常进而增加EC的患病风险。甲状腺功能减退往往伴随血清总胆固醇、低密度脂蛋白胆固醇及三酰甘油升高,是继发性血脂异常的常见病因之一。近年来流行病学研究显示仅有TSH升高的亚临床甲状腺功能减退也与血脂异常关系密切[12]。而血脂异常代谢很可能通过胰岛素抵抗及导致低脂联素血症促进EC的发生发展[13]。由此推测甲状腺功能减退可能导致血脂异常进而增加EC的发生风险。
3.2 甲状腺功能与EC病理因素的关系本研究显示低分化EC的TSH高于中分化EC(P=0.025),甲状腺功能与EC患者癌组织中雌激素受体、孕激素受体的表达无关。可能的原因有Ⅱ型EC大多分化差,且多见于老年女性,60岁以上的老年女性亚甲减患病率高于其他年龄人群[14],而亚临床甲减患者的TSH升高。
3.3 局限性讨论与展望本研究仅做了疾病之间相关性的研究。这些结论尚需要大样本的队列研究进一步证明,而且每位研究对象均应行甲状腺功能检查。本研究未动态监测EC组患者术后的TSH。甲状腺功能减退导致EC的发病机制尚不清楚,尚需实验性研究来探索其机制,其有利于为EC的预防、筛查、诊断与治疗提供新的思路,如患有甲状腺功能减退患者应积极治疗,以减少EC的发生风险;对有甲状腺功能减退等EC高危因素的患者,应定期体检,密切随访及监测。甲状腺功能有可能用于EC的筛查及作为EC患者预后评估及随访指标。
综上所述,甲状腺功能减退与EC具有相关性,但它们之间具体的相互作用机制如何,仍需实验性研究进一步探索,其有利于为EC的预防、筛查、诊断与治疗提供新的思路。
作者贡献
廖玉萍: 研究设计与实施、搜集临床资料、数据统计分析、论文撰写
杨冰: 指导研究设计及论文撰写
| [1] | Morice P, Leary A, Creutzberg C, et al. Endometrial cancer[J]. Lancet, 2016, 387(10023): 1094–108. DOI:10.1016/S0140-6736(15)00130-0 |
| [2] | 张阳阳, 张琨, 李冬, 等. 子宫内膜癌发病相关危险因素的研究进展[J]. 中国妇幼保健, 2018, 33(1): 219–22. [ Zhang YY, Zhang K, Li D, et al. Advances in risk factors related to endometrial carcinoma[J]. Zhongguo Fu You Bao Jian, 2018, 33(1): 219–22. ] |
| [3] | 殷冬梅, 阮祥燕. 妇科内分泌疾病与甲状腺功能的关系研究进展[J]. 医学综述, 2016, 22(24): 4852–5. [ Yin DM, Ruan XY. Research Advance of the Relationship between the Gynecological Endocrine Diseases and Thyroid Function[J]. Yi Xue Zong Shu, 2016, 22(24): 4852–5. DOI:10.3969/j.issn.1006-2084.2016.24.017 ] |
| [4] | Ajmani NS, Sarbhai V, Yadav N, et al. Role of Thyroid Dysfunction in Patients with Menstrual Disorders in Tertiary Care Center of Walled City of Delhi[J]. J Obstet Gynaecol India, 2016, 66(2): 115–9. DOI:10.1007/s13224-014-0650-0 |
| [5] | 葛均波, 徐永建, 王辰.内科学[M].第九版.北京: 人民卫生出版社, 2018: 689-91. [ Ge JB, Xu YJ, Wang C. Internal Medicine[M]. The Ninth Edition. Beijing: People's Medical Publishing House, 2018: 689-91. ] |
| [6] | 王亚茹, 张洁, 吴隆琦, 等. 甲状腺疾病与女性生殖[J]. 生殖与避孕, 2014, 34(3): 232–6. [ Wang YR, Zhang J, Wu LQ, et al. Thyroid Diseases and Femal Reproduction[J]. Sheng Zhi Yu Bi Yun, 2014, 34(3): 232–6. ] |
| [7] | 中国医师协会生殖医学专业委员会. 高龄女性不孕诊治指南[J]. 中华生殖与避孕杂志, 2017, 37(2): 87–100. [ Chinese Medical Doctor Association Reproductive Medicine Specialized Committee. Guideline for diagnosis and treatment of infertility in advanced age women[J]. Zhonghua Sheng Zhi Yu Bi Yun Za Zhi, 2017, 37(2): 87–100. ] |
| [8] | Aghajanova L, Stavreus-Evers A, Lindeberg M, et al. Thyroid-stimulating hormone receptor and thyroid hormone receptorsare involved in human endometrial physiology[J]. Fertil Steril, 2011, 95(1): 230–7. DOI:10.1016/j.fertnstert.2010.06.079 |
| [9] | Kar K, Sinha S. Variations of Adipokines and Insulin Resistance in Primary Hypothyroidism[J]. J Clin Diagn Res, 2017, 11(8): BC07-9. |
| [10] | 冯宗昊, 刘林枝, 张岩. 血浆瘦素水平与子宫内膜病变风险相关性研究[J]. 中国实用妇科与产科杂志, 2018, 34(6): 662–5. [ Feng ZH, Liu LZ, Zhang Y. Plasma leptin and risk of endometrial lesion[J]. Zhongguo Shi Yong Fu Ke Yu Chan Ke Za Zhi, 2018, 34(6): 662–5. ] |
| [11] | Shan W, Ning C, Luo X, et al. Hyperinsulinemia is associated with endometrial hyperplasia and disorderedproliferative endometrium: A prospective cross-sectional study[J]. Gynecol Oncol, 2014, 132(3): 606–10. DOI:10.1016/j.ygyno.2014.01.004 |
| [12] | 赵家军, 杨利波. 甲状腺功能减退与血脂异常[J]. 中国实用内科杂志, 2014, 34(4): 340–3. [ Zhao JJ, Yang LB. Hypothyroidism and dyslipidemia[J]. Zhongguo Shi Yong Nei Ke Za Zhi, 2014, 34(4): 340–3. ] |
| [13] | 曾秋平, 曾剑兵, 方秀兰. 子宫内膜癌患者血脂代谢临床分析[J]. 实用肿瘤杂志, 2018, 33(2): 158–61. [ Zeng QP, Zeng JB, Fang XL. Clinical analysis of lipid metabolism in patients with endometrial carcinoma[J]. Shi Yong Zhong Liu Za Zhi, 2018, 33(2): 158–61. ] |
| [14] | 秦恳, 唐国华, 李李, 等. 四川大学华西医院健康体检人群患亚临床甲状腺功能减退症的横断面调查[J]. 中国循证医学杂志, 2014, 14(4): 404–7. [ Qin K, Tang GH, Li L, et al. Subclinical hypothyroidism of health check-up population of West China Hospital, Sichuan University: A Cross-sectional study[J]. Zhongguo Xun Zheng Yi Xue Za Zhi, 2014, 14(4): 404–7. ] |
 2019, Vol. 46
2019, Vol. 46