文章信息
- 经皮椎体成形术治疗后壁缺失脊柱转移瘤的安全性和有效性
- Safety and Efficacy of Percutaneous Vertebroplasty on Spinal Metastases with Incomplete Posterior Wall
- 肿瘤防治研究, 2019, 46(7): 622-626
- Cancer Research on Prevention and Treatment, 2019, 46(7): 622-626
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2019.18.1791
- 收稿日期: 2019-02-11
- 修回日期: 2019-04-19
随着恶性肿瘤患者生存期延长,脊柱转移瘤患者人数逐年增加。对于椎体后壁完整、椎管未受累的患者,经皮椎体成形术能够有效缓解脊柱转移瘤患者的局部疼痛,增强脊柱的稳定性[1-5]。经皮椎体成形术相关严重并发症可以分为局部和全身两大类,前者由于骨水泥椎管内渗漏压迫脊髓或神经根,后者则由于骨水泥单体入血后造成广泛肺小血管栓塞。对于椎体后壁缺失,甚至硬膜受累的患者,上述严重并发症发生情况尚无详细的报道,其治疗效果及安全性文献报道较少[6-10]。
本研究回顾后壁缺失的脊柱转移瘤患者接受经皮椎体成形术治疗后疼痛和生活能力的改善情况,以及全身、局部并发症情况,分析经皮椎体成形术对此类患者的临床疗效和安全性。
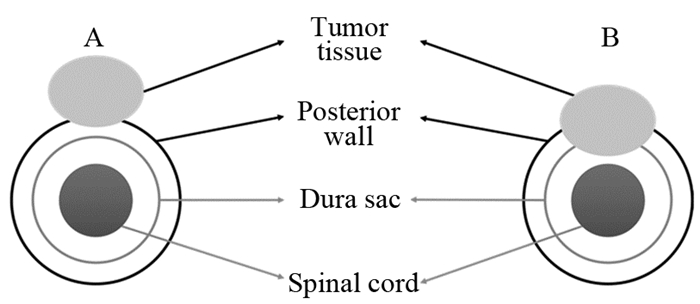
1 资料与方法 1.1 研究方案回顾我院2010年至2017年接受经皮椎体成形术治疗的患者资料,共106例脊柱转移瘤患者纳入本研究,共160节后壁缺失的椎体接受治疗。根据硬膜是否受侵犯将椎体分为两组:侵犯硬膜组和未侵犯硬膜组,见图 1。以病变最严重的椎体为依据,根据患者是否存在硬膜侵犯将患者同样分为两组。
|
| A: Without dural sac involvement; B: With dural sac involvement, no compression of spinal cord or nerve root 图 1 椎体后壁缺失示意图 Figure 1 Schematic diagram of vertebra with incomplete posterior wall |
入选标准:(1)恶性肿瘤病史,术前影像检查提示脊柱转移瘤;(2)无恶性肿瘤病史,术后病理证实脊柱转移瘤;(3)影像学检查显示在接受治疗的椎体中,至少一节椎体后壁缺失。排除标准:(1)血液系统恶性肿瘤;(2)肿瘤压迫脊髓或神经根引起临床症状。
对脊柱后壁缺失的脊柱转移瘤患者实施椎体成形术前,联合化疗科、放疗科、原发肿瘤科室、疼痛科、影像科医生共同讨论,适应证如下:(1)影像学检查提示肿瘤组织未压迫脊髓、神经根,且临床无脊髓、神经根相关症状;(2)保守治疗症状缓解不满意;(3)患者不耐受开放手术。本研究经我院伦理委员会批准实施。
1.2 术前临床资料查阅患者病历资料,记录患者性别、年龄、原发肿瘤病理类型、手术椎体数量、骨水泥注入量、水泥注入过程中血氧饱和度变化趋势、患者治疗前后VAS评分和巴氏量表情况(Barthel Index, BI)。查阅术后影像学资料,记录每节椎体骨水泥渗漏情况。
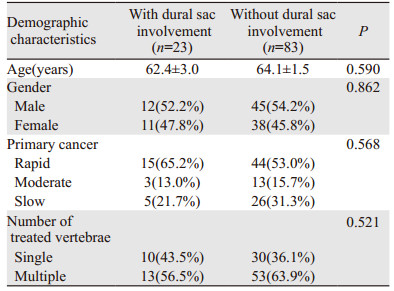
106例患者中,男57例,女49例,平均年龄(63.8±1.3)岁。根据Tomita评分标准,59例患者属于快速进展类型肿瘤,31例患者属于缓慢进展型,16例患者介于两者之间。66例患者实施多节段椎体成形手术,40例患者实施单节段椎体成形手术。术前VAS评分为7.0(6.0~9.0)分。83例患者无硬膜侵犯,23例患者有硬膜侵犯;两组患者在男女比例、肿瘤进展类型以及术前VAS评分间差异无统计学意义(P > 0.05),见表 1。
|
160节病变椎体中颈椎2节、上胸椎(T1-T6)33节、下胸椎(T7-T12)55节、腰椎67节、骶椎3节,两组间差异无统计学意义(P > 0.05),见表 2。
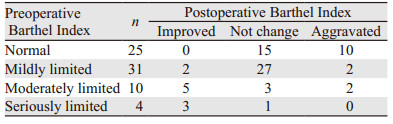
共70例患者接受巴氏量表分级评估日常生活能力,正常25例、轻度受限31例、中度受限10例、重度受限4例。
1.3 手术方法患者俯卧位进行手术。在C臂X射线机(SIEMENS公司,德国)的指导下进行穿刺针插入和骨水泥注射。局部麻醉(0.67%利多卡因和0.34%罗哌卡因)给药后,应用穿刺针(Kinetic公司,中国)经单侧或双侧椎弓根插入椎体的前三分之一。优先选择双侧置针,仅手术节段多且连续影响双侧置针时根据病变部位选择单侧置针,单侧置针水泥分布不满意时在对侧置针补充注入水泥。骨水泥(Tecres S.P.A.,中黏,意大利)混合后4 min,在“牙膏状”阶段缓慢注入椎体,以最大限度地减少外渗的风险。透视下见骨水泥椎管内渗漏或患者抱怨神经系统症状(局部压力增加)时立刻停止注射,观察症状变化,必要时给予地塞米松对症处理。
1.4 安全性和疗效评估采用VAS评分系统评估患者疼痛改善情况(0分代表无疼痛;10分代表难以忍受的疼痛);巴氏量表评估患者的日常生活能力改善情况,根据评分高低,将患者分为4组:生活自理100分;轻度功能障碍(61~99)分;中度功能障碍(41~60)分;重度功能障碍(0~40)分。术后VAS评分、巴氏量表均在患者出院时评估。
全身并发症:骨水泥注入期间血氧饱和度降至90%以下视为出现全身并发症,停止水泥注入并对症处理后仍不缓解视为严重并发症。局部并发症:出现局部骨水泥渗漏视为并发症,椎管渗漏视为严重并发症。
1.5 统计学方法数据结果用SPSS21.0统计软件进行分析,计量资料符合正态分布时采用均值±标准差(x±s)表示,不符合正态分布时采用中位数(四分位数)表示。两组数据比较前采用Shapiro-Wilk方法进行正态性检验,Levene检验方法进行方差齐性检验,满足条件时采用独立样本t检验;不满足条件时采用秩和检验。本研究样本量≥40,分类变量采用Pearson卡方或连续校正的卡方检验。P < 0.05为差异有统计学意义。
2 结果 2.1 患者术后疼痛、功能改善情况术后VAS评分3.0(2.0~3.0)分,下降5.0(4.0~ 5.0)分。两组患者VAS评分术后分别下降4.0(3.0,6.0)分和5.0(3.0~7.0)分,差异无统计学意义(P > 0.05)。93例患者术后VAS评分下降幅度大于3分,其中侵犯椎管组21例,未侵犯椎管组72例,两组间差异亦无统计学意义(P > 0.05),见表 3。
70例接受巴氏量表评估患者中,10例患者术后分级较术前提高,46例患者术后分级同术前,14例患者术后分级较术前下降。46例术后巴氏量表分级与术前相同患者中15例患者术前功能正常;31例患者术前功能轻度受限;14例术后巴氏量表分级下降中有10例患者术前日常生活能力正常,见表 4。术后巴氏量表分级改变在两组间差异无统计学意义(P > 0.05)。
106例患者术中骨水泥注入期间均未出现血氧饱和度下降至90%以下。
2.2.2 局部并发症160节接受治疗的后壁缺失的椎体中39节椎体(24.4%)发生骨水泥渗漏,其中32节椎体(20.0%)发生椎管外渗漏,7节椎体(4.4%)发生椎管内渗漏。所有患者术后均未出现骨水泥渗漏相关神经症状,典型病例见图 2~3。骨水泥渗漏在两组椎体中分布差异具有统计学意义(P=0.016),见表 5。

|
| A: preoperative X ray showed fracture of T11; B: preoperative MRI, sagittal showed multiple spinal metastasis; C: preoperative MRI, cross section showed incomplete posterior wall of T11; D: intraoperative image; E: postoperative CT showed no intraspinal bone cement leakage 图 2 典型病例1:62岁男性,前列腺癌 Figure 2 Typical case one: one 62-year-old male patient with prostate cancer |

|
| A: preoperative X ray showed fracture of L3; B: preoperative MRI, sagittal showed multiple spinal metastasis; C: preoperative MRI, cross section showed incomplete posterior wall of L3; D: postoperative CT showed that bone cement leaked into spinal canal through the incomplete posterior wall of vertebral body 图 3 典型病例2: 76岁男性,直肠腺癌 Figure 3 Typical case two: one 76-year-old male patient with rectal adenocarcinoma |
本组患者骨水泥渗漏率为24.4%,其中7例患者出现椎管内渗漏,渗漏率4.4%。骨水泥渗漏率低于Sun等[6]和Corcos等[11]报道的64%和55%。其原因与部分患者术后未行CT检查有关,应用X线片评估会低估骨水泥渗漏率。Bae等[12]回顾分析342例接受经皮椎体成形术治疗的脊柱转移瘤患者,指出椎体后壁缺失、甚至神经根性症状的出现并不影响手术疗效。但研究未对后壁缺失程度进行分级,亦未对骨水泥渗漏情况进行分析。本研究回顾性分析106例(160节)伴有椎体后壁缺失的脊柱转移瘤患者,术后VAS评分下降 > 3分患者93例(87.7%)。患者疼痛改善情况与Bae等的研究相同,且研究显示不同后壁缺失程度患者疼痛改善情况差异无统计学意义。70例接受日常生活能力评定的患者中,10例患者术后巴氏量表分级较术前提高,46例患者术后巴氏量表分级同术前。患者术后日常生活能力改善率较低,可能与巴氏量表不同分级间差距较大,量表分辨率低相关。
对于椎体后壁缺失的转移瘤患者来说,如何避免骨水泥沿后壁缺失处向椎管内渗漏,是至关重要的问题。Sun[6]、Appel[8]、Shimony[9]、Saliou[10]等分别对32例、51例、23例和50例(包含多发性骨髓瘤14例)伴有椎体后壁缺失或硬膜受压的脊柱转移瘤患者进行回顾分析,术后疗效满意,但研究样本量较少。其中,Sun等[6]报道椎管内渗漏率为15.1%,余下研究未对椎管内渗漏率进行报导,并且均未明确指出对如何避免骨水泥沿后壁缺失部位渗漏。
在骨水泥注入过程中,随着局部压力增大,骨水泥可能通过椎体后壁不完整薄弱部位向椎管内渗漏。为避免骨水泥沿后壁缺损部位渗漏,本研究穿刺点的选择更偏外,靠近横突和关节突移行区,穿刺针尽量进针至椎体中前1/3处。对于病灶主要位于一侧的患者,采取在相对健侧单侧进针,最大限度降低穿刺过程及骨水泥注入过程中对椎体后壁缺损部位的刺激[13]。研究均采用同一种中黏骨水泥,对骨水泥的工作时间有较好的把控,对于椎体后壁缺失严重的患者,适当延长骨水泥注射时间。术中应用1 ml注射器进行注入,根据注射阻力情况,每次推入0.1~0.2 ml。X线下连续监测骨水泥弥散情况,若出现向后方渗漏,则暂停注射30 s左右,待骨水泥适当凝固后再次注射,若水泥继续向后方渗漏则暂停注射。不强求达到骨水泥最大填充量,以骨水泥弥散情况为准,胸椎注入1~3 ml,腰椎注入2~5 ml[14]。
相比硬膜未受侵犯椎体,硬膜受侵犯椎体椎管内渗漏发生率高达14.3%,手术存在较高的骨水泥渗漏诱发神经症状的风险。上述结果与后纵韧带的完整性相关,结构完整的后纵韧带作为坚韧的结蹄组织,在椎体后壁骨性结构消失后能够提供一定的张力,从而防止骨水泥向后方薄弱区域渗漏入椎管。而随着后壁缺损加重,后纵韧带丧失其完整性,椎体后方压力降低,渗漏风险随之增加。同时,后壁缺损椎体在注入骨水泥过程中存在将实体瘤通过后方缺损部位推挤入椎管的风险。对于后壁缺失严重的高危患者,在穿刺完成后更换工作套筒,经工作套筒最大限度去除椎体内实性肿瘤组织,为骨水泥提供空间,降低骨水泥注入过程中产生的压力,降低骨水泥渗漏或肿瘤组织被推挤入椎管的风险[15-16]。
综上所述,本研究回顾性分析接受经皮椎体成形术治疗的106例(160节椎体)后壁缺失的脊柱转移瘤患者,术后患者疼痛缓解满意,功能得到一定程度改善,且无临床严重并发症发生。在熟练掌握椎体成形技术和严格把握手术适应证的前提下,应用经皮椎体成形术治疗后壁缺失的脊柱转移瘤患者具有良好的临床疗效和安全性。
作者贡献
崔云鹏、潘元星: 分析数据及撰写论文
米川、王冰: 分析统计结果及临床意义
林云飞: 收集数据
施学东: 研究设计及文章修改
| [1] | Xie P, Zhao Y, Li G. Efficacy of percutaneous vertebroplasty in patientswith painful vertebral metastases: a retrospective study in 47 cases[J]. Clin Neurol Neurosurg, 2015, 138: 157–161. DOI:10.1016/j.clineuro.2015.08.026 |
| [2] | Bao L, Jia P, Li J, et al. Percutaneous Vertebroplasty Relieves Pain in Cervical Spine Metastases[J]. Pain Res Manag, 2017, 2017: 3926318. |
| [3] | Tian QH, Sun XQ, Lu YY, et al. Percutaneous Vertebroplasty for Palliative Treatment of Painful Osteoblastic Spinal Metastases: A Single-Center Experience[J]. J Vasc Interv Radiol, 2016, 27(9): 1420–1424. DOI:10.1016/j.jvir.2016.04.033 |
| [4] | Zhang HT, Chen GD, Yang HL, et al. Percutaneous Kyphoplasty in the Treatment of Osteoblastic-Related Spinal Metastases[J]. Clin Spine Surg, 2016, 30(2): 80–84. |
| [5] | Berenson J, Pflugmacher R, Jarzem P, et al. Balloon kyphoplasty versus non-surgical fracture management for treatment of painful vertebral body compression fractures in patients with cancer: a multicentre, randomised controlled trial[J]. Lancet Oncol, 2011, 12(3): 225–235. DOI:10.1016/S1470-2045(11)70008-0 |
| [6] | Sun G, Jin P, Li M, et al. Percutaneous vertebroplasty for pain management in spinal metastasis with epidural involvement[J]. Technol Cancer Res Treat, 2011, 10(3): 267–274. DOI:10.7785/tcrt.2012.500202 |
| [7] | Hentschel SJ, Burton AW, Fourney DR, et al. Percutaneous vertebroplasty and kyphoplasty performed at a cancer center: refuting proposed contraindications[J]. J Neurosurg Spine, 2005, 2(4): 436–440. DOI:10.3171/spi.2005.2.4.0436 |
| [8] | Appel NB, Gilula LA. Percutaneous vertebroplasty in patients with spinal canal compromise[J]. AJR Am J Roentgenol, 2004, 182(4): 947–951. DOI:10.2214/ajr.182.4.1820947 |
| [9] | Shimony JS, Gilula LA, Zeller AJ, et al. Percutaneous vertebroplasty for malignant compression fractures with epidural involvement[J]. Radiology, 2004, 232(3): 846–853. DOI:10.1148/radiol.2323030353 |
| [10] | Saliou G, Kocheida el M, Lehmann P, et al. Percutaneous vertebroplasty for pain management in malignant fractures of the spine with epidural involvement[J]. Radiology, 2010, 254(3): 882–890. DOI:10.1148/radiol.09081698 |
| [11] | Corcos G, Dbjay J, Mastier C, et al. Cement Leakage in Percutaneous Vertebroplasty for Spinal Metastases: a retrospective evaluation of incidence and risk factors[J]. Spine(Phila Pa 1976), 2014, 39(5): E332–E338. DOI:10.1097/BRS.0000000000000134 |
| [12] | Bae JW, Gwak HS, Kim S, et al. Percutaneous vertebroplasty for patients with metastatic compression fractures of the thoracolumbar spine: clinical and radiological factors affecting functional outcomes[J]. Spine J, 2016, 16(3): 355–364. DOI:10.1016/j.spinee.2015.11.033 |
| [13] | Yan L, Jiang R, He B, et al. A Comparison between Unilateral Transverse Process-Pedicle and Bilateral Puncture Techniques in Percutaneous Kyphoplasty[J]. Spine(Phila Pa 1976), 2014, 39(26 Spec No.): B19–B26. |
| [14] | 许正伟, 贺宝荣, 郝定均, 等. 胸腰椎骨质疏松性骨折经皮椎体成形术后骨水泥渗漏的研究进展[J]. 中华骨科杂志, 2016, 36(17): 1142–1148. [ Xu ZW, He BR, Hao DJ, et al. Research advanced on bone cement leakage after percutaneous vertebroplasty for thoracolumbar osteoporotic fracture[J]. Zhonghua Gu Ke Za Zhi, 2016, 36(17): 1142–1148. DOI:10.3760/cma.j.issn.0253-2352.2016.17.011 ] |
| [15] | Gu YF, Li YD, Wu CG, et al. Safety and efficacy of percutaneous vertebroplasty and interventional tumor removal for metastatic spinal tumors and malignant vertebral compression fractures[J]. AJR Am J Roentgenol, 2014, 202(3): W298–305. DOI:10.2214/AJR.12.10497 |
| [16] | Gu YF, Tian QH, Li YD, et al. Percutaneous vertebroplasty and interventional tumor removal for malignant vertebral compression fractures and/or spinal metastatic tumor with epidural involvement: a prospective pilot study[J]. J Pain Res, 2017, 10: 211–218. DOI:10.2147/JPR.S122211 |
 2019, Vol. 46
2019, Vol. 46