文章信息
- 聚肌胞对活化早期T细胞PD-1表达的诱导及对黑色素瘤生长的抑制作用
- Polyinosinic-polycytidylic Acid Mediates PD-1 Expression in T Cells at Early Stage of Activation and Inhibits Melanoma Growth
- 肿瘤防治研究, 2019, 46(3): 222-226
- Cancer Research on Prevention and Treatment, 2019, 46(3): 222-226
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2019.18.1213
- 收稿日期: 2018-08-23
- 修回日期: 2018-11-07
肿瘤微环境可以通过多种机制导致免疫逃逸,其中程序性死亡受体1(PD-1)介导信号发挥关键作用。PD-1是一种Ⅰ型跨膜蛋白受体,表达于多种免疫细胞(包括活化的T细胞)表面,部分肿瘤细胞高表达PD-1配体PD-L1,PD-1与配体结合后诱导T细胞功能障碍,即T细胞衰竭,衰竭型T细胞无法合成IFN-γ。临床上广泛应用的抗PD-1治疗就是为了挽救衰竭型T细胞[1-3]。Tumeh等[4]指出抗PD-1治疗黑色素瘤有效的前提是治疗前肿瘤组织中存在能被PD-1信号调节的CD8+T细胞。然而,PD-1在T细胞活化后的哪个阶段开始表达并抑制T细胞功能?是否所有表达PD-1的T细胞都是衰竭型T细胞?这些问题仍不明确。因此,本课题聚焦T细胞的活化阶段,研究T细胞活化初期PD-1表达情况。
Poly I:C是合成的双链RNA类似物,为Toll样受体3(TLR3)配体,TLR3广泛分布于多种免疫细胞表面,包括树突状细胞和自然杀伤细胞等。Poly I:C与受体结合后能有效激活非特异性免疫系统并促进T细胞活化[5-6]。我们以黑色素瘤荷瘤小鼠为模型,研究发现Poly I:C可以有效促进T细胞活化; 同时,小鼠经OVA肽+Poly I:C免疫后7天,处于活化早期阶段的(仍在脾组织内,还未向靶器官迁移的)特异性CD8+T细胞表达PD-1,这部分细胞仍然具有功能,可以合成T细胞功能性标志IFN-γ。
1 材料与方法 1.1 动物、试剂、材料与仪器健康清洁级6~8周龄雌性C57BL/6小鼠购于上海斯莱克公司。B16F10小鼠黑色素瘤细胞购于中科院上海细胞库。鸡卵清蛋白(OVA257-264)抗原肽(OVA肽):SIINFEKL合成于上海淘普生物技术公司。CD8体内敲除抗体购于美国InvivoMab公司。Poly I:C购于美国InvivoGen公司。FITC标记的抗鼠CD3抗体、APC标记的抗鼠CD3抗体、PE标记的抗鼠IFN-γ抗体、Percp cy5.5标记的抗鼠CD8抗体、APC标记的抗鼠CD4抗体和FITC标记的抗鼠PD-1抗体购于美国eBioscience公司。胞内染色试剂盒和PMA购于美国BD公司。PBS磷酸盐缓冲液(粉剂)购于北京鼎国昌盛生物技术有限公司; DMEM高糖培养基购于美国Ionomycin公司。Iomomycin购于爱必信公司; 仪器:A6流式细胞仪,37℃恒温培养箱。
1.2 方法 1.2.1 小鼠免疫干预 1.2.1.1 Poly I:C对非特异性T细胞活化的影响将6只体重相近的6~8周龄C57BL/6小鼠随机分成两组:对照组和实验组。对照组小鼠腹腔注射200 μl PBS,实验组每只小鼠腹腔注射50 μg Poly I:C(Poly I:C溶解于总量为200 μl的PBS中)。7天后分别处死各组小鼠,取得脾组织。
1.2.1.2 Poly I:C对特异性CD8+T细胞(OVA257-264)活化的影响将12只体重相近的6~8周龄C57BL/6小鼠随机分成四组:对照组、OVA肽组、Poly I:C组和OVA肽+Poly I:C组。对照组:小鼠腹腔注射200 μl PBS; OVA肽组:每只小鼠腹腔注射200 μg OVA肽(肽段溶解于总量为200 μl的PBS中); Poly I:C组:每只小鼠腹腔注射100 μg Poly I:C(Poly I:C溶解于总量为200 μl的PBS中); OVA肽+Poly I:C组:每只小鼠腹腔注射100 μg Poly I:C+200 μg OVA肽(溶解于总量为200 μl的PBS中)。7天后分别处死各组小鼠,取得脾组织。
1.2.2 T细胞刺激活化研磨小鼠脾组织取得脾细胞混悬液,红细胞裂解液去除红细胞,300目滤网过滤,得到脾组织白细胞悬液; 离心后重悬细胞,使其浓度为1×107个/毫升,接种于96孔板,每孔100 μl(1×106个细胞)。(1)研究非特异性T细胞:每孔加入PMA、Ionomycin刺激T细胞,PMA终浓度为50 ng/ml,Ionomycin终浓度为1 μg/ml; 并加入golgi plug 4微升/孔。96孔板放入细胞培养箱孵育12 h。(2)研究特异性CD8+T细胞(OVA)活化:每孔加入OVA肽刺激脾细胞,OVA肽终浓度为10 μg/ml; 并加入golgi plug 4微升/孔。96孔板放入细胞培养箱孵育12 h。
1.2.3 细胞表面及胞内染色取上述刺激活化的T细胞,以CD3、CD8、CD4、PD-1等抗体进行细胞表面染色; 利用BD公司Cytofix/Cytoperm冰上避光孵育30 min,破细胞膜; 加入IFN-γ-PE抗体进行细胞内染色,冰上避光孵育30 min。染色后采用A6流式细胞仪与Flowjo 7.6.1软件分析染色结果。IFN-γ+CD3+CD8+细胞即活化的CD8+T细胞; IFN-γ+CD3+CD4+细胞为活化的CD4+T细胞。
1.2.4 荷黑色素瘤小鼠免疫干预取对数长期B16F10细胞,接种在20只C57BL/6雌性小鼠的右背外侧,每只接种5×105个B16F10细胞。10天后肿瘤生长至肉眼可见时,将20只荷瘤小鼠随机分成四组,分别为PBS组、CD8敲除组、Poly I:C组和Poly I:C +CD8敲除组。Poly I:C每隔5天腹腔注射一次,每只50微克/次,共注射3次。对照组在相应时间点腹腔注射等体积PBS。CD8敲除抗体分别在Poly I:C注射前2天、前1天及Poly I:C注射5天后进行腹腔注射,每只500微克/次。从第一次注射Poly I:C开始,每3天记录各组小鼠肿瘤的长径(L)和与之垂直的短径(W),并计算肿瘤体积(V=0.52×L×W2),当对照组小鼠肿瘤体积超过4 000 mm3时终止荷瘤实验。
1.3 统计学方法所有实验均独立重复3次。采用GraphPad Prism 5.0统计学软件进行数据处理。t检验、Two-way ANOVA进行统计学分析,P < 0.05为差异有统计学意义。
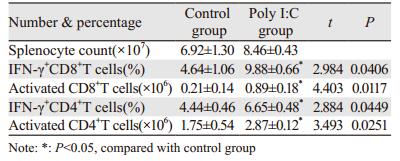
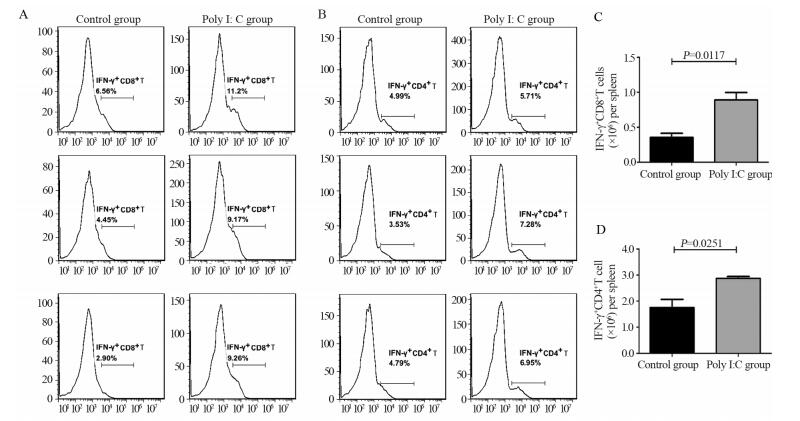
2 结果 2.1 Poly I:C促进小鼠非特异性T细胞活化脾细胞经PMA/Ionomycin刺激后,Poly I:C组活化的CD8+与CD4+T细胞百分比相对于对照组显著升高,见表 1、图 1A~B; Poly I:C组活化的CD8+与CD4+T细胞平均值也较对照组明显增加,见表 1、图 1C~D。
|
|
| A: gating on CD3+CD8+cells, the percentage of IFN-γ+CD8+T cells was analyzed; B: gating on CD3+CD4+cells, the percentage of IFN-γ+CD4+T cells was analyzed; C: the average number of IFN-γ+CD8+T cells per spleen in each group; D: IFN-γ+CD4+T cell count per spleen in each group 图 1 Poly I:C促进PMA/ionomycin介导的非特异性T细胞活化 Figure 1 Poly I:C promoted PMA/ionomycin-mediated activation of nonspecific T cells |
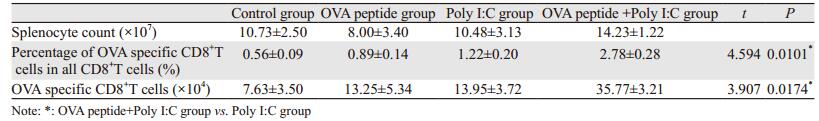
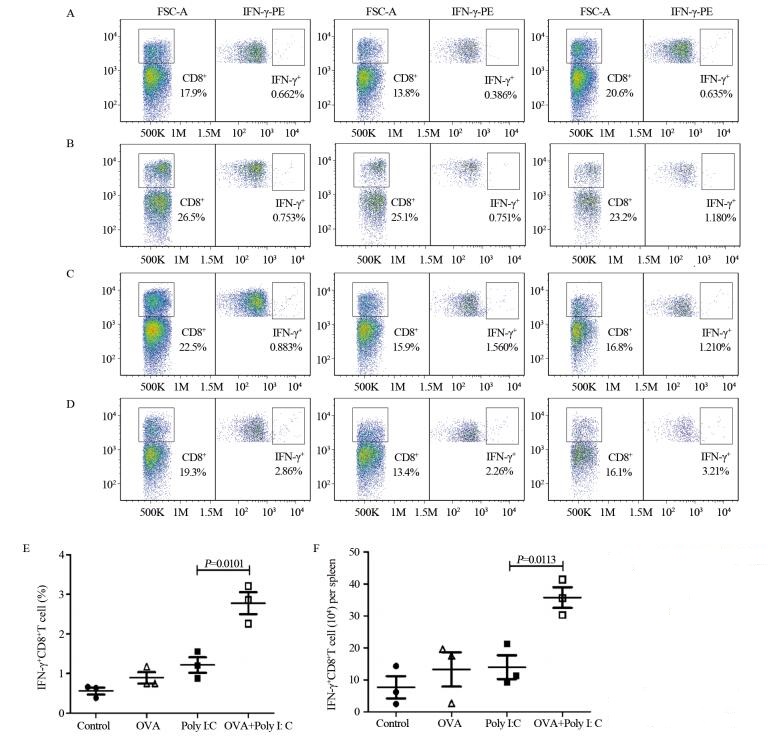
取对照组、OVA肽组、Poly I:C组、OVA肽+Poly I:C组的脾细胞,加入OVA肽段刺激,通过细胞内IFN-γ染色检测初次活化的OVA特异性CD8+T细胞数(IFN-γ+)。与Poly I:C组相比,OVA肽+Poly I:C组OVA特异性CD8+T显著增加,见表 2、图 2。
|
|
| 图 2 Poly I:C促进OVA特异性CD8+T细胞活化 Figure 2 Poly I:C promoted activation of OVA specific CD8+T cells |
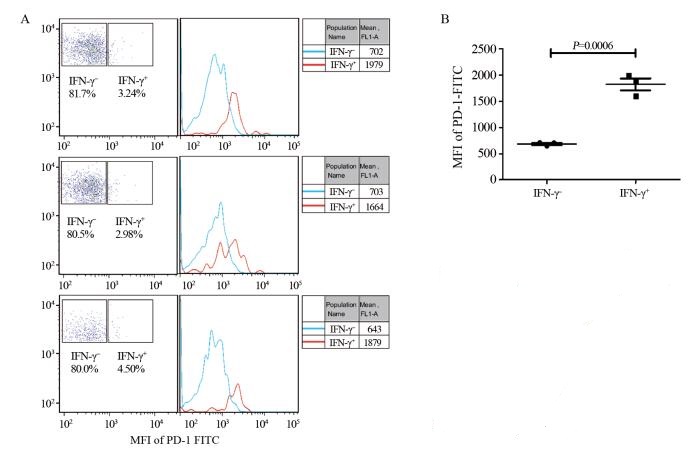
取OVA肽+Poly I:C组的脾细胞,加入OVA肽段刺激,检测初次活化的OVA特异性CD8+T细胞(IFN-γ+)与非活化的CD8+T细胞(IFN-γ-)表面PD-1表达差异。结果显示:IFN-γ+CD8+T细胞高表达PD-1,见图 3。这一结果说明在OVA肽+Poly I:C免疫后7天,还在脾组织内,尚未向靶器官迁移的特异性CD8+T细胞已经开始表达PD-1。
|
| A: gate on IFN-γ+ and IFN-γ- CD8+T cells, comparing mean fluroscent intensity (MFI) of PD-1 between these two cell populations; B: MFI of PD-1-FITC in each group 图 3 活化的OVA特异性CD8+T细胞(IFN-γ+)与非活化的CD8+T细胞(IFN-γ-)之间PD-1表达差异 Figure 3 Difference of PD-1 expression between activated OVA-specific CD8+T cells (IFN-γ+) and non-activated CD8+T cells (IFN-γ-) |
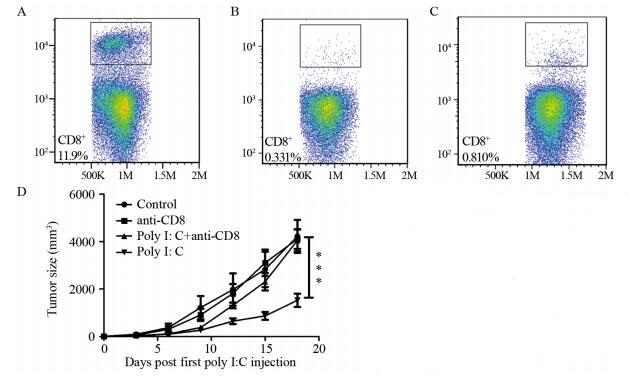
给予荷黑色素瘤小鼠PBS、CD8敲除、Poly I:C与CD8敲除、单用Poly I:C等方式干预,四组荷瘤小鼠肿瘤生长差异有统计学意义(F= 17.116, P < 0.0001),见图 4。与对照组相比,Poly I:C组小鼠黑色素瘤生长明显减慢(F=7.8353, P=0.0243); 经CD8敲除后,Poly I:C的抗肿瘤作用被明显削弱(即Poly I:C+CD8敲除组vs. Poly I:C组:F=7.3425, P=0.0285)。
|
| A-C: in CD8 knockout group, blood CD8+ cells were detected at different time point; A: before CD8 knockout, CD8+ cells in mice blood; B: 4 days after Poly I:C immunization, CD8+ cells in mice blood; C: 8 days after Poly I:C immunization, CD8+ cells in mice blood; D: after immunization with PBS, Poly I:C, CD8 knockout antibody or Poly I:C+CD8 knockout, tumor size in different groups was measured. (***: P < 0.0001) 图 4 Poly I:C显著抑制荷黑色素瘤小鼠肿瘤生长 Figure 4 Poly I:C significantly inhibited tumor growth of melanoma-bearing mice |
PD-1信号在T细胞衰竭过程中发挥重要作用。动物实验显示:肿瘤组织中大多数T细胞都是衰竭型T细胞,无法合成IFN-γ; 阻断PD-1/PD-L1信号,可以抑制T细胞衰竭,促进部分肿瘤浸润T细胞合成IFN-γ[7];因此,PD-1是T细胞衰竭的标志。然而, 也有学者发现患者体内可识别自身肿瘤抗原的T细胞都表达PD-1,指出PD-1表达是预示T细胞能产生抗肿瘤免疫的标志[8-9]。考虑到PD-1表达可能具有不同效应,非常有必要研究PD-1是在T细胞活化后的哪个阶段开始表达及该阶段的T细胞功能。要解决上述问题,首先需要活化T细胞,并探索PD-1表达与T细胞功能性分子IFN-γ之间的关系。
病原微生物介导的宿主T细胞活化机制为解决这一问题提供了新思路。当机体遇到免疫原性强的病原体感染时,可以快速有效激活天然免疫系统,促进特异性免疫应答,这一过程中,病原体相关分子识别模式(PAMPs)发挥关键作用。PAMPs指病原微生物所含有的某些高度保守的分子,这些分子可以和吞噬细胞(如树突状细胞、巨噬细胞等)表面的模式识别受体(PRR)结合,激活非特异免疫系统并提呈抗原,最终促进T细胞活化。PRR包括甘露糖受体、清道夫受体、Toll样受体(TLR)等; Poly I:C是TLR3配体,有研究报道Poly I:C可以促进树突状细胞表达CD80、CD86[10-11]。由于抗原提呈细胞表面CD80/CD86可以与T细胞表面CD28结合并为T细胞活化提供第二信号,因此Poly I:C具有促进T细胞活化的潜能,我们的实验结果也证实Poly I:C可以促进脾脏内特异性及非特异性T细胞活化。
我们的研究显示Poly I:C免疫后7天,脾组织内初次活化的特异性CD8+T细胞可以合成IFN-γ并高表达PD-1,且Poly I:C的抗肿瘤效应和CD8+T细胞有关。这一发现说明:(1)PD-1表达是早期事件,初次活化的、仍在外周淋巴器官内未向靶器官迁移的CD8+T细胞就已经开始表达PD-1;(2)脾组织内表达PD-1的CD8+T细胞是功能性的,可以合成IFN-γ,且Poly I:C的抗肿瘤效应与活化的CD8+T细胞有关; (3)进一步证实,在CD8+T细胞活化的不同阶段,PD-1表达具有不同的效应; 外周淋巴器官内可以合成IFN-γ的CD8+T细胞高表达PD-1,说明PD-1也可以是T细胞的功能性标志。
作者贡献
陈婷:实施具体实验及撰写文章
林万尊、郑伟丽:数据统计学分析、校对文章
谢贤和:对课题思路提出建议及指导文章写作
王自力:实验设计、提出文章思路及校对、项目负责人
| [1] | Pauken KE, Wherry EJ. Overcoming T cell exhaustion in infection and cancer[J]. Trends Immunol, 2015, 36(4): 265–76. DOI:10.1016/j.it.2015.02.008 |
| [2] | Topalian SL, Hodi FS, Brahmer JR, et al. Safety, activity, and immune correlates of anti-PD-1 antibody in cancer[J]. N Engl J Med, 2012, 366(26): 2443–54. DOI:10.1056/NEJMoa1200690 |
| [3] | Chen L, Han X. Anti-PD-1/PD-L1 therapy of human cancer: past, present, and future[J]. J Clin Invest, 2015, 125(9): 3384–91. DOI:10.1172/JCI80011 |
| [4] | Tumeh PC, Harview CL, Yearley JH, et al. PD-1 blockade induces responses by inhibiting adaptive immune resistance[J]. Nature, 2014, 515(7528): 568–71. DOI:10.1038/nature13954 |
| [5] | Salem ML, Diaz-Montero CM, El-Naggar SA, et al. The TLR3 agonist poly(I:C) targets CD8+ T cells and augments their antigen-specific responses upon their adoptive transfer into naïve recipient mice[J]. Vaccine, 2009, 27(4): 549–57. DOI:10.1016/j.vaccine.2008.11.013 |
| [6] | Ngoi SM, Tovey MG, Vella AT. Targeting Poly I:C to the TLR3-independent pathway boosts effector CD8 T cell differentiation through IFNα/β[J]. J Immunol, 2008, 181(11): 7670–80. DOI:10.4049/jimmunol.181.11.7670 |
| [7] | Ngiow SF, Young A, Jacquelot N, et al. A Threshold Level of Intratumor CD8+ T-cell PD1 Expression Dictates Therapeutic Response to Anti-PD1[J]. Cancer Res, 2015, 75(18): 3800–11. DOI:10.1158/0008-5472.CAN-15-1082 |
| [8] | Inozume T, Hanada K, Wang QJ, et al. Selection of CD8+PD-1+ lymphocytes in fresh human melanomas enriches for tumor-reactive T cells[J]. J Immunother, 2010, 33(9): 956–64. DOI:10.1097/CJI.0b013e3181fad2b0 |
| [9] | Gros A, Robbins PF, Yao X, et al. PD-1 identifies the patient-specific CD8+ tumor-reactive repertoire infiltrating human tumors[J]. J Clin Invest, 2014, 124(5): 2246–59. DOI:10.1172/JCI73639 |
| [10] | Forte G, Rega A, Morello S, et al. Polyinosinic-polycytidylic acid acid limits tumor outgrowth in a mouse model of metastatic lung cancer[J]. J Immunol, 2012, 188(11): 5357–64. DOI:10.4049/jimmunol.1103811 |
| [11] | Truxova I, Pokorna K, Kloudova K, et al. Day 3 Poly (I:C)-activated dendritic cells generated in CellGro for use in cancer immunotherapy trials are fully comparable to standard Day 5 DCs[J]. Immunol Lett, 2014, 160(1): 39–49. DOI:10.1016/j.imlet.2014.03.010 |
 2019, Vol. 46
2019, Vol. 46


