文章信息
- 下颌牙龈原发性皮脂腺癌1例报道并文献复习
- Primary Sebaceous Carcinoma of Mandibular Gingiva: A Case Report and Literature Review
- 肿瘤防治研究, 2019, 46(1): 93-95
- Cancer Research on Prevention and Treatment, 2019, 46(1): 93-95
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2019.18.1195
- 收稿日期: 2018-08-21
- 修回日期: 2018-10-15
2. 261021 潍坊,中国人民解放军第八十九医院口腔科
2. Department ofStomatology, 89th Hospital of PLA, Weifang 261021, China
口腔原发性皮脂腺癌(sebaceous carcinoma, SC)是一种极其少见的恶性肿瘤,检索国内外文献报道仅10余例,其主要发生于颊黏膜[1-5],其次为口底、唇黏膜、舌和上颌牙龈[6-11],仅见1例报道发生于下颌牙龈黏膜[12]。本文现报道1例发生于下颌牙龈黏膜的原发性SC,回顾性分析其临床病理特征,并复习相关文献,旨在提高对该疾病的认识,有利于正确诊断。
1 资料与方法 1.1 临床资料患者男,47岁。因下颌前牙区牙龈肿胀3年余,加重半年入院。2009年因下颌前牙松动到当地医院拔除后行活动假牙修复,2015年自觉下前牙区牙龈肿胀不适伴出血,曾抗炎治疗,近半年症状加重,门诊以“下颌肿物”收入院。下颌淋巴结未见明显肿大,全身体检未见阳性体征。专科检查:颌面部尚对称,颏部软组织肿胀,质地韧。张口度正常,张口约3.7 cm,下颌前牙区唇侧牙龈黏膜增生、肿胀(33~43对应牙齿),触之较韧,未见溃疡及糜烂,和正常牙龈无明显界限。31、41牙齿缺失,32、42牙齿Ⅲ度松动,33、43牙齿Ⅰ度松动,全口牙牙周状况较差,口腔卫生状况欠佳。颌骨CT示“下颌骨颏部前方病变伴颏部骨质改变,可见低密度影像,波及33~43牙齿”。入院后完善术前检查,将下颌骨双侧颏孔间下颌骨连带肿物完整摘除,并行带血管的腓骨肌皮瓣移植修复术。
1.2 病理学特征 1.2.1 眼观覆牙龈黏膜的颌骨组织一段,大小4 cm×3.5 cm×2 cm,表面见牙齿2枚,切面见一大小3.5 cm×3.2 cm×2 cm灰白色肿物,破坏骨组织,质中,与周围组织界限不清,两端切缘骨皮质完整。并见少许颊黏膜相连,大小约为1.5 cm×1 cm×0.3 cm。
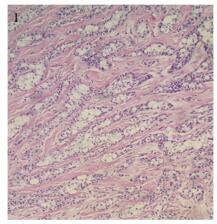
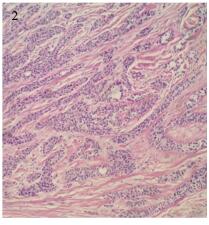
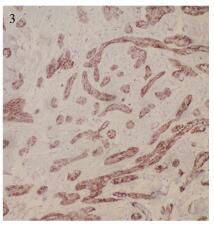
1.2.2 镜检低倍镜:肿瘤位于黏膜固有层内,呈大小不等的小叶状、条索状排列,浸润性生长,局部侵犯黏膜上皮及颊侧黏膜下横纹肌,间质纤维结缔组织增生。高倍镜:肿瘤为两种明显不同的形态,小叶状排列的肿瘤中心为皮脂腺样细胞,细胞大而浅染,界限清楚,胞质丰富、淡染、多泡或空泡状,核偏位,有明显的嗜酸性核仁;小叶周围有1~2层小而深染细胞,胞质嗜双色性,较少,胞核偏大,为基底层细胞或生发细胞,见图 1。条索状排列的肿瘤两型细胞区分不明显,由均一的生发细胞组成,局灶偶见胞质空亮、泡沫状胞质的细胞,部分区域周围细胞呈栅栏状排列,形如基底细胞癌,见图 2。局部可见两者移行过渡,组织化学:肿瘤细胞PAS和阿尔辛蓝染色均阴性。免疫表型:肿瘤细胞CK7、EMA、PMS-2、MLH-1、MSH-2及MSH-6均阳性,见图 3。AR、CK5/6、P63、CD10、S100、HMB45、MelanA均阴性。
|
| The tumor had a lobulated appearance. It was predominantly composed of round or polygonal large pale cells i.e. mature sebocytes (mainly located in the center and small primitive germinal cells (HE ×200) 图 1 皮脂腺分化 Figure 1 Differentiation of sebaceous gland |
|
| Tumour demonstrated basaloid pattern, composed of homogeneous germinal cells and less mature sebocytes with clear cytolymph and spumescent cytoplasms (HE ×200) 图 2 基底细胞癌样 Figure 2 Pattern of basal cell carcinoma |
|
| Immunohistochemical staining for EMA indicated cytoplasmic and membrane reactivity in the tumor cells (Envision ×200) 图 3 肿瘤免疫组织化学检测结果 Figure 3 Immunohistochemical image of tumour |
SC是一种罕见的皮肤恶性肿瘤,约3/4来源于眼周的皮脂腺,其次为头颈部,包括涎腺。过去SC分为两种类型:位于眼周的侵袭性SC和眼部以外的低侵袭性SC,近年来认识到两者具有相似的生物学行为。另外发生皮脂腺肿瘤时应注意进行全面体检,排除内脏恶性肿瘤,以免遗漏Torre-Muir综合征的诊断。复习文献发现发生于口腔黏膜的皮脂腺癌,未见与Muir-Torre综合征有关,本例免疫组织化学检测DNA错配基因(MMR)修复蛋白(PMS-2, MLH-1, MSH-2及MSH-6)均为阳性,提示无MMR基因胚系突变,可排除Muir-Torre综合征。而口腔原发性SC可能来源于异位的皮脂腺,即Fordyce斑,多位于唇红缘、口角或颊黏膜内。国内外文献报道仅10余例,而发生于牙龈黏膜的SC更为罕见。
2.1 临床特征复习相关文献,口腔内原发SC发病年龄多为60~80岁,中位年龄60.2岁,最小11岁[3]。男女之比为8:2,男性明显多于女性。5例位于颊黏膜[1-5],2例位于口底[6],2例位于上颌牙龈[10],1例位于上唇黏膜[8],1例位于舌部[9],国内有1例报道位于下颌牙龈[12],未见报道与Torre-Muir综合征相关。肿物最大径为1.5 cm~4.8 cm。本例为男性,年龄为47岁,位于下颌牙龈,最大径为3.5 cm,侵犯下颌骨。
2.2 病理特征(1)组织学:皮脂腺癌传统组织学分为五种亚型,即皮脂腺分化型、鳞状细胞型、基底细胞型、腺型、梭形细胞型,后四种统称为变异型,即非皮脂腺分化型[13]。皮脂腺分化型肿瘤组织呈大小不等的小叶状或巢状结构,由两种细胞组成,一种是含有丰富空泡样胞质的皮脂腺细胞,位于小叶中央,另一种是分布在外周较小的卵圆形、胞质较少的生发细胞。非皮脂腺分化型癌组织呈巢团状、条索样或弥漫片层状排列,异质性明显,多样性分化。部分呈栅栏状排列,形如基底细胞癌;部分发生角化,出现鳞状细胞癌成分,并形成微囊,提示皮脂腺导管方向分化。有的具有腺管状或者筛孔样结构,有的甚至呈梭形细胞或肉瘤样,细胞较幼稚,呈梭形或卵圆形,分化越差,胞质包含皮脂成分越少,有的甚至几乎见不到胞质空泡,而核异型性明显,核分裂较多,可见核仁,出现奇异性瘤细胞包括多核瘤巨细胞等,但常见胞质空泡样皮脂腺分化细胞。本例镜下可见明显的两种组织学形态,一是典型的分化型,二是基底细胞型,细胞巢内可见空泡状皮脂腺分化的细胞。(2)组织化学:肿瘤细胞富含脂质,冷冻切片中细胞质油红O或苏丹黑染色阳性,有助于鉴别诊断[8];但在石蜡切片制作过程中,脂质已溶解,糖原和黏液染色阴性,可考虑诊断皮脂腺癌。本例肿瘤细胞胞质PAS和阿辛蓝染色阴性,有助于皮脂腺癌的诊断。(3)免疫组织化学:上皮性标记如CK、EMA在皮脂腺癌中阳性表达[13],雄激素受体(AR)也呈阳性表达[14]。上述标记阳性表达可用于皮脂腺癌的诊断与鉴别诊断。本例EMA阳性表达,但AR阴性表达,可能与肿瘤的异质性有一定的关系。
2.3 鉴别诊断原发于皮肤的皮脂腺癌需与基底细胞癌、鳞状细胞癌、恶性黑色素瘤等鉴别,而发生于口腔黏膜的皮脂腺癌应与具有透明细胞形态的肿瘤鉴别,包括涎腺来源的肿瘤。(1)透明细胞型鳞状细胞癌,一般可见典型的鳞状细胞癌的区域,有单个细胞内角化及角化珠,部分可见细胞间桥。透明细胞的存在一般是糖原堆积的结果,PAS染色阳性可协助鉴别。(2)黏液表皮样癌,镜下可见典型黏液表皮样癌的结构,多为囊性,囊腔内衬黏液细胞和中间型细胞及少许的表皮样细胞,阿辛蓝染色阳性。肿瘤中可出现富含糖原的透明细胞,PAS染色阳性。(3)气球状细胞黑色素瘤,细胞呈气球样,含有丰富的嗜酸性或透明状胞质,细胞异型性明显,核分裂活跃,免疫组织化学S100、HMB45和MelanA阳性有助于诊断。(4)非特指型涎腺透明细胞癌,肿瘤由单一的胞质透明的多边形细胞排列成片状、巢状或条索状,无生发细胞和泡沫样胞质的皮脂腺细胞分化。免疫组织化学常弥漫表达PCK,大多数表达p63,而肌上皮标记Calponin、S-100、SMA等常为阴性。(5)肌上皮癌,具有特征性的多叶状结构,肿瘤细胞常为梭形、星状、浆细胞样或者偶尔有胞质空泡状印戒样黏液细胞,罕见情况下有单一的肌上皮特征的透明细胞组成,免疫组织化学肌上皮标记(SMA、GFAP、CD10、Calponin和SMMNC)阳性有助于诊断。
2.4 预后皮脂腺癌通常是局部浸润的低度恶性肿瘤, 有时发生区域淋巴结和远处转移。复习文献,3例有区域淋巴结转移[3],2例有肺转移[9],其中1例除肺转移外,还转移至大腿及臀部的皮下组织[11]。1例除发生区域淋巴结转移外,累及颌下腺[3],1例发生于口底的皮脂腺癌,侵犯下颌骨即咀嚼肌[7]。随访时间1~6年,只有1例有肺和淋巴结转移的患者术后1.5年死亡[9],1例肺和皮肤的患者术后随访1年带瘤生存[11],其余均为无瘤生存。本例术后随访3月,无复发及转移,但需长期随访。
发生于口腔黏膜的SC病例有限,与预后有关的因素不完全明了,外科手术切除是主要的治疗方式,若有淋巴结或肺转移,当辅以必要的化疗或放疗[7],并需要长期随访。
作者贡献
王美红:取材及病理报告初审;马建辉:提供临床病史;王涛:病理报告审核;靳玲燕、杨楠:病理、组织包埋及制片
| [1] | Gomes CC, Lacerda JC, Pimenta FJ, et al. Intraoral sebaceous carcinoma[J]. Eur Arch Otorhinolaryngol, 2007, 264(7): 829–32. DOI:10.1007/s00405-007-0248-6 |
| [2] | Liu CJ, Chang KW, Chang RC. Sebaceous carcinoma of the buccal mucosa. Report of a case[J]. Int J Oral Maxillofac Surg, 1997, 26(4): 293–4. DOI:10.1016/S0901-5027(97)80873-9 |
| [3] | Abuzeid M, Gangopadhyay K, Rayappa CS, et al. Intraoral sebaceous carcinoma[J]. J Laryngol Otol, 1996, 110(5): 500–2. |
| [4] | Li TJ, Kitano M, Mukai H, et al. Oral sebaceous carcinoma: report of a case[J]. J Oral Maxillofac Surg, 1997, 55(7): 751–4. DOI:10.1016/S0278-2391(97)90592-9 |
| [5] | Wang H, Yao J, Solomon M, et al. Sebaceous carcinoma of the oral cavity: a case report and review of the literature[J]. Oral Surg Oral Med Oral Pathol Oral Radiol Endod, 2010, 110(2): e37–40. DOI:10.1016/j.tripleo.2010.04.027 |
| [6] | Handschel J, Herbst H, Brand B, et al. Introral sebaceous carcinoma[J]. Br J Oral Maxillofac Surg, 2003, 41(2): 84–7. DOI:10.1016/S0266-4356(03)00036-6 |
| [7] | Gomes CC, Lacerda JC, Pimenta FJ, et al. Intraoral sebaceous carcinoma[J]. Eur Arch Otorhinolargngol, 2007, 264(7): 829–32. DOI:10.1007/s00405-007-0248-6 |
| [8] | Alawi F, Siddiqui A. Sebaceous carcinoma of the oral mucosa: case report and review of the literature[J]. Oral Surg Oral Med Oral Pathol Oral Radiol Endod, 2005, 99(1): 79–84. DOI:10.1016/j.tripleo.2004.05.007 |
| [9] | Oshiro H, Iwai T, Hirota M, et al. Primary sebaceous carcinoma of the tongue[J]. Med Mol Morphol, 2010, 43(4): 246–52. DOI:10.1007/s00795-010-0521-4 |
| [10] | Wetzel S, Pacelli P, Reich R, et al. Sebaceous carcinoma of the maxillary gingival: First reported case involving the gingiva[J]. Oral Surg Oral Med Oral Pathol Oral Radiol, 2015, 120(1): e1–3. DOI:10.1016/j.oooo.2014.10.018 |
| [11] | Rowe ME, Khorsandi AS, Urken GR, et al. Intraoral sebaceous carcinoma metastatic to the lung and subcutis: Case report and discussion of the literature[J]. Head Neck, 2016, 38(1): E20–4. DOI:10.1002/hed.24091 |
| [12] | 裴婧, 卓夏阳, 贾云香. 口腔黏膜皮脂腺癌1例报道并文献复习[J]. 实用口腔医学杂志, 2010, 26(5): 688–9. [ Pei J, Zhuo XY, Jia YX. A case report of intraoral sebaceous carcinoma and review of the literatures[J]. Shi Yong Kou Qiang Yi Xue Za Zhi, 2010, 26(5): 688–9. DOI:10.3969/j.issn.1001-3733.2010.05.036 ] |
| [13] | Prieto-Granada C, Rodriguez-Waitkus P. Sebaceous Carcinoma of the Eyelid[J]. Cancer Control, 2016, 23(2): 126–32. DOI:10.1177/107327481602300206 |
| [14] | Sramek B, Lisle A, Loy T. Immunohistochemistry in ocular carcinomas[J]. J Cutan Pathol, 2008, 35(7): 641–6. DOI:10.1111/j.1600-0560.2007.00871.x |
 2019, Vol. 46
2019, Vol. 46


