文章信息
- 维莫非尼在BRAF突变的肢端和黏膜型黑色素瘤患者中的有效性和安全性分析
- Efficacy and Safety of Vemurafenib in Acral and Mucosal Melanoma Patients with BRAF Gene Mutation
- 肿瘤防治研究, 2018, 45(11): 879-882
- Cancer Research on Prevention and Treatment, 2018, 45(11): 879-882
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2018.18.0250
- 收稿日期: 2018-02-26
- 修回日期: 2018-07-17
黑色素瘤是常见的恶性肿瘤之一,虽然患病人数相对较低,但是发病率增长迅速(3%~5%)且病死率较高[1]。近年来,免疫治疗药物及BRAF/MEK抑制剂等靶向药物相继出现[2-4],打破了晚期黑色素瘤无药可医的僵局。BRAF基因突变是黑色素瘤的独立预后因素[5],维莫非尼作为被批准用于治疗BRAF基因突变患者[6]的靶向药物之一,使患者的生存提高了50%以上[3, 7]。但是现有的临床数据均来自欧美国家的相关研究,欧美国家黑色素瘤的主要亚型为皮肤型,发病比例在95%以上[8],肢端和黏膜型黑色素瘤的发病比例在欧美国家仅为1%~5%[9-10]。而在亚洲人群中,肢端和黏膜型作为主要类型,其发病比例在60%以上[5, 11]。目前维莫非尼在中国仅有探索药代动力学和疗效的Ⅰ期临床试验,已有的一项回顾性研究[12]初步探究了BRAF抑制剂的效果,但由于使用了多种BRAF抑制剂,可能存在试验药物不同而引起的偏倚。基于此,本研究尝试在更长时间随访的基础上,探索维莫非尼在中国肢端和黏膜型黑色素瘤患者中的有效性和安全性,以期获得真实准确的临床数据,为维莫非尼在该类患者中的应用提供证据。
1 资料与方法 1.1 临床资料回顾性分析了2011年1月—2016年1月在北京大学肿瘤医院确诊为BRAF基因突变的肢端或黏膜型黑色素瘤住院、并接受维莫非尼治疗(推荐剂量:960 mg,2次/日)患者的临床资料,包括病理、基因检测、治疗、随访相关的数据,随访数据截至2017年1月,所有患者均出现死亡终点。评估指标包括总生存期(overall survival, OS)、无进展生存期(progression free survival, PFS)、疾病控制率(disease control rate, DCR)。按照RECIST version 1.1对肿瘤应答情况进行评估。
1.2 统计学方法对于分类变量利用频率和百分比进行描述,采用Fisher精确概率法进行组间比较;对于连续变量采取均数±标准差或中位数(四分位数)描述,利用t检验进行组间比较。利用Kaplan-Meier方法进行生存曲线的分析,组间比较采取Log rank检验。检验水准为α=0.05,统计分析过程在STATA SE 12.0中进行。
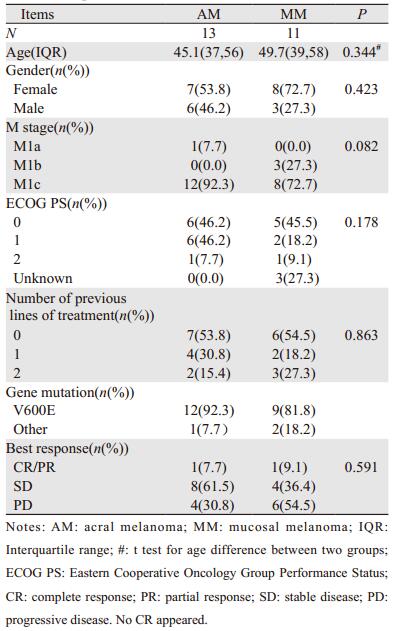
2 结果 2.1 基本资料本研究共筛选出24例患者,包括13例肢端型黑色素瘤(acral melanoma, AM)患者和11例黏膜型黑色素瘤(mucosal melanoma, MM)患者。中位年龄分别为45.1岁和49.7岁。AM患者中男女患者人数相近,MM患者中女性和男性分别占比72.7%和27.3%。筛选入组本研究时M1c期的患者在AM和MM类型中的占比分别为92.3%和72.7%。总体上约80%患者的ECOG PS评分为0或1。在接受维莫非尼治疗前,AM和MM患者中接受过一次及以上治疗的比例为46.2%和45.5%,基因突变类型以V600E突变为主,所占比例约为90%。以上指标在AM和MM患者中差异无统计学意义,见表 1。
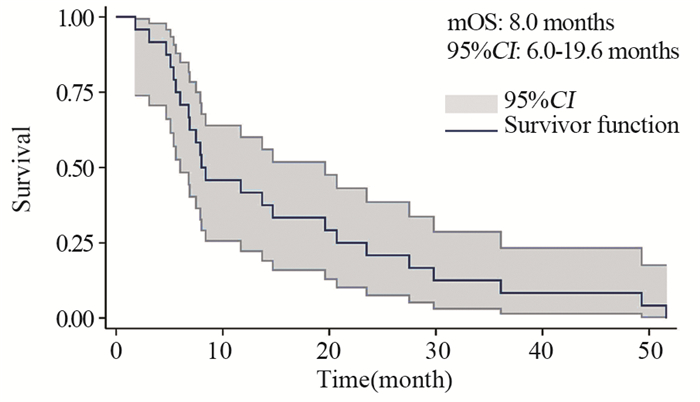
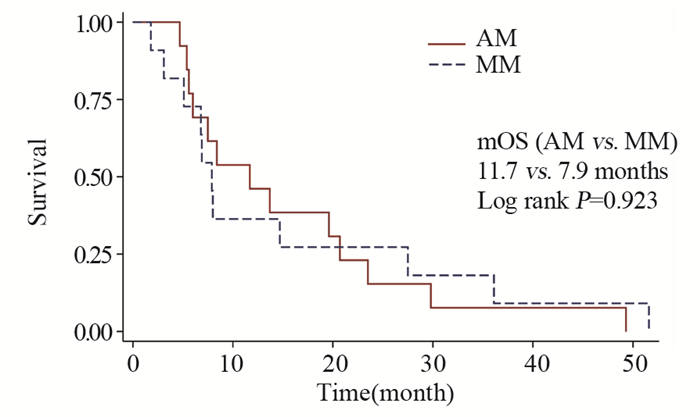
患者总体中位生存期为8.0月(95%CI: 6.0~19.6),前10月内的死亡速度快于后期,最短和最长生存时间分别为1.8和51.6月。AM患者的中位生存期为11.7月,高于MM患者约4月,但是两者的生存曲线差异无统计学意义(P=0.923),见图 1~2。
|
| 图 1 接受维莫非尼治疗的肢端和黏膜型黑色素瘤患者的总体生存曲线 Figure 1 Overall survival curves of acral melanomal(AM) and mucosal melanama(MM) patients receiving vemurafenib treatment |
|
| 图 2 接受维莫非尼治疗的肢端和黏膜型黑色素瘤患者的生存曲线 Figure 2 Overall survival curves of AM and MM patients receiving vemurafenib treatment |
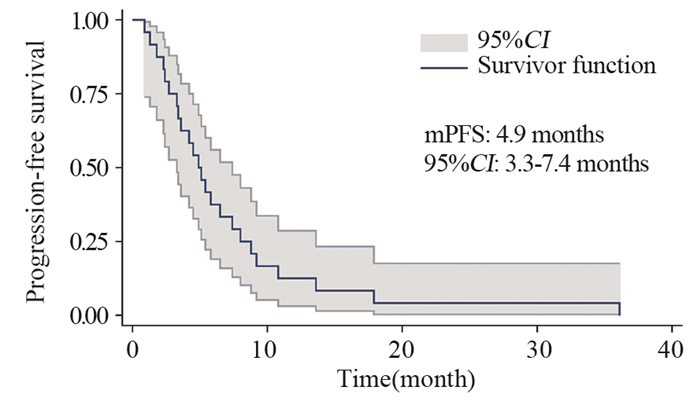
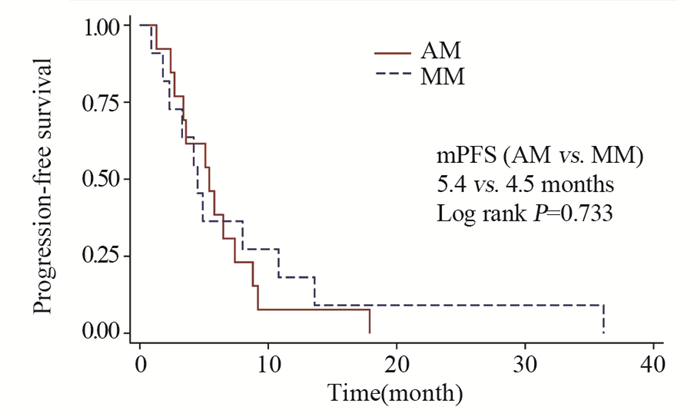
患者的总体中位无进展生存期为4.9月(95% CI: 3.3~7.4),最长和最短的无进展生存期分别为0.9月和36.1月。AM患者和MM患者的中位无进展生存期分别为5.4和4.5月,差异无统计学意义(P=0.733),见图 3~4。
|
| 图 3 接受维莫非尼治疗的肢端和黏膜型黑色素瘤患者的总体无进展生存曲线 Figure 3 Progression-free survival curves of AM and MM patients receiving vemurafenib treatment |
|
| 图 4 接受维莫非尼治疗的AM和MM患者的无进展生存曲线 Figure 4 Progression-free survival curves of AM and MM patients receiving vemurafenib treatment |
AM和MM中各有1例患者达到PR,8例和4例患者达到SD,4例和6例患者未出现有效应答,对应的DCR分别为69.2%和45.5%,二者之间差异无统计学意义(P=0.591),见表 1。
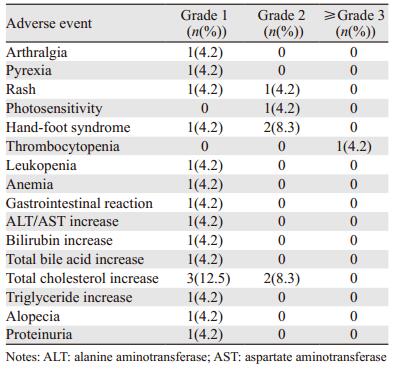
2.3 维莫非尼的安全性结果从维莫非尼的安全性数据看,患者的不良事件多数为1级。其中,关节痛、发热、脱发等不良事件只有1级不良事件;发生2级皮疹、光过敏、总胆固醇升高、手足综合征不良反应的患者例数分别为1例、1例、2例和2例。仅有1例患者出现3级血小板减少的不良事件。肢端型黑色素瘤出现不良事件的比例高于黏膜型黑色素瘤。整体而言,药物的安全性在可接受的范围之内,没有发生非预期不良事件,见表 2。
|
从研究结果看,肢端和黏膜型黑色素瘤患者的总体中位生存期和中位无进展生存期分别为8月和4.9月。肢端型黑色素瘤患者的中位生存期和无进展生存期为11.7月和5.4月,明显高于之前白雪等的6.2月和3.6月[12];黏膜型黑色素瘤患者对应的数据为7.9月和4.5月,与之前数据(分别为8.2月和4.4月[12])相近。分析其原因,主要有以下2点:(1)本研究经历了更长时间的随访,无截尾数据,所有的患者均出现了死亡终点的结局指标,因此结果更真实可信;(2)白雪等所选择的人群虽为应用BRAF抑制剂的患者,但是考虑到不同药物(维莫非尼、索拉菲尼等)的差异性影响,本研究只选取一部分“亚人群”,即只服用维莫非尼的患者,减少了偏倚。
虽然近50%的患者在服用BRAF抑制剂半年后会迅速发生疾病进展,但其效果仍然优于普通化疗,接受靶向治疗的患者有更长的生存期和无进展生存期(风险比值比、HR均小于0.50)[13-14]。已有的临床试验数据[13-15]表明,皮肤型基因突变患者的中位生存期为9~16月,中位无进展生存期为5~6.8月。白雪等的数据显示肢端和黏膜型的效果较差[12],但是通过减小偏倚和更长时间的随访,可以看出,维莫非尼在肢端和黏膜型黑色素瘤患者中的有效性与BRAF基因突变的皮肤型黑色素瘤基本一致,但生存获益偏低,需要更大样本量进一步探索其有效性。
3.2 维莫非尼相关不良事件发生情况与既往一致维莫非尼治疗相关的不良事件多为1~2级,3级及以上的不良事件较少。最常见的不良事件包括关节疼痛、继发性皮肤损伤等。Balmelli等[16]对接受维莫非尼治疗时间为1~2年的BRAF基因突变的黑色素瘤患者进行随访,发现患者耐受性良好,而且不良事件的发生主要发生在治疗的前6月。类似地,Blank等[17]随访了3 000多例患者,同样发现后期无新的不良事件发生。在本研究的24例肢端和黏膜型黑色素瘤患者中,最常见的不良事件是总胆固醇升高和皮肤相关反应。除了总胆固醇升高,安全性基本与已有的研究结果[15-17]一致。考虑到分析的样本量较少,该不良事件的分布仅作为参考。
3.3 本研究的局限性和意义样本量不足使本研究结论的效度不足。但是,本研究第一次提供了接受维莫非尼靶向治疗的肢端和黏膜型黑色素瘤患者的有效性和安全性数据。由于该亚型在欧美国家中的发病比例过低,因此难以通过现有的临床试验数据确定维莫非尼在肢端和黏膜型突变患者中的确切疗效。维莫非尼在中国刚批准上市[18],给中国黑色素瘤患者的治疗带来了希望。但是,中国黑色素瘤以肢端和黏膜型为主,BRAF突变在该类亚型中的比例在20%左右[5]。这一部分患者对维莫非尼的应答效果并不能确定,本研究为维莫非尼在该类亚型人群中的临床应用提供了初步证据,也为前瞻性临床试验的开展提供了重要参考。
| [1] | Ferlay J, Soerjomataram I, Dikshit R, et al. Cancer incidence and mortality worldwide: sources, methods and major patterns in GLOBOCAN 2012[J]. Int J Cancer, 2015, 136(5): E359–86. DOI:10.1002/ijc.29210 |
| [2] | Kim KB, Kefford R, Pavlick AC, et al. Phase Ⅱ study of the MEK1/MEK2 inhibitor Trametinib in patients with metastatic BRAF-mutant cutaneous melanoma previously treated with or without a BRAF inhibitor[J]. J Clin Oncol, 2013, 31(4): 482–9. DOI:10.1200/JCO.2012.43.5966 |
| [3] | Chapman PB, Hauschild A, Robert C, et al. Improved survival with vemurafenib in melanoma with BRAF V600E mutation[J]. N Engl J Med, 2011, 364(26): 2507–16. DOI:10.1056/NEJMoa1103782 |
| [4] | Robert C, Long G V, Brady B, et al. Nivolumab in previously untreated melanoma without BRAF mutation[J]. N Engl J Med, 2015, 372(4): 320–30. DOI:10.1056/NEJMoa1412082 |
| [5] | Si L, Kong Y, Xu X, et al. Prevalence of BRAF V600E mutation in Chinese melanoma patients: large scale analysis of BRAF and NRAS mutations in a 432-case cohort[J]. Eur J Cancer, 2012, 48(1): 94–100. DOI:10.1016/j.ejca.2011.06.056 |
| [6] | Flaherty KT, Puzanov I, Kim KB, et al. Inhibition of mutated, activated BRAF in metastatic melanoma[J]. N Engl J Med, 2010, 363(9): 809–19. DOI:10.1056/NEJMoa1002011 |
| [7] | Safaee Ardekani G, Jafarnejad SM, Khosravi S, et al. Disease progression and patient survival are significantly influenced by BRAF protein expression in primary melanoma[J]. Br J Dermatol, 2013, 169(2): 320–8. |
| [8] | Postow MA, Hamid O, Carvajal RD. Mucosal melanoma: pathogenesis, clinical behavior, and management[J]. Curr Oncol Rep, 2012, 14(5): 441–8. DOI:10.1007/s11912-012-0244-x |
| [9] | Spencer KR, Mehnert JM. Mucosal Melanoma: Epidemiology, Biology and Treatment[J]. Cancer Treat Res, 2016, 167: 295–320. DOI:10.1007/978-3-319-22539-5 |
| [10] | Butler M, Hamid O, Ribas A, et al. Efficacy of pembrolizumab in patients with advanced mucosal melanoma enrolled in the KEYNOTE-001, 002, and 006 studies[J]. Eur J Cancer, 2017, 72(1): S123. |
| [11] | Kong Y, Si L, Zhu Y, et al. Large-scale analysis of KIT aberrations in Chinese patients with melanoma[J]. Clin Cancer Res, 2011, 17(7): 1684–91. DOI:10.1158/1078-0432.CCR-10-2346 |
| [12] | Bai X, Mao LL, Chi ZH, et al. BRAF inhibitors: efficacious and tolerable in BRAF-mutant acral and mucosal melanoma[J]. Neoplasma, 2017, 64(4): 626–32. DOI:10.4149/neo_2017_419 |
| [13] | Chapman PB, Hauschild A, Robert C, et al. Improved Survival with Vemurafenib in Melanoma with BRAF V600E Mutation[J]. New Engl J Med, 2011, 364(26): 2507–16. DOI:10.1056/NEJMoa1103782 |
| [14] | Sosman JA, Kim KB, Schuchter L, et al. Survival in BRAF V600-mutant advanced melanoma treated with vemurafenib[J]. N Engl J Med, 2012, 366(8): 707–14. DOI:10.1056/NEJMoa1112302 |
| [15] | Larkin J, Del Vecchio M, Ascierto PA, et al. Vemurafenib in patients with BRAFV600 mutated metastatic melanoma: an open-label, multicentre, safety study[J]. Lancet Oncol, 2014, 15(4): 436–44. DOI:10.1016/S1470-2045(14)70051-8 |
| [16] | Balmelli C, Mark M, Spirig C, et al. Long-term tolerability of the BRAF inhibitor vemurafenib in patients with metastatic melanoma: current study data and real-life observations[J]. memo-Mag Eur Med Oncol, 2014, 7(3): 181–6. DOI:10.1007/s12254-014-0156-6 |
| [17] | Blank CU, Larkin J, Arance AM, et al. Open-label, multicentre safety study of vemurafenib in 3219 patients with BRAF(V600) mutation-positive metastatic melanoma: 2-year follow-up data and long-term responders' analysis[J]. Eur J Cancer, 2017, 79: 176–84. DOI:10.1016/j.ejca.2017.04.007 |
| [18] | 国家食品药品监督管理总局.药品信息-维莫非尼[EB/OL]. [2017-12-25]. http://app2.sfda.gov.cn/datasearchp/index1.do?tableId=36&tableName=TABLE36&tableView=%BD%F8%BF%DA%D2%A9%C6%B7&Id=16506.China [ Food and Drug Administration. Medicine information- Vemurafenib film-coated tablets[EB/OL]. [2017-12-25] http://app2.sfda.gov.cn/datasearchp/index1.do?tableId=36&tableName=TABLE36&tableView=%BD%F8%BF%DA%D2%A9%C6%B7&Id=16506. ] |
 2018, Vol. 45
2018, Vol. 45