文章信息
- 红细胞压积预测肺癌患者化疗耐受性的初步探讨
- Preliminary Investigation About Hematokrit Forecast of Chemotherapy Tolerance of Lung Cancer Patients
- 肿瘤防治研究, 2017, 44(1): 42-47
- Cancer Research on Prevention and Treatment, 2017, 44(1): 42-47
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2017.01.009
- 收稿日期: 2015-12-11
- 修回日期: 2016-08-07
2. 443000 宜昌,三峡大学科技学院临床医学系
2. Department of Clinical Medicine, College of Science and Technology of China Three Gorges University, Yichang 443000, China
肺癌发病率在发达及发展中国家逐年增高,尽管在发达国家,5年相对生存率也仅16%[1]。80%~85%的组织学类型为非小细胞肺癌(non-small cell lung cancer, NSCLC),在首次就诊时,约70%的患者已处于中晚期[2],失去手术根治的机会,因此化疗成为晚期NSCLC的主要治疗手段[3],但由于化疗后并发症或不良反应的产生,尤其是骨髓抑制[4-6],使患者生活质量下降[7],导致化疗耐受性差、无法正常化疗,影响化疗疗效及预后,尤其是在接受多疗程治疗(如放疗、化疗),骨髓造血能力下降,更易出现血液学异常,导致患者因耐受性差难以接受或完成正规化疗,影响化疗疗效及预后,失去了治疗机会,导致疾病进展,甚至危及生命。因此,本研究拟对2012年1月-2014年7月在河北医科大学第四医院肿瘤内科收治的311例患者进行回顾性分析,以期找到预测化疗耐受性相关的新指标。
1 资料与方法 1.1 临床资料及纳入标准收集2012年1月-2014年7月在河北医科大学第四医院肿瘤内科住院经手术、支气管镜、CT引导下肺穿刺或其他方式获得组织或细胞学诊断为肺癌的患者共311例,入院前后未行输血及促红细胞生成素(EPO)等抗贫血治疗。血液化验的总数目即总周期数为1 518周期。病历资料录入指标包括住院号、姓名、性别、年龄、病理、疾病分期、化疗疗程数;化验指标包括每次化验中的中性粒细胞百分比(the percent of neutrophile granulocyte, MEUT)、中性粒细胞计数(neutrophile count, NEUT)、红细胞计数(redblood cell, RBC)、血红蛋白(hemoglobin, Hgb)、红细胞压积(hematocrit, HCT)、红细胞平均容积(mean corpuscularvolume, MCV)、红细胞平均血红蛋白含量(mean corpuscular hemoglobin, MCH)、红细胞血红蛋白浓度(mean corpuscular concentration, MCHC)以及红细胞分布宽度(red blood cell distribution width, RDW)等数值。
1.2 病例排除标准原发性肺癌诊断不明确的患者;未能明确肿瘤分期及肿瘤部位的患者;无法进行贫血诊断的患者;精神病患者;非肿瘤因素所致贫血的患者。
1.3 贫血的诊断标准本研究血液学检验指标的结果由河北医科大学第四医院检验科室化验得出,根据美国国立肿瘤研究所(national cancer institute, NCI)贫血分级标准制定贫血的严重程度分为4级。无贫血时血红蛋白值:男性:14.0~18.0 g/dl,女性:12.0~16.0 g/dl;轻度贫血时血红蛋白值:男性:10.0~12.0 g/dl,女性:10.0~11.0 g/dL;中度贫血时血红蛋白值:8~10 g/dl。重度贫血时血红蛋白值:6.5~7.9 g/dl。极重度贫血时血红蛋白值:<6.5 g/dl。根据WHO(world health organization)将骨髓抑制程度分为4级。无骨髓抑制时中性粒细胞计数:≥2.0×109/L;Ⅰ度骨髓抑制时中性粒细胞计数:(1.5~1.9)×109/L;Ⅱ度骨髓抑制时中性粒细胞计数:(1.0~1.4)×109/L;Ⅲ度骨髓抑制时中性粒细胞计数:(0.5~0.9)×109/L;Ⅳ度: < 0.5×109/L。
1.4 肿瘤的临床分期本研究采用《AJCC癌症分期手册》第七版肺癌国际统一TNM分期法进行分期。
1.5 数据库的建立和数据分析处理分析肺癌患者化疗后血常规中粒红系指标阳性表达发生率与性别、年龄、分期、病理类型、化疗疗程数之间的相关性。首先对各个指标阳性表达相关因素采用单因素分析的方式进行初步的筛选,继而对单因素分析得出的提示对化疗耐受性有影响的相关变量进行多因素分析,最后得出化疗耐受性发生的相关的独立因素。其中本研究中各指标阳性表达是指各指标数值低于正常值,以下类同。
1.6 统计学方法应用SPSS20.0统计软件对数据进行分析,对变量的分析采用频次、频率等方式。应用χ2检验(chi-square test)进行组间分析。多变量之间采用Spearman相关分析,以P < 0.05为差异有统计学意义。
2 结果 2.1 临床资料分析结果 2.1.1 一般情况男222例,占总人数的71.38%,女89例,占总人数的28.62%;年龄≤50岁有62例,占总数的19.94%,年龄 > 50岁有249例,占总数的80.06%,中位年龄60岁(28~84岁)。
2.1.2 病理结果311例中,鳞癌46例(14.79%)、腺癌79例(25.40%)、小细胞癌186例(59.81%);病理分期:Ⅰ~Ⅱ期123例(39.55%),其中鳞癌12例(9.76%)、腺癌11例(8.94%)、小细胞癌100例(81.30%);Ⅲ~Ⅳ期188例(60.45%),其中鳞癌34例(18.09%)、腺癌68例(36.17%)、小细胞癌86例(45.74%)。
2.1.3 治疗情况化疗完成4疗程周期以下的135例(43.41%),化疗完成4疗程及以上的176例(56.59%)。
2.2 单因素分析化疗后各指标阳性表达的相关因素 2.2.1 化疗后各指标在肺癌中的阳性表达(阳性表达周期数/总周期数)中性粒细胞百分比为233周期(15.35%)、中性粒细胞计数为205周期(13.50%)、红细胞计数为403个周期(26.55%)、血红蛋白为412周期(27.14%)、红细胞压积为625周期(41.17%)、平均红细胞体积为21周期(1.38%)、平均红细胞血红蛋白为21周期(1.38%)、红细胞血红蛋白浓度为91周期(5.99%)、红细胞分布宽度为2周期(0.13%)。提示化疗药物干预后肺癌患者外周血红系较粒系易出现阳性表达,其中红细胞压积、血红蛋白、红细胞计数发生阳性表达率较高。
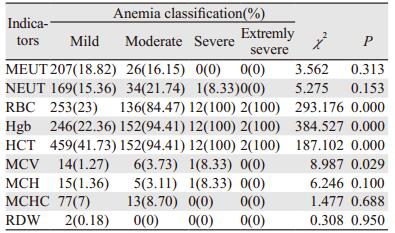
2.2.2 按照NCI标准评判贫血程度时肺癌各指标阳性表达化疗后发生贫血的周期数为1 269(83.60%),无贫血的为249(16.40%),其中轻度贫血为1 100(86.68%),中度贫血为155(12.21%),重度贫血为12(0.95%),极重度贫血为2(0.16%)。不同程度的贫血在各指标下的表达情况,见表 1。对数据进行统计学分析,红细胞计数、血红蛋白、红细胞压积及平均红细胞体积阳性表达在不同程度贫血之间不同,差异有统计学意义(P < 0.05)。
|
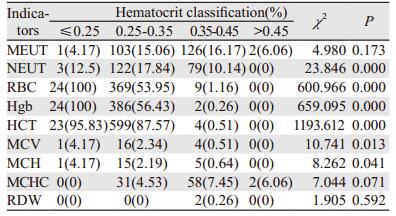
对于红细胞压积评判贫血程度时,我们定义≤0.25为重度贫血,0.25~0.35为中度贫血, > 0.35~0.45为轻度贫血, > 0.45为无贫血,化疗后发生贫血的周期数为1 485(97.17%),无贫血的为33(2.83%),其中轻度贫血为778(52.75%),中度贫血为683(46.31%),重度贫血为24(1.63%)。各指标在不同程度贫血表达情况,见表 2。中性粒细胞计数、红细胞计数、血红蛋白、红细胞压积、平均红细胞体积及平均红细胞血红蛋白阳性表达在不同程度贫血之间不同,差异有统计学意义(P < 0.05)。化疗干预后贫血程度多见于轻中度。
|
小细胞肺癌阳性表达为64.29%,鳞癌、腺癌分别为15.42%、20.29%。将311例患者按病理类型分类,进行X列卡方检验及两两之间四格表卡方检验。结果显示,化疗干预后,中性粒细胞计数阳性表达在鳞癌、腺癌及小细胞肺癌不同病理类型之间不同,差异有统计学意义(χ2=17.774, P=0.000),且出现阳性表达率由高至低分别为小细胞癌、鳞癌、腺癌。血红蛋白阳性表达在鳞癌、腺癌之间不同,差异有统计学意义(χ2=6.357, P=0.012),且腺癌较鳞癌更易出现阳性表达。此外,在化疗干预后,红细胞血红蛋白浓度出现阳性表达在小细胞癌与鳞癌之间不同,差异有统计学意义(χ2=5.536, P=0.019),即小细胞癌患者更易出现异常。而中性粒细胞百分比、红细胞计数、血红蛋白、红细胞压积、红细胞平均容积、红细胞平均血红蛋白含量、红细胞分布宽度阳性表达在鳞癌、腺癌及小细胞肺癌等不同病理类型间差异无统计学意义(P > 0.05)。
2.2.5 不同性别肺癌患者外周血粒红系阳性表达情况男性阳性表达周期数为1 222(80.50%),女性阳性表达周期数为296(19.50%),男性较女性更易出现中性粒细胞计数及红细胞计数阳性表达,两者差异有统计学意义(χ2=4.326, P=0.038; χ2=3.970, P=0.046)。中性粒细胞百分比、血红蛋白、红细胞压积、红细胞平均容积、红细胞平均血红蛋白含量、红细胞血红蛋白浓度、红细胞分布宽度阳性表达在不同性别中差异无统计学意义(P > 0.05)。
2.2.6 年龄因素在肺癌患者外周血粒红系阳性表达情况本研究以50岁为界限对年龄进行分组。化疗干预后,≤50岁患者阳性表达周期数279(18.38%), > 50岁患者阳性表达周期数1 239(81.62%)。各项指标在 > 50岁及≤50岁不同年龄组之间阳性表达差异无统计学意义(P > 0.05)。
2.2.7 肿瘤病情分期因素在不同病理类型患者外周血粒红系阳性表达情况化疗干预后,Ⅰ~Ⅱ期小细胞肺癌患者阳性表达周期数为529(83.97%),Ⅲ~Ⅳ期患者阳性表达周期数为447(50.34%)。Ⅲ~Ⅳ期患者比Ⅰ~Ⅱ期患者更易出现平均红细胞体积及平均红细胞血红蛋白阳性表达,两者差异有统计学意义(χ2=6.557, P=0.010;χ2=5.158, P=0.023)。中性粒细胞百分比、中性粒细胞计数、红细胞计数、血红蛋白、红细胞压积、红细胞血红蛋白浓度、红细胞分布宽度阳性表达在不同分期间比较差异无统计学意义(P > 0.05)。化疗干预后,Ⅰ~Ⅱ期鳞癌患者阳性表达周期数为59(9.37%),Ⅲ~Ⅳ期患者阳性表达周期数为175(19.71%),各指标在分期上比较差异均无统计学意义(P > 0.05)。化疗干预后,Ⅰ~Ⅱ期腺癌患者阳性表达周期数为42(6.66%),Ⅲ~Ⅳ期患者阳性表达周期数为266(29.95%),Ⅲ~Ⅳ期患者较Ⅰ~Ⅱ期患者更易出现红细胞计数异常,两者差异有统计学意义(χ2=7.210, P=0.007)。中性粒细胞百分比、中性粒细胞计数、血红蛋白、红细胞压积、红细胞平均容积、红细胞平均血红蛋白含量、红细胞血红蛋白浓度、红细胞分布宽度阳性表达在不同分期间差异无统计学意义(P > 0.05)。
2.2.8 化疗周期因素在肺癌患者外周血粒红系阳性表达情况本研究以4疗程为界限。化疗干预后, < 4疗程患者阳性表达周期数为666(43.87%),≥4疗程患者阳性表达周期数852(56.13%)。≥4化疗疗程组较 < 4疗程组患者更易出现平均红细胞体积、平均红细胞血红蛋白、红细胞血红蛋白浓度异常,两者差异有统计学意义(χ2=10.203, P=0.001; χ2=10.203, P=0.001; χ2=6.751, P=0.009)。中性粒细胞百分比、中性粒细胞计数、红细胞计数、血红蛋白、红细胞压积、红细胞分布宽度阳性表达在不同化疗疗程数间差异无统计学意义(P > 0.05)。
2.3 化疗耐受性相关因素通过上述结果,发现化疗后易出现异常的有红细胞压积、血红蛋白、红细胞计数、中性粒细胞百分比。而且在不同分类时,表达差异亦有统计学意义。因此将其作为评估化疗耐受性指标。
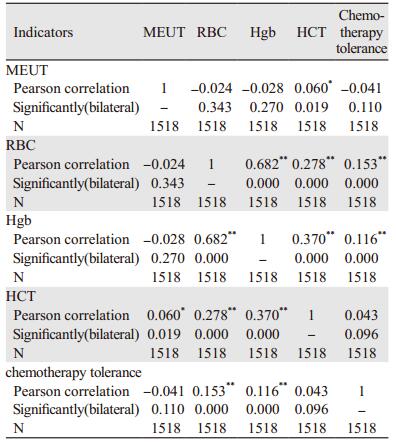
2.4 多变量之间及多变量与化疗耐受性之间的关系中性粒细胞百分比与红细胞压积之间有相关性,相关系数为0.060,差异有统计学意义(P=0.019)。红细胞计数与血红蛋白、红细胞压积之间有相关性,相关系数为0.682、0.278,差异有统计学意义(P=0.000、0.000)。血红蛋白与红细胞压积之间有相关性,相关系数为0.370,差异有统计学意义(P=0.000)。化疗耐受性与红细胞计数、血红蛋白有关,相关系数为0.153、0.116,差异有统计学意义(P=0.000、0.000),见表 3。
贫血是恶性肿瘤及其治疗过程中一种常见并发症,尤其在肿瘤进展期时更加明显。贫血不仅会使患者产生各种贫血的症状,降低生活质量,影响患者对放化疗的耐受性,使其不能顺利完成肿瘤的综合治疗,而且还会使肿瘤组织对放、化疗的敏感度降低[8-9],从而影响肿瘤的治疗效果及预后。
欧洲癌症贫血调查组对15 367例癌症患者的研究发现,化疗后肺癌发生贫血的机会为77% [10]。王剑等[11]对41例晚期非小细胞肺癌患者研究发现,贫血的发生与性别无相关性,(P=0.942)。本研究中,化疗干预后,男性阳性表达周期数为1 222(80.50%),女性阳性表达周期数为296(19.50%),两者表达差异有统计学意义,且男性较女性更易出现中性粒细胞计数及红细胞计数下降。这可能与性别不具有特异性,样本分布不均且数量不足有关,需增加样本量再行分析讨论。化疗干预后,不同年龄组与阳性表达周期总数之间关系为:≤50岁患者阳性表达周期数为279(18.38%), > 50岁患者阳性表达周期数为1 239(81.62%)。两组差异无统计学意义。Weiss等[12]曾报道77%的老年男性患者与68%的老年女性患者有贫血,说明老年肺癌患者更易发生贫血,但本研究结果与上述研究结果不一致,不同年龄组之间差异无统计学意义,考虑本研究年龄分布不均及样本数量少有关,虽然中、老年人是恶性肿瘤的高发人群,但近年来,肺恶性肿瘤发病呈现出年轻化趋势,且年轻恶性肿瘤患者的生物学行为相对较差,病情进展速度快,易早期复发转移,从而导致预后不佳,故需提高对年轻患者的重视。从临床分期看,在小细胞癌中平均红细胞体积及平均红细胞血红蛋白化疗后阳性表达在Ⅰ~Ⅱ期及Ⅲ~Ⅳ期分期之间不同,差异有统计学意义,且分期晚的患者更易出现平均红细胞体积及平均红细胞血红蛋白下降。在腺癌中红细胞计数阳性表达在Ⅰ~Ⅱ期及Ⅲ~Ⅳ期分期之间不同,差异有统计学意义,且分期晚的患者更易出现红细胞计数下降。与王莹等[13]调查分析得出贫血的发生率在肿瘤分期方面有统计学差异的结论相似。本研究中以4疗程为界限,化疗干预后,平均红细胞体积、平均红细胞血红蛋白、红细胞血红蛋白浓度异常在 < 4及≥4不同化疗疗程组之间不同,显示差异有统计学意义。且化疗疗程数多的患者更易出现平均红细胞体积、平均红细胞血红蛋白、红细胞血红蛋白浓度异常,说明化疗疗程数多了,患者体质变差,更易出现血象异常。Wan[14]、Holgersson[15]等研究发现,肿瘤贫血能减少肺癌患者的生存时间。化疗药物引起的贫血不仅可以影响患者的生活质量、化疗耐受性,还可以影响化疗疗效,而且疗效与血红蛋白浓度呈正比,因此随着贫血加重,化疗的有效率将会逐渐下降[16]。另外,贫血还可以引起肿瘤乏氧,进而导致肿瘤转移相关蛋白质变化,加速肿瘤扩散,影响化疗效果及患者的预后[17]。此外,贫血可以导致免疫功能紊乱,引起肿瘤进展。许多研究显示纠正患者的贫血,可以有效提高患者的生活质量及抗肿瘤治疗效果,改善患者的预后[18]。
综上所述,多程化疗可引起血液学异常,导致血液性毒性增加,尤其是贫血的发生率高,严重影响患者的生活质量,降低化疗的耐受性,应该受到我们的重视。本研究中发现红细胞压积是影响化疗耐受性的独立因素,由于临床资料样本数较少,后续将继续扩大样本进一步验证。使化疗耐受性的观测更加清晰,致使患者得到最适合的治疗。
| [1] | DeSantis C, Naishadham D, Jemal A, et al. Cancer statistics for African Americans, 2013[J]. CA Cancer J Clin, 2013, 63 (3) : 151–66. DOI:10.3322/caac.21173 |
| [2] | Jemal A, Bray F, Center MM, et al. Global cancer statistics[J]. CA Cancer J Clin, 2011, 61 (2) : 69–90. DOI:10.3322/caac.v61:2 |
| [3] | Wernyj RP, Morin PJ. Molecular mechanisms of plati-num resistance: still searching for the Achilles' heel[J]. Drug Resist Updat, 2004, 7 (4-5) : 227–32. DOI:10.1016/j.drup.2004.08.002 |
| [4] | Wang XS, Qin L, Gao SG, et al. Analysis of efficacy and safety of rhG-CSF used for myelosuppression patients after chemotherapy with TP program[J]. Zhongguo Xian Dai Yao Wu Ying Yong, 2011, 5 (16) : 7–8. [ 王新帅, 秦玲, 高社干, 等. rhG-CSF对TP方案化疗后骨髓抑制的有效性和安全性研究[J]. 中国现代药物应用, 2011, 5 (16) : 7–8. ] |
| [5] | Gai LH, Feng QM, Zuo DP, et al. Differentiation between neutropenia complicated by fever and infections and the treatment[J]. Zhonghua Yi Yuan Gan Ran Xue Za Zhi, 2013, 23 (5) : 1027–9. [ 盖绿华, 冯其梅, 左大鹏, 等. 中性粒细胞缺乏伴发热与感染鉴别诊断及治疗[J]. 中华医院感染学杂志, 2013, 23 (5) : 1027–9. ] |
| [6] | Wang BH, Zhang MZ, Fu XR, et al. Bone marrow inhibition mechanism and research progress of prevention and cure of the radiotherapy[J]. Zhong Liu Ji Chu Yu Lin Chuang, 2013, 26 (2) : 162–5. [ 汪变红, 张明智, 付晓瑞, 等. 化放疗骨髓抑制机制及防治研究进展[J]. 肿瘤基础与临床, 2013, 26 (2) : 162–5. ] |
| [7] | Mäenpää J, Puistola U, Riska H, et al. Impact of Epoetin-beta on Anemia and Health-related Quality of Life in Cancer Patients: A Prospective Observational Study Using the Generic 15D Instrument[J]. Anticancer RES, 2014, 34 (5) : 2325–9. |
| [8] | Harada H. How can we overcome tumor hypoxia in radiation therapy?[J]. J Radiat Res, 2011, 52 (5) : 545–56. DOI:10.1269/jrr.11056 |
| [9] | Qiu MZ, Yuan ZY, Luo HY, et al. Impact of pretreatment hemato-logic profile on survival of colorectal cancer patients[J]. Tumour Biol, 2010, 31 (4) : 255–60. DOI:10.1007/s13277-010-0024-x |
| [10] | Ludwig H, Van Belle S, Barrett-Lee P, et al. The European Cancer Anaemia Survey (ECAS): a large, multinational, prospective survey defining the prevalence, incidence, and treatment of anaemia in cancer patients[J]. Eur Cancer, 2004, 40 (15) : 2293–306. DOI:10.1016/j.ejca.2004.06.019 |
| [11] | Wang J, Ma RB, Chen XQ. Correlative factors of Anemia in advanced non-small cell lung cancer patients and its impact on prognosis[J]. Zhong Liu Xue Za Zhi, 2013, 19 (9) : 718–21. [ 王剑, 马若冰, 陈雪琴. 晚期非小细胞肺癌患者贫血相关因素及其对预后的影响[J]. 肿瘤学杂志, 2013, 19 (9) : 718–21. ] |
| [12] | Weiss G, Goodnough LT. Anemia of chronic disease[J]. New Engl Med, 2005, 352 (10) : 1011–23. DOI:10.1056/NEJMra041809 |
| [13] | Wang Y, Yan LX, Chen WZ. Analysis of anemia relevant factors in cancer patients[J]. Zhongguo Yi Yao Dao Kan, 2013, 15 (7) : 1156–7. [ 王莹, 燕丽香, 陈文彰. 恶性肿瘤贫血相关因素分析[J]. 中国医药导刊, 2013, 15 (7) : 1156–7. ] |
| [14] | Wan S, Lai Y, Myers RE, et al. Post-diagnosis hemoglobin change associates with overall survival of multiple malignancies -results from a 14-year hospital-based cohort of lung, breast, colorectal, and liver cancers[J]. BMC Cancer, 2013, 13 : 340. DOI:10.1186/1471-2407-13-340 |
| [15] | Holgersson G, Sandelin M, Hoye E, et al. Swedish lung cancer radiation study group: the prognostic value of anaemia, thrombocytosis and leukocytosis at time of diagnosis in patients with non-small cell lungcancer[J]. Med Oncol, 2012, 29 (5) : 3176–82. DOI:10.1007/s12032-012-0247-3 |
| [16] | Wu FX. Relationship between changes of cancer-related anemia pre and post chemotherapy and therapeutic effect and analysis of its relevant factors[J]. Zhongguo Dang Dai Yi Yao, 2013, 20 (19) : 41–4. [ 吴飞雪. 化疗前后肿瘤性贫血的变化与疗效的关系及相关因素分析[J]. 中国当代医药, 2013, 20 (19) : 41–4. ] |
| [17] | Wei W, He JM, Wang LW, et al. Study on the relationship between iron metabolism situation and the quality of life in tumou associated anemia patients[J]. Lin Chuang Zhong Liu Xue Za Zhi, 2009, 14 (4) : 350–3. [ 魏玮, 何俊民, 王理伟, 等. 肿瘤相关性贫血铁代谢情况与生活质量相关性的研究[J]. 临床肿瘤学杂志, 2009, 14 (4) : 350–3. ] |
| [18] | Verbeke N, Beguin Y, Wildiers H, et al. High prevalence ofanemia and limited use of therapy in cancer patients: a Belgian survey (Anemia Day 2008)[J]. Support Care Cancer, 2012, 20 (1) : 23–8. DOI:10.1007/s00520-010-1045-0 |
 2017, Vol. 44
2017, Vol. 44