文章信息
- 18F-FDG PET/CT在原发性乳腺癌治疗后随访期间血清CEA和(或)CA153升高患者中的应用
- Application of 18F-FDG PET/CT in Follow-up of Primary Breast Cancer Patients with Increased Serum CEA and(or) CA153
- 肿瘤防治研究, 2016, 43(6): 521-525
- Cancer Research on Prevention and Treatment, 2016, 43(6): 521-525
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2016.06.017
- 收稿日期: 2016-08-18
- 修回日期: 2015-12-30
乳腺癌(breast cancer,BC)是危害女性健康发病率最高的肿瘤,且发病率逐年攀升[1]。虽然BC的治疗方法很多,包括手术、放化疗、内分泌治疗、靶向治疗等,但治疗后复发和转移的概率高达20%~35%[2-3]。因此,早期发现BC复发、转移灶并进行准确的再分期,对临床治疗决策和提高患者总的生存期具有重要意义。
乳腺癌最常用的肿瘤标志物是糖类抗原153(carbohydrate antigen,CA153)和癌胚抗原(carcinoembryonicantigen,CEA),但是两者诊断敏感度和特异性均不尽人意。据文献报道,确诊BC复发和转移的患者中只有50%~60%出现CEA升高,75%~90%出现CA153升高[4]。
18F-FDG PET/CT显像是一种集成了核医学代谢显像与CT形态解剖成像于一身的高端影像学检查,已应用于包括BC在内的多种肿瘤[5]。本文旨在回顾性分析18F-FDG PET/CT显像在原发性乳腺癌治疗后血清CEA和(或)CA153升高的患者中的应用价值。
1 资料与方法 1.1 临床资料从北京大学肿瘤医院2010年4月至2014年6月门诊及住院患者中,选取原发性乳腺癌治疗后血清CEA和(或)CA153升高的病例总计56例,均为女性,中位年龄60岁(44~75岁),左乳癌20例、右乳癌36例。原发病变病理类型为浸润性导管癌36例、浸润性小叶癌8例、其他12例;原发病变临床分期为Ⅰ期7例、Ⅱ期18例、Ⅲ期27例、Ⅳ期4例。手术治疗6例、手术+化疗20例、手术+放化疗30例。末次治疗结束距发现血清CEA和(或)CA153升高的中位时间为57月。本院血清CEA和CA153正常参考值分别为0~5 ng/ml和0~25 u/ml。
1.2 显像方法发现血清CEA和(或)CA153升高后3天至1月内行18F-FDG PET/CT显像。采用飞利浦公司PET/CT显像仪(Gemini TF 16,Philips,Netherland),其中PET/CT部分采用LYSO晶体和微电子设备,CT部分为16排高分辨螺旋CT。所有患者均空腹4~6 h以上,指尖取血法测定空腹血糖<10 mmol/L后,经静脉注射18F-FDG(由我院的日本住友HM-20加速器生产),注射剂量为3.7 MBq/kg,平静休息(60±10)min后行常规PET/CT采集:躯干部PET 1分钟/床位,9或10床位;头部PET 7分钟/床位,1床位;衰减校正平扫CT管电压120 kv,管电流100mAs),采集数据采用OSEM法重建(重建层厚3mm)得到横断面、冠状面、矢状面的CT、PET图像及PET/CT融合图像。
1.3 18F-FDG PET/CT图像处理与分析由三位有多年影像诊断经验的核医学医师背对背阅片,两位或以上医师意见一致时方可做出诊断。PET/CT显像阳性是指PET图像中出现高于邻近正常组织的局灶性摄取,伴有或不伴有同机定位CT形态结构或密度改变。采用半定量法勾画病灶容积ROI,利用设备固有软件计算最大标准摄取值(maximum standardized uptake value,SUVmax)。PET/CT显像阴性是指PET图像放射性分布均匀,无局灶性高摄取。以病理结果或随访一年结果为诊断金标准。
1.4 统计学方法数据经IBM SPSS 20.0软件进行分析,两样本均数的比较采用t检验,两样本率的比较采用χ2检验。以P<.05为差异有统计学意义。
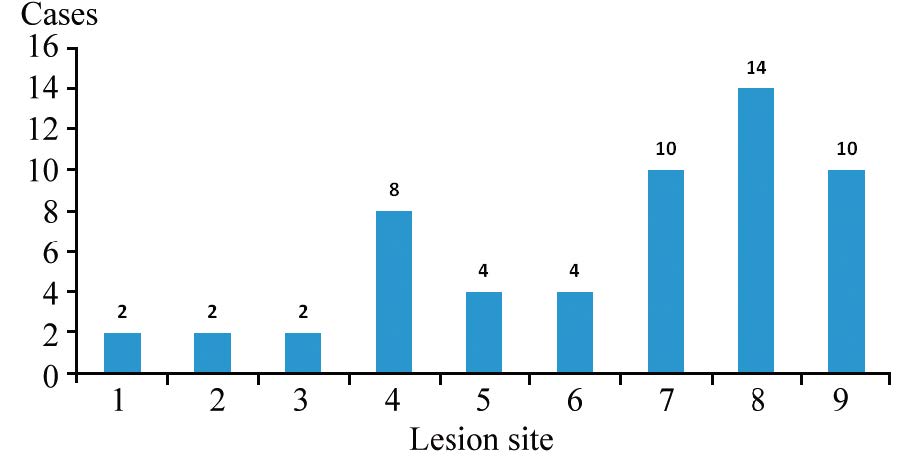
2 结果 2.1 56例患者确诊结果局部复发2例(占3.57%);转移30例(占53.57%),包括胸膜转移2例、肝转移2例、骨转移8例、肺转移4例、淋巴结转移4例、多脏器转移10例;无复发转移14例(占25%);第二原发癌10例(占17.86%),包括子宫内膜癌1例、胆管细胞癌1例和原发肺腺癌8例,见图 1。
|
| 1: local recurrence; 2: pleural metastases; 3: liver metastases; 4: bonemetastases; 5: lung metastases; 6: lymph node metastases; 7: multipleorgan metastases; 8: no recurrence or metastasis; 9: second primarycancer 图 1 56例原发性乳腺癌患者病理及随访1年结果 Figure 1 Results of pathology and one-year follow-up of 56 |
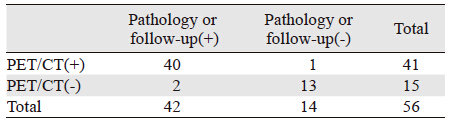
56例患者中18F-FDG PET/CT显像阳性者41例(占73.21%),其中复发转移30例SUVmax为(7.08±2.51),第二原发癌10例SUVmax为(6.40±2.27),两组SUVmax的差异无统计学意义(P=0.954),但同机CT征象有助于鉴别诊断。假阳性1例,为术后半年患侧胸壁摄取增高,SUVmax为2.5。18F-FDGPET/CT显像阴性者15例(占26.79%),其中无复发转移13例,假阴性病例2例(1例为肺微小转移结节,1例为胸腰椎成骨性转移),见表 1。典型病例见图 2、3。据此18F-FDG PET/CT显像的诊断效能为:敏感度95.24%(40/42),特异性92.86%(13/14),准确性94.64%(53/56),假阴性率4.76%(2/42),假阳性率7.14%(1/14),阳性预测值(PPV)97.56%(40/41),阴性预测值(NPV)86.67%(13/15)。
|
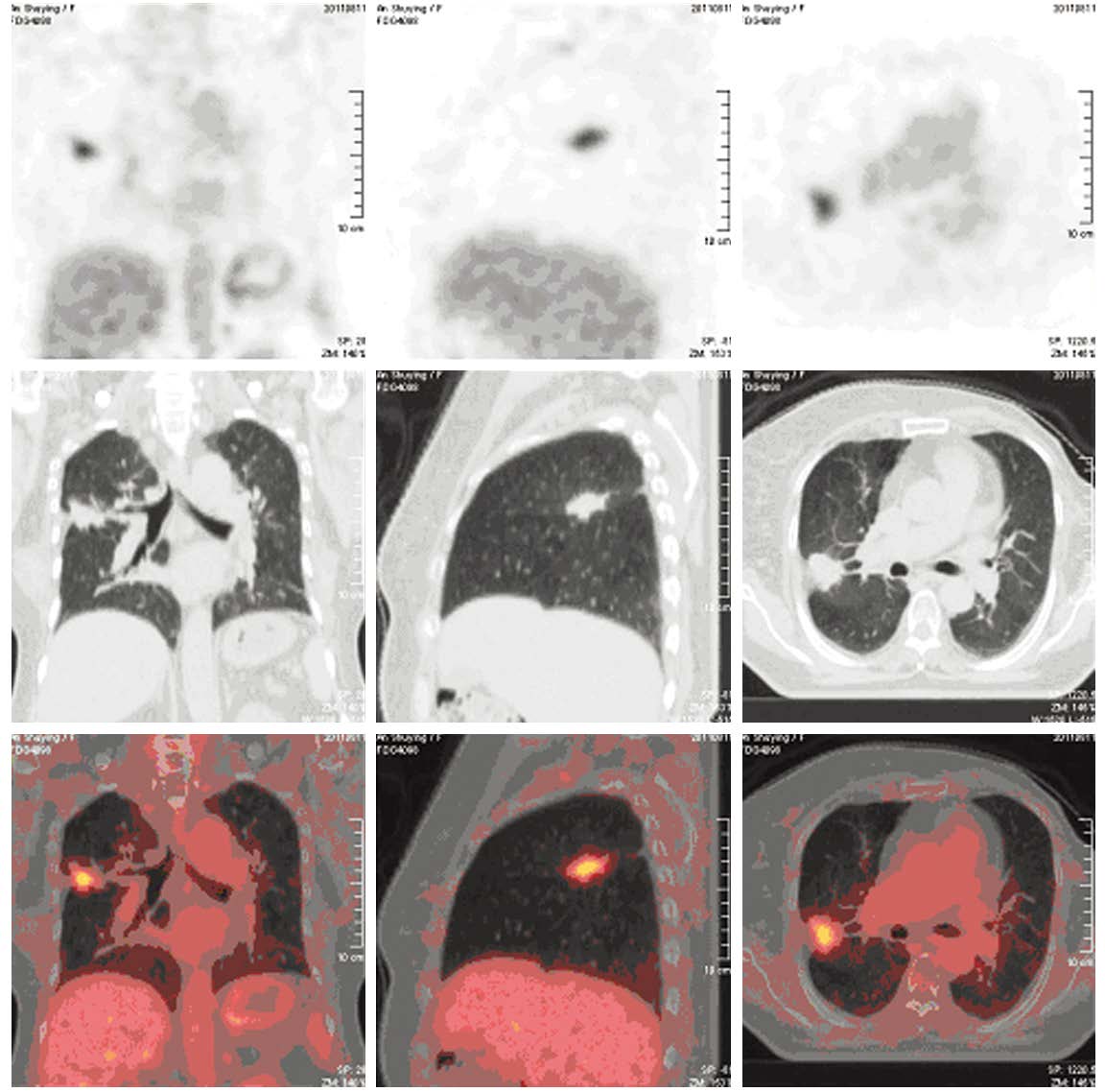
| Female, 64 years old, left breast cancer with increased CEAafter modified radical mastectomy. 18F-FDG PET/CT showeda high-uptake nodule in the posterior segment of right upperlobe confirmed as primary well-differentiated adenocarcinomaby pathology 图 2 第二原发癌典型病例 Figure 2 Typical case of second primary carcinoma |
|
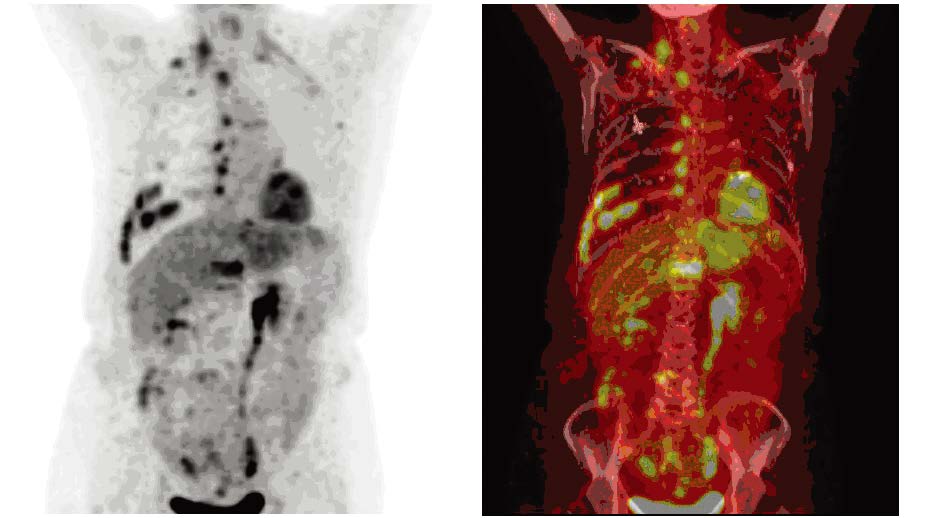
| Female, 66 years old, right breast cancer with increased CEA andCA153 after mastectomy and chemotherapy, 18F-FDG PET/CT showedmultiple metastases in lymph nodes, bones and liver 图 3 多脏器转移典型病例 Figure 3 Typical cases of multiple organ metastases |
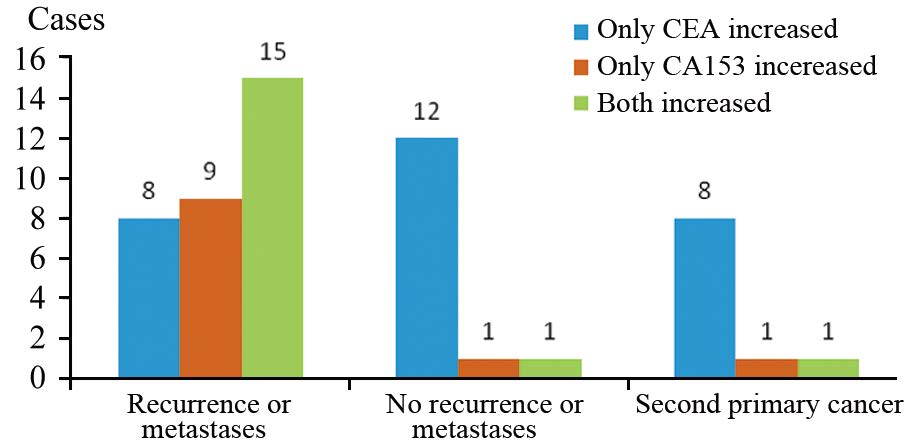
56例患者中单纯CEA升高者28例,其中8例复发转移、12例无复发转移、8例第二原发癌(7例原发肺腺癌,1例胆管细胞癌);单纯CA153升高者11例,其中9例复发转移、1例无复发转移、1例原发肺腺癌;CEA和CA153联合升高者17例,其中15例复发转移、1例无复发转移、1例子宫内膜癌,见图 4。单纯CEA升高、单纯CA153升高及二者联合升高的诊断乳癌治疗后恶性病变的PPV分别为:57.14%(16/28)、90.91%(10/11)和94.12%(16/17),其差异有统计学意义(χ2=10.430,P=0.005),总PPV为75%(42/56)。单纯CEA升高、单纯CA153升高及二者联合升高的诊断乳癌治疗后复发转移的PPV分别为:28.57%(8/28)、81.82%(9/11)和88.24%(15/17),其差异有统计学意义(χ2=20.236,P=0.000),总PPV为57.14%(32/56)。
|
| 图 4 三组患者CEA和(或)CA153升高情况 Figure 4 Increased CEA and(or) CA153 in three groups |
如表 2所示,原发乳腺癌治疗后CEA和(或)CA153升高的患者若18F-FDG PET/CT显像阳性,可将诊断乳癌治疗后恶性病变的PPV从75%提升至97.56%,两者的差异有统计学意义(χ2=9.216,P=0.002)。可将诊断乳癌治疗后复发转移的PPV从57.14%提升至73.17% ,但两者的差异无统计学意义(χ2=2.637,P=0.104)。
乳腺癌复发转移的早期监测和早期治疗对预后影响很大[5]。可乳腺癌复发或转移的早期常常无症状或症状轻微,因此临床迫切需要敏感、准确且无创的探测复发转移灶的方法。
血清肿瘤标志物检测是肿瘤临床随访中常用的、简便经济的筛查肿瘤复发转移的方法,其中最普遍应用于乳腺癌的是CEA和CA153。2015年Stieber等[6]选取743例乳腺癌治疗后患者(187例转移,556例无病生存)分析CEA和CA153升高在检测肿瘤早期转移的价值,结果发现两者的诊断特异性均>98%,但诊断敏感度CEA仅为40.6%、CA153为55.6%、二者联合66.3%。因此,2013版ASCO和2015版NCCN乳腺癌指南中不推荐临床查体阴性且无症状的乳癌患者常规应用CEA和CA153进行随访[7]。本研究结果显示CEA和(或)CA153升高诊断复发转移的PPV不尽如人意,无复发转移组和第二原发癌组均有CEA和(或)CA153升高的情况。
18F-FDG PET/CT显像在CT形态解剖显像的基础上,有机联合了18F-FDG PET葡萄糖代谢显像的信息,在诊断乳腺癌治疗后复发转移方面具有独到的优势:(1)乳腺癌术后或放疗后,胸壁及腋窝区的瘢痕或纤维化常常影响B型超声、CT、钼靶等常规影像方法对局部复发的正确诊断,但18FFDGPET功能代谢显像受其影响较小,能够弥补CT等常规影像方法的缺陷;(2)探测敏感度高,能够发现较小、较早期的复发转移病灶,因此比较适用于乳腺癌治疗后肿瘤标志物升高而常规影像检查阴性患者的进一步检查,以便尽早发现复发转移灶,降低影像学检查的假阴性率;(3)PET/CT是一种全身性影像学检查,扫描范围大,影像信息充分、详尽,往往能发现常规影像方法难以确诊部位的转移(如内乳淋巴链转移、胸膜转移等)和临床意想不到的远隔脏器的转移。因此文献报道18F-FDG PET/CT诊断乳腺癌复发转移的效能优异。Champion等[8]选取228例血清CA153和(或)CEA升高但无临床症状的患者,发现PET/CT诊断复发的敏感度、特异性、PPV、NPV以及准确性分别为93.6%、85.4%、96.7%、74.5%和92.1%。Evangelista等对2001至2011年间发表的13篇文献进行Meta分析,发现乳腺癌治疗后患者出现肿瘤标志物升高(多数为CA153升高)时,18F-FDG PET/CT诊断乳腺癌复发的汇总敏感度、特异性和准确性分别为87.8%、69.3%和82.8%[4]。陈建伟等[9]对乳腺癌术后PET/CT检出的372个病灶进行研究发现,PET/CT总的敏感度、特异性、准确性、PPV分别为88.0%、50.0%、84.9%、95.3%、26.8%。本研究以患者为统计单位,18FFDGPET/CT显像同样显示出良好的诊断效能。但与既往研究不同的是,本研究发现:乳腺癌治疗后CEA和(或)CA153升高且18F-FDG PET/CT显像阳性的病例中第二原发癌也占一定比例24.39%(10/41),而且80%为原发肺腺癌。
当然,本研究也客观地发现了18F-FDG PET/CT显像在诊断乳腺癌治疗后复发转移方面的一些问题:(1) 有1例假阳性病例,主要为术后半年患侧胸壁摄取增高,SUVmax为2.5,这提示我们术后半年术区炎性摄取依然可能存在,因此在这一时间段内依据PET摄取增高诊断乳腺癌局部复发应慎重,最好有同机CT的阳性征象或其他影像学方法的辅助诊断;(2) 有2例假阴性病例(1例为肺微小转移结节、1例为椎体成骨性转移)。这提示我们受PET空间分辨率及部分容积效应的影响,微小病变的代谢可能被低估,而且部分成骨性转移灶可能糖代谢活跃不明显,从而造成PET诊断的假阴性,因此针对PET阴性的病例应细心观察同机CT表现,并应提示临床定期随访;(3) 复发转移组和第二原发癌组均表现为18F-FDG高摄取,且两组的SUVmax差异无统计学意义,说明尽管18F-FDGPET/CT能够进行准确良恶性鉴别,但不具备病理鉴别的能力,因此参考同机CT的典型征象并有针对性的进行病理学检测是必要的。
| [1] | Bernard WS, Christopher PW. World Cancer Report 2014. Lyon: International Agency for Research on Cancer[M]. 2014 : 509 -27. |
| [2] | Kennecke H, Yerushalmi R, Woods R, et al. Metastatic behavior ofbreast cancer subtypes[J]. J Clin Oncol, 2010, 28 (20) : 3271–7. |
| [3] | Berman AT, Thukral AD, Hwang WT, et al. Incidence and patternsof distant metastases for patients with early stage breast cancerafter breast conservation treatment[J]. Clin Breast Cancer, 2013, 13 (2) : 88–94. |
| [4] | Evangelista L, Cervino AR, Ghiotto C, et al. Tumor marker-guidedPET in breast cancer patients-a recipe for a perfect wedding: asystematic literature review and meta-analysis[J]. Clin Nucl Med, 2012, 37 (5) : 467–74. |
| [5] | Bourgeois AC, Warren LA, Chang TT, et al. Role of positronemission tomography/computed Tomography in breast cancer[J]. Radiol Clin North Am, 2013, 51 (5) : 781–98. |
| [6] | Stieber P, Nagel D, Blankenburg I, et al. Diagnostic efficacy of CA15-3 and CEA in the early detection of metastatic breast cancer-Aretrospective analysis of kinetics on 743 breast cancer patients[J]. Clin Chim Acta, 2015, 448 : 228–31. |
| [7] | Khatcheressian JL, Hurley P, Bantug E, et al. Breast cancer followupand management after primary treatment: American Societyof Clinical Oncology clinical practice guideline update[J]. J ClinOncol, 2013, 31 (7) : 961–5. |
| [8] | Champion L, Brain E, Giraudet AL, et al. Breast cancer recurrencediagnosis suspected on tumor marker rising: value of whole-body18FDG-PET/CT imaging and impact on patient management[J]. Cancer, 2011, 117 (8) : 1621–9. |
| [9] | Chen JW, Wang J, Liu B, et al. Impact of 18F-FDG PET/CTcompared with diagnostic CT on following-up breast cancer aftersurgery[J]. Nanjing Yi Ke Da Xue Xue Bao(Zi Ran Ke Xue Ban), 2010, 30 (2) : 195–8. [陈建伟, 王杰, 刘标, 等. PET/CT与胸部诊断CT在乳腺癌术后随访中的比较[J]. 南京医科大学学报(自然科学版),2010, 30 (2) : 195–8. ] |
 2016, Vol. 43
2016, Vol. 43