骨质疏松症是以骨量丢失和骨微结构劣化为特征的一种骨骼疾病,已成为严重危害现代人健康的公共疾病之一[1]。骨质量降低会直接导致骨折风险增加。对于骨质疏松症的防治,除了药物、营养、饮食和运动外,有研究结果显示,电磁场干预青年大鼠可以通过提升其峰值骨量,延缓或减少骨质疏松的发生[2-3]。
生物力学是在物理学和应用数学的基础上将力学原理应用于生物体中进行研究,从而评价生命现象的学科[4]。骨生物力学研究不仅可以评价骨的质量与功能,还可以对骨骼疾病治疗药物的疗效进行评价[5]。低频电磁场干预作为一种新型的物理治疗方法,在实验和临床中不断证实可降低骨折发生的风险[6],但不同参数的低频电磁场对骨微结构的改变情况不同,对骨的抗骨折能力影响亦不同[7]。本研究采用不同频率的1.8 mT电磁场对青年大鼠进行干预,通过比较大鼠骨密度、离体骨的生物力学性能和显微CT的结果,筛选出能有效提升青年大鼠骨密度的电磁场参数,为低频电磁场预防骨质疏松症的发生以及电磁场增加骨量、改善骨微结构的机制研究提供有效的依据。
1 材料与方法 1.1 试剂与仪器水合氯醛溶液(中国人民解放军第一医院),高分辨率活体显微CT(Micro-CT SkyScan1176,比利时Bruker microCT公司),双能X线骨密度仪(美国GE公司),AG-IS型电子万能试验机(日本岛津公司),游标卡尺0~125 mm(无锡锡工量具有限公司),酶标仪(美国BioTek 公司)。
1.8.mT正弦交变电磁场由中国科学院近代物理研究所研制的多功能波形扫描电磁场发生仪提供,该仪器可生成四种波形的电磁场:三角波、正弦波、梯形波、锯齿波。磁场发生仪线圈内径为120 mm,产生磁场强度范围为0~5.5 mT,频率范围为0~100 Hz,电磁场波形、频率、占空比等参数均可自行选择和设定。经高斯计多次检测,仪器运行时,输出的电磁场强度均匀,频率稳定。
1.2 实验动物及分组32只6周龄雌性SD大鼠由甘肃中医药大学动物实验中心提供[许可证号:SCXK(甘)2015-0001],体质量为(100±5) g。购买的大鼠在本院实验动物中心饲养适应一周后,随机分成对照组和10 Hz组、25 Hz组、40 Hz组,每组8只。后三组每天用对应频率的1.8 mT正弦交变电磁场处理90 min。对照组除不进行磁场干预外,其他条件均相同。实验期间大鼠进食、饮水自由,每日观察大鼠的身体和精神状态,每周称量一次体质量。干预前各组体质量和全身骨密度比较差异均无统计学意义(均P>0.05) 。
1.3 双能X线骨密度仪检测骨密度电磁场处理4周后,所有大鼠经腹腔麻醉后(10%的水合氯醛)用双能X线骨密度仪检测骨密度。磁场处理8周后,麻醉大鼠并检测全身骨密度,经腹腔主动脉采血后处死,剥离大鼠两侧的股骨、胫骨及腰椎骨,检测左侧股骨与腰椎骨的骨密度。
1.4 游标卡尺测量股骨长度、直径及内、外两髁外侧间距用游标卡尺测量大鼠左侧股骨的长度,股骨中部的直径,股骨内、外两髁外侧间距。
1.5 股骨三点弯曲试验测量股骨生物力学指标将所有大鼠的右侧股骨编号后,用电子万能材料试验机进行三点弯曲试验,记录载荷变形曲线,应用C语言编程处理载荷变形曲线得出股骨生物力学指标,包括最大载荷、弹性模量。
1.6 腰椎骨压缩实验测量L5椎体生物力学指标将大鼠的腰椎整体剥离后,统一取得L5椎体,除去L5椎体的附件及两端椎间盘后,用1200目的砂纸将椎体两侧打磨平整,依次编号后置于电子万能材料试验机的钢制平台上。保持椎体上下两平面与钢制平台平行,压力加载方向与钢台平面垂直,加载速度为5 mm/min。压缩过程以最大载荷为限,计算机记录载荷—位移曲线,应用C语言编程处理载荷位移曲线得出L5椎体的生物力学指标,包括最大载荷、屈服强度。
1.7 显微CT成像分析骨形态参数将大鼠胫骨用活体显微CT成像后分析,分析区域选在骨骺线中间下凹点正下5 mm处。用显微CT系统软件对所选区域进行三维重建,得出三维重建效果图及胫骨最大纵剖面图。同时对松质骨骨微结构进行骨形态参数分析,包括骨小梁数量、骨小梁厚度、骨小梁分离度及骨体积百分比。
1.8 统计学方法采用SPSS 18.0软件进行统计分析,所有检测数据采用均数±标准差(x±s)表示,组间比较采用单样本t检验。P<0.05为差异有统计学意义。
2 结果 2.1 各组体质量及精神状况比较实验过程中,各组大鼠饮食及精神状态无明显差异;干预4、6和8周时各组大鼠体质量差异无统计学意义(均P>0.05) ,见表 1。
| (x±s,g) | ||||
| 组别 | n | 4周 | 6周 | 8周 |
| 对照组 | 8 | 152.3±6.5 | 168.4±6.4 | 184.1±9.7 |
| 10 Hz组 | 8 | 154.5±6.0 | 172.7±6.3 | 183.0±6.6 |
| 25 Hz组 | 8 | 153.6±5.5 | 171.6±7.1 | 182.8±6.8 |
| 40 Hz组 | 8 | 154.7±7.0 | 171.3±8.1 | 185.2±8.5 |
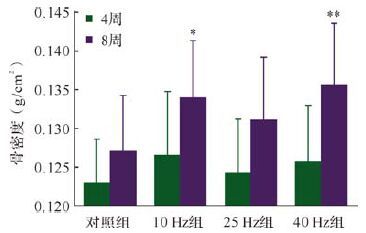
电磁场处理4周后,各组大鼠骨密度差异均无统计学意义(均P>0.05) ;处理8周后,与对照组比较,10 Hz组和40 Hz组大鼠的全身骨密度增加(P<0.05或P<0.01) ,见图 1。说明10 Hz与40 Hz的正弦交变电磁场可有效提升青年大鼠的骨密度。
|
| 与对照组比较,*P<0.05,**P<0.01. 图 1 电磁场处理4、8周后各组全身骨密度比较 Fig. 1 Bone mineral density of rats received magnetic field treatment |
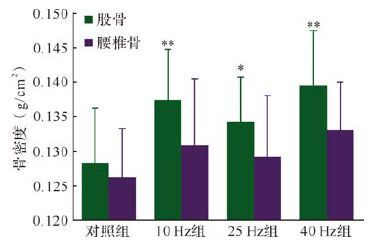
电磁场干预各组大鼠股骨骨密度均高于对照组(P<0.05或P<0.01) ;电磁场干预各组大鼠腰椎骨的骨密度与对照组差异无统计学意义(均P>0.05) ,见图 2。提示正弦电磁场可提升青年大鼠股骨骨密度。
|
| 与对照组比较,*P<0.05,**P<0.01. 图 2 电磁场处理8周后各组股骨和腰椎骨骨密度比较 Fig. 2 Bone mineral density of femur and lumbar vertebra in rats received 8 weeks' magnetic field treatment |
电磁场干预各组大鼠的股骨长度、直径及内外两髁的外侧间距与对照组差异均无统计学意义(均P>0.05) ,见表 2。说明正弦交变电磁场在提升青年大鼠骨密度的同时,并未明显影响到大鼠股骨的长度及直径,电磁场干预是一种的安全治疗方式。
| (x±s,mm) | ||||
| 组别 | n | 长度 | 直径 | 两髁外侧间距 |
| 对照组 | 8 | 31.48±1.24 | 2.81±0.25 | 6.42±0.25 |
| 10 Hz组 | 8 | 31.07±0.84 | 2.78±0.17 | 6.29±0.18 |
| 25 Hz组 | 8 | 30.66±0.94 | 2.70±0.14 | 6.26±0.34 |
| 40 Hz组 | 8 | 31.13±0.82 | 2.75±0.14 | 6.29±0.17 |
如表 3所示,10 Hz组、40 Hz组大鼠的股骨最大载荷和屈服强度均高于对照组(P<0.05或P<0.01) ,而25 Hz组股骨最大载荷和屈服强度与对照组比较差异无统计学意义(均P>0.05) 。股骨的三点弯曲试验结果与大鼠全身骨密度及股骨骨密度的变化一致,说明10 Hz与40 Hz的1.8 mT正弦交变电磁场可提高股骨的生物力学性能。
| (x±s) | |||
| 组别 | n | 最大载荷(N) | 屈服强度(MPa) |
| 对照组 | 8 | 68±5 | 43±5 |
| 10 Hz组 | 8 | 88±6** | 56±5* |
| 25 Hz组 | 8 | 72±6 | 48±5 |
| 40 Hz组 | 8 | 90±8** | 55±7* |
| 与对照组比较,*P<0.05,**P<0.01. | |||
与对照组比较,10 Hz组、40 Hz组大鼠L5椎骨的最大载荷增加(均P<0.05) ;40 Hz组大鼠L5椎骨的弹性模量增加(P<0.05) ;25 Hz组大鼠L5椎骨的两项压力性能指标与对照组差异均无统计学意义(均P>0.05) ,见表 4。大鼠L5椎骨的压缩试验结果与大鼠全身骨密度变化一致,说明频率为40 Hz的1.8 mT正弦电磁场可改善大鼠腰椎骨的生物力学性能。
| (x±s) | |||
| 组别 | n | 最大载荷(N) | 弹性模量(MPa) |
| 对照组 | 8 | 82±6 | 79±5 |
| 10 Hz组 | 8 | 108±7* | 96±6 |
| 25 Hz组 | 8 | 89±6 | 88±6 |
| 40 Hz组 | 8 | 112±8* | 105±7* |
| 与对照组比较,*P<0.05. | |||
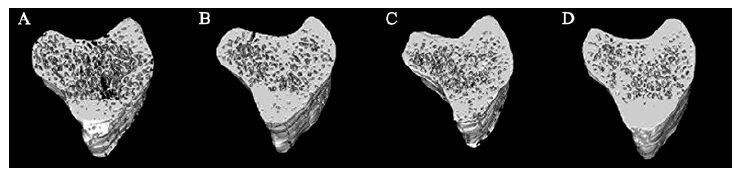
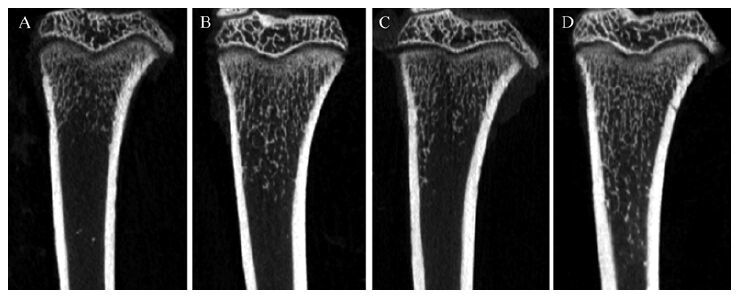
与对照组比较,10 Hz组、40 Hz组大鼠胫骨骨小梁数量、骨小梁分离度以及松质骨体积百分比差异均有统计学意义(均P<0.01) ;25 Hz组大鼠胫骨的骨小梁分离度和松质骨体积百分比均高于对照组(均P<0.05) ,但骨小梁数量与对照组比较差异无统计学意义(P>0.05) ,见表 5。从显微CT重建的三维图(图 3) 和最大纵向剖面图(图 4) 可看出,10、40 Hz的1.8 mT正弦交变电磁场可增加骨小梁的数量,进而提高骨密度。
| (x±s) | |||||
| 组别 | n | 骨小梁数量(/mm) | 骨小梁厚度(mm) | 骨小梁分离度(mm) | 松质骨体积百分比(%) |
| 对照组 | 8 | 2.308±0.333 | 0.141±0.005 | 0.288±0.014 | 38.263±4.342 |
| 10 Hz组 | 8 | 3.351±0.365** | 0.159±0.011 | 0.195±0.004** | 54.746±4.193** |
| 25 Hz组 | 8 | 2.714±0.238 | 0.150±0.012 | 0.227±0.013* | 47.521±4.308* |
| 40 Hz组 | 8 | 3.529±0.385** | 0.160±0.024 | 0.168±0.015** | 67.342±3.925** |
| 与对照组比较,*P<0.05,**P<0.01. | |||||
|
| A:对照组骨小梁离散度最高;B:10 Hz组骨小梁明显增多、致密;C:25 Hz组骨小梁也明显致密;D:40 Hz组骨小梁最为致密. 白色部分为大鼠胫骨骨骺线下同一断层中的所有骨小梁. 图 3 电磁场处理8周后大鼠胫骨显微CT成像分析三维重建图 Fig. 3 Tibia micro-CT imaging analysis of three-dimensional map in rats received 8 weeks' magnetic field treatment |
|
| A:对照组骨小梁数量最少,最为稀疏;B:10 Hz组骨小梁密度明显增加;C:25 Hz组骨小梁稍有增多;D:40 Hz组骨小梁数量最多. 图中胫骨骨骺线下方白色网状部分为骨小梁. 图 4 电磁场处理8周后大鼠胫骨显微CT成像分析纵向最大剖面图 Fig. 4 Tibial micro-CT imaging analysis of maximum longitudinal cross-sectional view of rats received 8 weeks' magnetic field treatment |
骨质疏松的实质是骨量的减少和骨微结构的劣化,在骨生物力学方面表现为骨的韧性和弹性下降,从而使得骨脆性增加,大大提升了骨折发生的概率,严重影响现代人的生活质量及生命安全。低频电磁场应用于去卵巢大鼠,证实具有治疗骨质疏松症的作用[8],而用低频电磁场来增加青年大鼠骨密度,通过提高峰值骨量来预防或延缓骨质疏松症发生的报道并不多见。不同类型的电磁场与不同参数的电磁场对骨微结构的影响和骨功能的改善有差异[9]。在正弦电磁场强度的研究中,Zhou等[10]发现,1.8 mT正弦电磁场能够促进成骨细胞的成熟和矿化。在正弦交变电磁场对大鼠的干预时间上,高玉海等[11]筛选出每日90 min的磁场干预可显著改善大鼠的骨密度状况。本实验在课题组前期细胞实验和动物实验的基础上,选用对成骨细胞有明显增殖作用的1.8 mT正弦交变电磁场,通过比较不同频率组的大鼠骨密度、骨生物力学性能、骨微结构等差异来筛选最佳频率。
骨密度作为骨质量评价的黄金指标,是衡量骨强度的一个重要因素。通常由全身骨密度的检测来判定人体的骨质量及骨强度[12]。本实验中,10、40 Hz的1.8 mT正弦交变电磁场均提高了大鼠全身骨密度,而25 Hz电磁场干预的大鼠全身骨密度却无明显提升,说明在提升青年大鼠骨密度方面,10 Hz与40 Hz均为有效频率,且不同频率的正弦电磁场对大鼠全身骨密度的影响效果不同。大鼠股骨骨密度的变化与全身骨密度的变化一致;而腰椎骨的骨密度各组间比较无明显差异,提示正弦电磁场就提升青年大鼠骨密度的效果而言,股骨优于腰椎骨。电磁场干预后,股骨并没有明显变长或增粗,提示正弦电磁场可有效而安全地增加骨密度。
骨生物力学是在工程力学理论的基础上,对骨组织在外界作用下的力学特性以及骨在受到外力后产生的生物效应进行研究,它是客观评价骨质量的一种方法[13]。骨的整体性能由骨的微结构、几何形态和材料力学性能等方面决定。其中,骨的几何形态决定了骨的结构力学特性,而骨的微结构决定了骨的材料学性能[14]。骨常用的结构力学指标最大载荷反映骨的整体抗骨折能力;材料力学指标弹性模量和屈服强度不受骨的形状及大小的影响,侧重于反映骨自身的强度和韧性,与骨中矿物质含量和骨密度有密切关系[15]。本研究中施以10 Hz电磁场和40 Hz电磁场的大鼠股骨的最大载荷及屈服强度较对照组均有提高;施以40 Hz电磁场大鼠腰椎骨的最大载荷及弹性模量也有显著提升。从骨的材料力学和结构力学两方面进行性能比较,说明10、40 Hz的1.8 mT正弦交变电磁场可提高青年大鼠的骨强度。
显微CT扫描成像可准确而直观地反映骨微结构的状况,是评价骨质优劣的重要参考之一[16]。本研究中施以10、40 Hz电磁场大鼠胫骨的骨小梁数量、骨体积百分比显著增加,三维重建图和最大纵向剖面图直观地反映出这些大鼠胫骨骨小梁的网状结构交联度显著提升,表现为大鼠骨质更加紧密,骨微结构改善。然而,电磁场干预后,青年大鼠的骨小梁厚度并没有明显增加,提示正弦交变电磁场改善骨微结构是以增加骨小梁的数量来实现的,而非增加骨小梁的厚度。
综上所述,在10 Hz、40 Hz的1.8 mT正弦交变电磁场干预8周后,青年大鼠的骨密度、骨生物力学性能均有明显提升,同时,10 Hz、40 Hz的1.8 mT正弦交变电磁场可有效改善骨微结构、提高骨的质量。本实验所筛选的电磁场频率参数将为骨质疏松症的预防提供重要参考。
| [1] | ALEJANDRO P, CONSTANTINESCU F. A review of osteoporosis in the older adult[J]. Clin Geriatr Med, 2017, 33(1): 27–40. doi:10.1016/j.cger.2016.08.003 |
| [2] | GIORDANO N, BATTISTI E, GERACI S, et al. Effect of electromagnetic fields on bone mineral density and biochemical marker of bone turnover in osteoporosis:a single-blind, randomized pilot study[J]. Curr Therap Res, 2001, 62(3): 187–193. doi:10.1016/S0011-393X(01)80030-8 |
| [3] | WANG Y N, ZHANG W. The effect of plused electromagnetic field on the bone volume of human being[J]. Procidia Technology, 2015, 20: 66–71. doi:10.1016/j.protcy.2015.07.012 |
| [4] | ABRAHAM A C, AGARWALLA A, YADAVALLI A, et al. Microstructural and compositional contributions towards the mechanical behavior of aging human bone measured by cyclic and impact reference point indentation[J]. Bone, 2016, 87: 37–43. doi:10.1016/j.bone.2016.03.013 |
| [5] | OSTERHOFF G, MORGAN E F, SHEFELBINE S J, et al. Bone mechanical properties and changes with osteoporosis[J]. Injury, 2016, 47(Suppl 2): S11–S20. |
| [6] | CAO Z, CHEN Y, CHEN Y, et al. Electromagnetic irradiation may be a new approach to therapy for peri-implantitis[J]. Med Hypotheses, 2012, 78(3): 370–372. doi:10.1016/j.mehy.2011.12.004 |
| [7] | YOON S H, CHEN J, GRYNPAS M D, et al. Prophylactic pamidronate partially protects from glucocorticoid-induced bone loss in the mdx mouse model of Duchenne muscular dystrophy[J]. Bone, 2016, 90: 168–180. doi:10.1016/j.bone.2016.06.015 |
| [8] | JING D, SHEN G, HUANG J, et al. Circadian rhythm affects the preventive role of pulsed electromagnetic fields on ovariectomy-induced osteoporosis in rats[J]. Bone, 2010, 46(2): 487–495. doi:10.1016/j.bone.2009.09.021 |
| [9] | QU C Y, YU S W. The damage and healing of bone in the disuse under mechanical and electro-magnetic loading[J]. Procedia Engineering, 2011, 10(7): 171–176. |
| [10] | ZHOU J, MING L G, GE B F, et al. Effects of 50 Hz sinusoidal electromagnetic fields of different intensities on proliferation, differentiation and mineralization potentials of rat osteoblasts[J]. Bone, 2011, 49(4): 753–761. doi:10.1016/j.bone.2011.06.026 |
| [11] | 高玉海, 甄平, 周建, 等. 不同时间正弦交变电磁场对大鼠骨密度及骨形态计量指标的影响[J]. 中国医学科学院学报, 2014, 36(6): 660–667. GAO Yuhai, ZHEN Ping, ZHOU Jian, et al. Effect of sinusoidal electromagetic field on bone mineral density and histomorphometry of rats at different time points[J]. Acta Academiae Medicinae Sinicae, 2014, 36(6): 660–667. (in Chinese) |
| [12] | LEE J E, JEON H R, PARK J K, et al. Sex differences in the association between stroke and bone mineral density in elderly Koreans:the Korean national health and nutrition examination survey, 2008-2010[J]. Maturitas, 2017, 95: 1–5. doi:10.1016/j.maturitas.2016.10.006 |
| [13] | VANLEENE M, SHEFELBINE S J. Therapeutic impact of low amplitude high frequency whole body vibrations on the osteogenesis imperfecta mouse bone[J]. Bone, 2013, 53(2): 507–514. doi:10.1016/j.bone.2013.01.023 |
| [14] | CORTET B, MARCHANDISE X. Bone microarchitecture and mechanical resistance[J]. Bernard Cortet, 2001, 68(4): 297–305. |
| [15] | 高玉海, 成魁, 葛宝丰, 等. 不同强度正弦交变电磁场对大鼠骨密度及骨形态计量学的影响[J]. 中国骨伤, 2014, 27(11): 933–937. GAO Yuhai, CHENG Kui, GE Baofeng, et al. Effect of different-intensity SEMFs on bone mineral density and histomorphometry in SD rats[J]. China Journal of Orthopaedics and Traumatology, 2014, 27(11): 933–937. (in Chinese) |
| [16] | EHNERT S, FALLDORF K, FENTZ A K. Primary human osteoblasts with reduced alkaline phosphatase and matrix mineralization baseline capacity are responsive to extremely low frequency pulsed electromagnetic field exposure-clinical implication possible[J]. Bone Reports, 2015, 3: 48–56. doi:10.1016/j.bonr.2015.08.002 |




