2. 浙江省人民医院病理科, 浙江 杭州 310014
2. Department of Pathology, Zhejiang Provincial People's Hospital, Hangzhou 310014, China
2010年WHO有关胃神经内分泌肿瘤的定义中,混合性神经内分泌癌是指恶性肿瘤在形态学上形成可识别的腺上皮和神经内分泌细胞两种成分,其中任何一种成分至少占30%以上[1]。但对于在形态学上表现为腺癌,而神经内分泌标志物阳性细胞散在于腺癌中的现象未进行明确定义。胃神经内分泌肿瘤是一组异质性极强的肿瘤,从低度恶性的神经内分泌瘤到高转移性的神经内分泌癌;而普通胃腺癌中的神经内分泌成分对肿瘤进展及预后的影响目前还存有争议。本文结合组织形态学与免疫组织化学染色法对胃腺癌中神经内分泌成分进行观察,并分析其与临床病理指标及患者预后的关系。
1 材料与方法 1.1 材 料标本来源于浙江省人民医院接受根治性手术治疗的240例胃腺癌患者。男性173例,女性67例;年龄(57.5±10.8)岁;组织学分型按Lauren分型结果为肠型131例、弥漫型85例、混合型22例;TNM分期Ⅰ期47例、Ⅱ期63例、Ⅲ期93例、Ⅳ期36例、不明1例。其中200例有完整随访信息,死亡99例,随访时间(50±25)个月。
依据HE切片选择肿瘤主体部位制备组织芯片,每份标本选择一个直径为1 mm的肿瘤组织,加入到事先准备好的空白受体蜡块中,重新注蜡,制备成每个蜡块包含42例组织的组织芯片。
1.2 检测试剂嗜铬素A(chromogranin A,CgA)抗体购自丹麦DAKO公司(兔单克隆抗体,1∶10 000稀释),突触素(synaptophysin,Syn)购自美国Epitomics公司(鼠单克隆抗体,1∶600稀释),促泌素(secretagogin,SCGN)系浙江大学医学院蛋白质组学重点实验室(兔单克隆抗体,1∶2000稀释)自制。二抗采用的是通用型二步法检测试剂盒PV-9000,购自北京中杉金桥生物技术有限公司。
1.3 患者一般情况及临床病理分析因素①患者年龄:分为≤60岁及>60岁;②患者性别;③肿瘤部位:分为贲门部、胃体部、胃角部、胃窦部及其他;④肿瘤Lauren分型:分为肠型、弥漫型及混合型;⑤肿瘤组织学类型:分为管状腺癌、黏液腺癌、印戒细胞癌及其他;⑥肿瘤组织学分化程度:分为低级别和高级别;⑦肿瘤浸润深度:分为浆膜内和浆膜外;⑧肿瘤淋巴结转移;⑨肿瘤远处转移;⑩肿瘤TNM分期。
1.4 神经内分泌标志物表达检测采用二步法免疫组织化学染色法检测胃神经内分泌分化经典标志物CgA、Syn及新兴神经内分泌标志物SCGN。具体步骤如下:将组织芯片切成4 μm厚的白片,脱蜡至水,3%过氧化氢甲醇15 min,高压修复2 min,10%小羊血清非特异性抗原封闭,一抗4 ℃冰箱孵育过夜,二抗增强剂37 ℃孵育10 min后再加二抗工作液37 ℃孵育30 min,DAB染色3 min后流水终止,Gill改良苏木精染液复染后脱水封片。过程中芯片出现浮点脱点现象则相关病例信息缺失。每个病例计数四个低倍视野(×10),当阳性细胞数占总细胞数5%以上时判定为阳性。
1.5 统计学方法
采用IBM SPSS Statistics 21.0软件进行统计学分析。连续变量(如年龄和随访时间)用均数±标准差( ±s)表示。组间构成比比较采用χ2检验或Fisher's精确检验法。用Kaplan-Meier法进行单因素生存分析,log-rank法进行差异显著性检验,并绘制生存曲线。将单因素分析对预后有统计学意义的因素再纳入多因素Cox比例风险模型进行分析,P<0.05为差异具有统计学意义。
±s)表示。组间构成比比较采用χ2检验或Fisher's精确检验法。用Kaplan-Meier法进行单因素生存分析,log-rank法进行差异显著性检验,并绘制生存曲线。将单因素分析对预后有统计学意义的因素再纳入多因素Cox比例风险模型进行分析,P<0.05为差异具有统计学意义。
在240份胃腺癌标本中,组织学分化程度为低级别者69份,高级别者163份,不明8份;浸润深度局限于浆膜内138份,浸润至浆膜外98份,不明4份;无淋巴结转移者92份,有转移者147份,不明1份;无远处转移者196份,有转移者43份,不明1份。
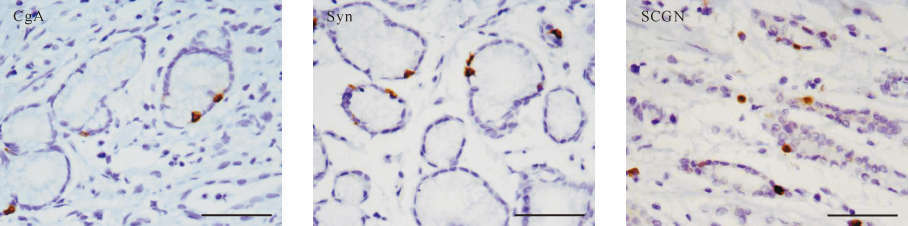
神经内分泌标志物CgA阴性196份,阳性44份;Syn阴性205份,阳性35份;SCGN阴性159份,阳性32份。CgA、Syn、SCGN阳性见图1,三者之间表达一致性良好(均P<0.01)。SCGN阴性共159份,同时表现为CgA阴性者147份,Syn阴性者147份;SCGN阳性共32份,同时表现为CgA阳性者23份,Syn阳性者14份。
|
| 图1 神经内分泌分化免疫组织化学染色示例 Fig.1 Immunohistochmical staining of neuroendocrinemarkers 腺管中散在的棕褐色着色的细胞为免疫组织化学染色阳性细胞.CgA:嗜铬素A; Syn:突触素; SCGN:促泌素.标尺=50 μm. |
观察各神经内分泌标志物与患者年龄、性别、肿瘤部位和Lauren分型、组织学类型、组织学分化程度、肿瘤浸润深度、淋巴结转移、远处转移及TNM分期之间的关系,结果提示Syn阳性分布没有部位差异,但SCGN阳性细胞最多见于贲门部而最少见于胃角部;CgA阳性与所有临床病理指标均不相关(均P>0.05),Syn阳性时肿瘤浸润深度达浆膜外者较多(P=0.042),SCGN阳性时发生淋巴结转移者较多(P=0.047),见表1。当结合CgA、Syn、SCGN,只要其中任一阳性即认为存在神经内分泌成分,其与各临床病理指标间均无相关性(均P>0.05)。
| 变量 | CgA | Syn | SCGN | |||||
| 阴性 | 阳性 | 阴性 | 阳性 | 阴性 | 阳性 | |||
| 患者年龄(岁) | ||||||||
| <60 | 106 | 26 | 114 | 18 | 89 | 19 | ||
| ≥60 | 89 | 18 | 90 | 17 | 70 | 13 | ||
| 患者性别 | ||||||||
| 男性 | 137 | 36 | 147 | 26 | 116 | 26 | ||
| 女性 | 59 | 8 | 58 | 9 | 43 | 6 | ||
| Lauren分型 | ||||||||
| 肠型 | 108 | 23 | 113 | 18 | 87 | 16 | ||
| 弥漫型 | 69 | 16 | 73 | 12 | 59 | 13 | ||
| 混合型 | 17 | 5 | 18 | 4 | 13 | 3 | ||
| 组织学分级 | ||||||||
| 低级别 | 55 | 14 | 58 | 11 | 43 | 11 | ||
| 高级别 | 133 | 30 | 141 | 22 | 111 | 20 | ||
| 肿瘤直径(cm) | ||||||||
| <3 | 55 | 9 | 57 | 7 | 43 | 11 | ||
| 3~6 | 97 | 23 | 104 | 16 | 81 | 13 | ||
| >6 | 43 | 11 | 43 | 11 | 33 | 8 | ||
| 组织学类型 | ||||||||
| 管状腺癌 | 135 | 26 | 141 | 20 | 112 | 18 | ||
| 其他 | 61 | 18 | 64 | 15 | 47 | 14 | ||
| 浸润深度 | ||||||||
| 浆膜内 | 116 | 22 | 123* | 15 | 86 | 17 | ||
| 浆膜外 | 76 | 22 | 78 | 20 | 69 | 15 | ||
| 淋巴结转移 | ||||||||
| 无 | 77 | 15 | 79 | 13 | 64 Δ | 7 | ||
| 有 | 119 | 28 | 126 | 21 | 94 | 25 | ||
| 远处转移 | ||||||||
| 无 | 161 | 35 | 167 | 29 | 133 | 25 | ||
| 有 | 34 | 9 | 37 | 6 | 25 | 7 | ||
| TNM分期 | ||||||||
| Ⅰ期 | 39 | 8 | 38 | 9 | 28 | 6 | ||
| Ⅱ期 | 52 | 11 | 55 | 8 | 46 | 4 | ||
| Ⅲ期 | 74 | 19 | 79 | 14 | 65 | 15 | ||
| Ⅳ期 | 30 | 6 | 32 | 4 | 19 | 7 | ||
| 与浆膜外比较,*P<0.05;与有淋巴结转移比较,ΔP<0.05. | ||||||||
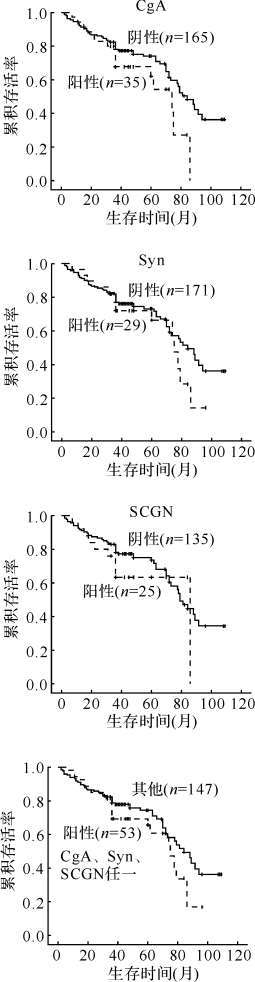
240例检测了CgA、Syn的患者中有完整随访信息者200例,191例检测了SCGN的患者中有完整随访信息者160例。对免疫组织化学染色结果进行单因素生存分析结果表明,在胃腺癌患者中,CgA阳性患者与阴性患者预后差异无统计学意义(P=0.092),但CgA阳性患者预后有更差趋势;而Syn阳性(P=0.281)和SCGN阳性(P=0.332)与患者累积存活率无关;三者任一指标阳性与其他胃腺癌患者累计存活率差异无统计学意义(P=0.185),见图2。
|
| 图2 胃腺癌组织CgA、Syn、SCGN阳性与否患者累积存活率比较 Fig.2 The prognostic significance of neuroendocrine biomarkers in gastric adenocarcinoma CgA:嗜铬素A; Syn:突触素; SCGN:促泌素. |
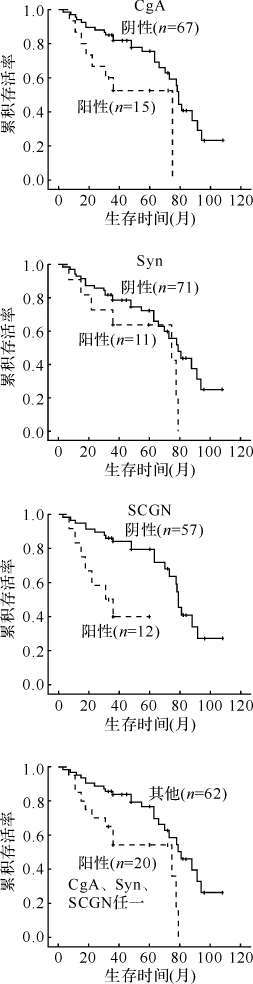
在Lauren分型为弥漫型患者中CgA、SCGN阳性者累积存活率不如CgA、SCGN阴性者(P=0.019、0.001),而Syn阳性与否患者累积存活率差异无统计学意义(P=0.102);CgA、Syn、SCGN任一阳性患者累积存活率低于其他患者(P=0.006),见图3。在Lauren分型肠型和混合型患者中,CgA、Syn、SCGN阳性与否累积存活率差异均无统计学意义(均P>0.05)。
|
| 图3 胃腺癌Lauren分型弥漫型患者CgA、Syn、SCGN阳性与否患者累积存活率比较 Fig.3 The prognostic significance of neuroendocrine biomarkers in Lauren diffuse type of gastric adenocarcinoma CgA:嗜铬素A; Syn:突触素; SCGN:促泌素. |
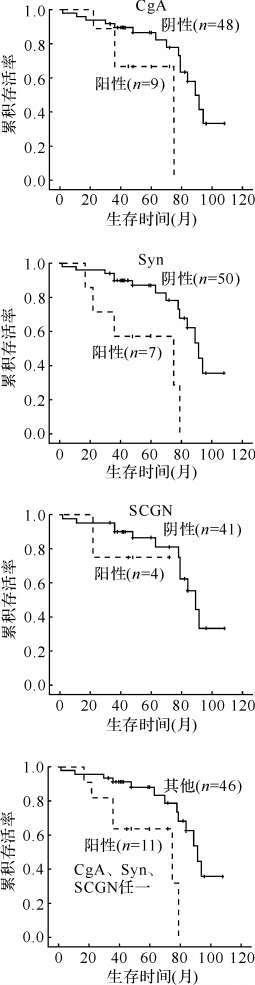
TNM分期Ⅱ期63例患者获随访信息57例。TNM分期Ⅱ期患者中,CgA、Syn阳性患者累积存活率不如CgA、Syn阴性患者(P=0.049、0.002),但SCGN阳性与否患者累积存活率差异无统计学意义(P=0.529);CgA、Syn、SCGN任一阳性患者累积存活率低于其他患者(P=0.006),见图4。
|
| 图4 胃腺癌TNM分期Ⅱ期患者CgA、Syn、SCGN阳性与否患者累积存活率比较 Fig.4 The prognostic significance of neuroendocrine biomarkers in TNM Ⅱstage of gastric adenocarcinoma CgA:嗜铬素A; Syn:突触素; SCGN:促泌素. |
TNM 分期Ⅱ期患者单因素分析具有预后意义的因素还有年龄、肿瘤浸润深度,与CgA、Syn阳性一并纳入多因素Cox比例风险模型,并将性别作为校正因素,结果显示年龄、Syn阳性是患者独立的预后指标,见表2。如果只将性别、年龄、肿瘤浸润深度和CgA、Syn、SCGN任一阳性纳入多因素Cox比例风险模型,则年龄(RR=2.989,95%CI:1.138~7.852,P=0.026)和CgA、Syn、SCGN任一阳性(RR=4.631,95%CI:1.526~14.055,P=0.007)为独立的预后指标。
| 变量 | β值 | RR值 | 95%CI | P值 | |
| 年龄 | 1.045 | 2.843 | 1.082 | 7.469 | 0.034 |
| Syn阳性 | 1.665 | 5.287 | 1.705 | 16.398 | 0.004 |
尽管神经内分泌肿瘤是低到中度恶性的肿瘤,但是其中的神经内分泌癌却是极度恶性,较普通腺癌表现为更高的临床分期和较早发生淋巴结转移及远处转移[2, 3]。由于在肿瘤发生过程中存在异质性,因此在普通腺癌中也会出现具有神经内分泌分化特点的肿瘤细胞,这些细胞与其他肿瘤细胞有着同样的克隆起源[4],但胃腺癌中神经内分泌分化是否能做为一个预后指标尚无定论。
神经内分泌分化的定义往往依赖于神经内分泌标志物的免疫组织化学染色检测,经典的胃肠神经内分泌标志物包括CgA和Syn,SCGN作为一个新兴的神经内分泌标志物正越来越受到关注。SCGN是由Wagner等[5]利用免疫筛选技术从人胰腺β细胞cDNA文库中筛选出来的一个新基因,在正常神经内分泌组织包括胃肠道、胰腺中的神经内分泌细胞有表达,其表达与CgA、Syn等有良好的一致性。本研究结果也提示SCGN的表达与CgA、Syn有着较好的一致性。同时SCGN表达时,淋巴结转移发生率较高,这可能与胃腺癌中神经内分泌细胞可促进血管内皮细胞生长因子的表达,并因此促进淋巴结转移发生有关[6]。
虽然WHO将神经内分泌标志物阳性率30%作为一个临界点来定义混合性神经内分泌癌,但其必须具有明确的神经内分泌形态及相关标志物的表达。在本研究标本中,CgA、Syn、SCGN阳性率30%以上均有几例,但其中阳性细胞散在分布于明确的腺管中,并不形成巢团状结构,在WHO分类中未对此种情况进行单独命名。有文献报道利用免疫组织化学染色和电镜下免疫金标记法,发现在胃腺癌中高达69.2%的标本中存在CgA表达[7]。Yao等[8]运用免疫组织化学染色检测CgA,发现39.6%胃腺癌患者存在CgA表达,而且这些神经内分泌细胞比正常黏膜上皮分泌较多的激素产物。
TNM分期Ⅱ期患者的术后辅助治疗一直有争议。有研究认为在术前新辅助治疗后若残留的肿瘤中存在神经内分泌细胞,患者预后较差[9]。从本文研究结果看,当胃腺癌中出现5%以上的神经内分泌分化细胞时,预示TNM分期Ⅱ期胃癌患者的预后不佳,而且这是一个独立预后指标,有助于判断TNM分期Ⅱ期患者是否进行术后辅助治疗。弥漫型胃腺癌肿瘤细胞间缺乏细胞连接,一般不形成腺管,分化较差,通常TNM分期较高,多见于年轻女性[10],其预后往往较肠型差。本研究结果表明,在弥漫型胃腺癌中神经内分泌成分的存在是预后的不利因素。
综上所述,SCGN是一个与CgA及Syn有着高度一致性的神经内分泌标志物。神经内分泌成分的出现与肿瘤浸润深度及淋巴结转移呈正相关,在TNM分期Ⅱ期胃腺癌和Lauren分型弥漫型胃腺癌中是相对不利的预后指标。
| [1] | BUSMAN F T, CANNIER F, HUMAN R H, et al. WHO Classifictation of Tumours of the Digestive system[M]. 4th ed. Lyon:International Agency for Research on Cancer, 2010:45-80. |
| [2] | JIANG S X, MIKAMI T, UMEZAWA A, et al. Gastric large cell neuroendocrine carcinomas:a distinct clinicopathologic entity[J]. Am J Surg Pathol, 2006, 30(8):945-953. |
| [3] | KUBOTA T, OHYAMA S, HIKI N, et al. Endocrine carcinoma of the stomach:clinicopathological analysis of 27 surgically treated cases in a single institute[J]. Gastric Cancer, 2012, 15(3):323-330. |
| [4] | WANG L L, YAO G Y, ZHAO Z S, et al. Clonality analysis of neuroendocrine cells in gastric adenocarcinoma[J]. World J Gastroenterol, 2013, 19(32):5340-5346. |
| [5] | WAGNER L, TEMPLE E, REINING G, et al. Culture of human insulinoma cells:development of a neuroendocrine tumor celland human pancreatic islet cell-specific monoclonal antibody[J]. J Endocrinol, 1998, 156(3):469-476. |
| [6] | EREN F, CELIKEL C, GVLLVOLU B. Neuroendocrine differentiation in gastric adenocarcinomas; correlation with tumor stage and expression of VEGF and p53[J]. Pathol Oncol Res, 2004, 10(1):47-51. |
| [7] | MARTINSEN T C, SKOGAKER N E, FOSSMARK R, et al. Neuroendocrine cells in diffuse gastric carcinomas:an ultrastructural study with immunogold labeling of chromogranin A[J]. Appl Immunohistochem Mol Morphol, 2010, 18(1):62-68. |
| [8] | YAO G Y, ZHOU J L, LAI M D, et al. Neuroendocrine markers in adenocarcinomas:an investigation of 356 cases[J]. World J Gastroenterol, 2003, 9(4):858-861. |
| [9] | WANG K L, YANG Q, CLEARY K R, et al. The significance of neuroendocrine differentiation in adenocarcinoma of the esophagus and esophagogastric junction after preoperative chemoradiation[J]. Cancer, 2006, 107(7):1467-1474. |
| [10] | QIU M Z, CAI M Y, ZHANG D S, et al. Clinicopathological characteristics and prognostic analysis of Lauren classification in gastric adenocarcinoma in China[J]. J Transl Med, 2013, 11:58. |




