不同形式的突触活动可以引起突触效能的改变[1],出现长时间的效能增强,即长时程增强(long-term potentiation,LTP)。LTP是大脑内信息储存和记忆形成的细胞机制。一般来说,根据LTP的持续时间,将各种条件下形成的LTP分为几个时相,LTP形成后1 h内称为早时相LTP,持续时间长于3 h的称为晚时相LTP。有研究表明,晚时相LTP在海马长期记忆的巩固中具有非常重要的作用[2]。但是还有一些研究表明,LTP可被诱导之后的神经元的活动所翻转,使LTP的幅度降低或彻底恢复到基线水平[3]。这种LTP幅度的减小或者LTP的翻转又称为去强化[3]。研究表明只有在LTP诱导后的一个短暂的时间窗内,给予低频刺激才能有效翻转LTP,并且翻转的程度和诱导LTP的刺激与翻转刺激之间的时间间隔有关,该间隔增大,LTP的翻转程度降低[3]。本课题组之前的研究表明,LTP诱导后2 h给予高强度的双脉冲低频刺激(high-intensity paired-pulse low frequency stimulation,HI-PP-LFS)可以部分翻转晚时相LTP,并且这种翻转依赖于N-甲基-D-天门冬氨酸受体NR2A亚基(NR2A-N-methy-D-aspartate receptors,NR2A-NMDARs)[4]。以前的研究表明,新蛋白质的合成是LTP维持所必需的[5]。应用蛋白合成抑制剂,LTP的幅度很快降低至基线水平。而晚时相LTP维持以及去强化和蛋白合成之间的关系目前还不清楚。
去强化具有非常重要的意义,有学者认为去强化可以阻止神经发育过程中病理性突触的稳定,而且去强化还参与了神经环路的细化过程[6],在这其中晚时相LTP翻转的研究具有更大的吸引力,它可能是消除病理性记忆(如成瘾记忆和痛觉记忆)的机制之一[6, 7]。目前有关晚时相LTP翻转的机制研究报道甚少。为了判断LTP翻转与蛋白质合成之间的关系,本研究采用成年大鼠海马脑组织切片标本,在LTP诱导之前和诱导之后给予蛋白合成抑制剂,探讨新蛋白合成在CA1区LTP和去强化中的作用。
1 材料与方法 1.1 实验动物健康成年雄性SD大鼠,体质量160~200 g,由西安交通大学实验动物中心提供。大鼠在12 h/12 h明暗交替的环境中饲养,自由取食饮水。实验遵从西安交通大学动物中心的动物伦理规定以及相关条例,减少动物使用数量以及减轻动物的痛苦。
1.2 试剂和仪器人工脑脊液配方如下:氯化钠溶液124 mmol/L、氯化钾溶液4.4 mmol/L、磷酸二氢钠溶液 1 mmol/L、硫酸镁溶液1.3 mmol/L、氯化钙溶液 2.5 mmol/L、碳酸氢钠溶液26 mmol/L、葡萄糖溶液10 mmol/L,渗透浓度为305~310 mmol/L,以上试剂购自西安化学试剂厂;DMSO、茴香霉素和放线菌酮购自美国Sigma公司,茴香霉素和放线菌酮溶于0.017% DMSO。
SEN-7103电子刺激器、SS-202J隔离器、VC-11记忆示波器、MEZ-8301微电极放大器和PF5-1微电极推进器均购自日本光电公司;ML-820 Powerlab 200数据采集器购自澳大利亚Powerlab公司;CAT 2001微电极拉制仪购自日本成茂株式会社;MA752型振动切片机购自英国Campden Instrument 公司;减震台、屏蔽箱购自西安交通大学修配厂。
1.3 电生理实验大鼠乙醚麻醉后迅速断头,取出全脑置于冰水降温的解剖台上,用冰预冷的、混合气(95 % 氧气和 5 %二氧化碳)饱和的人工脑脊液冲洗脑,使其快速降温。剥离出含有海马的脑组织,使用振动切片机将海马垂直于其长轴切成400 μm厚的脑片,迅速将脑片移至气—液界面式记录浴槽内孵育2 h。记录槽温度控制在(28±1) ℃。记录玻璃微电极(冲灌2 mol/L 氯化钠溶液,1~3 MΩ)置于海马CA1区辐射层,记录细胞外场电位(field excitatory postsynaptic potential)。双极刺激电极置于海马CA1区Schaffer传入纤维。刺激引起的诱发反应由记录电极输入微电极放大器,同时使用数据采集系统采集并储存于计算机中。
首先描绘强度—反应曲线,界定刺激强度。刺激频率为0.1 Hz、刺激持续时间0.2 ms,逐渐增加刺激强度,相邻两个刺激之间的间隔为1 min,描记强度—反应曲线,以能诱出40%~50%最大反应的强度作为刺激强度,刺激波宽为0.2 ms。实验中所使用的刺激参数:①基线刺激:刺激频率为0.017 Hz,记录诱发反应至少30 min,如反应的波幅稳定(变化<10%)则给予条件刺激。②诱导LTP的高频刺激 (high-frequency stimulation):共6组θ波刺激(theta burst stimulation),组间隔为10 min。每组4串,串间隔10 s,每串5小串,间隔200 ms,每小串4个脉冲,脉冲间隔10 ms(图1A);刺激强度及波宽与测试刺激一致。高频刺激后,再使用基线刺激参数给予刺激。③双脉冲低频刺激(paired-pulse low frequency stimulation,PP-LFS):共2组,组间隔10 min,每组900对,双脉冲间隔为200 ms,双脉冲频率1 Hz,刺激强度及波宽与基线刺激一致(图1B)。④ HI-PP-LFS:共2组,每组900对双脉冲,组间隔10 min,双脉冲间隔为200 ms,双脉冲频率为1 Hz,刺激强度是测试刺激的2倍,刺激波宽与测试刺激一致(图1B)。取每相邻3 min的场电位斜率平均值作统计学处理以及点线图绘制。

|
| A:诱导长时程增强的高频刺激参数模式图,由6个间隔10 min的θ波刺激组成;B:诱导去强化的双脉冲低频刺激(PP-LFS)和高强度双脉冲低频刺激(HI-PP-LFS)模式图,由两个间隔10 min的双脉冲低频刺激组成. 图1 刺激参数模式示意图 Fig.1 Schematic diagram of stimulation protocols |
为研究PP-LFS对LTP的翻转作用,随机选取31只SD大鼠,分为对照组(在LTP诱导后不给予翻转刺激,仅给予基线刺激,n=11)、PP-LFS组(在LTP诱导后2 h给予PP-LFS,n=10)和HI-PP-LFS组(在LTP诱导后2 h给予HI-PP-LFS,n=10)。
为研究LTP诱导前蛋白合成抑制剂对去强化作用,在LTP诱导前30 min给予茴香霉素和放线菌酮,后者在实验过程中持续存在。随机选取40只SD大鼠,每组10只,分为对照组(正常人工脑脊液孵育脑片)、溶媒对照组(人工脑脊液中加入0.017% DMSO)、茴香霉素组(人工脑脊液中加入25 μmol/L 茴香霉素溶液)和放线菌酮组(人工脑脊液中加入60 μmol/L 放线菌酮溶液)。
为研究LTP诱导后蛋白合成抑制剂对去强化作用,在LTP诱导后90 min给予茴香霉素和放线菌酮。随机选取24只SD大鼠,每组6只,分组同上。另随机选取36只SD大鼠,每组9只,测试蛋白合成抑制剂和DMSO是否对基础突触传递有影响。
1.5 统计学方法
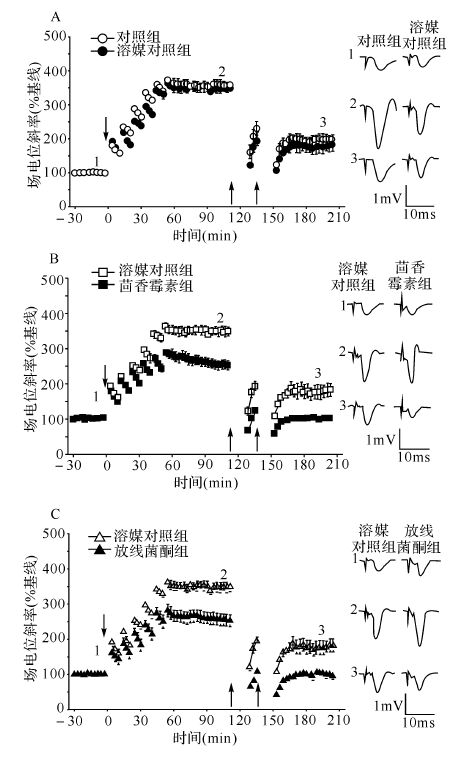
采用统计软件SPSS 16.0分析数据,所有数据均以均数±标准误(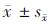 )表示。两组间的比较采用t检验,多组比较采用单因素方差分析。以P<0.05为差异有统计学意义。
)表示。两组间的比较采用t检验,多组比较采用单因素方差分析。以P<0.05为差异有统计学意义。
给予高频刺激诱导稳定的LTP,结果表明高频刺激可诱导出稳定的LTP,在高频刺激刺激后2 h场电位斜率增大为基线的(332.3 ± 21.4)% (P<0.001)。在LTP诱导后2 h给予PP-LFS,场电位斜率明显减小,但很快恢复至PP-LFS刺激之前的水平,即PP-LFS不能翻转晚时相LTP。在第二组PP-LFS后30 min,场电位斜率为基线的(346.2 ± 26.3)%,只接受高频刺激的对照组场电位斜率为基线的(345.8 ± 21.1)%,两组差异无统计学意义(P>0.05)。见图2。
|
| 向下箭头表示给予高频刺激,向上箭头表示给予翻转刺激.1、2、3分别表示该时间记录的原始场电位波形. 图2 两组PP-LFS不能翻转晚时相LTP Fig.2 PP-LFS does not reverse late-phase LTP |
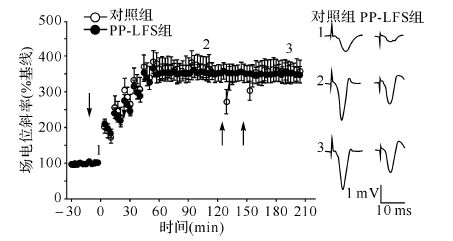
在LTP诱导后2 h给予HI-PP-LFS,结果如图3,两组LTP均被翻转。第一组HI-PP-LFS后场电位短暂减小;第二组HI-PP-LFS刺激后场电位斜率减小到接近基线水平,之后场电位斜率增加,但始终没有达到HI-PP-LFS刺激之前的水平。场电位斜率在第二组HI-PP-LFS后30 min是基线的(207.1±21.6)%,低于HI-PP-LFS刺激前的强化水平[(346.2±26.3)%,P<0.001]。使用HI-PP-LFS后的场电位斜率为基线的(345.8±21.1)%,也小于未给予翻转刺激的对照组(P<0.001)。这一结果表明,HI-PP-LFS可诱导晚时相LTP的去强化,但这种去强化并不完全,因而是晚时相LTP的部分翻转。实验中这种部分翻转至少维持了30 min。HI-PP-LFS引起晚时相LTP的翻转率是59.8%。
|
| 向下箭头表示给予高频刺激,向上箭头表示给予翻转刺激.1、2、3分别表示该时间记录的原始场电位波形. 图3 HI-PP-LFS可部分翻转晚时相LTP Fig.3 HI-PP-LFS partially reversed late-phase LTP |
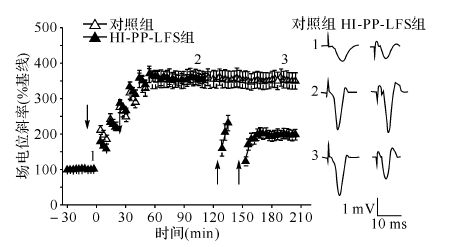
溶媒对照组场电位斜率在翻转刺激前和刺激后45 min分别为基线的(340.2±16)%和(178.6±14.2)% ,与对照组差异均无统计学意义(均 P>0.05),见图4A,提示0.017%DMSO溶液对LTP的维持和翻转均没有影响。茴香霉素组高频刺激依然可以诱导出LTP,但LTP的幅度比溶媒对照组减小。在LTP诱导后2 h给予翻转刺激HI-PP-LFS,晚时相LTP可被翻转至基线水平,见图4B。 LTP诱导后60 min和给予HI-PP-LFS后45 min,场电位斜率分别是(253.2±13.0)%和(102.4±11.4)%,LTP幅度小于溶媒对照组[场电位斜率分别是(340.2±16.0)% 和 (178.6±14.2)% ,均P<0.001]。放线菌酮组实验结果与茴香霉素组相似 (图4C),LTP诱导后60 min和给予HI-PP-LFS后45 min,场电位斜率分别为(250.7±15.3)%和(100.2±9.0)%,均小于溶媒对照组(均P<0.001)。
|
| A:溶媒对照组晚时相LTP的诱导及翻转对场电位斜率没有影响; B:茴香霉素组LTP诱导后场电位斜率幅度减小,翻转刺激可使晚时相LTP诱导的场电位斜率减小到基线水平;C:放线菌酮组LTP诱导和翻转刺激对场电位斜率的影响与茴香霉素组相同. 向下箭头表示给予高频刺激,向上箭头表示给予翻转刺激,横线表示给予蛋白合成抑制剂,1、2和3分别表示该时间记录的原始场电位波形. 图4 LTP诱导前给予蛋白合成抑制剂对晚时相LTP诱导与翻转的影响 Fig.4 The effect of protein synthesis inhibitors on late-phase LTP induction and reversal when applied prior to tetanus |
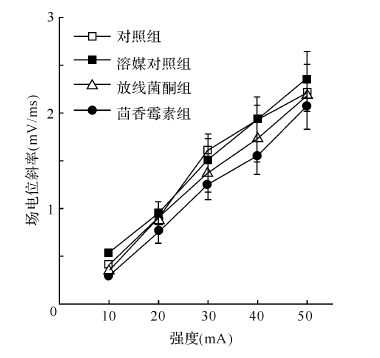
可见,在LTP诱导前给予蛋白合成抑制剂,LTP诱导后60 min LTP的幅度分别减少为溶媒对照组的76.82%和76.10%;而在LTP诱导前给予蛋白合成抑制剂,HI-PP-LFS可将LTP翻转至基线水平。同时,茴香霉素组、放线菌酮组和溶媒对照组的强度—反应曲线差异无统计学意义(P>0.05),见图5。提示无论是蛋白合成抑制剂或其溶媒DMSO都对基础突触传递没有影响。
|
| 图5 海马脑片CA1区刺激强度—场电位斜率关系曲线 Fig.5 Stimulation intensity-slope of field excitatory postsynaptic potential curve in CA1 of hippocampal slices of rats |
以上结果表明,在给予LTP诱导刺激之前给予蛋白合成抑制剂可明显减小LTP,其幅度减少为溶媒对照组的76%左右,而且此时高强度双脉冲低频刺激可以完全翻转晚时相LTP。
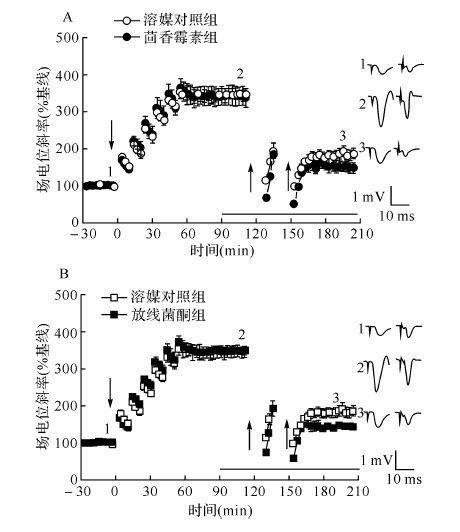
随后,在LTP诱导之后使用了蛋白合成抑制剂,结果如图6所示,茴香霉素组LTP的幅度在给予茴香霉素30 min没有变化(图6A)。在给予HI-PP-LFS前后各45 min,场电位斜率分别为基线的(335.2±24.9)% 和(149.6±13.5)%,差异有统计学意义(P<0.001),表明该刺激依然可以部分翻转LTP。可见在LTP诱导后给予蛋白合成抑制剂,HI-PP-LFS依然可引起晚时相LTP的部分翻转。如图6B所示,放线菌酮组实验结果与茴香霉素相似 (P<0.001)。场电位斜率在给予HI-PP-LFS前后各45 min分别是(349.3±11.5)%和(140.5±7.9)%。上述结果表明,在LTP诱导后90 min给予蛋白合成抑制剂,HI-PP-LFS依然可诱导晚时相LTP的部分翻转。
|
| A:茴香菌素组HI-PP-LFS能引起更强的晚时相LTP的部分翻转;B:放线菌酮组LTP没有影响,HI-PP-LFS 依然部分翻转了晚时相LTP. 向下箭头表示给予高频刺激,向上箭头表示给予翻转刺激,横线表示给予蛋白合成抑制剂,1、2、3分别表示该时间记录的原始场电位的波形. 图6 蛋白合成抑制剂对晚时相LTP维持及翻转的影响 Fig.6 The effect of protein synthesis inhibitors on maintenance and reversal of late-phase LTP,when applied 90 min after LTP induction |
LTP具有突触特异性、协同性和持续性的特点,这些特点使得LTP成为一种非常重要的记忆储存模型[8]。目前的研究表明,虽然LTP具有持续性的特点,但随后神经元的活动可以使其翻转。1976年文献首次报道了去强化现象,即LTP可被后续神经元的活动翻转的现象[9]。Hesse等[9]发现,在海马CA1区LTP诱导后给予诱发癫痫的电刺激可以明显减小LTP。随后的研究还发现了去强化的特点。其一,给予翻转刺激的时间对去强化的诱导非常重要。在LTP诱导后30 min内给予翻转刺激才能有效诱导去强化[10],即时间窗的概念,给予在时间窗内的翻转刺激才能引起去强化。其二,去强化的幅度与LTP的诱导刺激和翻转刺激之间的时间间隔呈反变关系[3]。而在时间窗之外LTP能否被翻转,或者说晚时相LTP能否被翻转并不清楚。之前的一些研究表明,在成年大鼠海马CA1区PP-LFS可诱导LTP[11],一般认为引起LTP的刺激参数可能是诱发翻转的有效刺激。本研究表明,在LTP诱导后2 h,给予两组间隔10 min的PP-LFS并没有诱导出LTP翻转;我们之前的研究表明,LTP诱导后2 h给予双倍强度的PP-LFS可以部分翻转晚时相LTP[4]。
LTP作为记忆存储的细胞机制,两者有一些相似特征。其一,它们都可以分为两个阶段,记忆分为短期记忆与长期记忆,LTP有早时相LTP和晚时相LTP之分;其二,在它们的不同阶段对新蛋白质合成的依赖性不同,普遍的观点是,短期记忆与早时相LTP是蛋白合成非依赖的,而长期记忆与晚时相LTP是蛋白合成依赖性的。研究中发现,LTP的诱导不需要新蛋白质的合成,但LTP的长时间维持却离不开新蛋白质的合成。Sutton等[12]研究表明,蛋白质合成过程中的转录和翻译在晚时相LTP的维持中均有着重要作用,并且这种新合成的蛋白质来自于新转录的mRNA。新蛋白质的合成在L-LTP的维持中非常重要,抑制蛋白质的合成会影响LTP的维持以及LTP持续过程中多核糖体向活化树突棘的移动[13]。
但是有一些研究提出LTP过程中合成的相关蛋白质只是用来补充突触活动过程中消耗掉的一些蛋白[14]。由于不同的研究存在着实验条件、动物种属和诱导方式等诸多差异,使得至今关于蛋白合成在LTP维持以及去强化中的作用仍无一致结论。
为了判断晚时相LTP维持以及去强化和蛋白合成之间的关系,本研究在LTP诱导前和诱导后的两种不同条件下给予蛋白合成抑制剂,结果表明,在高频刺激诱导LTP之前给予蛋白合成抑制剂,所诱导出的LTP的幅度小于对照组,HI-PP-LFS完全翻转晚时相LTP。但是当LTP诱导90 min后给予蛋白合成抑制剂,LTP的幅度没有变化,HI-PP-LFS依然诱导了晚时相LTP的部分翻转。Fonseca等[14]研究结果表明,在LTP诱导后给予蛋白合成抑制剂对LTP幅度没有影响,他们对这一现象的解释是随后的测试刺激强度在其中发挥着重要作用。研究表明新合成的蛋白质在活动依赖性的突触结构变化中起重要作用,抑制蛋白质的合成,会影响LTP的维持[15]。然而近年来的一些研究表明,在没有新蛋白质合成的情况下,LTP依然能够维持。该研究又引发了蛋白质合成在LTP维持中必要性的讨论。Pang等[16]研究表明,当脑源性神经营养因子存在时,加入蛋白合成抑制剂茴香菌素不影响LTP的稳定,因此提出在有足够脑源性神经营养因子的情况下,LTP可以是蛋白合成非依赖的。本研究在LTP诱导后给予蛋白合成抑制剂,并不影响晚时相LTP的幅度,可能是由于观测和记录的时间仍嫌不足,尚需进一步的实验证实。
总之,无论是否应用蛋白合成抑制剂,HI-PP-LFS均能部分翻转晚时相LTP,表明HI-PP-LFS是诱导LTP翻转的有效刺激;蛋白合成抑制剂在晚时相LTP的诱导和维持以及去强化的诱导中均具有重要作用。
| [1] | ABRAHAM W C, BEAR M F. Metaplasticity:the plasticity of synaptic plasticity[J]. Trends Neurosci, 1996,19(4):126-130. |
| [2] | LYNCH M A. Long-term potentiation and memory[J]. Physiol Rev, 2004,84(1):87-136. |
| [3] | HUANG C C, HSU K S. Progress in understanding the factors regulating reversibility of long-term potentiation[J]. Rev Neurosci, 2001,12(1):51-68. |
| [4] | ZHANG L, MENG K, LI Y H, et al. NR2A-containing NMDA receptors are required for L-LTP induction and depotentiation in CA1 region of hippocampal slices[J]. Eur J Neurosci, 2009,29(11):2137-2144. |
| [5] | GELINAS J N, NGUYEN P V. Beta-adrenergic receptor activation facilitates induction of a protein synthesis-dependent late phase of long-term potentiation[J]. J Neurosci, 2005,25(13):3294-3303. |
| [6] | ZHOU Q, POO M M. Reversal and consolidation of activity-induced synaptic modifications[J]. Trends Neurosci, 2004,27(7):378-383. |
| [7] | 张 莉,韩太真. 长时程增强翻转的研究进展[J]. 生理科学进展, 2010,41(4):275-278. ZHANG Li,HAN Tai-zhen.Progress in research of long-term potentiation reversal[J]. Progress in Physiological Sciences, 2010,41(4):275-278.(in Chinese) |
| [8] | BLISS T V, COLLINGRIDGE G L. A synaptic model of memory:long-term potentiation in the hippocampus[J]. Nature, 1993,361(6407):31-39. |
| [9] | HESSE G W, TEYLER T J. Reversible loss of hippocampal long term potentiation following electronconvulsive seizures[J]. Nature, 1976,264(5586):562-564. |
| [10] | KANG-PARK M H, SARDA M A, JONES K H, et al. Protein phosphatases mediate depotentiation induced by high-intensity theta-burst stimulation[J]. J Neurophysiol, 2003,89(2):684-690. |
| [11] | KEMP N, MCQUEEN J, FAULKES S, et al. Different forms of LTD in the CA1 region of the hippocampus:role of age and stimulus protocol[J]. Eur J Neurosci, 2000,12(1):360-366. |
| [12] | SUTTON M A, SCHUMAN E M. Local translational control in dendrites and its role in long-term synaptic plasticity[J]. J Neurobiol, 2005,64(1):116-131. |
| [13] | ABRAHAM WC. How long will long-term potentiation last?[J]. Philos Trans R Soc Lond B Biol Sci, 2003,358(1432):735-744. |
| [14] | FONSECA R, NAGERL U V, BONHOEFFER T. Neuronal activity determines the protein synthesis dependence of long-term potentiation[J]. Nat Neurosci, 2006,9(4):478-480. |
| [15] | OSTROFF L E, FIALA J C, ALLWARDT B, et al. Polyribosomes redistribute from dendritic shafts into spines with enlarged synapses during LTP in developing rat hippocampal slices[J]. Neuron, 2002,35(3):535-545. |
| [16] | PANG P T, TENG H K, ZAITSEV E, et al. Cleavage of proBDNF by tPA/plasmin is essential for long-term hippocampal plasticity[J]. Science, 2004,306(5695):487-491. |




