2. 浙江大学药学院, 浙江杭州 310058
2. College of Pharmaceutical Sciences, Zhejiang University, Hangzhou 310058, China
聚腺苷二磷酸核糖聚合酶(poly ADP-ribose polymerase,PARP)广泛地存在于多数真核细胞中,PARP通过ADP—核糖单元从烟酰胺腺嘌呤二核苷酸(NAD+)转移到各种受体蛋白的谷氨酸残基上,最后通过一系列的催化调节反应,完成DNA修复过程,为抗癌药物的研发提供了新的方向[1]。因此,在当今肿瘤的临床治疗研究中产生了一种以PARP为靶点的药物联用策略:DNA损伤类化疗药物与PARP抑制剂联用,即在肿瘤细胞DNA损伤的基础上,再对细胞DNA 修复功能进行抑制,从而增强对肿瘤的抑制效果,通过减少化疗药物剂量以减少其不良反应[2, 3]。临床试验表明PARP抑制剂副作用小、抑制效果明显并且短期的肿瘤耐受性好,对于将来癌症的治疗具有广阔的前景。
乳腺癌是严重危害妇女身体健康的常见肿瘤之一。近年来我国乳腺癌发病率呈明显上升趋势,2010年中国肿瘤登记年报显示我国乳腺癌发病率位居女性恶性肿瘤第一位,已成为当前社会的重大公共卫生问题[4]。ABT888是一种强效的PARP抑制剂,是第三代PARP抑制剂的代表。卡铂是第二代铂类,主要引起靶细胞DNA的链间及链内交联,使DNA不能复制而失去活性。临床前和临床研究结果均显示,由于三阴性乳腺癌患者常伴有人类乳腺癌易感基因1的突变和DNA损伤修复机制的异常,而铂类药物作为一种作用于DNA的细胞毒药物,对三阴性乳腺癌有较好的疗效[5, 6, 7]。本研究拟探讨ABT888与常用化疗药卡铂联用对乳腺癌细胞MDA-MB-435s的增殖与凋亡的影响,通过蛋白质印迹法观察细胞凋亡相关蛋白的表达水平,以初步探讨两者合用的可能机制,为乳腺癌的临床治疗提供理论依据。
1 材料与方法 1.1 细胞株和试剂人乳腺癌细胞MDA-MB-435s购自中国科学院上海生命科学研究院细胞资源中心。Leibovitzs L-15培养液、FBS购自美国Gibco公司,卡铂购自中国上海研生实业有限公司,ABT888购自美国Selleck公司,蛋白提取试剂盒购自中国碧云天生物技术研究所,BCA蛋白定量试剂盒购自美国Thermo公司,MTT购自美国Sigma公司,凋亡检测试剂盒购自美国Biovision公司,β-actin、羊抗兔IgG HRP二抗购自美国Santa cruz公司,Bcl-2、Bax、Caspase-3、cleaved(c)-Caspase-3抗体购自美国Cell Signaling Technology公司。
1.2 细胞培养MDA-MB-435s细胞用含10%FBS的Leibovitzs L-15培养液培养,于5%二氧化碳、37 ℃培养箱内培养。
1.3 MTT法检测药物对肿瘤细胞增殖的抑制取对数生长期MDA-MB-435s细胞,以5×103/孔的密度接种于96孔板,培养24 h后加入药物。实验分组:浓度为0、0.25、0.5、1、2、4 μmol/L 的ABT888分别与浓度为0、15、30、60 μg/mL的卡铂联合处理。每组设3个复孔,孵育120 h后,每孔加入6 mg/mL MTT 20 μL,37 ℃孵育4 h,弃上清液,加入150 μL DMSO溶解结晶,测定570 nm处的吸光度值,计算细胞增殖抑制率。抑制率(%)=(对照组吸光度值-实验组吸光度值)/对照组吸光度值×100%。
1.4 流式细胞术检测肿瘤细胞凋亡率将MDA-MB-435s细胞分为ABT888 1 μmol/L、卡铂30 μg/mL和ABT888 1 μmol/L+卡铂30 μg/mL三组培养120 h后,收集细胞,PBS清洗3次,取1×105细胞加入100μL 1×结合缓冲液重悬细胞,加入5 μL Annexin V-FITC和5 μL PI,避光反应20 min,洗净后用流式细胞术检测细胞凋亡率。
1.5 蛋白质印迹法检测细胞凋亡相关的蛋白表达水平蛋白质经12%SDS-PAGE电泳1.5 h后,250 mA 2 h转移至PVDF膜,5%牛血清白蛋白(BSA)封闭1 h,β-actin(1∶3000稀释),Bcl-2、Bax、Caspase-3、c-Caspase-3抗体(均1∶500稀释)4 ℃孵育过夜后PBST洗3次,加入二抗室温孵育1 h,PBST洗3次后作化学发光免疫分析,采用荧光化学发光凝胶成像分析系统检测蛋白水平变化,Image Lab 4.0(beta7)软件对蛋白条带的灰度进行分析。
1.6 统计学方法所有数据应用SPSS 16进行统计学分析,计量资料采用均数±标准差(±s)表示,组间比较采用单因素方差分析,P<0.05为差异有统计学意义。
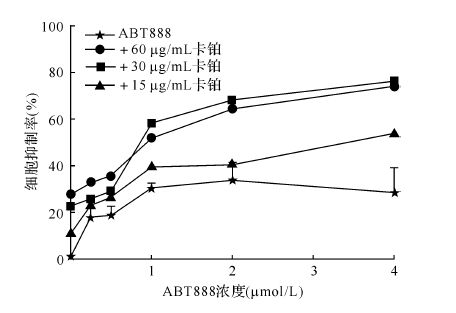
2 结 果 2.1 卡铂与ABT888合用对乳腺癌细胞MDA-MB-435s生长的抑制作用MTT结果显示,不同浓度ABT888与三种浓度卡铂合用MDA-MB-435s细胞抑制率见图1。其中1 μmol/L ABT888 +30 μg/mL卡铂在给药120 h 时MDA-MB-435s细胞抑制率较高,而此时两种药物浓度均低,表现为协同作用。因此,选取1 μmol/L ABT888和30 μg/mL卡铂为最佳给药浓度用于后续实验。
|
| 图1 MTT法检测不同浓度卡铂和ABT888联合处理120 h后MDA-MB-435s细胞抑制率的变化 Fig.1 The inhibition rate of MDA-MB-435s cells 120 h after treatment of combination of carbo and ABT888 with different concentrations detected by MTT |
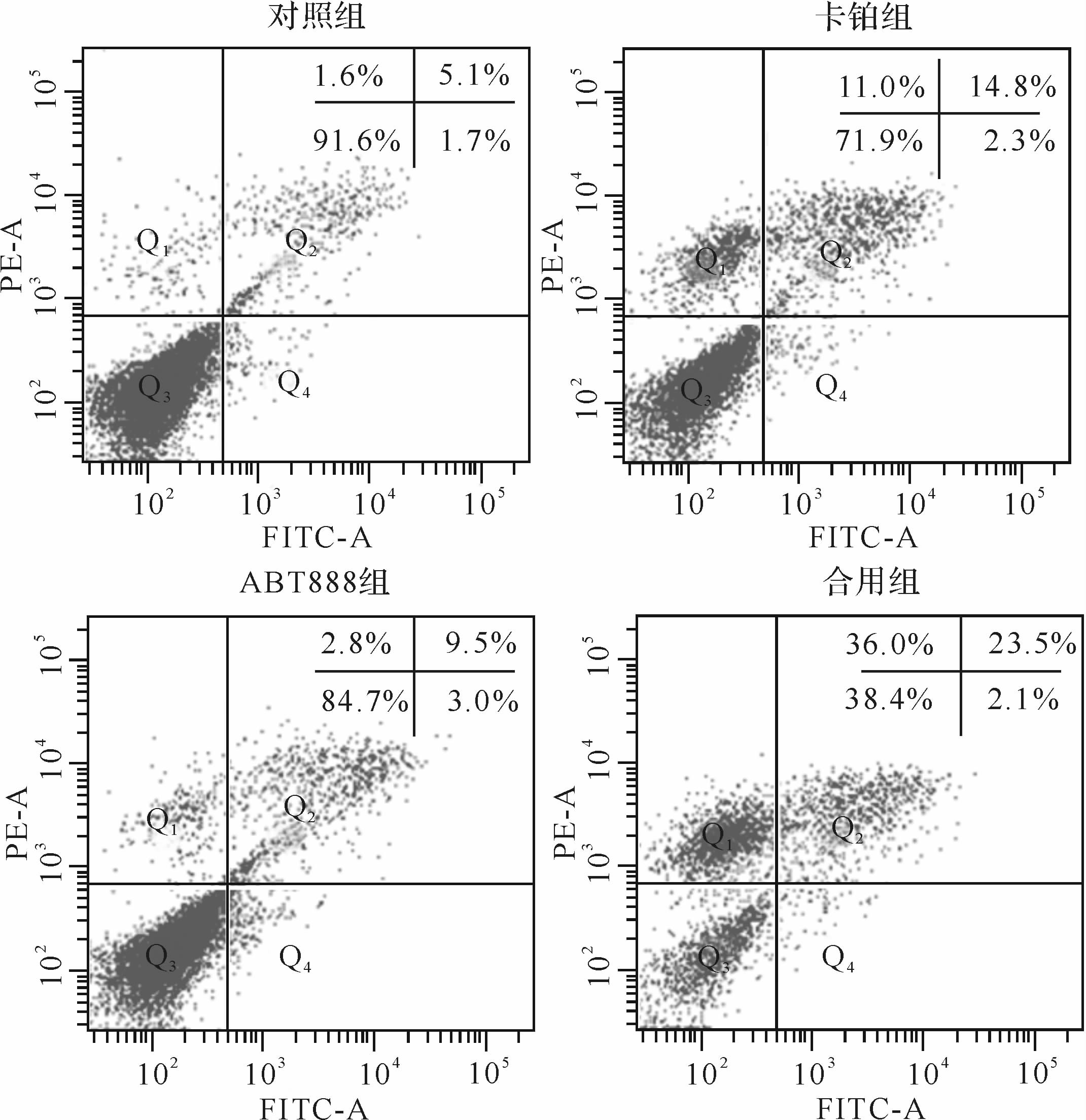
如图2所示,将MDA-MB-435s细胞分成4组:对照组、卡铂组、ABT888组、合用组。作用120 h后,合用组细胞凋亡率(26.3%±1.5%)高于对照组(8.1%±1.5%,P<0.01)、卡铂组(18.6%±1.6%,P<0.01)和ABT888组(14.7%±2.3%,P<0.01)。提示卡铂与ABT888合用可提高MDA-MB-435s细胞凋亡率。
|
| 图中Q1为细胞死亡率,Q2为细胞晚期凋亡率,Q3为细胞存活率,Q4为细胞早期凋亡率;Q2+Q4为细胞凋亡率. 图2 流式细胞术检测卡铂组、ABT888组、合用组MDA-MB-435s细胞凋亡率变化 Fig.2 The effect of carbo,ABT888 and their combination on cell apoptosis rate of MDA-MB-435s |
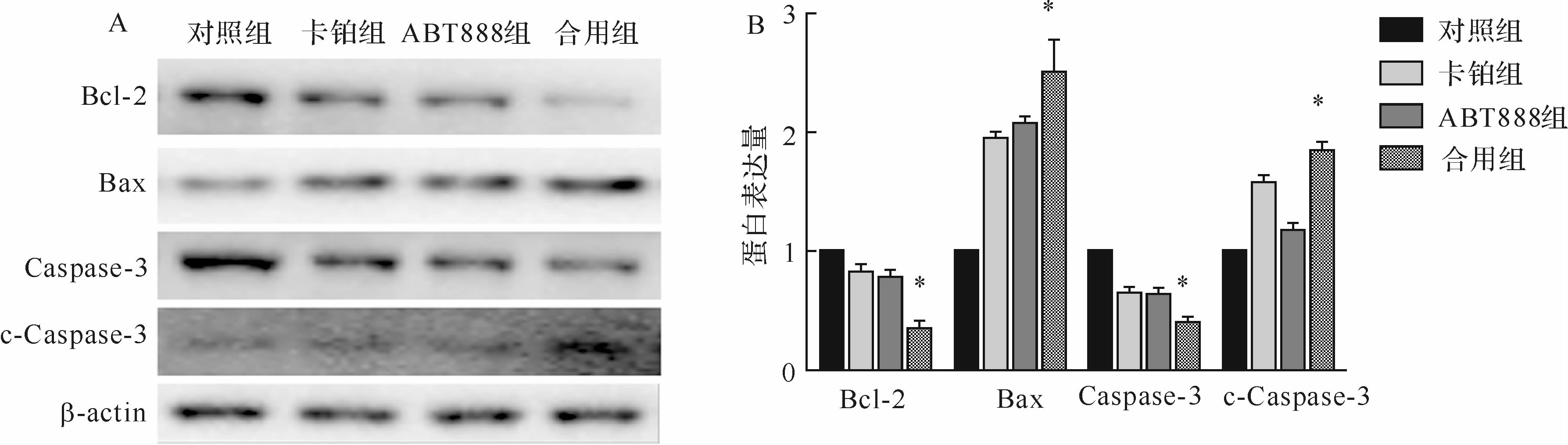
对照组、卡铂组、ABT888组、合用组作用MDA-MB-435s细胞120 h后,合用组抗凋亡蛋白Bcl-2表达低于对照组和卡铂组、ABT888组(均P<0.05),凋亡蛋白Bax的表达高于对照组和卡铂组、ABT888组(均P<0.05),并且合用组Caspase-3和c-Caspase-3高于其他各组(均P<0.05),见图3。提示卡铂与ABT888联用能够促进细胞凋亡。
|
| A:蛋白质印迹法图谱;B:蛋白质印迹法定量分析结果,对照组设为1,与其他三组比较,*P<0.05. 图3 蛋白质印迹法分析卡铂与ABT888合用对MDA-MB-435s细胞中凋亡相关蛋白的影响 Fig.3 The expression of apoptosis-related proteins in MDA-MB-435s cells after treatment of carbo,ABT888 and their combination |
PARP在细胞DNA 损伤修复中起着关键作用。PARP识别并结合断裂的DNA链,然后募集NAD依赖的ADP核糖单位、组蛋白以及各种DNA修复相关酶,在DNA碱基切除修复过程中发挥着重要作用[8] 。PARP抑制剂和化疗药物的联合应用的主要机制是化疗药物损伤肿瘤细胞DNA之后,再通过PARP抑制剂损伤DNA的修复作用。目前大多数抗肿瘤化疗药物是通过直接或间接作用于DNA链并阻止其修复过程,使其产生对肿瘤细胞的毒性作用[9]。 铂类是目前临床上应用最广泛的一类化疗药物,本实验结果显示,乳腺癌细胞MDA-MB-435s经卡铂与PARP抑制剂ABT888联合作用后出现了明显的协同抑制作用;相对于各对照组,合用组细胞凋亡率显著升高,这提示在本实验体系中,ABT888的使用增加了MDA-MB-435s细胞对化疗药物卡铂的药敏作用。蛋白质印迹法结果则反映出卡铂与ABT888联用抑制凋亡蛋白Bcl-2明显少于单用者,而Bax、c-Caspase-3蛋白显著增加。因此,ABT888通过抑制PARP活性阻碍了卡铂诱导的DNA损伤的修复,进而促进细胞凋亡,其相关的分子生物学机制有待进一步研究。
在本实验中,30 μg/mL卡铂+1 μmol/L ABT888共同处理MDA-MB-435s细胞120 h后表现出极高的协同作用,可显著增加MDA-MB-435s细胞对卡铂的药敏作用,为今后乳腺癌的药物治疗研究提供了一个可能的治疗靶点。
| [1] | 韩 炜,钟 俊,王永峰,等. PARP 抑制剂用于肿瘤治疗的研究进展[J]. 中国新药杂志,2011,20(12):1086-1092. HAN Wei, ZHONG Jun, WANG Yong-feng,et al. PARP inhibitors-therapeutic progress in cancer treatment[J]Chinese Journal of New Drugs,2011,20(12):1086-1092.(in Chinese) |
| [2] | PERALTA-LEAL A,RODRIGUEZ-VARGAS J M,AGUILAR-QUESADA R et al.PARP inhibitors:new partners in the therapy of cancer and inflammatory diseases[J]. Free Radic Biol Med,2009,47(1):13-26. |
| [3] | CHALMERS A J.The potential role and application of PARP inhibitors in cancer treatment[J]. Br Med Bull, 2009,89(9):23-40. |
| [4] | 赵 平,陈万青.2010中国肿瘤登记年报[M].北京:军事医学科学出版社,2010,60-61. ZHAO Ping, CHEN Wan-qing. 2010 Chinese Cancer Registry Annual Report[M].Beijing:Military Medical Science Press, 2010,60-61.(in Chinese) |
| [5] | 郭胜春,袁 泉.紫杉醇联合卡铂治疗晚期乳腺癌的疗效分析[J].实用临床医药杂志,2008,12(6):46-47. GUO Sheng-chun, YUAN Quan. The analysis of curative effect of paclitaxel with carboplatin in the treatment of advanced breast cancer[J]Journal of Clinical Medicine of Practice, 2008,12(6):46-47.(in Chinese) |
| [6] | LEONG C O,VIDNONIC N,DEYOUNG M P,et al.The p63/p73 network mediates chemosensitivity to cisplatin in a biologically defined subset of primary breast cancers[J]. J Clin Invest, 2007,117(5):1370-1380. |
| [7] | BYRSKI T,HUZARSKI T,DENT R,et al.Response to neoadjuvant therapy with cisplatin in BRCAl-positive breast cancer patients[J]. Breast Cancer Res Treat,2009,115(2):359-363. |
| [8] | KRISHNAKUMAR R, KRAUS W L. The PARP side of the nucleus:molecular actions, physiological outcomes, and clinical targets[J]. Mol Cell, 2010, 39(1):8-24. |
| [9] | 黄 河,曹 阳,吴英理,等. PARP抑制剂联合化疗药物治疗恶性肿瘤的研究进展[J].肿瘤,2013,33(4):372-377. HUANG He, CAO Yang, WU Ying-li, et al. The research progress of PARP inhibitors with chemotherapeutic drugs to treat malignant tumors[J]Tumor, 2013,33(4):372-377.(in Chinese) |




