胃食管反流病(gastroesophageal reflux disease, GERD)是一种常见病, 特别在超过50岁的人群中。尽管大多数患者的症状可以通过以制酸剂为主的药物治疗得到很好的控制, 但是还有一部分患者药物治疗效果不佳或不能长期服药, 需要接受进一步手术治疗。目前腹腔镜抗反流手术已经成为治疗GERD的常规手术, 但是术后可能出现症状反复仍然是外科医师关注的问题。手术治疗时是否需要缩小食管裂孔、是否需要补片加强修补和使用何种补片等问题目前存在较大争议, 缺乏统一的标准。
我们认为采用补片加强修补食道裂孔有助于改善患者的术后症状。生物补片作为一种具有良好生物相容性的生物可降解材料, 适合于食管裂孔的加强修补。因此我们尝试在腹腔镜抗反流手术治疗GERD患者的同时, 使用4层猪小肠黏膜下层基质补片(small intestinal mucosa, SIS)(Biodesign TM, Surgsis®)进行食管裂孔的加强修补。本文通过回顾性分析初步探讨其使用效果。
1 对象与方法 1.1 对 象2012年12月至2014年4月在浙江大学医学院附属邵逸夫医院普外科连续收治的20例GERD患者。男性14例, 女性6例, 中位年龄57(25~79)岁, 所有患者均有GERD的典型症状, 如烧心、反流, 14例患者合并食管外症状, 如慢性咳嗽、咽痛、鼻炎、咽部异物感、胸闷等。术前均行胃镜检查, 部分患者行上消化道造影, 若胃镜和消化道造影未提示食管裂孔疝或反流性食管炎则行24 h食管下端pH监测。患者至少有以下情况之一者考虑诊断为GERD并入组: ①胃镜发现食管裂孔疝或反流性食管炎; ②上消化道造影发现食管裂孔疝; ③24 h食管pH值监测提示GERD; ④有典型症状, 通过制酸剂治疗可缓解。11例患者术前通过胃镜或消化道造影检查发现有食管裂孔疝, 其中11例为Ⅰ型, 2例为Ⅲ型; 9例患者术前未发现食管裂孔疝。手术前均告知手术的风险、使用SIS修补的可能风险及经济负担, 所有患者均签署手术知情同意书。
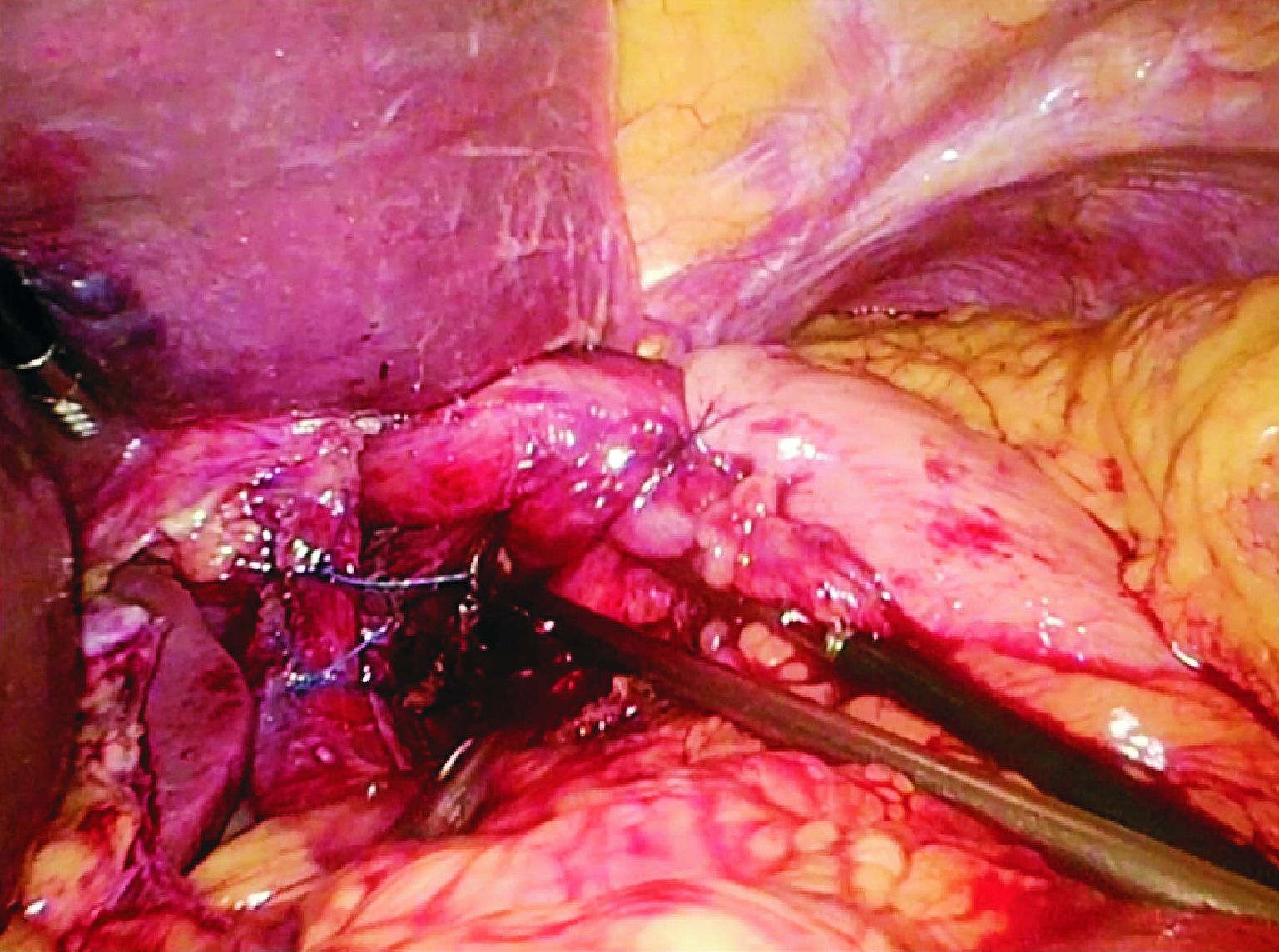
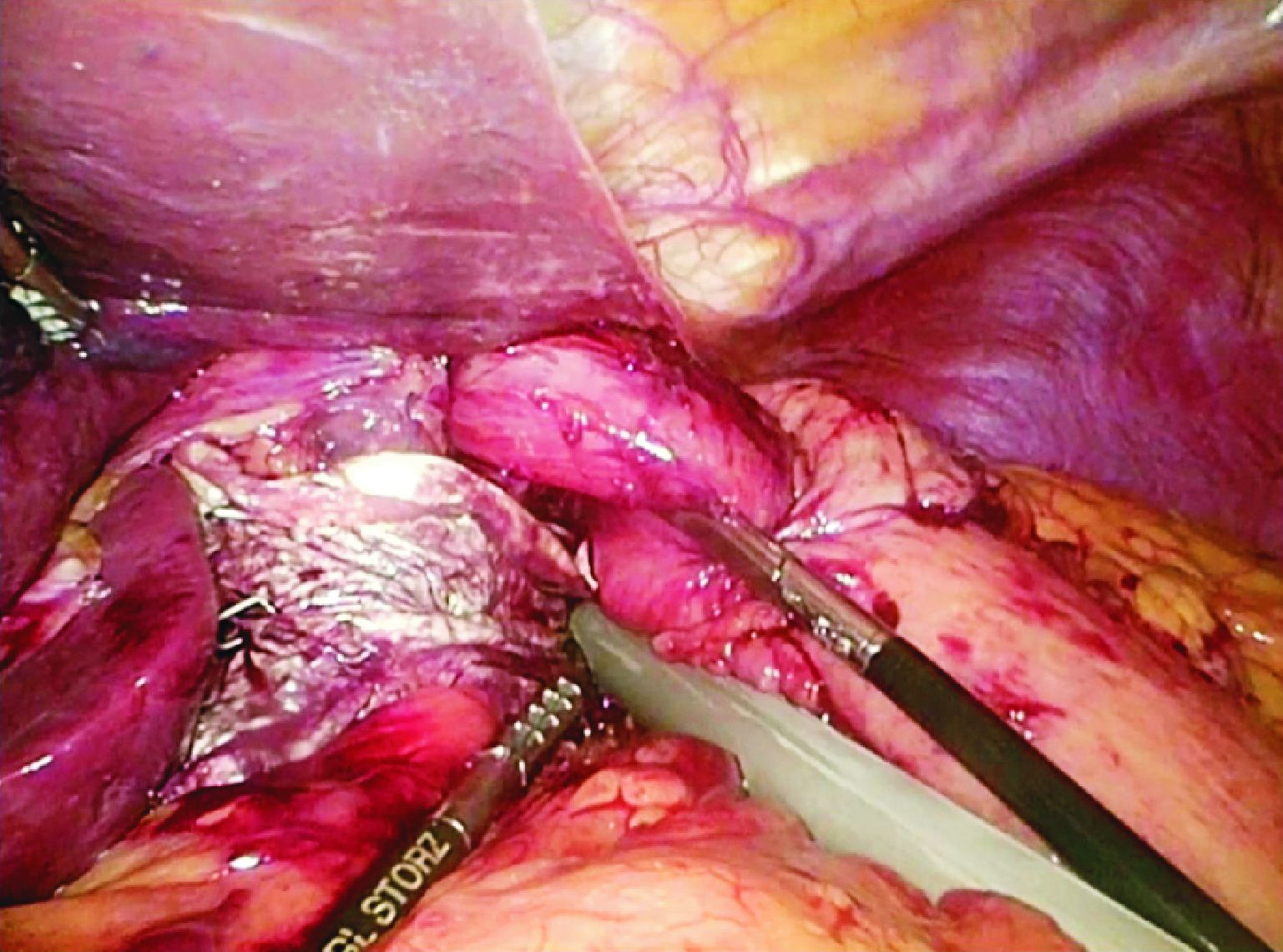
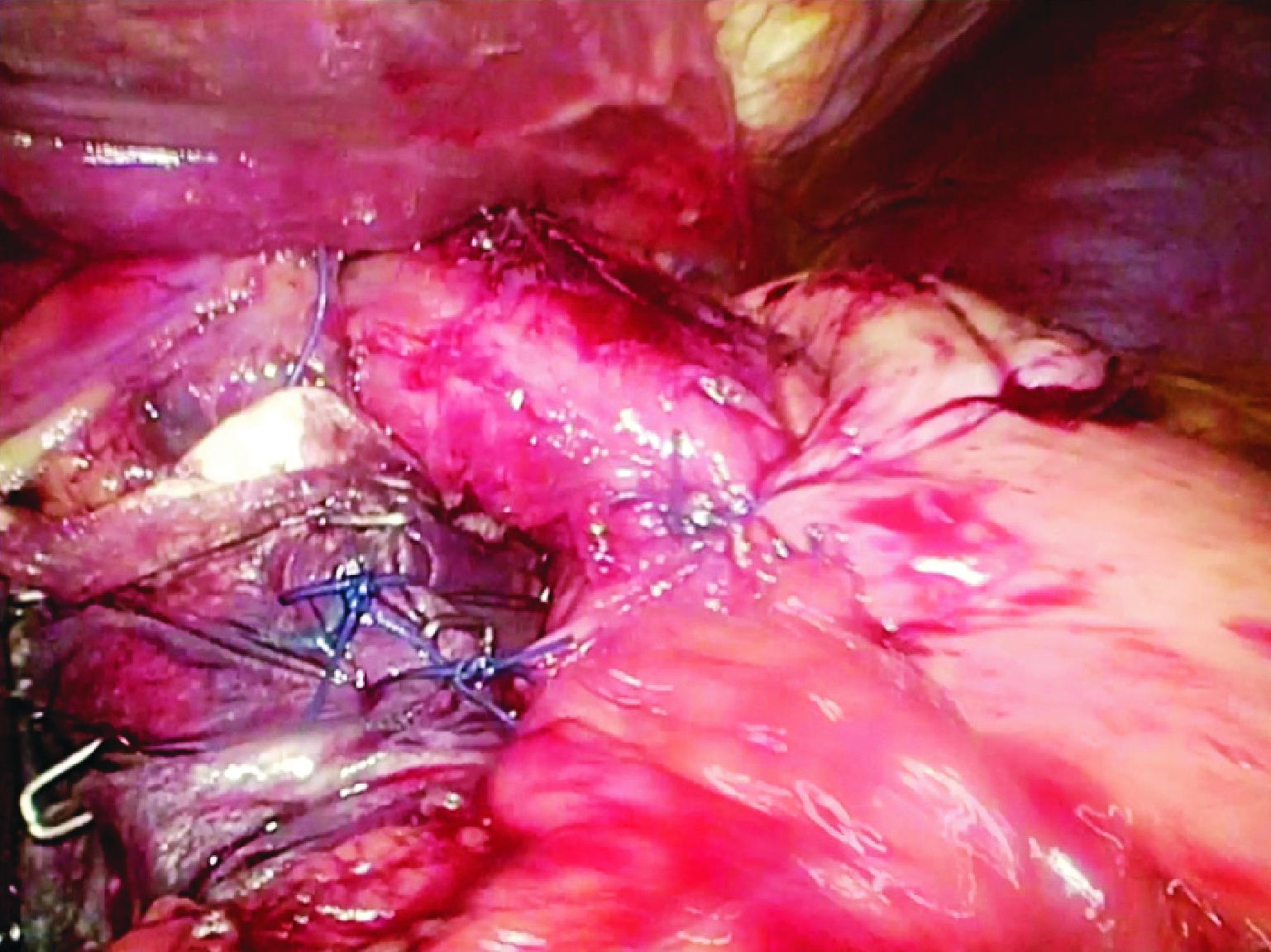
1.2 手术方式及术后处理采用气管插管全身麻醉。麻醉成功后, 患者两腿分开, 术者站在患者两腿之间。根据患者身高情况, 在脐部至脐上5 cm范围内中线穿刺建二氧化钛气腹, 压力维持15 mm Hg (1 mm Hg=0.133 kPa)。穿刺点做10 mm切口, 置入套管, 探查腹腔后, 患者改取头高脚低位, 探查食管裂孔处是否有缺损。右侧锁骨中线及剑突下各置入一个5 mm套管, 左侧锁骨中线分别置入一个10 mm和一个5 mm套管。先分离胃短血管, 充分游离胃底直至左侧膈肌脚, 暴露食管裂孔, 然后将胃向左侧牵引, 游离出右侧膈肌脚并与左侧膈肌脚汇合, 完全暴露食管裂孔。若有疝囊, 则将疝囊从纵隔内完全游离出, 将疝入胸腔的胃和腹段食管完全回纳腹腔。用丝线测量食管裂孔长径并记录。先行胃底折叠, 将游离好的胃底从后方拉到右侧, 在食管下端前方与胃大弯侧缝合, 一般使用3-0带针丝线间断缝合3针, 针距1 cm, 其中最上一针要与食管末端前壁缝合固定, 以保持折叠环在食管下端括约肌水平, 防止患者术后吞咽困难。折叠完成后检查折叠环是否过紧以及近端胃是否有扭曲, 然后行食管裂孔修补。用3-0带针丝线间断从食管后方缝合食管裂孔2~3针。若食管裂孔明显增大则需多缝1~2针, 保持重建后的食管裂孔与食管之间有约0.5 cm的空隙(图1)。食管前方不做缝合。根据食管裂孔的缺损大小, 取一张修剪后的4 cm×7 cm或7 cm×10 cm的4层SIS平铺于食管裂孔处, 补片的上缘稍低或齐平于重建后的食管裂孔下缘, 两侧充分展平并与组织贴合。用连发型吻合器(endoscopic multifeed stapler, EMS)(ETHICON ENDO-SURGERY, LLC)将补片固定于膈肌上, 再用3-0带针丝线将补片与两侧膈肌脚缝合处纵行缝合固定2针(图2)。用3-0带针丝线将胃底间断缝合固定于膈肌脚上(图3)。放置腹腔引流管一根, 不常规放置胃管。
|
| 图1 完成胃底折叠, 缝合食管裂孔 Fig.1 Completion of the Nissen fundoplication and suturing the esophageal hiatus |
|
| 图2 以连发型吻合器固定小肠黏膜下层基质补片 Fig.2 Fixation of the SIS by using EMS |
|
| 图3 缝合固定小肠黏膜下层基质补片, 并将胃底缝合固定于膈肌脚 Fig.3 Suturing and fixation of SIS, and fixing stomach bottom in the diaphragm on the foot |
术后6 h开始喝水, 术后24 h开始进食流质, 若无明显不适术后48 h开始进食半流质, 半个月后让患者尝试进食固体食物, 若有吞咽困难则继续进食半流质, 并反复尝试进食固体食物。
1.3 术后观察及随访住院期间观察患者恢复情况及并发症发生情况。术后2周、1个月和3个月患者门诊随访, 部分患者通过电话随访。随访内容为患者一般情况如精神情况、食欲、睡眠等, 症状缓解或复发的情况, 不良反应如吞咽困难、腹胀、腹泻等的发生情况。必要时行上消化道造影或胃镜检查。随访至2014年5月。
2 结 果术中发现所有患者的食管裂孔都较正常人大, 平均(5.9±1.8) cm(3.7~10.1 cm)。所有患者腹腔镜手术均成功, 无中转开腹, 未发生术中并发症, 手术时间95~180 min, 平均(133.8±39.6)min。患者住院期间均未发生手术相关并发症, 有1例患者术后第3天出现急性心肌梗死, 转心内科治疗后缓解。出院时所有患者的术前症状均消失, 术后随访未发现有症状复发者。
术后1月随访时, 有6例患者出现明显的吞咽困难, 均表现为进食固体食物时有较明显的哽噎感, 只能进食半流质, 后经调整生活习惯、使用胃肠动力药物和心理疏导后, 其中5例患者症状明显缓解, 可正常生活。还有1例患者吞咽困难始终无法缓解, 伴胃纳下降、消瘦, 术后1个月行上消化道造影提示食管稍扩张, 造影剂通过较缓慢, 但是未见明显梗阻; 保守治疗1个月后复查, 患者情况仍无好转, 再行上消化道造影, 提示食管扩张较前好转, 造影剂通过仍缓慢, 但较前好转。患者强烈要求进行食管扩张, 接受了胃镜检查, 发现食管下端较狭窄, 但胃镜能通过, 并可见折叠瓣, 遂用食管探条进行了食管下端扩张术, 将食管下端稍做扩张后症状明显好转。
3 讨 论GERD是一种常见病, 长期以来以质子泵抑制剂为主的药物治疗是主要的治疗手段, 但停药后复发率很高, 且部分患者药物治疗效果不佳。手术治疗, 尤其是腹腔镜手术, 因其长期疗效确切、复发率低、创伤小等优势, 目前在该疾病治疗中的地位不断提高。
GERD最主要的手术方法是胃底折叠术。胃底折叠手术的手术方式很多, 在西方国家采用最广泛的还是Nissen胃底折叠术, 尤其是短松型Nissen手术, 其抗反流效果确切, 术后吞咽困难等并发症较少, 适用于大多数患者。本组患者采用的术式全部是短松型Nissen胃底折叠术。
GERD的发病机制目前尚不十分明确, 但是食管裂孔疝是发生GERD的主要原因之一, 尤其是症状较重者, 几乎都合并有食管裂孔疝。本文资料中有13例患者术前检查即发现合并食管裂孔疝, 其中11例为Ⅰ型, 2例为Ⅲ型。对于不合并明显的食管裂孔疝的患者, 在胃底折叠的同时, 是否需要缝合两侧膈肌脚以缩小食管裂孔是有争议的。有研究认为缩小食管裂孔有助于改善预后[1], 有些研究却认为没有显著的意义[2], 也有提出应根据食管裂孔的大小来决定是否缝合缩小[3]。因这些研究都不是随机对照研究, 说服力不强。我们在手术中发现, 即使没有明显食管裂孔疝的胃食管反流病患者, 其食管裂孔也较正常人明显增大, 这与其他研究者观察到的情况一致[4]。因此我们对所有患者都缝合膈肌脚缩小食管裂孔。
单纯缝合膈肌脚以修补食管裂孔的方法简单易行, 但是GERD复发率较高, 尤其是Ⅱ型和Ⅲ型食管裂孔疝, 患者术后复发率高达42%, 腹腔镜手术的复发率更高, 而采用补片修补可以大大降低复发率。目前对于使用补片修补的适应证、理想的补片材料、修补方式和补片的固定方式都没有统一的标准。随机对照研究显示缺损范围超过5 cm的食管裂孔疝需要使用补片修补[5, 6], 但对于小于此范围的缺损是否需要补片修补尚无定论。我们认为食管裂孔疝最理想的补片修补方式是Onlay法, 因此不可能做到无张力修补。膈肌脚处缺乏强劲的组织如韧带、筋膜等, 而且膈肌和食管始终处于运动状态, 在肌肉上缝合容易撕裂导致修补失败, 因此应尽量使用补片进行加强。并且很多这类患者的膈肌本身就比较纤弱, 在进行缝合时常会发现膈肌有被缝线割裂的风险。另外, GERD和食管裂孔疝患者多为老年人, 老年人的膈肌脚纤维组织常被脂肪组织代替而强度减弱[7]。因此我们采用生物补片进行加强修补, 术后随访3~18个月, 未发现一例复发。
适合修补食管裂孔的补片材料目前尚无定论, 对补片的要求应该是在保证修补强度的前提下尽量减少补片相关并发症。单纯的聚丙烯补片会侵蚀食管、导致严重的肠粘连甚至肠瘘, 不适合用于食管裂孔疝的修补。合成材料制作的各种防粘连切口疝补片也不适合用于食管裂孔疝, 因为这些补片必须剪开后才能包绕食管, 而剪开处聚丙烯纤维就会暴露并接触到食管, 从而导致食管瘘[8, 9]。目前比较理想的修补材料是U型的聚丙烯-膨体聚四氟乙烯复合补片和各种生物补片。前者的外形是为食管裂孔疝优化设计的, 操作简便, 而且可防止腹腔内脏器和食管的粘连, 理论上也不会侵蚀食管和胃。但是该材料不可吸收, 可能导致纤维增生而增加术后吞咽困难的发生率, 甚至导致胃瘘[10], 国外文献有该种补片侵蚀胃腔的病例报道[11]。我们认为, 当食管裂孔缺损较大, 无法进行缝合关闭, 必须采用桥接法进行修补时, 该材料是非常理想的选择。本组所有患者的食管裂孔均能关闭而通过Onlay法进行修补, 因此我们未选择使用该材料。生物材料已经被应用于腹股沟疝、切口疝的修补, 是一种安全可靠的补片材料, 其应用于食管裂孔的修补也有其独特的优势。生物补片不会发生侵蚀胃和食管的并发症, 其造成的腹腔粘连也轻微, 其降解和组织重塑形的过程同步进行, 补片被自身组织完全替代, 不残留异物, 因此我们认为这是一种理想的修补材料。我们所选用的生物材料是4层SIS, 若食管裂孔缺损小于5 cm, 规格选择4 cm×7 cm; 若大于5 cm, 则选择7 cm×10 cm的规格, 足以保证补片在缺损两侧有3~5 cm的覆盖范围。SIS的层数与其降解速度和最后形成的纤维组织强度密切相关。用于腹股沟疝修补的单层SIS强度可能不足, 而用于切口疝修补的8层SIS尽管强度足够, 但是价格昂贵, 而且因其厚度较大, 操作不方便, 尤其是比较难固定。我们认为比较理想的厚度是4~6层SIS, 这与其他一些研究者的选择相同[12]。
食管裂孔疝的补片修补方式主要是Onlay法和桥接法两种, 其中大多数研究者推荐前者, 而后者主要用于食管裂孔缺损过大、无法进行缝合的病例。本文资料所有的患者都采用Onlay法进行修补。我们的体会是, 术前影像学检查所提示的食管裂孔缺损很大程度上其实是被疝入的胃所撑开的, 其实并非真正的缺损范围, 而当手术中将疝入纵膈的胃和食管拉回腹腔后, 可见缺损范围明显缩小, 本文资料有1例患者术前判断其缺损范围为10 cm, 然而将疝内容物完全回纳后, 两侧膈肌脚分离的距离不足5 cm, 完全可以进行缝合修补。另外, SIS的特点要求其必须与组织紧密贴合, 才能起到诱导组织重塑形的作用, 因此只有在能实现Onlay法修补的患者中才能够使用该种补片, 否则应使用不可降解的合成补片。根据文献报道, 不同研究者选用的补片的固定方式包括缝合、螺旋钉钉合、生物胶等, 目前并无依据证明何种方式有优势。本组采用的固定方式是缝合+钉合, 补片展平后, 先将其正中处与后方的膈肌缝合2针, 将补片与缺损修补处可靠固定, 然后再用EMS将补片平铺固定于膈肌上, 一般钉合和间距是1 cm左右, 必须保证补片充分展平, 并与组织充分接触。为防止复发, 必须将折叠后的胃底缝合固定于被补片覆盖的膈肌脚上, 以防止胃折叠袢上移重新撑开食管裂孔。
对生物补片的主要担忧是其修补强度是否足够, 尤其是远期的复发率, 有报道发现其术后5年左右的复发率接近单纯缝合[12]。但有资料显示, 使用SIS补片修补食管裂孔疝的效果与使用聚丙烯-膨体聚四氟乙烯复合补片相同[13]。4层SIS补片在植入后随着降解其强度逐步下降, 而自身组织塑型的强度逐渐增强, 在这个过程中, 总的强度呈先下降后上升逐步稳定的趋势。SIS 植入体内2周左右修复区强度降低约45%, 1个月后强度回复到初始水平, 之后逐步升高, 至3个月时达到稳定。本组患者术后随访时间最少为3个月, 至投稿时未发现复发病例。有一例食管裂孔疝患者因为术后出现反复的急性胃肠炎, 患者感到腹胀恶心并反复诱发呕吐却不成功, 证实手术的抗反流效果很确切, 术后反复查腹部CT也未发现食管裂孔疝复发。当然本文资料大多数患者的缺损并不大, 而且仍处于术后观察期, 还需要进一步随访以证实上述结论。
| [1] | DEMEESTER T R, BONAVINAL L, ALBERTUCCI M. Nissen fundoplication for gastroesophageal reflux disease. Evaluation of primary repair in 100 consecutive patients[J]. Ann Surg, 1986, 204(1):9-20. |
| [2] | WATSON D I, JAMIESON G G, DEVITT P G, et al. A prospective randomized trial of laparoscopic Nissen fundoplication with anterior vs posterior hiatal repair[J]. Arch Surg, 2001, 136(7):745-751. |
| [3] | ROSENTHAL R, PETERLI R, GUENIN M O, et al. Laparoscopic antireflux surgery: long-term outcomes and quality of life[J]. J Laparoendosc Adv Surg Tech A, 2006, 16(6):557-561. |
| [4] | LEE Y Y, MCCOLL K E. Pathophysiology of gastroesophageal reflux disease[J]. Best Pract Res Clin Gastroenterol, 2013, 27(3):339-351. |
| [5] | FRANTZIDES C T, MADAN A K, CARLSON M A, et al. A prospective, randomized trial of laparoscopic polytetrafluoroethylene (PTFE) patch repair vs simple cruroplasty for large hiatal hernia[J]. Arch Surg, 2002, 137(6):649-652. |
| [6] | GRANDERATH F A, SCHWEIGER U M, KAMOLZ T, et al. Laparoscopic Nissen fundoplication with prosthetic hiatal closure reduces postoperative intrathoracic wrap herniation: preliminary results of a prospective randomized functional and clinical study[J]. Arch Surg, 2005, 140(1):40- 48. |
| [7] | CURCI J A, MELMAN L M, THOMPSON R W, et al. Elastic fiber depletion in the supporting ligaments of the gastroesophageal junction: a structural basis for the development of hiatal hernia[J]. J Am Coll Surg, 2008, 207(2):191-196. |
| [8] | JANSEN M, OTTO J, JANSEN P L, et al. Mesh migration into the esophageal wall after mesh hiatoplasty: comparison of two alloplastic materials[J]. Surg Endosc, 2007, 21(12):2298-2303. |
| [9] | DALLY E, FALK G L.Teflon pledget reinforced fundoplication causes symptomatic gastric and esophageal lumenal penetration[J]. Am J Surg, 2004, 187(2):226-229. |
| [10] | TATUM R P, SHALHUB S, OELSCHLAGER B K, et al. Complications of PTFE mesh at the diaphragmatic hiatus[J]. J Gastrointest Surg, 2008, 12(5):953-957. |
| [11] | CARPELAN-HOLMSTR M M, KRUUNA O, SALO J, et al. Late mesh migration through the stomach wall after laparoscopic refundoplication using a dual-sided PTFE/ePTFE mesh[J]. Hernia, 2011, 15(2):217-220. |
| [12] | OELSCHLAGER B K, PELLEGRINI C A, HUNTER J G, et al. Biologic prosthesis to prevent recurrence after laparoscopic paraesophageal hernia repair: long-term follow-up from a multicenter, prospective, randomized trial[J]. J Am Coll Surg, 2011, 213(4):461- 468. |
| [13] | ROMAO R L, NASR A, CHIU P P, et al. What is the best prosthetic material for patch repair of congenital diaphragmatic hernia? Comparison and meta-analysis of porcine small intestinal submucosa and polytetrafluoroethylene[J]. J Pediatr Surg, 2012, 47(8):1496-1500. |



