2. 浙江大学药学院, 浙江 杭州 310058
2. College of Pharmaceutical Science, Zhejiang University, Hangzhou 310058, China
癫痫是由各种原因引起的脑细胞群异常放电所致脑功能障碍综合征,患者常表现为突然、短暂的运动、感觉、意识或精神等异常。大脑经外伤、肿瘤和感染等损伤后,经过一定潜伏期,开始出现自发性癫痫发作。目前,癫痫的药物治疗均为抑制离子通道的对症治疗(anti-seizure),极少有针对癫痫发生病理生理机制的对因治疗药物(anti-epilepsy)。具有更小副作用及更高疗效的对因治疗药物亟待研发[1, 2]。 最近,癫痫持续状态与氧化应激之间的关系开始逐渐引起人们关注,有研究表明,长期癫痫发作通过多种离子通道以及由此伴发的生化级联反应,引发钙离子内流,从而导致神经细胞死亡和活性氧产生[3, 4]。反过来,氧化应激增加可引发癫痫所致脑损伤和其随后所带来的一些反应,并可能诱发癫痫形成[5, 6, 7]。 我们以往的研究表明,甘草中提取的黄酮类混合物(甘草苷、芹糖甘草苷和甘草素)是很好的抗氧化剂[8],且能显著降低红藻氨酸(kainic acid)致痫小鼠的氧化应激,从而减少神经元死亡,降低癫痫所致的学习记忆损害[9]。这些结果提示甘草黄酮可能对癫痫有一定的防治作用。本研究中,我们分别观察甘草黄酮在造模前后给药对红藻氨酸致痫小鼠在急性痫性发作期和自发性癫痫发作期的治疗作用,并从苔藓纤维发芽和神经元再生探讨其抗癫痫作用的可能机制。
1 材料与方法 1.1 试剂及动物甘草黄酮为自制,水提后经甲醇及C18硅胶柱纯化和色谱分析,最终得到甘草苷、芹糖甘草苷和甘草素的混合物(含量分别为3.81%、1.38% 和0.52%)。BrdU和抗鼠 BrdU抗体购自美国Sigma-Aldrich有限公司,红藻氨酸购自美国Nanocs有限公司,其他一般试剂购自杭州程正科技有限公司。5周龄雄性ICR小鼠购自上海斯莱克实验动物中心(证书: SCXK 2007-0005)。
1.2 动物造模和用药方法动物实验遵守浙江大学医学院动物实验管理规范。动物的饲养条件为温度(24±1)°C,湿度40%~60%,昼/夜各12 h。以25 mg/kg的剂量单次腹腔注射红藻氨酸诱发小鼠急性痫性发作。癫痫发作的分级参照之前的报道[10]。Ⅰ级:静止伴面部抽搐;Ⅱ级:出现点头运动;Ⅲ级:前肢阵挛;Ⅳ级:站立;Ⅴ级:站立及跌倒;Ⅵ级:奔跑。达到4级或5级且发作持续60 min以上视为痫性发作持续状态,用于下一步实验。
甘草黄酮的给药方式分为预防性给药(预防组)和治疗性给药(治疗组)。预防组在造模前1周,甘草黄酮按照每天10 mg/kg的剂量灌胃(注明低中高剂量组除外),连续7 d。治疗组在造模后24 h开始甘草黄酮10 mg/kg灌胃,连续7 d。空白对照组除注射红藻氨酸外其他给予相同剂量的溶剂。正常对照组全部给予生理盐水或溶剂。
1.3 录像监测小鼠自发性癫痫发生情况造模后第2天,将待观察小鼠放入小鼠专用录像笼中,每天持续记录10 h,连续6周。视频由两人分别观看,记录小鼠每日发生自发性癫痫的次数。
1.4 BrdU 注射及显微镜下观察脑组织神经元再生情况造模后24 h开始给予BrdU 100 mg/kg腹腔内注射7 d,第8天麻醉处死后行心脏灌注固定。脑组织经冠状切面制作连续冰冻切片,片厚20 μm,每隔5片取一片,贴附于涂有铬矾明胶的载玻片上。切片先加2 mol/L 盐酸经37 ℃ 20 min变性后,再加pH值为8.5的硼酸盐缓冲液中和10 min。经磷酸盐缓冲液充分洗涤后,切片在0.2% Triton X-100 破膜30 min后,用5 % 山羊血清室温封闭1 h,与抗鼠BrdU抗体(1∶500)4 ℃孵育48 h后,再与荧光标记的二抗反应,结果在荧光显微镜下观察,荧光着色细胞为BrdU阳性,代表再生神经元。随机选定区域进行拍照计数,计算单位视野内各组BrdU阳性细胞数量。
1.5 Timm 染色检测海马齿状回分子细胞层苔藓纤维发芽情况录像观测结束后,动物麻醉后先用硫化钠灌流,再经PFA灌流固定和蔗糖脱水。如上法获取切片,切片在含银的缓冲液中避光孵育80~120 min后,Timm染色检测海马齿状回分子细胞层苔藓纤维发芽状况。苔藓纤维发芽的程度分级参照1991年Cavazos的半定量标准,即:0级,未见出芽;1级,偶见点状出芽;2级,可见点状或稀疏状出芽;3级,可见片状出芽;4级,可见高度集中的片状出芽;5级,可见浓密片状出芽。
1.6 统计学分析采用SPSS 16.0 统计软件进行分析。所有数据用均数±标准差 ($\bar x$±s) 表示。癫痫发生潜伏期、发作次数、发作程度及神经元死亡、苔藓纤维发芽的比较采用单因素方差分析,组间两两比较采用Dunnett-t检验。以P<0.05为差异有统计学意义。
2 结 果 2.1 甘草黄酮对模型小鼠急性痫性发作的影响空白对照组与各种浓度甘草黄酮的预防组模型小鼠急性癫痫发作潜伏期、发作程度和持续时间比较见图1(n=12~15)。结果显示甘草黄酮低(3 mg/kg)、中(10 mg/kg)、高(30 mg/kg)剂量给药与空白对照组小鼠在急性癫痫发作潜伏期、癫痫发作程度及癫痫发作持续时间差异均无统计学意义(均P>0.05),提示甘草黄酮对模型小鼠急性痫性发作无治疗作用。

|
| 图1 不同浓度甘草黄酮预防组模型小鼠急性痫性发作潜伏期、发作程度和持续时间比较 Fig.1 Effect of licorice flavonoid on acute seizure latency,seizure stage and duration in kainic acid-induced seizure mice |
空白对照组小鼠从第1周开始即出现自发性癫痫发作,且随时间延长发作频率有增加趋势。预防给药和治疗给药均能减少模型小鼠自发性癫痫的发生频率,与空白对照组比较,从第3周开始,预防组和治疗组癫痫的发生率均显著下降(均P<00.05,n=10~15),但预防组与治疗组癫痫的发生率差异无统计学意义(均P>0.05),见图2。提示甘草黄酮预防或治疗给药均能减少自发性癫痫发生频率。

|
| 与空白对照组比,*P<00.05. 图2 各组自发性癫痫发作频率比较 Fig.2 Licorice flavonoid pre-and post-treatment decreased the frequency of spontaneous seizure in kainic acid-induced seizure mice |
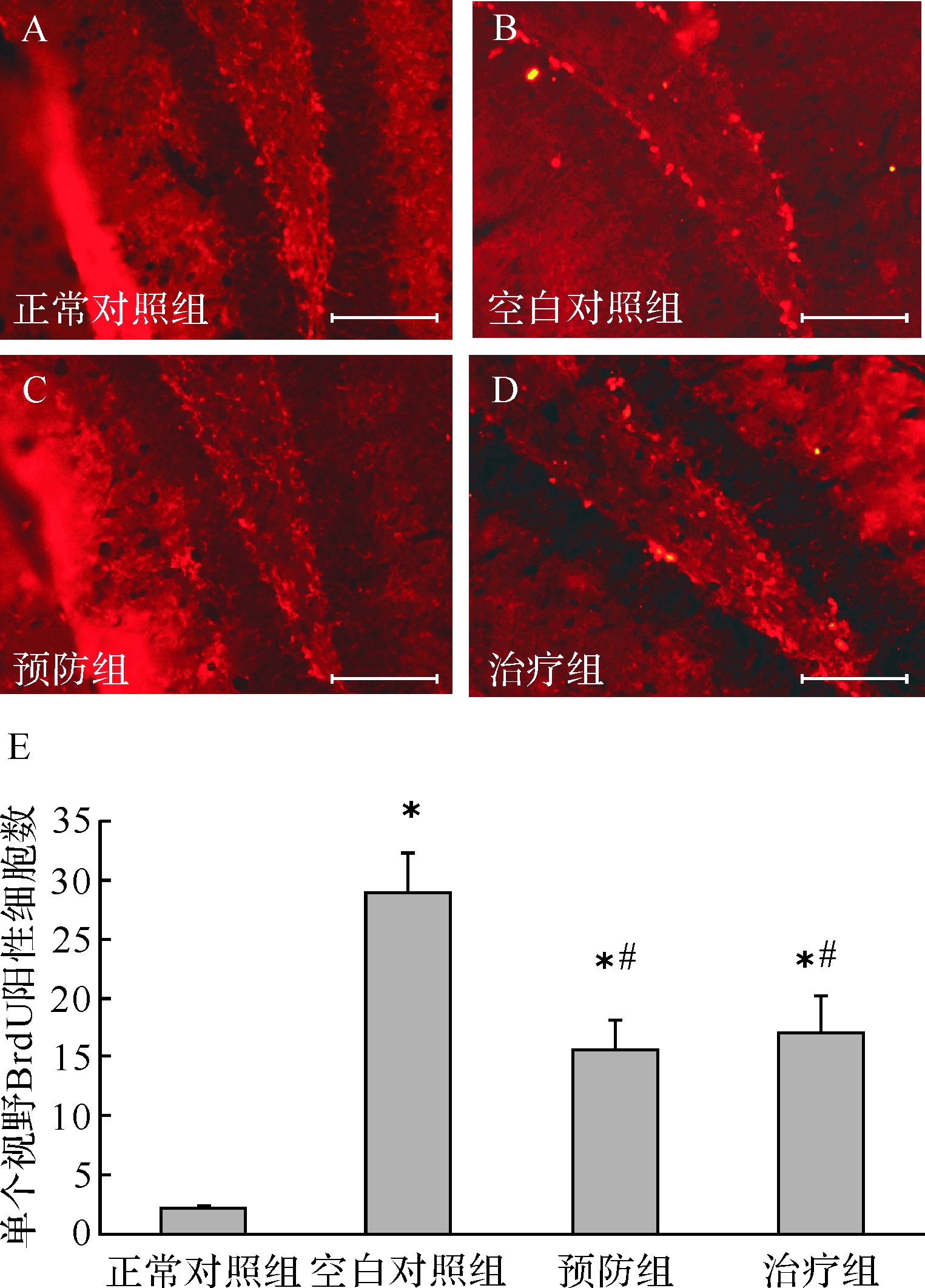
如图3所示,正常对照组小鼠几乎未见BrdU阳性细胞,但空白对照组可见大量BrdU阳性的细胞,平均每个视野可见(28.9±3.5)个阳性细胞。而预防组和治疗组固定视野下BrdU阳性细胞数目分别为(15.6±2.6)和(17.1±2.2)个,虽较正常对照组增加(P<00.05),但较空白对照组均下降(均P<00.05),提示甘草黄酮对神经元再生有抑制作用。
|
| A~D:各组BrdU染色组织的代表图片. A:正常对照组未见明显阳性细胞;B:空白对照组可见大量阳性细胞;C: 预防组见少量阳性细胞;D: 治疗组见少量阳性细胞;E:各组BrdU染色阳性细胞数比较.与正常对照组比较,*P<00.05;与空白对照组比较,#P<00.05;n=8,标尺=100 μm. 图3 各组脑组织神经元再生情况 Fig.3 Licorice flavonoid pre-and post-treatment suppressed neurogenesis in kainic acid-induced seizure mice |
Timm染色结果,空白对照组苔藓纤维发芽明显,Timm染色分级为3.0±0.37,而预防组和治疗组仅分别为1.33±0.31和1.56±0.42,虽然比正常对照组增加(P<00.05),但比空白对照组减少(P<00.05),提示甘草黄酮能显著降低苔藓纤维发芽程度(图4)。

|
| A~H:各组Timm染色组织的代表图片. A、B:正常对照组海马DG及CA3区均未见明显出芽;C、D:空白对照组海马DG及CA3区均可见浓密状出芽(箭头所示);E、F: 预防组海马DG区未见明显出芽,CA3区可见片状出芽(箭头所示);G、H:治疗组海马DG区未见明显出芽,CA3区可见片状出芽(箭头所示); I:各组Timm染色分级比较. 与正常对照组比较,*P<00.05;与空白对照组比较,#P<00.05. n=8~10,标尺=100 μm. 图4 各组海马苔藓纤维发芽情况 Fig.4 Licorice flavonoid pre-and post-treatment inhibited mossy fiber sprouting in kainic acid-induced seizure mice |
甘草根茎在中国是一种很普遍的药食两用的药物。从甘草中分离出的黄酮类化合物在神经系统通过其抗氧化和抗凋亡活性具有抗局部脑缺血—再灌注的作用[11, 12],对慢性不可预测应激引起的大鼠抑郁行为具有良好的抗抑郁药理活性及对应激引起的海马神经再生损害起到保护作用[13],对帕金森病小鼠多巴胺能神经元具有神经保护效应[14],但对癫痫的作用尚未见报道。
红藻氨酸致痫模型是常用的化学性癫痫模型。红藻氨酸是脑内的兴奋性神经递质,腹腔注射后导致脑内兴奋性神经递质与抑制性神经递质的不平衡,诱发急性痫性发作,造成大脑初始损伤。经过一定潜伏期后,小鼠表现为不同程度的自发性癫痫发作。在本研究中,我们采用这一癫痫模型,探讨了甘草黄酮对急性痫性发作与自发性癫痫形成的作用。结果显示甘草黄酮对急性痫性发作无显著影响,提示甘草黄酮并不影响神经细胞的膜稳定性,也不像经典的抗癫痫药那样影响离子通道的开放。然而,甘草黄酮在造模前后给药均能显著降低模型小鼠自发性癫痫的发作频率,因此我们在此基础上探讨了自发性癫痫形成时的生理病理机制改变——神经元再生和苔藓纤维发芽。神经元再生和苔藓纤维发芽是导致神经环路兴奋性增高的典型病理改变[15, 16]。当海马神经再生时,新生的细胞分化成颗粒细胞,成熟的神经元在分子层及多形层产生树突、轴突,形成突触联系,最终整合至海马功能的神经环路中,参与海马的各种功能活动,尤其是神经细胞兴奋性的增强。我们发现甘草黄酮造模前后给药均能显著抑制神经元再生及苔藓纤维发芽,进一步验证甘草黄酮对自发性癫痫形成的防治效果。
甘草黄酮抑制神经元再生及苔藓纤维发芽的作用机制不甚明确。已有文献报道表明其他来源的黄酮类物质如橙皮苷、黄芩苷和牡荆苷对红藻氨酸、匹罗卡品或戊四唑致痫模型有神经保护作用,其作用与其抗氧化作用紧密相关[17, 18, 19]。本课题组在前期的研究中亦发现甘草黄酮能显著逆转红藻氨酸致痫模型超氧化物歧化酶、丙二醛改变,且能显著降低致痫后氧化应激导致的神经元死亡及学习记忆障碍[9]。这种保护作用为后续级联式反应最终导致癫痫自发性发作亦提供了壁垒,最终减少了神经元再生和苔藓纤维发芽。其他的可能机制正在进一步探讨中。
综上而言,本研究结果表明,具有强抗氧化作用的甘草黄酮对红藻氨酸致痫的自发性癫痫形成具有一定的防治作用。基于其毒性低、取材易等特点,甘草黄酮有望作为一种潜在的防治自发性癫痫的药物。
| [1] | LöSCHER W, SCHMIDT D. New horizons in the development of antiepileptic drugs: innovative strategies [J]. Epilepsy Res, 2006, 69(3):183-272. |
| [2] | ELGER C E, SCHMIDT D. Modern management of epilepsy: a practical approach [J]. Epilepsy Behav, 2008, 12(4):501-539. |
| [3] | BRUCE A J, BAUDRY M. Oxygen free radicals in rat limbic structures after kainate-induced seizures [J]. Free Radic Biol Med, 1995, 18(6):993-1002. |
| [4] | FRANTSEVA M V, PEREZ VELAZQUEZ J L, TSORAKLIDIS G , et al. Oxidative stress is involved in seizure-induced neurodegeneration in the kindling model of epilepsy [J]. Neuroscience, 2000, 97(3):431- 435. |
| [5] | AGUIAR C C, ALMEIDA A B, ARA AU’G JO P V, et al. Oxidative stress and epilepsy: literature review [J]. Oxid Med Cell Longev, 2012, 2012: 795259. |
| [6] | MARTINC B, GRABNAR I, VOVK T. The role of reactive species in epileptogenesis and influence of antiepileptic drug therapy on oxidative stress [J]. Curr Neuropharmacol, 2012, 10(4):328-343. |
| [7] | RYAN K, BACKOS D S, REIGAN P, et al. Posttranslational oxidative modification and inactivation of mitochondrial complex I in epileptogenesis [J]. J Neurosci, 2012, 32(33):11250-11258. |
| [8] | XIE Y C, DONG X W, WU X M, et al. Inhibitory effects of flavonoids extracted from licorice onlipopolysaccharide-induced acute pulmonary inflammation in mice [J]. Int Immunopharmacol, 2009, 9(2):194-200. |
| [9] | ZENG L H, ZHANG H D, XU C J, et al. Neuroprotective effects of flavonoids extracted from licorice on kainate-induced seizure in mice through their antioxidant properties [J]. J Zhejiang Univ Sci B, 2013, 14(11):1004-1012. |
| [10] | CHEN L L, FENG H F, MAO X X, et al. One hour of pilocarpine-induced status epilepticus is sufficient to develop chronic epilepsy in mice, and is associated with mossy fiber sprouting but not neuronal death [J]. Neurosci Bull, 2013, 29(3) :295-302. |
| [11] | SUN Y X, TANG Y, WU A L, et al. Neuroprotective effect of liquiritin against focal cerebral ischemia/reperfusion in mice via its antioxidant and antiapoptosis properties [J]. J Asian Nat Prod Res, 2010, 12(12) :1051-1060. |
| [12] | ZHAN C, YANG J. Protective effects of isoliquiritigenin in transient middle cerebral artery occlusion-induced focal cerebral ischemia in rats [J]. Pharmacol Res, 2006, 53(3) : 303-309. |
| [13] | 樊紫周, 赵伟鸿, 果 嘉, 等. 甘草黄酮的抗抑郁作用及对海马脑区神经再生的保护作用[J]. 药学学报, 2012, 47(12)1612-1617. FAN Zi-zhou, ZHAO Wei-hong, GUO Jia, et al. Anti-depressant activities of flavonoids from Glycyrrhiza uralensis and its neurogenesis protective effect in rats [J]. Acta Pharmaceutica Sinica, 2012, 47(12):1612-1617. (in Chinese) |
| [14] | 陈 浩, 师 亮, 王燕宏, 等.甘草黄酮对MPTP帕金森病小鼠多巴胺能神经元的影响[J]. 山西医科大学学报, 2013, 44(10):755-757. CHEN Hao, SHI Liang, WANG Yan-hong, et al. Influence of licorice flavonoids on the dopaminergic neurons of mice with MPTP-induced Parkinson disease [J]. Journal of Shanxi Medical University, 2013, 44(10):755-757. (in Chinese) |
| [15] | ZENG L H, RENSING N R, WONG M. The mammalian target of rapamycin signaling pathway mediates epileptogenesis in a model of temporal lobe epilepsy [J]. J Neurosci, 2009, 29(21):6964-6972. |
| [16] | PAIZANIS E, KELAR S, RENOIR T, et al. Life-long hippocampal neurogenesis: environmental, pharmacological and neurochemical modulations [J]. Neurochem Res, 2007, 32: 1762-1771. |
| [17] | ABBASI E, NASSIRI-ASL M, SHAFEEI M, et al. Neuroprotective effects of vitexin, a flavonoid, on pentylenetetrazole-induced seizure in rats [J]. Chem Biol Drug Des, 2012, 80(2) :274-278. |
| [18] | GOLECHHA M, CHAUDHRY U, BHATIA J, et al. Naringin protects against kainic acid-induced status epilepticus in rats: evidence for an antioxidant, anti-inflammatory and neuroprotective intervention [J]. Biol Pharm Bull, 2011, 34(3):360-365. |
| [19] | LIU Y F, GAO F, LI X W, et al. The anticonvulsant and neuroprotective effects of baicalin on pilocarpineinduced epileptic model in rats [J]. Neurochem Res, 2012, 37(8): 1670-1680. |



