| 不同投喂-停喂时间对大口黑鲈摄食、生长和废物排放的影响 |
2. 浙江大学海洋学院,浙江 舟山 316021;
3. 浙江省淡水水产研究所,浙江鱼类健康与营养重点实验室,浙江 湖州 310001
2. Ocean College, Zhejiang University, Zhoushan 316021, Zhejiang, China;
3. Key Laboratory of Fish Health and Nutrition of Zhejiang Province, Zhejiang Institute of Freshwater Fisheries, Huzhou 313001, Zhejiang, China
鱼类需要从食物中获取营养以满足生长和代谢的需求,并可通过调整摄食量应对食物丰歉和营养组成的变化。确定合理的饲喂策略,包括食物营养结构、投喂量和投喂方法,是鱼类养殖技术体系研究的重要内容。有关鱼类饲料营养需求和投喂方法已分别开展了大量的研究[1-5],但针对特定养殖条件下鱼类的饲喂策略的系统研究尚不多见。补偿生长指动物在恶劣环境条件下经过一段时间的生长停滞或失重后,当环境条件重新恢复正常所表现出的超常生长现象或能力[6-8]。自20世纪80年代以来,鱼类补偿生长强度以及利用补偿生长原理提高水产养殖鱼类生长速度和饲料利用效率的方法一度是鱼类生理生态学和水产养殖学研究的热点,但迄今针对不同鱼类种类和不同环境限制条件研究得出的结论存在分歧:部分研究认为一些鱼类种类经过营养限制后可表现出超补偿或完全补偿生长[9];部分研究表明经过营养限制鱼类仅能实现部分补偿生长[10-11]或不表现出补偿生长[12-13]。因此,有关补偿生长原理在制定鱼类养殖饲喂策略中的作用有待进一步探讨。
大口黑鲈(Micropterus salmoides)属鲈形目、太阳鱼科、黑鲈属,俗称加州鲈,为淡水肉食性鱼类[1]。大口黑鲈原产地为北美洲,20世纪80年代引入我国进行人工养殖,目前在广东、浙江、江苏等省已形成较大的池塘养殖规模。有关大口黑鲈饲料营养需求已有较多的研究[1-4],但关于大口黑鲈补偿生长能力尚未见报道。本文研究了不同投喂-停喂时间对大口黑鲈摄食、生长、食物利用、鱼体组成和氮、磷废物排放的影响,目的是确定能否利用补偿生长原理来改进大口黑鲈的投喂技术。
1 材料与方法 1.1 实验鱼和养殖系统饲养实验在浙江大学紫金港校区水产养殖基地进行。所用大口黑鲈鱼种购自浙江省德清县某淡水鱼苗种场。实验前挑选出270尾大小规格相近的鱼,在9个室内玻璃钢循环水水槽(直径80 cm,高70 cm,容积350 L)内驯养2周。驯养密度为30尾/水槽。驯养期间,每天分2次(8:00和16:00)投喂根据浙江大学水域生态系统与水产养殖实验室配方制作的配合饲料(含粗蛋白质50%,粗脂肪9%,灰分13%)[2]。
1.2 实验设计采用单因素实验设计。设S0、S1和S23个处理。S0:每天正常投喂;S1:每投喂3 d停喂1 d;S2:每投喂7 d停喂1 d。实验时间为8周;在实验期间S1组交替投喂-停喂14次,S2组交替投喂-停喂7次。
实验开始前将驯养的鱼停喂24 h,然后集中在一个水槽中。每次随机选取25尾鱼,成群称量后随机放入9个室内玻璃钢循环水水槽中。实验鱼初始体质量为(14.4±0.3)g。放养后从剩余的暂养鱼中随机取3组鱼(每组5尾),分别测量鱼体质量、体长和肝质量,然后保存在冰箱(-20 ℃)中作为分析鱼体组成的样品。
实验期间,每天8:00和16:00按饱食量投喂。每天下午换水1次,换水量约100 L。水槽内连续充气,并按3 L/min流速与水处理系统循环。每天下午用虹吸方法将水槽内的鱼粪吸出。实验期间,水温为(21.1±1.3)℃,pH为6.8±0.1,溶解氧为(8.6±0.2)mg/L。采用自然光照,光照周期为14 h光照,10 h黑暗。
实验结束时,将鱼停喂24 h,然后将每个水槽内的鱼捕出并成群称量。从每个水槽内随机取3尾鱼,分别测量体质量、体长和肝质量,然后保存在冰箱(-20 ℃)中作为分析鱼体组成的样品。
1.3 化学分析将所取的实验鱼样品在室温下化冻、称量后,放在高压灭菌锅内(125 ℃)蒸煮20 min,在105 ℃下烘干至恒量。将干燥样品粉碎并通过40目筛。根据AOAC方法[14]分析饲料及实验鱼水分、粗蛋白质、脂肪、灰分和磷含量。
1.4 数据计算与统计分析摄食率(feed intake,FI)、体质量增加(mass gain,MG)、特定生长率(specific growth rate,SGR)、饲料系数(feed conversion ratio,FCR)、氮保留效率(nitrogen retention efficiency,NRE)、磷保留效率(phosphorus retention efficiency,PRE)、肥满度(condition factor,CF)、肝体比(hepatosomatic index,HSI)、饲料氮废物排放(nitrogen waste output,NWO)和饲料磷废物排放(phosphorus waste output,PWO)分别按下列公式计算:
FI/(%/d)=I/[(m0+mt)/2×t]×100;
MG/g=mt/Nt-m0/N0;
SGR/(%/d)=[ln(mt/Nt)-ln(m0/N0)]/t×100;
FCR=I/(mt-m0);
NRE/%=(mt×CNt-m0×CN0+md×CN0)/(I×CNf);
PRE/%=(mt×CPt-m0×CPo+md×CPo)/(I×CPf)×100;
CF/(g/cm3)=ms/Ls3×100;
HSI/%=mL/ms×100;
NWO/(g/kg)=1000×(I×CNf)×(1-NRE/100)/(mt-m0+md);
PWO/(g/kg)=1000×(I×CPf)×(1-PRE/100)/(mt-m0+md).
其中:I为实验期间每个水槽内投喂的饲料量,g;m0和mt分别为实验开始和结束时鱼体质量,g;N0和Nt为实验开始和结束时每个水槽内鱼尾数;t为实验时间,d;md为每个水槽内死鱼的总质量,g;CN0和CNt分别为实验开始和结束时鱼体氮含量,%;CP0和CPt分别为实验开始和结束时鱼体磷含量,%;CNf和CPf分别为饲料氮、磷含量,%;ms为实验开始和结束时所取样品鱼的体质量,g;Ls为实验开始和结束时所取样鱼的体长,cm;mL为实验开始和结束时所取样品鱼的肝质量,g。
采用单因素方差分析检验不同投喂-停喂时间对FI、MG、SGR、FCR、NRE、PRE、CF、HSI、全鱼组成(水分、蛋白质、脂肪、灰分和磷)、NWO和PWO的影响。若方差分析差异显著,用邓肯检验进一步比较不同处理间的差异。FI、SGR、NRE、PRE、HSI、鱼体组成(水分、蛋白质、脂肪、灰分和磷)等用百分数表示的数据进行方差分析前先经过反正弦变换。取P<0.05为差异显著性水平。
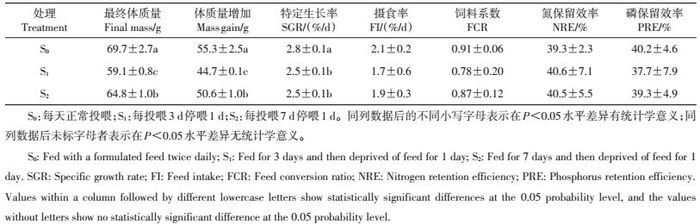
2 结果与分析 2.1 大口黑鲈的摄食、生长和饲料利用效率从表 1可见:实验结束时S0组鱼体质量和体质量增加显著高于S1和S2组(P<0.05),S1组最终体质量和体质量增加明显高于S2组(P<0.05);SGR变化趋势与体质量增加相同;随投喂-停喂时间比例下降,FI和FCR呈下降趋势,但不同处理组间FI和FCR差异均无统计学意义(P>0.05);不同处理之间NRE和PRE差异也均无统计学意义(P>0.05)。
| 表1 不同投喂-停喂时间大口黑鲈摄食、生长和饲料利用效率 Table 1 Feed intake, growth and feed utilization efficiency of largemouth bass fed with different regimes of feeding and feed deprivation |
 |
| 点击放大 |
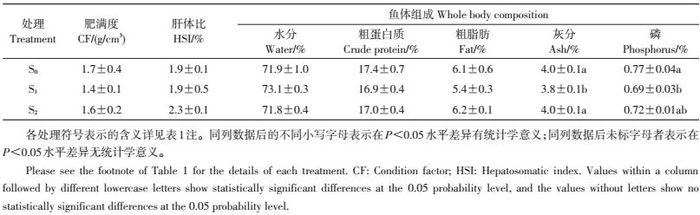
从表 2可见:随投喂-停喂时间比例的降低,CF、HSI、鱼体粗蛋白质和粗脂肪含量均呈下降趋势,鱼体水分含量呈上升趋势,但不同处理间差异无统计学意义(P>0.05);S0组实验鱼体灰分及磷含量在统计学上显著高于S1组(P<0.05),而与S2组间差异无统计学意义(P>0.05)。
| 表2 不同投喂-停喂时间大口黑鲈肥满度、肝体比及鱼体组成 Table 2 Condition factor, hepatosomatic index and whole body composition of largemouth bass fed with different regimes of feeding and feed deprivation |
 |
| 点击放大 |
从图 1可见:交替进行投喂和停喂对氮、磷废物排放量未产生显著影响(P>0.05);实验期间S0、S1和S2组大口黑鲈氮排放量相对于鱼产量为41.6~44.1 g/kg,磷排放量为11.6~12.2 g/kg。
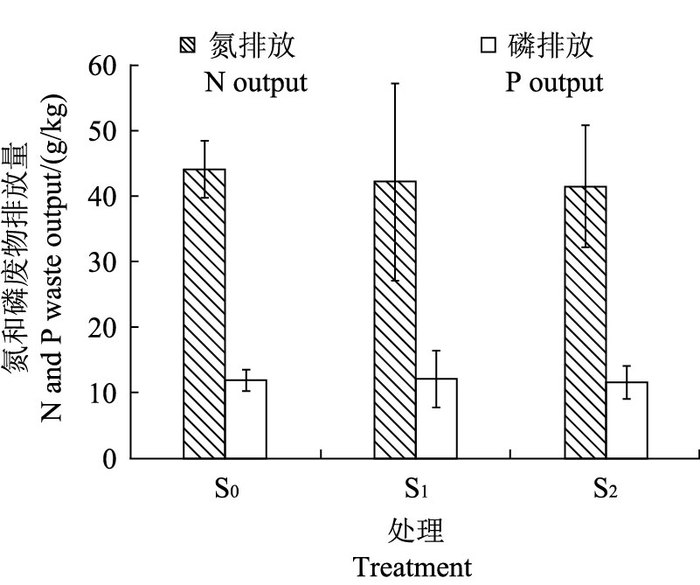 |
| 各处理符号表示的含义详见表 1注。 Please see the footnote of Table 1 for the details of each treatment. 图1 不同投喂-停喂时间大口黑鲈的氮和磷废物排放 Fig. 1 Nitrogen (N) and phosphorus (P) waste output of largemouth bass fed with different regimes of feeding and feed deprivation |
通常,根据前期经过营养限制的鱼在恢复营养阶段的特定生长率(SGR)和体质量与对照鱼(未受过营养限制)的差异来判定是否发生补偿生长以及补偿生长的强度。完全补偿指前期经过营养限制的鱼在恢复营养阶段结束时体质量与对照鱼无显著差异;部分补偿指前期经过营养限制的鱼在恢复营养阶段结束时体质量仍明显低于对照鱼,但在恢复期间SGR明显高于对照鱼[7-8]。在本研究中,S0组鱼饲料系数和氮保留效率与HUANG等[2]报道的相关实验相比无显著差异,说明对照鱼摄食正常。S1和S2组在实验结束时鱼体质量明显低于S0组:表明大口黑鲈经过停喂后再恢复投喂未实现完全补偿。由于本实验采用交替投喂和停喂的方法,每次停喂或投喂的时间较短,难以确定每次停喂结束时以及恢复投喂结束时的鱼体质量和鱼体组成。假定S1和S2组停喂期间鱼体质量未变化(MG = 0),根据实际投喂时间(S1组停喂14 d,投喂42 d;S2组停喂7 d,投喂49 d)计算出S1和S2组投喂期间的SGR分别为(3.4± 0.1)%/d和(3.1± 0.1)%/d,明显高于S0组(P<0.05),由此判断S1和S2组在恢复投喂期间表现出部分补偿生长。
对鱼类补偿生长能力的认识至今存在分歧。部分研究表明,一些鱼类种类经过饥饿后在恢复投喂期间表现出部分补偿生长[11];但另外的研究表明,同种鱼类经过饥饿后恢复投喂可表现出超补偿或完全补偿能力,如HAYWARD等[9]报道,交替投喂-停喂杂交太阳鱼时其体质量增加可达到正常投喂时的2倍:表明交替停喂-投喂较一次性投喂-停喂有利于诱导补偿生长。CUI等[15]发现,交替停喂-投喂时银鲫(Carassius auratus gibelio)未表现出完全补偿生长,认为采用该种投喂策略不能增强银鲫的补偿生长。本研究采用2种交替投喂-停喂周期时大口黑鲈表现出部分补偿生长,这与早期对罗非鱼(Oreochromis niloticus L.)和银鲫的研究结论一致[15-20]。S1和S2组投喂期间的体质量增加分别为(1.06±0.10)g/d和(1.03±0.10)g/d;鉴于大口黑鲈的体质量增加随着停喂时间的增加而降低,据此推算,使鱼产量不至于下降的交替投喂-停喂时间应为每投喂13 d后停喂1 d。
3.2 交替投喂-停喂对大口黑鲈摄食和饲料利用效率的影响鱼类实现补偿生长的机制包括:1)增加摄食[8, 21-22];2)提高食物利用效率[23-24];3)增加摄食和提高食物利用效率[16]。在本研究中,按实际投喂时间计算的S1和S2组的摄食率分别为(2.2±0.6)%/d和(2.3±0.3)%/d,均高于S0组。鉴于S1和S2组的饲料系数(FCR)和氮保留效率(NRE)与S0组无显著差异,可以认为在恢复投喂期间大口黑鲈是通过增加摄食,而非提高食物利用效率来实现补偿生长。整个实验期间,S1组和S2组的摄食率和FCR均低于S0组:表明采用交替投喂和停喂的方法有助于降低大口黑鲈养殖中的FCR。
3.3 交替投喂-停喂对大口黑鲈鱼体形态和组成的影响鱼类饥饿时会利用体内贮存的蛋白质、脂肪和碳水化合物来提供能量[6]。CUI等[20]报道:银鲫在饥饿的第1周内主要利用脂肪提供代谢能量,随饥饿时间延长鱼体脂肪含量迅速下降,而蛋白质消耗速率保持相对恒定;当鱼体蛋白质消耗量超过脂肪消耗量时耗氧率降低至最低点。王岩[16]报道,鱼类在补偿生长期间鱼体组成恢复往往先于体质量恢复。在本研究中,实验结束时S1和S2组肥满度、肝体比、全鱼粗蛋白质和粗脂肪含量与S0组无显著差异,表明交替投喂3 d停喂1 d或交替投喂7 d停喂1 d未导致大口黑鲈鱼体形态和全鱼组成发生显著变化;而S2组全鱼磷含量低于S0组,表明交替投喂3 d停喂1 d可导致鱼体内磷的流失。至于长期交替投喂-停喂是否会影响大口黑鲈体内磷含量有待进一步的实验检验。
3.4 交替投喂-停喂对大口黑鲈氮、磷废物排放的影响HUANG等[2]报道,在不同饲料蛋白质和脂肪水平下大口黑鲈氮排放和磷排放分别为43~56 g/kg和10~16 g/kg,认为大口黑鲈在养殖中的氮废物排放量低于多数温水性海水鱼类(氮排放往往超过50 g/kg)。在本研究中,大口黑鲈氮排放为41.6~44.1 g/kg,磷排放为11.6~12.2 g/kg,与前期研究[3]结果接近,进一步证实了投喂配合饲料时大口黑鲈的氮、磷废物排放量较低。S1和S2组大口黑鲈氮排放和磷排放略低于S0组:表明采用交替投喂-停喂策略可降低大口黑鲈的氮、磷排放量,有利于减轻大口黑鲈养殖水体内氮、磷废物的积累。
4 结论本文研究了不同投喂-停喂时间对大口黑鲈摄食、生长、食物利用、鱼体组成和氮、磷废物排放的影响。结果表明,采用交替投喂-停喂方法可影响大口黑鲈的摄食率、体质量增加、饲料系数、饲料氮和磷废物排放,并且该影响与投喂-停喂时间的比例有关。在实际生产中,通过利用补偿生长原理,可以适当改进大口黑鲈投喂技术,以期获得更好的生产效益。根据本实验结果,当在大口黑鲈池塘养殖中采用交替投喂-停喂策略时,合理的停喂-投喂时间应为投喂13 d停喂1 d。
| [1] |
陈乃松, 肖温温, 梁勤朗, 等. 饲料中脂肪与蛋白质比对大口黑鲈生长、体组成和非特异性免疫的影响. 水产学报, 2012, 36(8): 1270-1280. CHEN N S, XIAO W W, LIANG Q L, et al. Effects of dietary lipid to protein ratios on growth performance, body composition and non-specific immunity of largemouth bass (Micropterus salmoides). Journal of Fisheries of China, 2012, 36(8): 1270-1280. (in Chinese with English abstract) |
| [2] | HUANG D, WU Y, LIN Y Y, et al. The suitable dietary protein and lipid levels for juvenile largemouth bass (Micropterus salmoides). Journal of the World Aquaculture Society, 2017(online). DOI:10.1111/jwas.12417 |
| [3] | PORTZ L, CYRINO J E P, MARTINO R C. Growth and body composition of juvenile largemouth bass Micropterus salmoides in response to dietary protein and energy levels. Aquaculture Nutrition, 2002, 7(4): 247-254. |
| [4] | TIDWELL J H, WEBSTER C D, COYLE S D. Effects of dietary protein level on second year growth and water quality for largemouth bass (Micropterus salmoides) raised in ponds. Aquaculture, 1996, 145(1/2/3/4): 213-223. |
| [5] | WU Y B, HAN H, QIN J G, et al. Effect of feeding frequency on growth, feed utilization, body composition and waste output of juvenile golden pompano (Trachinotus ovatus) reared in net pens. Aquaculture Research, 2015, 46(6): 1435-1443. |
| [6] |
谢小军, 邓利, 张波. 饥饿对鱼类生理生态学影响的研究进展. 水生生物学报, 1998, 22(2): 181-188. XIE X J, DENG L, ZHANG B. Advances and studies on ecophysiological effects of starvation on fish. Acta Hydrobiologica Sinica, 1998, 22(2): 181-188. (in Chinese with English abstract) |
| [7] | ALI M, NICIEZA A, WOOTTON R J. Compensatory growth in fishes: A response to growth depression. Fish and Fisheries, 2003, 4(2): 147-190. DOI:10.1046/j.1467-2979.2003.00120.x |
| [8] | BILTON H T, ROBINS G L. The effect of starvation and subsequent feeding on survival and growth of Fulton Channel sockeye salmon fry (Oncorhynchus nerka). Journal of the Fisheries Research Board of Canada, 1973, 30(1): 1-5. DOI:10.1139/f73-001 |
| [9] | HAYWARD R S, NOLTIE D B, WANG N. Use of compensatory growth to double hybrid sunfish growth rates. Transactions of the American Fisheries Society, 1997, 126(2): 316-322. DOI:10.1577/1548-8659(1997)126<0316:NUOCGT>2.3.CO;2 |
| [10] | QUINTON J C, BLAKE R W. The effect of feed cycling and ration level on the compensatory growth response in rainbow trout, Oncorhynchus mykiss. Journal of Fish Biology, 1990, 37(1): 33-41. DOI:10.1111/jfb.1990.37.issue-1 |
| [11] | JOBLING M, MELOY O H, DOS S J, et al. The compensatory growth response of the Atlantic cod: Effects of nutritional history. Aquaculture International, 1994, 2(2): 75-90. DOI:10.1007/BF00128802 |
| [12] | DOBSON S H, HOLMES R M. Compensatory growth in the rainbow trout, Salmo gairdneri Richardson. Journal of Fish Biology, 1984, 25(6): 649-659. DOI:10.1111/jfb.1984.25.issue-6 |
| [13] |
线薇薇, 朱鑫华. 摄食水平对梭鱼生长和能量收支的影响. 海洋与湖沼, 2001, 32(6): 612-620. XIAN W W, ZHU X H. Effect of ration size on the growth and energy budget of the mullet Liza Haematocheila (T. ET S.). Oceanologia et Limnologia Sinica, 2001, 32(6): 612-620. (in Chinese with English abstract) |
| [14] | AOAC (Association of Official Analytical Chemists). Official Methods of Analysis. AOAC, Arlington, Virgini, USA, 1995. |
| [15] | CUI Z H, WANG Y, QIN J G. Compensatory growth of group-held gibel carp, Carassius auratus gibelio (Bloch), following feed deprivation. Aquaculture Research, 2006, 37(3): 313-318. DOI:10.1111/are.2006.37.issue-3 |
| [16] |
王岩. 海水养殖罗非鱼补偿生长的生物能量机制. 海洋与湖沼, 2001, 32(3): 233-239. WANG Y. Bioenergetics of hybrid tilapia (Oreochromis niloticus × O. aueus) reared in seawater, in relation to compensatory growth. Oceanologia et Limnologia Sinica, 2001, 32(3): 233-239. (in Chinese with English abstract) |
| [17] | WANG Y, CUI Y, YANG Y, et al. Partial compensatory growth in hybrid tilapia (Oreochromis mossambicus × O. niloticus) following food deprivation. Journal of Applied Ichthyology, 2005, 21(5): 389-393. DOI:10.1111/jai.2005.21.issue-5 |
| [18] |
崔正贺, 王岩. 初始体重差异对异育银鲫补偿生长的影响. 海洋与湖沼, 2007, 38(1): 8-14. CUI Z H, WANG Y. Compensatory growth in gibel carp (Carassius auratus gibelio): The effect of initial body size. Oceanologia et Limnologia Sinica, 2007, 38(1): 8-14. (in Chinese with English abstract) |
| [19] | WANG Y, CUI L, QIN J G, et al. Cyclical regimes of food deprivation and re-feeding fail to enhance compensatory growth magnitude for Nile tilapia, Oreochromis niloticus L. Aquaculture Research, 2009, 40(2): 204-210. DOI:10.1111/are.2009.40.issue-1 |
| [20] | CUI Z, WANG Y. Temporal changes in body mass, body composition and metabolism of gibel carp (Carassius auratus gibelio) during food deprivation. Journal of Applied Ichthyology, 2007, 23(3): 215-220. DOI:10.1111/jai.2007.23.issue-3 |
| [21] | WEATHERLEY A H, GILLS H S. Recovery growth following periods of restricted rations and starvation in rainbow trout Salmo gairdneri Richardson. Journal of Fish Biology, 1981, 18(2): 195-208. DOI:10.1111/jfb.1981.18.issue-2 |
| [22] | KIM M K, LOVELL R T. The effect of restricted feeding regimens on compensatory weight gain and body tissue changes in channel catfish Ictalurus punctatus in ponds. Aquaculture, 1995, 135(4): 285-293. DOI:10.1016/0044-8486(95)01027-0 |
| [23] |
邓利, 张波, 谢小军. 南方鲇继饥饿后的恢复生长. 水生生物学报, 1999, 23(2): 167-173. DENG L, ZHANG B, XIE X J. The recovery growth in the southern catfish (Silurus meridionalis) following starvation. Acta Hydrobiologica Sinica, 1999, 23(2): 167-173. (in Chinese with English abstract) |
| [24] |
李程琼, 冯健, 刘永坚, 等. 奥尼罗非鱼多重周期饥饿后的补偿生长. 中山大学学报(自然科学版), 2005, 44(4): 99-102. LI C Q, FENG J, LIU Y J, et al. Compensatory growth on hybrid tilapia, Oreochromis aureus × Oreochromis niloticus. Acta Scientiarum Naturalium Universitatis Sunyatseni, 2005, 44(4): 99-102. (in Chinese with English abstract) |
 2017, Vol. 43
2017, Vol. 43


