


2. 延安大学附属医院内分泌代谢科,陕西 延安 716000
庞静(1978-),女,学士,主任医师,研究方向:结直肠癌致病机制,共同第一作者,E-mail: rlslzh@163.com。
李芳(1990-),女,博士,讲师,硕士生导师,研究方向:结直肠癌分子调控机制,通信作者,E-mail: 18792873198@163.com
2. Dept of Endocrinology and Metabolism, Affiliated Hospital of Yan′an University, Yan′an Shaanxi 716000, China
结直肠癌(colorectal cancer,CRC)是临床上常见的一种消化系统恶性肿瘤,是肿瘤相关死亡的主要原因之一[1]。晚期CRC一线化疗药物—伊立替康可通过结合DNA单链断裂位点上的DNA拓扑异构酶Ⅰ,形成伊立替康—DNA拓扑异构酶Ⅰ—DNA复合物,进而使DNA单链断裂转变为双链断裂来抑制DNA复制,从而发挥抑制肿瘤的作用[2]。但部分CRC患者会出现获得性耐药,最终影响伊立替康的化疗效果[3]。因此,深入探究IRI的耐药机制并改善其化疗耐药性是目前CRC临床治疗亟待解决的关键问题之一。
白藜芦醇(resveratrol,RES)是一种天然的植物抗毒素,广泛存在于葡萄、虎杖、花生等多种植物中;其不仅具有抗氧化和抗炎作用,还具有良好的抗肿瘤活性,在肿瘤的发生、进展及转移等阶段均有一定的化学预防作用[4-5]。如RES可通过调节糖代谢重编程,在肝癌的癌前阶段抑制二乙基亚硝胺诱导的大鼠肝细胞过度增殖[6]。RES可诱导CRC细胞凋亡,并抑制CRC细胞的上皮-间充质转化(epithelial-mesenchymal transition,EMT)进程和干细胞样转变,从而在CRC的发生发展过程中发挥抑癌作用[7]。此外,RES还被证实能够通过PI3K/AKT/mTOR通路逆转卵巢癌细胞对顺铂的化疗耐药性[8]。但目前鲜有关于RES在CRC细胞IRI化疗耐药性调控中的作用及其分子机制的相关报道。另一方面,EGFR/AKT/mTOR信号通路在肿瘤进展和放化疗耐受性调控等方面扮演重要角色[9-11]。如CD109可通过激活EGFR/AKT/mTOR信号通路促进肺癌的转移和化疗耐药[10]。TBMS1可部分通过抑制EGFR诱导的PI3K/AKT/mTOR/NF-κB信号通路活化来提高替莫唑胺耐药胶质母细胞瘤细胞的化疗敏感性[11]。但RES能否通过下调EGFR/AKT/mTOR信号通路来改善CRC细胞的IRI化疗耐药性目前尚未见报道。
本研究以CRC细胞系HT-29和RKO为研究对象,通过MTT实验、克隆形成实验及划痕实验等探究分析RES在CRC细胞增殖、迁移及IRI化疗耐药性方面的调控作用,并进一步阐明RES通过下调EGFR/AKT/mTOR信号通路来改善CRC细胞IRI化疗耐药性的相关分子机制。这对于提高CRC患者的化疗效果并延长其生存期具有重要意义。
1 材料与方法 1.1 主要试剂RES购自源叶生物(B20044);伊立替康购自Selleck(S5026);EGFR激活剂NSC 228155购自MCE(HY-101084);AKT激活剂SC79购自Selleck(S7863);AKT抑制剂MK2206购自碧云天(SF2712);MTT试剂购自索莱宝(M8180)。MMP2、MMP9、EGFR、p-AKT、AKT、p-mTOR、mTOR等抗体均购自Proteintech,货号分别为:10373-2-AP、10375-2-AP、51071-2-AP、66444-1-Ig、60203-2-Ig、67778-1-Ig、66888-1-Ig;β-actin抗体购自全式金生物(HC201-02)。
1.2 细胞培养所用细胞均来自延安大学医学研究实验中心细胞库。人CRC细胞系HT-29和RKO细胞分别用含10%胎牛血清的5A培养液与DMEM培养液培养于37 ℃、5% CO2的培养箱中。除特殊说明外,均选取对数生长期的CRC细胞用于后续实验。除特殊说明外,药物处理浓度如下:HT-29细胞RES处理浓度为80 μmol·L-1,IRI处理浓度为10 μmol·L-1;而RKO细胞RES处理浓度为40 μmol·L-1,IRI处理浓度为2.5 μmol·L-1;且NSC 228155、SC79、MK2206的药物处理浓度分别为2 μmol·L-1、10 μmol·L-1和2 μmol·L-1。
1.3 MTT实验将细胞接种于96孔板中(HT-29细胞:3×103个/孔,RKO细胞:2.5×103个/孔),24 h后分别加入不同浓度的药物,置于37 ℃、5% CO2培养箱中培养。分别于24 h、48 h、72 h时加入MTT试剂(20 μL/孔),37 ℃孵育4 h,酶标仪检测490 nm处A值,并计算细胞的存活率。
1.4 克隆形成实验药物处理48h后,将细胞以1×103个/孔的密度接种于12孔板中,置于37 ℃、5% CO2培养箱中培养7-10 d。接着用PBS冲洗细胞2次,4%多聚甲醛固定30 min,0.1%结晶紫染色30 min,冲洗、干燥并拍照。用500 μL DMSO溶解后,酶标仪检测570 nm处A值。
1.5 划痕实验将细胞接种于6孔板中,培养至细胞密度80%~90%时,用10 μL移液器枪尖垂直划线;PBS冲洗2次后,更换为含药的1%胎牛血清培养基,记为0 h,拍照。药物处理细胞24 h和48 h后,更换为新鲜含药的1%胎牛血清培养基,拍照,计算细胞迁移率。
1.6 Western blot药物作用48h后,用RIPA裂解液提取CRC细胞总蛋白,BCA蛋白定量,取20 μg进行电泳、转膜和封闭等。一抗4 ℃孵育过夜,二抗室温孵育1.5 h,加入ECL发光液曝光显影。
1.7 统计学分析本研究以SPSS 22.0软件为统计工具,对所得实验数据进行统计学分析,结果以x±s表示。两组间比较采用独立样本t检验,多组间比较采用单因素方差分析,检验水准α=0.05。
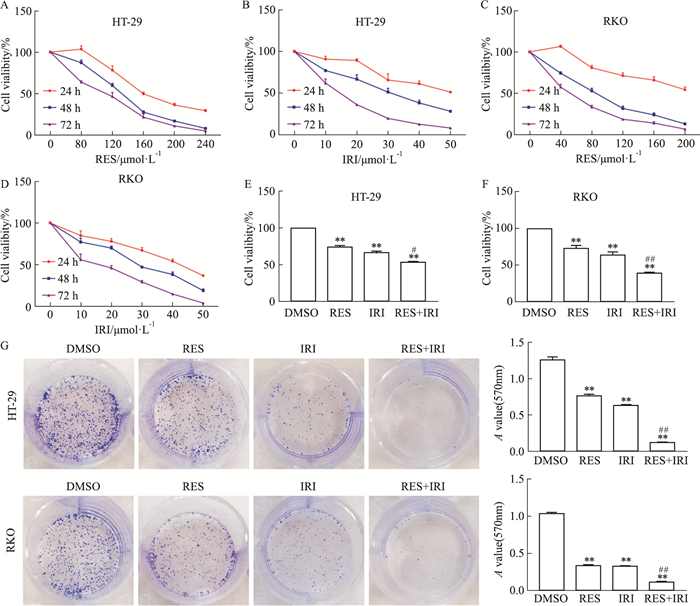
2 结果 2.1 RES可改善CRC细胞的IRI化疗耐药性为探究RES与IRI对CRC细胞增殖的影响,分别用不同浓度梯度的RES和IRI处理人CRC细胞HT-29(RES:0、80、120、160、200、240 μmol·L-1;IRI:0、10、20、30、40、50 μmol·L-1)与RKO(RES:0、40、80、120、160、200 μmol·L-1;IRI:0、2.5、5、10、20、40 μmol·L-1),采用MTT法检测分析CRC细胞的增殖能力。结果如Fig 1A-D所示,RES和IRI均可明显抑制HT-29和RKO细胞增殖,且呈时间与剂量依赖性。经GraphPad Prism 8软件计算,RES作用于HT-29和RKO细胞的48 h半数抑制浓度(IC50)分别为130.9 μmol·L-1和78.98 μmol·L-1,IRI作用于HT-29和RKO细胞的48 h半数抑制浓度(IC50)分别为28.88 μmol·L-1和10.12 μmol·L-1。根据量效曲线,选取起效浓度RES 80 μmol·L-1联合IRI 10 μmol·L-1作用于HT-29细胞,RES 40 μmol·L-1联合IRI 2.5μmol·L-1作用于RKO细胞。MTT与克隆形成实验结果表明,与对照组(DMSO处理组)相比,RES单药处理组、IRI单药处理组、RES与IRI联合处理组的CRC细胞增殖能力均明显降低,且RES与IRI联合处理组的细胞增殖能力明显低于IRI单药处理组,提示RES可明显增强IRI对CRC细胞能力的抑制作用(Fig 1E-G)。
|
| Fig 1 RES combined with IRI inhibited proliferation of CRC cells(x±s, n=3) A, B: The effect of RES and IRI on the proliferation of HT-29 cells; C, D: The effect of RES and IRI on the proliferation of RKO cells; E, F: The effect of RES combined with IRI on the proliferation of CRC cells; G: The effect of RES, IRI and their combination on the colony forming ability of CRC cells. **P < 0.01 vs DMSO group; #P < 0.05, ##P < 0.01 vs IRI group. |
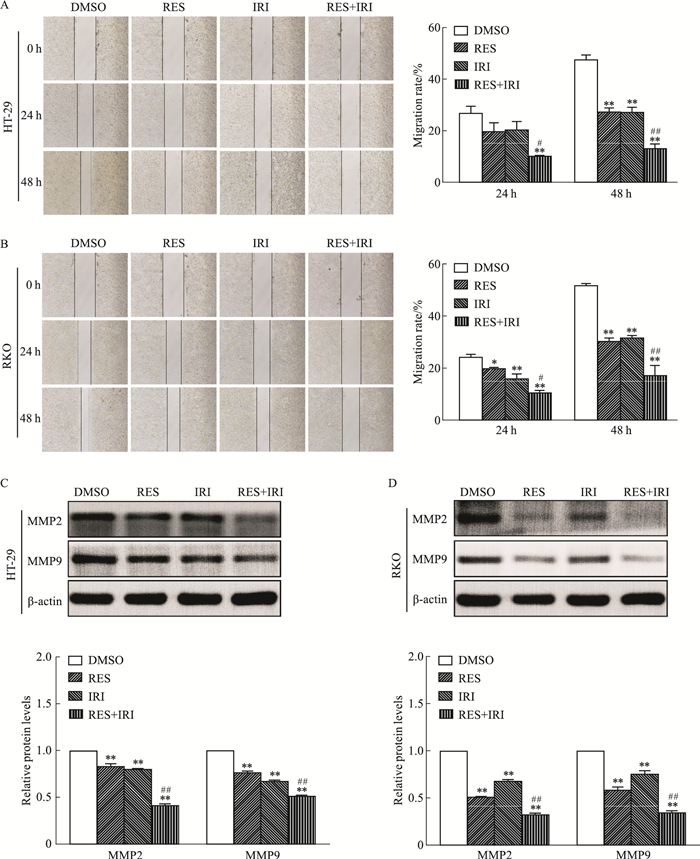
接下来,通过划痕实验检测分析了RES、IRI及这两者联合对CRC细胞迁移的影响。与对照组相比,RES单药处理组、IRI单药处理组及RES与IRI联合处理组CRC细胞的迁移能力均明显降低;且RES与IRI联合处理组CRC细胞的迁移能力明显低于IRI单药处理组(Fig 2A,B)。与此一致,Western blot结果表明,与对照组相比,RES单药处理组、IRI单药处理组及RES与IRI联合处理组CRC细胞中迁移标志分子MMP2及MMP9的蛋白表达水平均明显降低;且RES与IRI联合处理组CRC细胞中这两种蛋白的表达水平均明显低于IRI单药处理组(Fig 2C, D)。这些实验结果表明,RES可明显增强IRI对CRC迁移的抑制作用。综上可得,RES能够改善CRC细胞的IRI化疗耐药性。
|
| Fig 2 RES combined with IRI inhibited migration of CRC cells(x±s, n=3) A, B: The effect of RES, IRI and their combination on the migration of CRC cells; C, D: Western blot analysis was performed to analyze the effect of RES, IRI and their combination on the protein expression levels of migration markers MMP2 and MMP9 in CRC cells. *P < 0.05, **P < 0.01 vs DMSO group; #P < 0.05, ##P < 0.01 vs IRI group. |
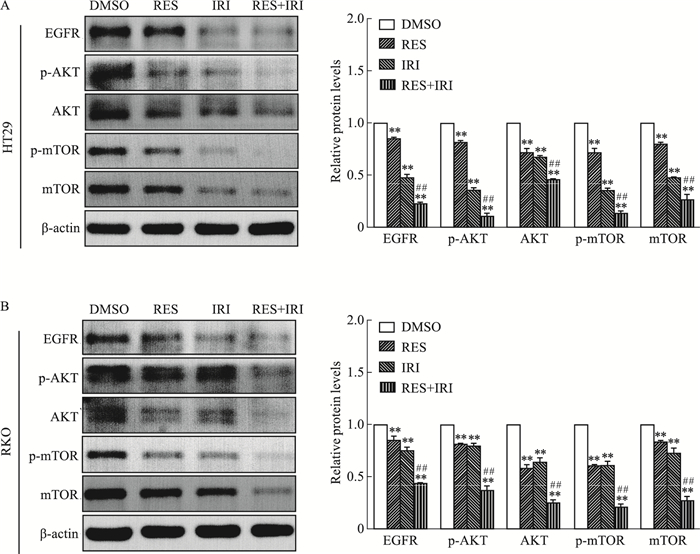
鉴于EGFR/AKT/mTOR信号通路在肿瘤化疗耐药中的重要作用,通过Western blot探究分析RES是否通过下调EGFR/AKT/mTOR信号通路来改善CRC细胞IRI化疗耐药性。结果表明,相比于对照组,RES单药处理组、IRI单药处理组及RES与IRI联合处理组CRC细胞中EGFR、p-AKT、AKT、p-mTOR、mTOR的蛋白表达水平均明显降低;且这些蛋白在RES与IRI联合处理组CRC细胞中的表达水平均明显低于IRI单药处理组(Fig 3A, B)。这些研究结果提示,RES可能通过下调EGFR/AKT/mTOR信号通路来抑制CRC细胞增殖和迁移,进而改善其IRI化疗耐药性。
|
| Fig 3 RES ameliorated IRI chemoresistance of CRC cells through EGFR/AKT/mTOR pathway(x±s, n=3) A, B: The effect of RES, IRI and their combination on the protein expression levels of EGFR/AKT/mTOR signaling pathway in CRC cells. **P < 0.01 vs DMSO group; ##P < 0.01 vs IRI group. |
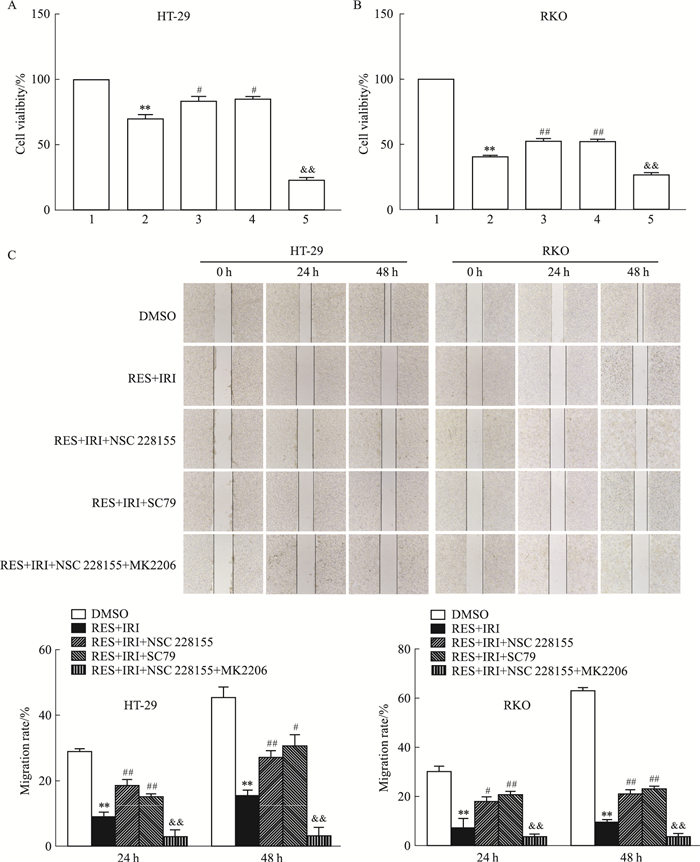
用EGFR激活剂(NSC 228155)、AKT激活剂(SC79)及AKT抑制剂(MK2206)进一步验证RES是否通过下调EGFR/AKT/mTOR信号通路来改善CRC细胞的IRI化疗耐药性。这里共分为5个处理组:DMSO组、RES+IRI组、RES+IRI+NSC 228155组、RES+IRI+SC79组、RES+IRI+NSC 228155+MK2206组。结果发现RES+IRI+NSC 228155组与RES+IRI+SC79组CRC细胞的增殖和迁移能力均明显高于RES+IRI组,而RES+IRI+NSC 228155+MK2206组CRC细胞的增殖和迁移能力均明显低于RES+IRI+NSC 228155组(Fig 4A-C)。以上研究结果表明,NSC 228155与SC79均可逆转RES对IRI化疗耐药性的改善作用,而MK2206能够部分逆转NSC 228155的这种作用。
|
| Fig 4 Both NSC 228155 and SC79 reversed ameliorating effect of RES on IRI chemoresistance of CRC cells(x±s, n=3) 1:DMSO; 2:RES+IRI; 3:RES+IRI+NSC 228155; 4:RES+IRI+SC79; 5:RES+IRI+NSC 228155+MK2206. A, B: The effect of NSC 228155, SC79 and MK2206 on the proliferation of CRC cells; C: The effect of NSC 228155, SC79 and MK2206 on the migration of CRC cells. **P < 0.01 vs DMSO group; #P < 0.05, ##P < 0.01 vs RES+IRI group; && P < 0.01 vs RES+IRI+NSC 228155 group. |
RES作为一种广泛存在于葡萄、虎杖、花生等多种植物中的天然有机化合物,除具有很好的抗炎、抗氧化作用,还被证实具有良好的抗肿瘤活性[4-5]。有研究表明,RES能够以浓度依赖的方式来抑制CRC细胞HCT116与SW480的增殖和集落形成[12]。与此一致,本研究发现RES可明显抑制CRC细胞HT-29和RKO的增殖、迁移,表明其在CRC中具有良好的抗肿瘤活性。除抗肿瘤活性外,RES可能在肿瘤化疗耐药中也发挥了重要调控作用。据报道,RES不仅能够逆转甲状腺未分化癌对多西他赛/阿霉素的继发性耐药,还可通过降低ADAM9的蛋白表达水平来抑制食管鳞状细胞癌和肺癌细胞的迁移,且RES与达沙替尼、5-FU等临床化疗药物联用具有良好的协同抗癌作用[13-14]。但目前鲜有关于RES在CRC细胞IRI化疗耐药中的调控作用及其分子机制的相关报道。本研究发现,相比于IRI单药处理组,RES与IRI联合处理组CRC细胞的增殖和迁移能力明显降低,即RES可增强IRI对CRC细胞增殖和迁移的抑制作用。提示:RES能够改善CRC细胞的IRI化疗耐药性,在CRC的临床治疗中具有很好的应用前景。
EGFR为受体酪氨酸激酶ErbB家族成员之一,其可通过激活下游AKT/mTOR信号通路参与调控肿瘤发生发展过程中的多个环节,包括细胞增殖、细胞分化、细胞凋亡、血管生成及自噬等[15]。众多研究证据表明,EGFR/AKT/mTOR信号通路激活在肿瘤细胞的增殖、迁移、侵袭及其放化疗抗性中发挥关键调控作用[9]。但EGFR/AKT/mTOR信号通路在CRC细胞IRI化疗耐药性中的调控作用相关研究报道较少。研究表明,相比于非靶向脂质体,运载IRI的EGFR靶向脂质体在体内外表现出更好的抗肿瘤活性[16]。IRI处理可使CRC细胞中MSH2蛋白表达水平上调,反过来,MSH2表达上调又能够减弱CRC细胞的CPT-11敏感性,而AKT信号通路已被发现可调节这一过程[17]。与此一致,本研究结果表明,RES可通过下调EGFR/AKT/mTOR信号通路来改善CRC细胞的IRI化疗耐药性。即与IRI单药处理组相比,RES与IRI联合处理组CRC细胞中EGFR、p-AKT、AKT、p-mTOR、mTOR的蛋白表达水平均明显降低,提示EGFR/AKT/mTOR信号通路转导受到抑制。有趣的是,本研究发现,RES不仅能下调AKT和mTOR的磷酸化水平,还能够降低AKT及mTOR的总蛋白表达水平,从而抑制CRC细胞增殖迁移并改善其IRI化疗耐药性。这与姜黄素等其他药物通过下调AKT和mTOR的磷酸化水平来发挥肿瘤抑制作用有所不同[18]。这些研究证据提示,RES通过EGFR/AKT/mTOR信号通路调控CRC细胞IRI化疗耐药性的分子调控网络机制可能比我们设想的更为复杂,接下来我们将对此展开更为深入的研究。而EGFR激活剂(NSC 228155)与AKT激活剂(SC79)均可逆转RES对CRC细胞IRI化疗耐药性的改善作用,反之AKT抑制剂(MK2206)能够部分逆转EGFR激活剂的这种作用。这些研究结果表明,RES至少部分通过下调EGFR/AKT/mTOR信号通路来改善CRC细胞的IRI化疗耐药性。
综上,RES可能通过下调EGFR/AKT/mTOR信号通路来抑制CRC细胞增殖和迁移,进而改善CRC细胞的IRI化疗耐药性。这为RES与IRI联合治疗CRC提供了坚实的理论基础,对于CRC患者化疗效果的改善及其生存期的延长具有重要意义。
| [1] |
Sung H, Ferlay J, Siegel R L, et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2021, 71(3): 209. doi:10.3322/caac.21660 |
| [2] |
Benson A B, Venook A P, Al-Hawary M M, et al. NCCN guidelines insights: colon cancer, version 2.2018[J]. J Natl Compr Canc Netw, 2018, 16(4): 359-69. doi:10.6004/jnccn.2018.0021 |
| [3] |
Dekker E, Tanis P J, Vleugels J L A, et al. Colorectal cancer[J]. The Lancet, 2019, 394(10207): 1467. doi:10.1016/S0140-6736(19)32319-0 |
| [4] |
杨君, 沙前坤, 李玉先, 等. 白藜芦醇苷通过MAPK和Nrf2/HO-1通路减轻LPS引起的炎症反应[J]. 中国药理学通报, 2021, 37(12): 1674-9. Yang J, Sha Q K, Li Y X, et al. Resveratrol glycosides reduce LPS-induced inflammatory response through MAPK and Nrf2/HO-1 pathways[J]. Chin Pharm Bull, 2021, 37(12): 1674-9. |
| [5] |
Boxu R, Marabeth X Y K, Cuiliu L, et al. Resveratrol for cancer therapy: challenges and future perspectives[J]. Cancer Lett, 2021, 515: 63-72. doi:10.1016/j.canlet.2021.05.001 |
| [6] |
齐晓茹, 孙思语, 程金妞, 等. 白藜芦醇通过糖代谢重编程抑制DEN诱导大鼠肝细胞癌前阶段的恶性增殖[J]. 中国生物化学与分子生物学报, 2019, 38(9): 1213-25. Qi X R, Sun S Y, Cheng J N, et al. Resveratrol inhibits DEN induced precancerous proliferation of rat hepatocytes by glucose metabolic reprogramming[J]. Chin J Biochem Mol Biol, 2019, 38(9): 1213-25. doi:10.13865/j.cnki.cjbmb.2022.07.1642 |
| [7] |
Constanze B, Mina Y, Bastian P, et al. Resveratrol chemosensitizes tnf-β-induced survival of IRI-treated colorectal cancer cells[J]. Nutrients, 2018, 10(7): 888. doi:10.3390/nu10070888 |
| [8] |
Muhanmode Y, Wen M K, Maitinuri A, et al. Curcumin and resveratrol inhibit chemoresistance in cisplatin-resistant epithelial ovarian cancer cells via targeting P13K pathway[J]. Hum Exp Toxicol, 2021, 40(12 suppl): S861-8. |
| [9] |
Wu M, Zhang P. EGFR-mediated autophagy in tumourigenesis and therapeutic resistance[J]. Cancer Lett, 2020, 469: 207-16. doi:10.1016/j.canlet.2019.10.030 |
| [10] |
Lee K Y, Shueng P W, Chou C M, et al. Elevation of CD109 promotes metastasis and drug resistance in lung cancer via activation of EGFR-AKT-mTOR signaling[J]. Cancer Sci, 2020, 111(5): 1652-62. doi:10.1111/cas.14373 |
| [11] |
Tang Q, Cao H, Tong N, et al. Tubeimoside-I sensitizes temozolomide-resistant glioblastoma cells to chemotherapy by reducing MGMT expression and suppressing EGFR induced PI3K/Akt/mTOR/NF-κB-mediated signaling pathway[J]. Phytomedicine, 2022, 99: 154016. doi:10.1016/j.phymed.2022.154016 |
| [12] |
Brockmueller A, Shayan P, Shakibaei M. Evidence that β1-integrin is required for the anti-viability and anti-proliferative effect of resveratrol in CRC cells[J]. Int J Mol Sci, 2022, 23(9): 4714. doi:10.3390/ijms23094714 |
| [13] |
Xiong L, Lin X M, Nie J H, et al. Resveratrol and its nanoparticle suppress doxorubicin/Docetaxel-resistant anaplastic thyroid cancer cells in vitro and in vivo[J]. Nanotheranostics, 2021, 5(2): 143-54. doi:10.7150/ntno.53844 |
| [14] |
Lin Y S, Hsieh C Y, Kuo T T, et al. Resveratrol-mediated ADAM9 degradation decreases cancer progression and provides synergistic effects in combination with chemotherapy[J]. Am J Cancer Res, 2020, 10(11): 3828-37. |
| [15] |
Alzahrani A S. PI3K/Akt/mTOR inhibitors in cancer: at the bench and bedside[J]. Semin Cancer Biol, 2019, 59: 125-32. doi:10.1016/j.semcancer.2019.07.009 |
| [16] |
Liu Y, Li X, Pen R, et al. Targeted delivery of irinotecan to colon cancer cells using epidermal growth factor receptor-conjugated liposomes[J]. Biomed Eng Online, 2022, 21(1): 53. doi:10.1186/s12938-022-01012-8 |
| [17] |
Lee K C, Yen C K, Chen C N, et al. Drug resistance of CPT-11 in human DLD-1 colorectal cancer cells through MutS homolog 2 upregulation[J]. Int J Med Sci, 2021, 18(5): 1269-76. doi:10.7150/ijms.52620 |
| [18] |
Gong X, Jiang L, Li W, et al. Curcumin induces apoptosis and autophagy inhuman renal cell carcinoma cells via Akt/mTOR suppression[J]. Bioengineered, 2021, 12(1): 5017-27. doi:10.1080/21655979.2021.1960765 |

