


2. 贵州医科大学 天然药物资源优效利用重点实验室,贵州 贵阳 550025;
3. 暨南大学肿瘤药理研究所,广东 广州 510632
 ,
SONG Yu-xuan2,
FAN Shuang-qin2,
REN Shuang2,
ZHANG Yue2,
CHEN Yan2,
SHEN Xiang-chun2,
LIU Tong-zheng2,
ZHANG Min1,2
,
SONG Yu-xuan2,
FAN Shuang-qin2,
REN Shuang2,
ZHANG Yue2,
CHEN Yan2,
SHEN Xiang-chun2,
LIU Tong-zheng2,
ZHANG Min1,2

2. Key Laboratory of Optimal Utilization of Natural Medicinal Resources, Guizhou Medical University, Guiyang 550025, China;
3. Jinan University Institute of Tumor Pharmacology Research, Guangzhou 510632, China
乳腺癌是全球女性中最常见的恶性肿瘤[1]。约70%为雌激素受体(estrogen receptor,ER)阳性,抗雌激素的内分泌治疗是该类患者主要的治疗手段[2]。作为最有效和最常用的抗雌激素药物,他莫昔芬(Tamoxifen,TAM)已被证实可大大延长乳腺癌患者的生存期[3]。尽管大多数患者从这种治疗中获益,但临床数据显示,大约50%的患者对他莫昔芬产生耐药性,最终导致复发和死亡[4]。
G蛋白偶联雌激素受体(G-protein coupled estrogen receptor,GPER),又称GPR30,在结构上不同于经典的ERα和ERβ,是一种新型雌激素受体,介导多种雌激素反应[5],并在获得性他莫昔芬耐药中起重要作用。据有关文献报道,他莫昔芬对GPER具有激动作用,体内外研究数据表明,GPER的表达与他莫昔芬耐药密切相关[6],同时也是影响他莫昔芬治疗过程的一个不利生存因素。G15是一种取代的二氢喹啉类似物,可抑制GPER,有望应用于增加他莫昔芬耐药细胞敏感性[7]。因此,本研究探讨GPER抑制剂G15能否增加TAM对T-47DTR耐药细胞诱导凋亡的作用,恢复耐药细胞对他莫昔芬的敏感性,为抑制GPER增加耐药细胞对治疗药物敏感性提供理论依据。
1 材料与方法 1.1 药品与试剂人乳腺癌他莫昔芬耐药细胞株T47D Tam1(CRL-3436TM,T-47DTR)购自美国ATCC公司,人乳腺癌T-47D细胞株购于中国科学院昆明细胞库。高糖DMEM培养基(Gibco公司),胎牛血清(Gibco公司)。4-OHT(Cat#ab143638)购自Abcam公司,G15(Cat#14673)购自Sigma公司;BCA蛋白定量试剂盒(Cat#23227)购自赛默飞世尔科技(中国)有限公司;Annexin V-FITC/PI双染细胞凋亡检测试剂盒购自江苏凯基生物技术股份有限公司;细胞膜蛋白与细胞质蛋白抽提试剂盒(Cat#P0033)购自碧云天生物技术有限公司。MTT粉末(Cat#M8180)购自北京索莱宝公司。caspase-9/p35/p10单克隆抗体(Cat#66169-1-Ig),caspase-3/p17/p19单克隆抗体(Cat#66470-2-Ig),BAX多克隆抗体(Cat#50599-2-Ig),Bcl2多克隆抗体(Cat#26593-1-AP)抗体均购自proteintech公司;Na+, K+-ATPase α1(Y10)多克隆抗体(BS1436),β-actin(4D3)单克隆抗体-HRP(Cat#BS6007M),羊抗鼠IgG(H+L)HRP(Cat#BS12478),羊抗兔IgG(H+L)HRP(Cat#BS13278)抗体均购自Bio-World公司;GPER多克隆抗体(Cat#PA5-28647)购自美国Invitrogen公司。
1.2 主要仪器3111二氧化碳培养箱(赛默飞世尔科技(中国)有限公司);ChemiDoc XRS+凝胶成像系统(美国Bio-Rad公司);ACEA NovoCyte 3008流式细胞仪(美国艾森公司);MicrofugeⓇ 20R冷冻离心机(美国Beckman Coulter公司);ELX800酶标仪(美国BioTek公司)。
1.3 方法 1.3.1 细胞培养T47D Tam1(T-47DTR)细胞系按照ATCC的标准方案进行培养,在培养基中补充1 μmol·L-1 4-OHT以维持他莫昔芬的耐药性。其中T-47DTR使用含有10%胎牛血清(FBS)和10 mg·L-1胰岛素的DMEM培养液培养。T47D细胞系在添加10% FBS的DMEM中培养。所有细胞均在5% CO2和37 ℃条件下培养。
1.3.2 MTT法检测细胞存活率取对数生长期T-47D/TR耐药细胞或其亲本细胞T-47D, 按照8×103个/孔接种于96空板内,培养24 h后,给予不同浓度4-OHT(0.5、1、2.5、5、10 μmol·L-1)作用48 h,另设阴性对照(Control组),每组5个复孔。然后将MTT溶液(5 g·L-1,20 μL)添加到每个孔中并再孵育4 h。然后除去培养基,加入DMSO(100 μL/孔)并充分混合。使用酶标仪在570 nm处测量吸光度(OD)值。重复3次,将所得数据进行计算,得出各浓度药物下的抑制率(inhibition rate,IR),IR/%=[(OD对照组-OD4-OHT)/OD对照组]×100%。
1.3.3 Western blot检测蛋白表达取对数生长期T-47DTR耐药细胞接种于6孔板内,按照实验分组T-47DTR、T-47DTR+4-OHT(2 μmol·L-1)、T-47DTR+G15(5 μmol·L-1)和T-47DTR+4-OHT(2 μmol·L-1)+G15(5 μmol·L-1)给药48 h后。使用含有PMSF(1 mmol·L-1)和蛋白酶抑制剂混合物(1 ∶100)的裂解缓冲液提取细胞总蛋白,离心并收集上清,采用BCA蛋白定量试剂盒进行蛋白定量。按照45 μɡ共20 μL分装各组蛋白并进行电泳,湿法转膜,2%牛血清白蛋白封闭。封闭完成后,根据抗体说明书稀释一抗,4 ℃孵育过夜,再加入相应二抗室温孵育90 min,采用Bio-Rad凝胶成像系统获取图像,并使用Image Lab分析软件计算蛋白印迹结果的灰度值。
1.3.4 细胞凋亡检测取对数生长期T-47DTR耐药细胞接种于6孔板内,按“1.3.3”项给药48 h后,用不含EDTA胰酶消化收集细胞,PBS洗涤细胞两次,2 000 r·min-1,5 min收集1×105细胞,进行FITC/PI双染,室温避光反应15 min后进行流式细胞仪检测。
1.3.5 膜浆分离分析根据试剂盒说明书方法,分离细胞膜蛋白和细胞质蛋白,通过Western blot定量分析GPR30在细胞内分布的变化。
1.3.6 统计学处理所有结果均表示为至少3个独立实验的平均值±标准差。使用t检验分析两组之间的差异,并使用单因素方差分析分析多组之间的差异。
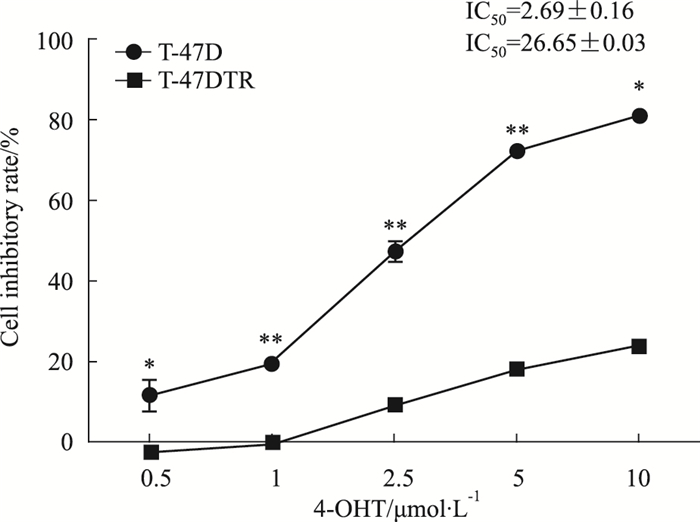
2 结果 2.1 4-OHT对T-47D和T-47DTR细胞生长抑制的影响MTT结果显示,不同浓度4-OHT(0.5、1、2.5、5、10 μmol·L-1)作用48 h后,与T-47D亲本细胞相比,T-47DTR耐药细胞对4-OHT的抵抗性明显增强,其4-OHT对T-47D和T-47DTR细胞的IC50值分别为(2.69±0.16)μmol·L-1、(26.65±0.03)μmol·L-1,两者比较差异具有统计学意义(Fig 1)。
|
| Fig 1 Effect of 4-OHT on growth inhibition of T-47D and T-47DTR cells(x±s, n=3) *P < 0.05, **P < 0.01 vs T-47D/TR |
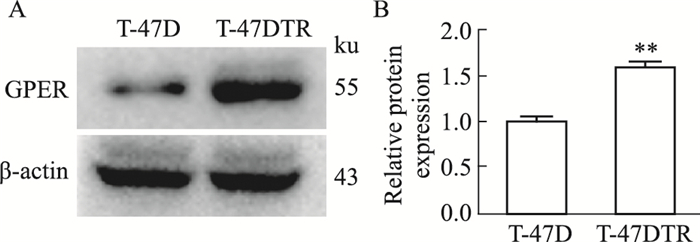
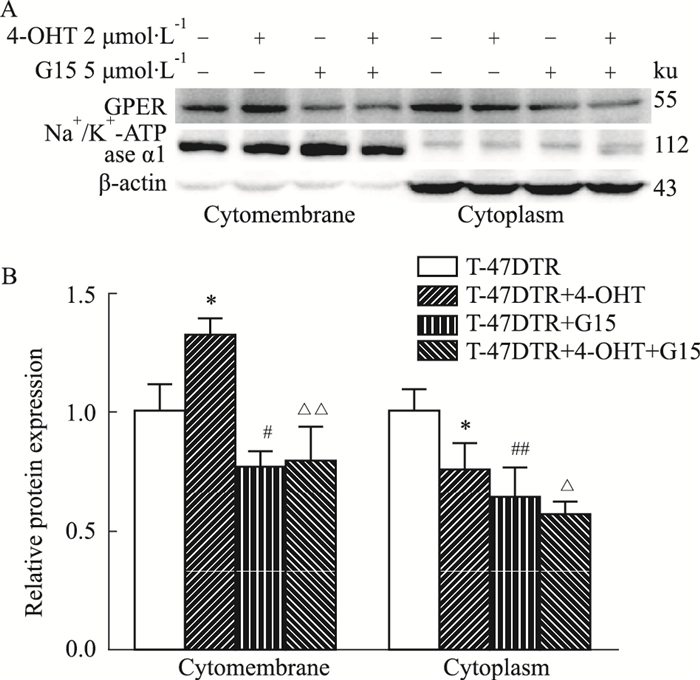
如Fig 2所示,与T-47D亲本细胞相比,T-47DTR耐药细胞中GPER蛋白表达明显上调;在T-47DTR耐药细胞中,给予4-OHT作用48 h后,与空白对照组比较,GPER在细胞膜内易位增加,给予G15处理后能明显降低4-OHT诱导的T-47DTR细胞中GPER蛋白表达上调(Fig 3)。
|
| Fig 2 Expression of GPER protein in T-47D and T-47DTR cells(x±s, n=3) A: The representative photographs; B: The statistical analysis. **P < 0.01 vs T-47D. |
|
| Fig 3 Effect of G15 on GPER protein expression of T-47D/TR cells(x±s, n=3) A: The representative photographs; B: The statistical analysis. *P < 0.05 vs T-47D/TR; #P < 0.05, ##P < 0.01 vs T-47D/TR; ΔP < 0.05, ΔΔP < 0.01 vs T-47D/TR+4-OHT. |
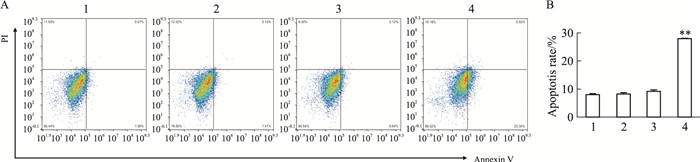
与单用4-OHT组或对照组相比,4-OHT联用G15组总凋亡率增加,表明G15可增强4-OHT对T-47DTR细胞的抑制作用(Fig 4),结果提示,G15能够增加T-47DTR耐药细胞对他莫昔芬的敏感性。
|
| Fig 4 Apoptosis in T-47DTR cells induced by G15(x±s, n=3) A: The representative photographs; B: The statistical analysis. 1:T-47DTR; 2:T-47DTR+4-OHT; 3: T-47DTR+G15; 4: T-47DTR+4-OHT+G15. **P < 0.01 vs T-47DTR+4-OHT. |
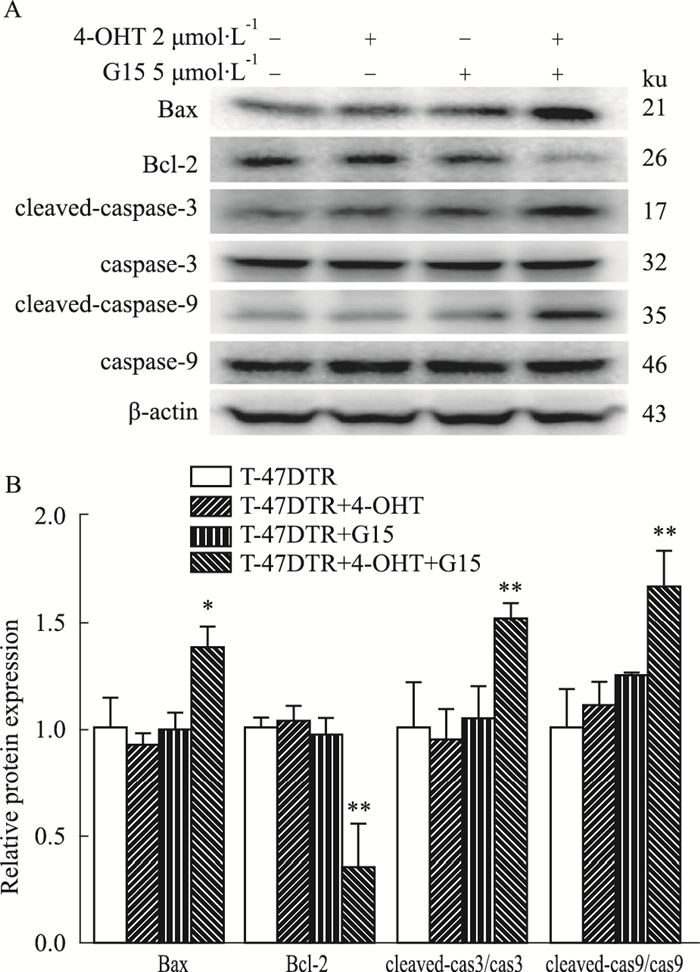
Western blot结果显示,与单用4-OHT组或对照组相比,4-OHT联用G15处理48 h后,T-47DTR耐药细胞中Bax表达显著增加,Bcl-2表达显著降低;cleaved-caspase 3和cleaved-caspase 9表达增加(Fig 5)。表明G15影响凋亡相关蛋白的表达从而恢复T-47DTR耐药细胞对他莫昔芬的敏感性。
|
| Fig 5 Effect of G15 on expression of apoptosis-related proteins in T-47DTR cells(x±s, n=3) A: The representative photographs; B: The statistical analysis. *P < 0.05, **P < 0.01 vs T-47DTR+4-OHT. |
他莫昔芬是一种选择性雌激素受体(ER)调节剂,是世界范围内ER阳性转移性乳腺癌女性最常见的内分泌治疗药物,或作为疾病早期的辅助治疗药物,虽然极大地提高了患者生存率,但并非所有患者都能从其使用中获益[8]。在治疗过程中,原发性或获得性耐药经常出现,并成为乳腺癌内分泌治疗的主要障碍[9],因此,迫切需要探索新的治疗策略,通过克服乳腺癌细胞的耐药性来提高TAM的疗效。
GPER是一种新的膜结合雌激素受体,约在50%的乳腺癌患者中表达,并被认为可以在乳腺癌细胞[10]中介导雌激素的快速效应。在长期使用他莫昔芬治疗的过程中可导致耐药的发生以及GPER的激活[11-13],这与细胞表面GPER的表达增加有关,导致与生长因子受体的串扰增加,并导致细胞增殖增加[14-16]。同样,与我们上述观察到的结果一致,GPER在TAM耐药细胞中表达明显高于其亲本细胞,表明TAM耐药细胞中GPER被激活,以及GPER的膜易位在4-OHT处理后在TAM耐药细胞中增加。提示,GPER受体在TAM治疗的过程中起着关键作用。然而,目前,并未有针对GPER的药物上市。因此,本研究探讨GPER特异性抑制剂G15诱导T-47DTR耐药细胞凋亡,恢复耐药细胞对他莫昔芬的敏感性。首先,我们检测了T-47DTR耐药细胞中4-OHT联用G15对T-47DTR耐药细胞中GPER蛋白表达的影响。结果显示,给予G15可显著减少GPER的表达,与单用4-OHT或对照组相比4-OHT联用G15显著减少GPER表达。
已有研究表明,在TAM耐药的乳腺癌细胞中,GPER通过激活MAPK/ERK-TRIM2信号减少Bim (仅BH3促凋亡蛋白家族成员BCL2-L11),从而减少TAM诱导的凋亡,促进ER阳性乳腺癌细胞中的他莫昔芬耐药性[17]。与上述研究结果相似,本研究结果显示,联用G15能够增加4-OHT诱导T-47DTR耐药细胞发生凋亡,上调凋亡相关蛋白Bax、cleaved-caspase-3、cleaved-caspase-9的活性,下调抗凋亡蛋白Bcl-2,表明G15可增强T-47DTR对他莫昔芬的敏感性。
综上所述,本研究表明G15通过抑制GPER的表达影响T-47DTR耐药细胞凋亡,恢复其对他莫昔芬的敏感性,GPER受体抑制剂G15有望作为耐药增敏剂应用于临床肿瘤耐药患者的治疗。
| [1] |
Miller K D, Nogueira L, Mariotto A B, et al. Cancer treatment and survivorship statistics, 2019[J]. CA Cancer J Clin, 2019, 69(5): 363-85. doi:10.3322/caac.21565 |
| [2] |
沈敬堃, 朱海涛, 梅珈彬, 等. 地高辛和他莫昔芬协同抑制乳腺癌MCF-7细胞的增殖、迁移和侵袭[J]. 中国药理学通报, 2021, 37(9): 1256-63. Shen J K, Zhu H T, Mei J B, et al. Digoxin and Tamoxifen synergistically suppress proliferation, migration and invasion in breast cancer MCF-7 cells[J]. Chin Pharmacol Bull, 2021, 37(9): 1256-63. doi:10.3969/j.issn.1001-1978.2021.09.013 |
| [3] |
Cuzick J, Sestak I, Cawthorn S, et al. Tamoxifen for prevention of breast cancer: extended long-term follow-up of the IBIS-I breast cancer prevention trial[J]. Lancet Oncol, 2015, 16(1): 67-75. doi:10.1016/S1470-2045(14)71171-4 |
| [4] |
Mishra A, Srivastava A, Pateriya A, et al. Metabolic reprograming confers tamoxifen resistance in breast cancer[J]. Chem Biol Interact, 2021, 347: 109602. doi:10.1016/j.cbi.2021.109602 |
| [5] |
Hsu L H, Chu N M, Lin Y F, et al. G-protein coupled estrogen receptor in breast cancer[J]. Int J Mol Sci, 2019, 20(2): 306. doi:10.3390/ijms20020306 |
| [6] |
Ignatov A, Ignatov T, Weissenborn C, et al. G-protein-coupled estrogen receptor GPR30 and tamoxifen resistance in breast cancer[J]. Breast Cancer Res Treat, 2011, 128(2): 457-66. doi:10.1007/s10549-011-1584-1 |
| [7] |
Dennis M K, Field A S, Burai R, et al. Identification of a GPER/GPR30 antagonist with improved estrogen receptor counterselectivity[J]. J Steroid Biochem Mol Biol, 2011, 127(3-5): 358-66. doi:10.1016/j.jsbmb.2011.07.002 |
| [8] |
Saha P, Mandal T, Talukdar A D, et al. DNA polymerase eta: A potential pharmacological target for cancer therapy[J]. J Cell Physiol, 2021, 236(6): 4106-20. doi:10.1002/jcp.30155 |
| [9] |
邹辣, 吴绮楠. 激素受体阳性乳腺癌的内分泌治疗[J]. 重庆医科大学学报, 2021, 46(1): 91-6. Zou L, Wu Q N. Endocrine therapy in hormone receptor positive breast cancer[J]. J Chongqing Med Univ, 2021, 46(1): 91-6. |
| [10] |
赵丕文, Lee D Y, 陶仕英, 等. G蛋白偶联雌激素受体在雌激素相关肿瘤发生中的作用[J]. 中国药理学通报, 2014, 30(8): 1037-41. Zhao P W, Lee D Y, Tao S Y, et al. Effect of G protein-coupled estrogen receptor on the occurrence and development of estrogen related cancer[J]. Chin Pharmacol Bull, 2014, 30(8): 1037-41. doi:10.3969/j.issn.1001-1978.2014.08.001 |
| [11] |
Ignatov A, Ignatov T, Roessner A, et al. Role of GPR30 in the mechanisms of tamoxifen resistance in breast cancer MCF-7 cells[J]. Breast Cancer Res Treat, 2010, 123(1): 87-96. doi:10.1007/s10549-009-0624-6 |
| [12] |
Liu Q, Chen Z, Jiang G, et al. Epigenetic down regulation of G protein-coupled estrogen receptor (GPER) functions as a tumor suppressor in colorectal cancer[J]. Mol Cancer, 2017, 16(1): 87. doi:10.1186/s12943-017-0654-3 |
| [13] |
Sjostrom M, Hartman L, Grabau D, et al. Lack of G protein-coupled estrogen receptor (GPER) in the plasma membrane is associated with excellent long-term prognosis in breast cancer[J]. Breast Cancer Res Treat, 2014, 145(1): 61-71. doi:10.1007/s10549-014-2936-4 |
| [14] |
Jacenik D, Cygankiewicz A I, Krajewska W M. The G protein-coupled estrogen receptor as a modulator of neoplastic transformation[J]. Mol Cell Endocrinol, 2016, 429: 10-8. doi:10.1016/j.mce.2016.04.011 |
| [15] |
Wang D, Hu L, Zhang G, et al. G protein-coupled receptor 30 in tumor development[J]. Endocrine, 2010, 38(1): 29-37. doi:10.1007/s12020-010-9363-z |
| [16] |
王婧, 洪端阳, 陈林, 等. GPER抑制剂对雌激素长期诱导的MCF-12A乳腺上皮细胞生长和克隆形成的影响[J]. 中国医院药学杂志, 2017, 37(3): 235-8. Wang J, Hong D Y, Chen L, et al. Effect of G protein-coupled receptor inhibitor on long-term exposure to 17β-estradiol-induced cell growth and clone formation in MCF-12A cells[J]. Chin J Hosp Pharm, 2017, 37(3): 235-8. |
| [17] |
Yin H, Zhu Q, Liu M, et al. GPER promotes tamoxifen-resistance in ER+ breast cancer cells by reduced Bim proteins through MAPK/ERK-TRIM2 signaling axis[J]. Int J Oncol, 2017, 51(4): 1191-8. doi:10.3892/ijo.2017.4117 |