

2. 河北医科大学病理学教研室,河北 石家庄 050017;
3. 河北医科大学诊断学教研室,河北 石家庄 050017
杨亚坤(1992-),男,硕士生,共同第一作者,研究方向:肾脏病发病机制,E-mail:yangyk611@126.com。
2. Dept of Pathology, Hebei Medical University, Shijiazhuang 050017, China;
3. Dept of Clinical Diagnostics, Hebei Medical University, Shijiazhuang 050017, China
慢性肾脏疾病(chronic kidney disease,CKD)可导致渐进性、不可逆性的肾单位丢失和肾组织损伤,继而出现肾功能障碍,并最终进展至终末期肾功能衰竭(end-stage renal disease,ESRD)。肾脏纤维化是多种慢性肾脏疾病发生、发展的中心环节和重要特征,是其进展至ESRD的共同通路之一[1-2]。早期明确诊断并采取针对性治疗,可有效延缓肾脏纤维化的发生和进展。但是,一直以来,由于纤维化的诊断缺乏早期、精准的特异性标志物,使得其治疗亦缺乏针对性。因此,阐明其发病机制,对于预防及早期干预疾病的发生发展具有重要意义。转化生长因子β(transforming growth factor-β,TGF-β)是一类重要的致纤维化生长因子,其家族成员TGF-β1在肾脏细胞中有广泛表达,可通过抑制细胞外基质(extracellular matrix,ECM)降解,在肾间质基质沉积中发挥重要作用。细胞周期素依赖性蛋白激酶5(cyclin-dependent kinase 5,Cdk5)作为一种蛋白激酶,通过磷酸化相应底物发挥其生理学作用。本课题组前期研究发现,高糖、TGF-β1等因素,可导致p35断裂为p25,继而激活Cdk5,使其激酶活性异常升高,在糖尿病肾病足细胞损伤及凋亡的发生、发展过程中发挥重要作用[3-4]。本文在此基础上,以人肾小球系膜细胞为研究对象,重点探讨TGF-β1调控Cdk5表达在系膜细胞外基质沉积中所起的作用,以期进一步明确TGF-β1促进肾脏纤维化的作用机制,为探索肾脏纤维化的有效防治提供理论依据。
1 材料与方法 1.1 材料 1.1.1 实验试剂DMEM/F12培养基(Gibco)、胎牛血清(Gibco,No.10100147)。TGF-β1(MCE,HY-P7118),Roscovitine(Abcam,ab141847),0.25%胰蛋白酶(Solarbio,No.T1300)。DN-Cdk5质粒(Addgene,#1871)。兔抗Cdk5单克隆抗体(Abcam,ab40773),兔抗p35/25多克隆抗体(CST,#2680),兔多克隆Collagen Ⅳ抗体(Proteintech,No.55131-1AP)、鼠单克隆FN抗体(Proteintech,No.66042-1-Ig),FITC标记羊抗鼠IgG二抗(Jackson ImmunoResearch,115-095- 003),Cy3标记羊抗兔IgG二抗(Jackson ImmunoResearch,111-165-003)。PCR引物(上海生工),Real time-PCR试剂盒(TaKaRa Biotechnology,RR820A)。
1.1.2 细胞人肾小球系膜细胞(HMC)为本实验室冻存细胞,复苏、传代后备用。
1.1.3 仪器设备CO2培养箱(美国Thermo Scientific),恒温孵育箱(天津泰斯特),超低温冰箱(青岛海尔),高速低温离心机(德国Eppendorf),电泳槽、电泳仪(美国Bio-Rad),光学显微镜、荧光显微镜(日本Olympus),荧光实时定量PCR仪(美国Agilent),Odyssey FC成像仪(美国Li-COR Biosciences)。
1.2 方法 1.2.1 细胞分组 1.2.1.1 TGF-β1对Cdk5蛋白及mRNA表达的影响HMC接种于6孔板,10 μg·L-1的TGF-β1分别刺激0、3、6、12、24 h,Western blot、免疫荧光化学法检测Cdk5、p35/25蛋白表达情况,Real time-PCR检测Cdk5 mRNA表达。
1.2.1.2 Cdk5对系膜细胞FN、Collagen Ⅳ表达的影响转染Cdk5过表达质粒,并设置空白对照组和质粒对照组,Western blot、免疫荧光化学法检测FN、Collagen Ⅳ蛋白表达情况。
1.2.1.3 Cdk5抑制剂Roscovitine对TGF-β1刺激HMC后FN、Collagen Ⅳ表达的影响细胞随机分为Control组、TGF-β1刺激组(10 μg·L-1的TGF-β1刺激24 h),TGF-β1+Roscovitine组(10 μg·L-1的TGF-β1和10 μmol·L-1 Roscovitine混合培养基刺激24 h),Western blot、免疫荧光化学法检测FN、Collagen Ⅳ蛋白表达情况,Real time-PCR检测FN、Collagen Ⅳ mRNA的表达。
1.2.1.4 Cdk5干扰质粒对TGF-β1刺激HMC后FN、Collagen Ⅳ表达的影响细胞随机分为Control组、TGF-β1+质粒对照Vector组,TGF-β1+DN-Cdk5组。TGF-β1+Vector组和TGF-β1+DN-Cdk5组,分别转染相应质粒24 h后,再给予TGF-β1(10 μg·L-1)刺激24 h,Western blot、免疫荧光化学法检测FN、Collagen Ⅳ蛋白表达情况,Real time-PCR检测FN、Collagen Ⅳ mRNA的表达。
1.2.2 质粒构建与细胞转染Cdk5过表达质粒和干扰质粒购自Addgene公司。1×108·L-1密度的HMC接种于6孔板,待其生长至约80%密度时,准备转染。将3 μL FuGENE HD、1 μg质粒溶于100 μL不含血清与抗生素的培养基中,混匀,室温静置15 min,加入6孔板中,轻摇,培养6-8 h后改为普通培养基培养。
1.2.3 Western blot检测相关蛋白表达收集细胞,提取总蛋白,BCA法定量。取50 μg总蛋白,加6×上样缓冲液,100 ℃变性5 min,SDS-PAGE凝胶电泳,转移至PVDF膜。5%脱脂奶粉37 ℃封闭2 h,分别加入Cdk5(1∶500)、p35/25(1∶1 000)、FN(1∶1 000)、Collagen Ⅳ(1∶1 000)和β-actin (1∶1 000)抗体,4 ℃孵育过夜。洗膜,加入辣根过氧化物酶标记的IgG(1∶5 000),37 ℃孵育2 h。TTBS洗膜,滴加ECL发光剂,于Odyssey FC成像系统中显影,并对条带进行定量分析。以目的条带和β-actin条带积分光密度值比值代表目的蛋白的相对表达量。
1.2.4 Real time-PCR检测相关mRNA表达TRIzol法提取细胞总RNA,1.5%琼脂糖凝胶电泳鉴定RNA完整性,NanoDrop 1000微量核酸蛋白检测仪测定RNA纯度。按照PrimeScriptTMRT regent Kit说明书进行反转录。取2 μL cDNA产物作为PCR反应模板,荧光实时定量PCR仪检测相关mRNA的表达。Cdk5引物:上游5′-CTTAGGTGACGGCCCATAGT-3′,下游5′-GTAACCTGCCACTTCCACCT-3′;FN引物:上游5′-GAGCTATTCCCTGCACCTGATG-3′,下游5′-CGTGCAAGGCAACCACACT-3′;Col Ⅳ引物:上游5′-GATGGCCAGAAAGGACCAGT-3′,下游5′-GGGATTCGGGGACAGTCATC-3′;18S引物:上游5′-CATTCGAACGTCTGCCCTATC-3′,下游5′-CCTGCTGCCTTCCTTGGA-3′。扩增条件:95 ℃变性15 min,95 ℃ 10 s,55 ℃ 1 min,45个循环,以18S作内参基因,用△△Ct法分析基因的相对表达。
1.2.5 免疫细胞荧光法检测相关蛋白的表达从处理好的细胞培养板底部取出盖玻片,4%多聚甲醛固定;0.3%的Triton X-100打孔;血清封闭,37 ℃孵育;加入相应抗体Cdk5(1∶50)、p35/25(1∶100)、FN(1∶100)、Collagen Ⅳ(1∶100),4 ℃过夜。滴加带FITC或Cy3标记的二抗(1∶50或1∶100稀释),37 ℃避光孵育;用含DAPI的防荧光淬灭封片剂封片,荧光显微镜下观察相应蛋白的表达情况并照片。
1.2.6 统计学处理采用SPSS 17.0统计软件进行统计学分析,数据用x±s表示,各组数据均呈正态分布,方差齐,采用最小显著差异法(LSD)作两两比较;方差不齐,采用Tamhane's T2法作两两比较。
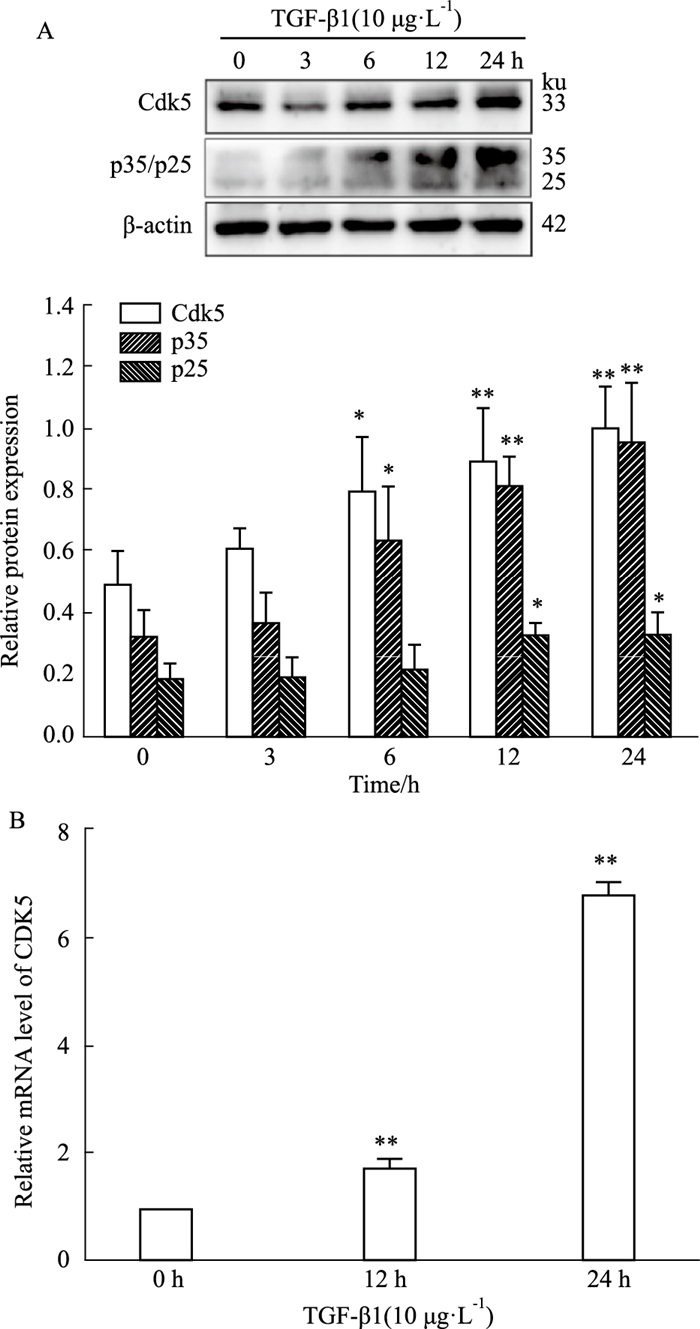
2 结果 2.1 TGF-β1对系膜细胞Cdk5、p35/p25表达的影响TGF-β1(10 μg·L-1)作用于肾小球系膜细胞0、3、6、12、24 h后,随着刺激时间的延长,Western blot检测Cdk5蛋白表达呈时间依赖性增加。p35/p25是Cdk5的特异性协同激动剂,TGF-β1作用后,其蛋白表达与Cdk5一致,也呈时间依赖性增加(Fig 1A)。Real time-PCR法检测TGF-β1作用于系膜细胞0、12、24 h后,Cdk5 mRNA表达的变化。与0 h相比,TGF-β1作用12 h、24 h后,Cdk5 mRNA均明显增加(P<0.01,Fig 1B),作用24 h时,Cdk5 mRNA增加约6.82倍。
|
| Fig 1 Effect of TGF-β1 on expression of Cdk5 and p35/p25 in human mesangial cells (x±s, n=6) A: Western blot; B: Real time-PCR;*P<0.05, **P<0.01 vs 0 h group; TGF-β1: 10 μg·L-1 |
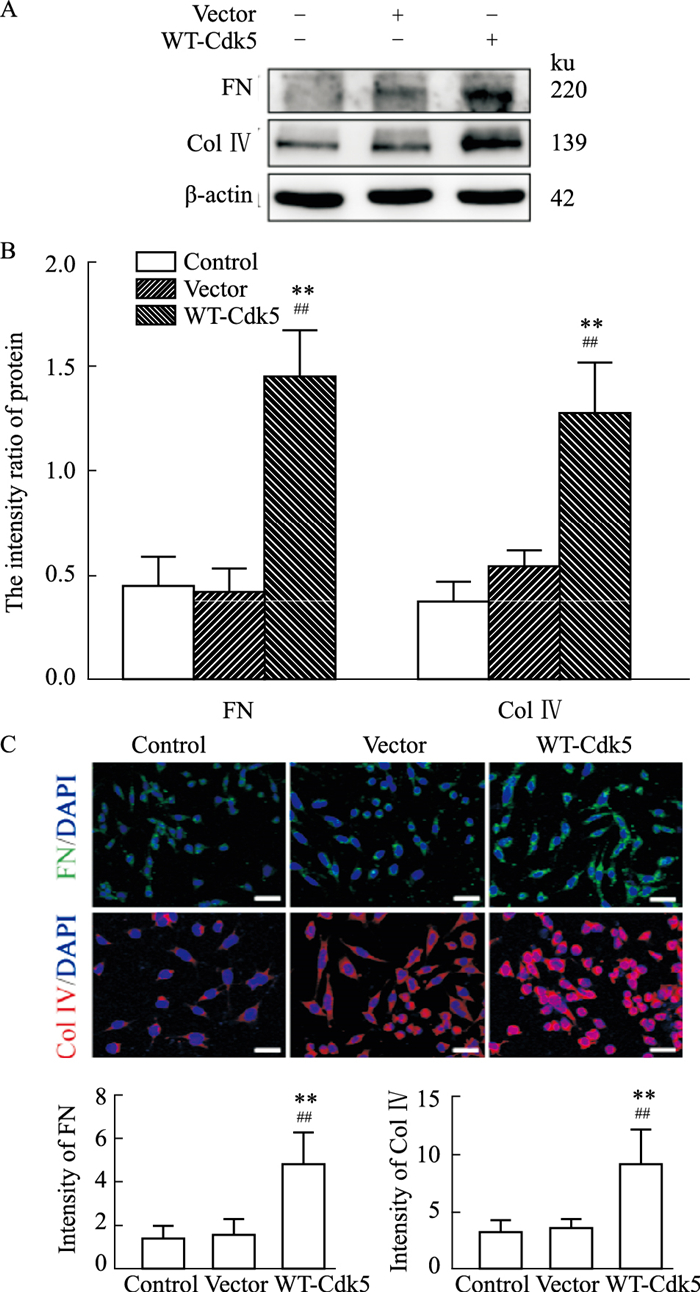
与空白对照组和空白质粒转染组相比,转染Cdk5过表达质粒后,Western blot检测FN、Collagen Ⅳ蛋白表达均明显增高(P<0.01,Fig 2A、B);免疫荧光结果也显示,转染Cdk5质粒后,FN(绿色荧光)、Collagen Ⅳ(红色荧光)蛋白表达明显增强(P<0.01,Fig 2C)。
|
| Fig 2 Effect of Cdk5 on expression of FN and collagen Ⅳ in human mesangial cells (x±s, n=6) A-B: Western blot; C: Immunofluorescence staining;**P<0.01 vs Control group; ##P<0.01 vs Vector group |
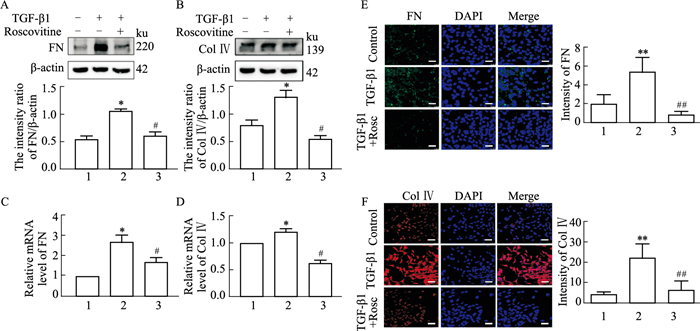
与空白对照组相比,TGF-β1刺激后,Western blot结果显示系膜细胞FN、Collagen Ⅳ蛋白表达均明显增加,而应用Cdk5激酶活性抑制剂Roscovitine后,FN、Collagen Ⅳ表达明显降低(P<0.05,Fig 3A、B);Real time-PCR结果显示,TGF-β1刺激后,FN、Collagen Ⅳ mRNA表达明显增加,应用Roscovitine后,mRNA表达降低(P<0.05,Fig 3C、D);免疫荧光结果显示,与对照组相比,TGF-β1刺激后,FN(绿色荧光)、Collagen Ⅳ(红色荧光)表达明显增多,应用Roscovitine干预后,FN、Collagen Ⅳ表达减少(Fig 3E、F)。
|
| Fig 3 Effect of Roscovitine on expression of FN and collagen Ⅳ in HMC stimulated by TGF-β1 (x±s, n=6) 1. Control; 2. TGF-β1; 3. TGF-β1+Roscovitine. A-B: Western blot; C-D: Real time-PCR; E-F: Immunofluorescence staining;*P<0.05, **P<0.01 vs Control group; #P<0.05, ##P<0.01 vs TGF-β1 group; TGF-β1: 10 μg·L-1; Roscovitine: 10 μmol·L-1 |
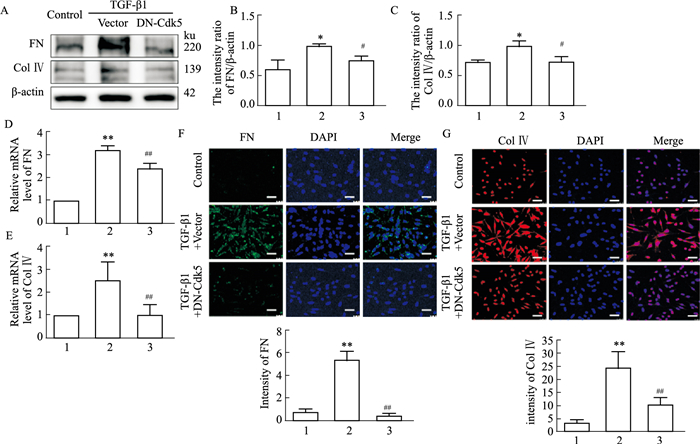
与对照组相比,TGF-β1加空白质粒转染组,Western blot结果检测系膜细胞FN、Collagen Ⅳ蛋白表达均明显增加,而转染Cdk5干扰质粒后,FN、Collagen Ⅳ表达明显降低(P<0.05,Fig 4A-C);Real time-PCR结果可见,TGF-β1加空白质粒转染后,FN、Collagen Ⅳ mRNA表达明显增加,转染Cdk5干扰质粒后,mRNA表达降低(P<0.05,Fig 4D、E);免疫荧光结果显示,与对照组相比,TGF-β1加空白质粒转染组,FN(绿色荧光)、Collagen Ⅳ(红色荧光)表达明显增多,转染Cdk5干扰质粒后,FN、Collagen Ⅳ表达减少(Fig 4F、G)。
|
| Fig 4 Effect of Cdk5 knockdown plasmid on expression of FN and collagen Ⅳ in HMC stimulated by TGF-β1 (x±s, n=6) 1. Control; 2. TGF-β1+vector; 3. TGF-β1+DN-Cdk5. A-C: Western blot; D-E: Real time-PCR; F-G: Immunofluorescence staining;*P<0.05, **P<0.01 vs Control group; #P<0.05, ##P<0.01 vs Vector group; TGF-β1: 10 μg·L-1 |
在我国,慢性肾脏疾病的发病率约为10.8%,正日益成为危害人民身体健康的公共卫生问题之一。肾脏纤维化是多种慢性肾脏疾病的共同病理学特征,主要表现为ECM的大量堆积和肾小管萎缩,并最终导致ESRD。大量研究表明,TGF-β上调与糖尿病肾病、膜性肾病和其他多种慢性肾脏疾病的发生、进展均关系密切,被认为是致肾脏纤维化的关键介质之一,但其具体机制目前尚未完全阐明[5]。
Cdk5是脯氨酸限定性的丝/苏氨酸(Ser/Thr)蛋白激酶,主要通过磷酸化相应底物发挥其生理学作用。一直以来,关于Cdk5生物学功能的研究多集中于神经系统,认为其在维持神经元正常功能和神经系统发育过程中起了关键作用[6-7]。近年来,考虑到Cdk5及其激活亚基p35在许多神经系统外组织,如胰腺、肾脏、卵巢等部位也有广泛表达,其神经系统外作用逐渐引起关注[8]。有研究报道,在抗肾小球基底膜肾炎模型鼠和HIV转基因鼠肾组织中,Cdk5在增殖和去分化足细胞中的表达明显降低;抑制Cdk5的表达可明显改变体外培养的已分化足细胞的形态,出现胞体延长,足突消失;抑制足细胞中p35的表达可显著增加UV辐射、嘌呤霉素氨基核苷等引起的足细胞凋亡,提示肾脏疾病中足细胞的损伤可能与Cdk5/p35的表达异常有关[9-11]。本课题组前期针对糖尿病肾病足细胞的研究也发现,高糖、TGF-β1等因素,可导致p35断裂为p25,继而激活Cdk5,使其激酶活性异常升高,在足细胞损伤及凋亡的发生、发展过程中发挥重要作用[3-4]。
本研究在此基础上,以人肾小球系膜细胞为研究对象,重点探讨TGF-β1调控Cdk5表达在系膜细胞外基质沉积中所起的作用。我们的研究发现,10 μg·L-1的TGF-β1刺激后,随着时间的延长,系膜细胞Cdk5蛋白及mRNA表达呈时间依赖性增加;作为Cdk5的特异性协同激动剂,p35、p25也呈现出与Cdk5一致的表达趋势,可见TGF-β1作用于系膜细胞后,Cdk5被激活。
胶原蛋白是细胞外基质的主要成分,为了观察Cdk5在肾脏纤维化中所起的作用,我们在系膜细胞中转染了Cdk5过表达质粒,观察其对FN、Collagen Ⅳ表达的影响。研究发现,与空白对照组和空白质粒转染组相比,转染Cdk5过表达质粒后,FN、Collagen Ⅳ蛋白表达均明显增高,可见Cdk5在胶原蛋白合成、细胞外基质沉积中起了促进作用。进一步,我们应用Cdk5激酶活性抑制剂Roscovitine或转染Cdk5干扰质粒,目的是降低Cdk5表达,来观察其在TGF-β1促进细胞外基质合成中所起的作用。结果显示,与对照组相比,TGF-β1刺激后,系膜细胞FN、Collagen Ⅳ蛋白及mRNA表达均明显增加;而无论是应用Roscovitine还是转染Cdk5干扰质粒后,FN、Collagen Ⅳ蛋白及mRNA表达均明显降低,可见Cdk5在TGF-β1促进系膜细胞外基质合成的过程中发挥了重要作用。
关于TGF-β1引起肾脏纤维化的机制,目前较多的研究集中在两个方面:即Smad信号通路和非Smad信号通路[12]。在Smad依赖的信号转导通路中,研究报道,TGF-β1可以通过结合TGF-β受体I(TGF-β receptor I,TβRI)表面的丝/苏氨酸激酶受体发挥其细胞效应,导致锚定蛋白SARA与Smad2/3结合并促进其磷酸化;随后,Smad2/3磷酸化复合物与Smad4形成一高阶复合物并在细胞核内积聚;在细胞核中,活性的Smad2/3/4复合物可以调节a-SMA、胶原IA2、PAI-1和MMP-2等的转录,继而促进上皮-间充质转化(epithelial to mesenchymal transition,EMT),导致ECM成分的合成和沉积[13-14]。此外,也有越来越多的证据表明,TGF-β1可以通过Smad信号通路调控多种microRNAs(miRs),进而促进肾纤维化的进程[15]。而TGF-β1的非Smad通路,可刺激平行的下游信号通路,如丝裂原活化蛋白激酶(mitogen-activated protein kinases,MAPK)途径,细胞外信号调节激酶(extracellular signalregulated kinase,ERK)1/2、JNK和p38,以及生长和存活激酶,磷酸肌醇-3-激酶(phopshatidylinositol-3-kinase,PI3K)、Akt和小GTP结合蛋白(Ras、RhoA、Rac1和Cdc42),Notch和Wnt/β-catenin途径等,间接参与EMT、凋亡、分化和基质形成[16]。本课题组前期在对足细胞的研究中发现,TGF-β1可通过ERK1/2通路增强足细胞中Cdk5的表达,而Smads通路并不参TGF-β1对Cdk5的调节过程[3]。因此,我们推测,在系膜细胞,TGF-β1可能同样通过非Smad通路调节Cdk5的表达,发挥对细胞外基质合成的调控作用,其具体作用机制尚需进一步研究。
综上,我们的研究发现,TGF-β1作用于人肾小球系膜细胞,可激活Cdk5,导致FN、Collagen Ⅳ表达增加。而抑制Cdk5后,可降低FN、Collagen Ⅳ的表达水平。可见,Cdk5在TGF-β1致肾小球系膜细胞细胞外基质沉积中发挥了重要作用。抑制Cdk5表达及激酶活性的异常增高,可能是减缓慢性肾脏病肾小球纤维化的重要手段和治疗靶点。我们的研究进一步明确了TGF-β1促进肾脏纤维化的作用机制,为探索肾脏纤维化的有效防治提供理论依据。
| [1] |
Humphreys B D. Mechanisms of renal fibrosis[J]. Annu Rev Physiol, 2018, 80: 309-26. doi:10.1146/annurev-physiol-022516-034227 |
| [2] |
Lv W, Booz G W, Wang Y, et al. Inflammation and renal fibrosis: Recent developments on key signaling molecules as potential therapeutic targets[J]. Eur J Pharmacol, 2018, 820: 65-76. doi:10.1016/j.ejphar.2017.12.016 |
| [3] |
Zhang Y, Li H, Hao J, et al. High glucose increases Cdk5 activity in podocytes via transforming growth factor-β1 signaling pathway[J]. Exp Cell Res, 2014, 326(2): 219-29. doi:10.1016/j.yexcr.2014.04.014 |
| [4] |
Zhang Y, Gao X, Chen S, et al. Cyclin-dependent kinase 5 contributes to endoplasmic reticulum stress induced podocyte apoptosis via promoting MEKK1 phosphorylation at Ser280 in diabetic nephropathy[J]. Cell Signal, 2017, 31: 31-40. doi:10.1016/j.cellsig.2016.12.009 |
| [5] |
Hills C E, Squires P E. The role of TGF-β and epithelial-to mesenchymal transition in diabetic nephropathy[J]. Cytokine Growth Factor Rev, 2011, 22(3): 131-9. |
| [6] |
Shah K, Rossie S. Tale of the good and the bad Cdk5: Remodeling of the actin cytoskeleton in the brain[J]. Mol Neurobiol, 2018, 55(4): 3426-38. doi:10.1007/s12035-017-0525-3 |
| [7] |
Shupp A, Casimiro M C, Pestell R G. Biological functions of CDK5 and potential CDK5 targeted clinical treatments[J]. Oncotarget, 2017, 8(10): 17373-82. doi:10.18632/oncotarget.14538 |
| [8] |
Sharma S, Sicinski P. A kinase of many talents: Non-neuronal functions of CDK5 in development and disease[J]. Open Biol, 2020, 10(1): 190287. doi:10.1098/rsob.190287 |
| [9] |
Griffin S V, Hiromura K, Pippin J, et al. Cyclin-dependent kinase 5 is a regulator of podocyte differentiation, proliferation, and morphology[J]. Am J Pathol, 2004, 165(4): 1175-85. doi:10.1016/S0002-9440(10)63378-0 |
| [10] |
Zheng Y L, Zhang X, Fu H X, et al. Knockdown of expression of Cdk5 or p35 (a Cdk5 activator) results in podocyte apoptosis[J]. PLoS One, 2016, 11(8): e0160252. doi:10.1371/journal.pone.0160252 |
| [11] |
Brinkkoetter P T, Wu J S, Ohse T, et al. p35, the non-cyclin activator of Cdk5, protects podocytes against apoptosis in vitro and in vivo[J]. Kidney Int, 2010, 77(8): 690-9. doi:10.1038/ki.2009.548 |
| [12] |
Chen L, Yang T, Lu D W, et al. Central role of dysregulation of TGF-beta/Smad in CKD progression and potential targets of its treatment[J]. Biomed Pharmacother, 2018, 101: 670-81. doi:10.1016/j.biopha.2018.02.090 |
| [13] |
Ma T T, Meng X M. TGF-beta/Smad and renal fibrosis[J]. Adv Exp Med Biol, 2019, 1165: 347-64. |
| [14] |
李承德, 王煜, 曲敬蓉, 等. 黄芪多糖对糖尿病大鼠肾脏TGF-β1/Smads信号通路的影响[J]. 中国药理学通报, 2018, 34(4): 512-6. Li C D, Wang Y, Qu J R, et al. Effects of astragalus polysaccharide on renal TGF-β1/Smads signaling pathway in rats with diabetes mellitus[J]. Clin Pharmacol Bull, 2018, 34(4): 512-6. doi:10.3969/j.issn.1001-1978.2018.04.015 |
| [15] |
Loboda A, Sobczak M, Jozkowicz A, et al. TGF-beta1/Smads and miR-21 in renal fibrosis and inflammation[J]. Mediators Inflamm, 2016, 2016: 8319283. |
| [16] |
Zhang Y E. Non-Smad signaling pathways of the TGF-beta family[J]. Cold Spring Harb Perspect Biol, 2017, 9(2): a022129. doi:10.1101/cshperspect.a022129 |

