

2. 重庆医科大学药理学教研室,重庆 400016;
3. 重庆市垫江县人民医院药剂科,重庆 408300
2. Dept of Pharmacology, Pharmacy School, Chongqing Medical University, Chongqing 400016, China;
3. Pharmacy Dept, Dianjiang People′s Hospital of Chongqing, Dianjiang Chongqing 408300, China
脑卒中是世界上致死率、致残率最高的疾病之一,严重威胁人类的生命健康[1]。其中缺血性卒中占脑卒中的60%-80%,目前临床上针对缺血性脑卒中主要治疗方式是通过物理或药物溶栓,恢复缺血区血流供应,但血流复灌又会引起脑缺血/再灌注损伤[2]。脑缺血/再灌注损伤的发生发展十分复杂,其发病机制与氧化应激、神经炎症、神经元凋亡、细胞内钙离子超载等多种因素相关,且尚不完全明确。越来越多研究发现自噬参与脑缺血/再灌注损伤的发生发展,且在脑缺血/再灌注不同时期,发挥着截然不同的作用[3-5]。因此,深入探究脑缺血/再灌注中自噬的调控机制,寻找缺血性脑卒中的干预新靶点,为脑缺血/再灌注损伤的预防和治疗提供新的方向显得十分必要。
锌指/环指蛋白2(zinc and ring finger 2,ZNRF2)是一类特殊的膜相关E3泛素连接酶,在中枢和外周神经系统高表达,在维持突触建立发挥着重要的作用[6];ZNRF2还参与氨基酸调节,维持细胞的生长[7]。最新研究表明,ZNRF2在肿瘤细胞的增殖、凋亡进程上发挥着重要作用,然而目前尚未见ZNRF2在神经系统疾病中的作用相关研究报道。因此,本实验拟采用氧糖剥夺/复糖复氧模型(oxygen-glucose deprivation/reoxygenation, OGD/R)模拟脑缺血/再灌注损伤体外模型,初步探讨ZNRF2对脑缺血/再灌注损伤的作用及机制。
1 材料与方法 1.1 细胞PC12细胞(大鼠肾上腺嗜铬瘤细胞),购于武汉普诺赛生命科技有限公司。
1.2 主要试剂DMEM高糖培养基(D649)购于Sigma公司;DMEM无糖培养基(2177535)购于美国Gibco公司;胎牛血清购于以色列Biological Industries公司;马血清(abs989)购于上海爱必信生物科技有限公司;胰蛋白酶(BL512A)、双抗(BL505A)、PBS(BL302A)均购于biosharp公司;ZNRF2过表达慢病毒(LVCON294)载体构建委托上海吉凯基因公司完成;ZNRF2 siRNA干扰序列(R11077.2)由锐博公司合成;ZNRF2抗体(20200-1-AP)购于武汉三鹰生物公司;mTOR(A5866)、LC3B(A52502)、β-actin(A5538)等抗体购于bimake公司;p62(ab56416)、Beclin-1一抗均购于美国Abcam公司;p-mTOR(ser2448)(D9C2)抗体购于CST公司。
1.3 实验仪器细胞超净台(SW-CJ-2FD),高速低温离心机(iCEN-24R),二氧化碳细胞培养箱(311),三气培养箱(3423),多功能酶标仪(721BR05752)均购于美国Thermo Scientific公司;电泳仪(041BR304570),成像仪(VLBL00D2)购于BIO-RAD。
1.4 实验方法 1.4.1 实验分组首先将PC12细胞分为正常组(normal)、模型组(OGD/R),观察ZNRF2在OGD/R模型中的改变;为了进一步观察ZNRF2对OGD/R致PC12细胞损伤的作用,我们采用ZNRF2过表达慢病毒上调ZNRF2表达以及ZNRF2小干扰RNA抑制ZNRF2表达,分别以ZNRF2空载病毒组、siRNA阴性对照作为空白对照组;将PC12细胞分为6组:正常组(normal)、氧糖剥夺/复糖复氧组(OGD/R)、ZNRF2空载病毒组(LV-NC)、ZRNF2过表达慢病毒组(LV-ZNRF2)、siRNA阴性对照组(siNC)、ZNRF2小干扰RNA组(siR-ZNRF2)。
1.4.2 OGD/R模型建立除正常组外,其他组均需氧糖剥夺1 h,复糖复氧24 h建立OGD/R模型:将原有的DMEM高糖培养基弃去,加入DMEM无糖培养基,放入三气培养箱(95% N2、5% O2,37 ℃)氧糖剥夺1 h后,将DMEM无糖培养基替换成DMEM高糖培养基,在5% CO2,37 ℃细胞培养箱中继续培养24 h。
1.4.3 细胞培养与传代在DMEM高糖培养基中加入10%马血清和5%胎牛血清,1%双抗(抗青霉素/链霉素)培养PC12细胞,PC12置于5% CO2、37 ℃温度适宜的培养箱中培养2 d,待细胞生长密度达到85%左右进行传代。
1.4.4 细胞转染PC12按需求密度接种于细胞培养板后,分别加入ZNRF2过表达慢病毒(滴度:4×108 kU·L-1)、空载病毒(病毒滴度:1×109 kU·L-1)感染细胞6-8 h,更换新鲜培养基,继续培养96 h后观察荧光。按riboFECTTMCP Reagent转染试剂说明书转染ZNRF2 siRNA,转染浓度为100 nmol·L-1,于培养箱中培养36 h,经预实验筛选,确定siRNA2为有效序列,后续实验均用siRNA2序列进行,ZNRF2 siRNA序列分别为: siRNA1:5′-CAGATGAAATGGATTTGCA-3′;siRNA2: 5′-AGAGCACCCTTCGGATTAA-3′; siRNA3: 5′-GCAATATGCCTTGAAGAAT-3′; siNC: 5′-GGCUCUAGAAAAGCCUAUGC-3′; 3′-TCCGAGAUCUUUUCGGAUACG-5′。
1.4.5 MTT实验将PC12细胞以8 000个/孔接种于96孔板中培养24 h,建立OGD/R模型后,避光加入配置好的MTT溶液(0.5 g·L-1)20 μL/孔于37 ℃孵育4 h,弃去培养基,避光加入DMSO 150 μL/孔,水平摇床上震荡15 min后,用多功能酶标仪于490 nm处测定吸光度值。
1.4.6 流式细胞术检测各组细胞凋亡率接种于6孔板中的PC12细胞给药造模后,收集上清于15 mL离心管中,用不含EDTA的0.25%胰酶将细胞细化为单个细胞,然后用PBS缓冲液1 000 r·min-1离心5 min,弃去上清,反复两次。最后将细胞重悬于PBS(pH 7.2)500 μL缓冲液中,装于1.5 mL的EP管中,及时送于重庆医科大学生命科学研究院进行细胞凋亡检测。
1.4.7 qRT-PCR检测细胞中ZNRF2mRNA的表达细胞接种于6孔板中培养,OGD/R后,弃去培养基,加入预冷PBS缓冲液轻轻清洗后,加入1 mL TRIzol提取细胞总RNA,根据cDNA逆转录试剂盒操作步骤得到cDNA,以大鼠源β-actin作为内参,采用qRT-RCR检测ZNRF2 mRNA的相对表达量。大鼠源ZNRF2引物序列:前引物:3′-TAAGTGCCCGGTATGCTCAA-5′;后引物:5′-ATATACACAGGCAAGGCAGT-3′。
1.4.8 Western blot检测细胞各类蛋白表达各组细胞给药造模后,用预冷的PBS缓冲液清洗3次,加入RIPA ∶PMSF ∶磷酸酶抑制剂=100 ∶1 ∶2裂解液,用细胞刮收集细胞裂解液置于冰上裂解30 min,低温高速离心12 000 r·min-1,15 min,取上清用BCA试剂盒测量蛋白浓度。凝胶电泳分离蛋白后,转膜后,将含有蛋白的PVDF膜于5% BSA封闭液中室温封闭2 h,加入ZNRF2 (1 ∶800)、LC3B (1 ∶1 000)、p62 (1 ∶2 000)、Beclin-1 (1 ∶1 000)、mTOR (1 ∶1 000)、p-mTOR (1 ∶1 000)、β-actin (1 ∶1 000)一抗4 ℃过夜,TBST缓冲液清洗3次(每次5 min),加入辣根过氧化物标记的二抗(1 ∶4 000)室温孵育1 h,洗膜后,ECL发光液作用后,置于成像仪中成像,Image Lab软件分析,β-actin作为内参。
1.4.9 统计学分析采用SPSS 21.0软件分析数据,数据用x±s表示,多组间比较用单因素方差分析(One-way ANOVA),两组间比较用t检验。
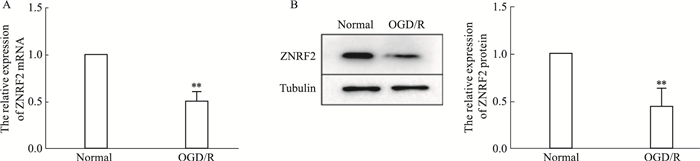
2 结果 2.1 ZNRF2在OGD/R处理PC12细胞损伤模型中明显下调为了探究ZNRF2在OGD/R致PC12细胞损伤中的变化,采用qRT-PCR、Western blot实验分别检测ZNRF2 mRNA、蛋白的表达变化。与Normal组相比,氧糖剥夺1 h,复糖复氧24 h后,ZNRF2 mRNA和蛋白均明显下调,见Fig 1。
|
| Fig 1 Expression of ZNRF2 down-regulated significantly in OGD/R-induced PC12 cells(x±s, n=3) A: The relative expression of ZNRF2 mRNA; B: The relative expression of ZNRF2 protein. **P < 0.01 vs normal group. |
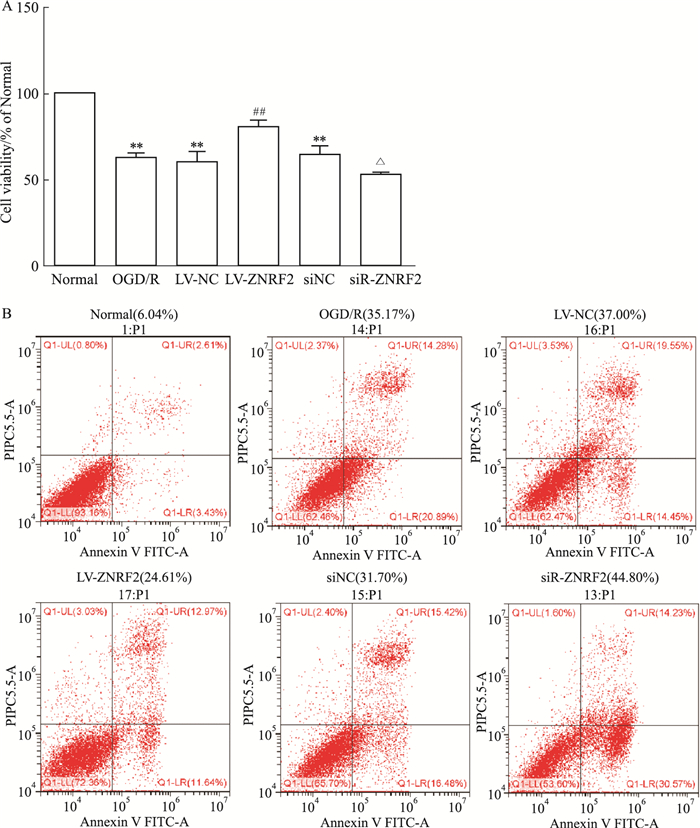
为了进一步观察ZNRF2对OGD/R诱导的PC12细胞损伤的影响,采用MTT实验、流式细胞术观察细胞活力和细胞凋亡情况。结果如Fig 2所示,与Normal组相比,PC12细胞经氧糖剥夺/复糖复氧处理后,PC12细胞活力明显减低、凋亡率明显增加,LV-NC组、siNC组与OGD/R组相比无统计学差异,与LV-NC组相比,给予ZNRF2过表达慢病毒组后,PC12细胞活力、细胞凋亡明显改善,而与siNC组相比,siR-ZNRF2组细胞活力进一步降低,细胞凋亡率增加,加重了细胞损伤。结果表明,ZNRF2保护OGD/R导致的PC12细胞损伤。
|
| Fig 2 Effect of ZNRF2 on cell viability and apoptosis of OGD/R-induced PC12 cells(x±s, n=3) A: Cell viability of PC12 cells in different groups; B: Apoptotic rate of PC12 cells with different treatment.**P < 0.01 vs normal group, ##P < 0.01 vs LV-NC, △P < 0.05 vs siNC. |
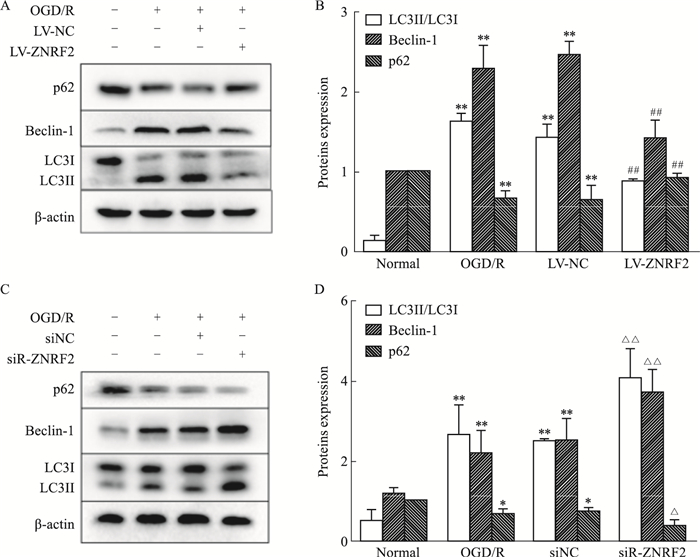
为了初步探讨ZNRF2保护OGD/R导致的PC12细胞损伤的机制,通过Western blot实验观察PC12细胞中自噬相关蛋白LC3II、Beclin-1以及p62的表达改变。结果如Fig 3所示,氧糖剥夺/复糖复糖后,与Normal组相比,PC12细胞中自噬相关蛋白p62蛋白表达减少、Beclin-1蛋白和LC3II蛋白明显增多,自噬被激活;与LV-NC组相比,LV-ZNRF2组中p62蛋白明显上调,Beclin-1蛋白和LC3II蛋白表达降低,说明上调ZNRF2后,自噬被抑制;而相比于siNC组,下调ZNRF2后,p62蛋白表达降低,Beclin-1蛋白和LC3II蛋白表达增加,自噬加剧,差异具有统计学意义。
|
| Fig 3 ZNRF2 inhibited OGD/R-induced excessive activation of autophagy in PC12 cells(x±s, n=3) A, C: Representative Western blot images depicting, p62, Beclin-1, LC3I and LC3II expressions; B, D: A bar graph presenting the quantification of p62, Beclin-1 and LC3II/LC3I. *P < 0.05, **P < 0.01 vs normal group; #P < 0.05, ##P < 0.01 vs LV-NC group, △P < 0.05, △△P < 0.01 vs siNC. |
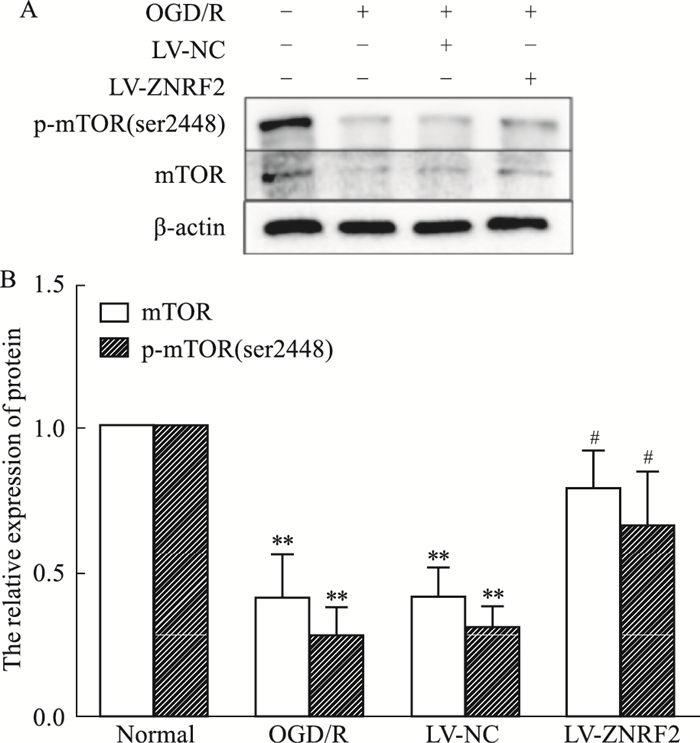
为了初步探究ZNRF2调控自噬的机制,采用Western blot检测mTOR、p-mTOR(ser2448)蛋白的表达变化。结果如Fig 4所示,与Normal组相比,模型组中,mTOR、p-mTOR(ser2448)蛋白表达降低,给予ZNRF2过表达慢病毒后,mTOR、p-mTOR(ser2448)蛋白均明显上调。
|
| Fig 4 The protein expressions of mTOR and p-mTOR (ser2448) upregulated after transfecting ZNRF2 overexpression lentivirus in OGD/R-treated PC12 cells(x±s, n=3) A: Representative Western blot images depicting, mTOR, p-mTOR(ser2448) expression; B: A bar graph presenting the quantification of mTOR, p-mTOR(ser2448). **P < 0.01 vs normal group; #P < 0.05 vs LV-NC group. |
自噬是真核细胞中通过溶酶体降解胞质中受损细胞器或错误蛋白的细胞自我保护途径,在维持细胞内环境稳态中发挥着重要作用[8]。自噬不仅在许多生理过程如细胞增殖、分化与衰老中扮演着重要角色,亦在病理条件下也发挥着重要的作用,其中包括神经退行性疾病、糖尿病、癌症、脑血管疾病等。研究表明,脑缺血/再灌注损伤中自噬被激活,在不同阶段发挥着不同的作用,在再灌注前期,自噬通过清除细胞内受损细胞器或错误折叠蛋白产生保护作用;再灌注后期自噬持续激活,导致细胞自噬性死亡或造成细胞二次伤害[9]。有研究发现,黄芪甲苷可以通过上调自噬减轻氧糖剥夺诱导PC12细胞的氧化应激,从而产生保护作用[10];而TP53介导糖酵解和细胞凋亡调节因子上调明显改善OGD/R导致的原代培养的皮层神经元的损伤,且自噬激活剂雷帕霉素可以逆转其保护作用[11];自噬抑制剂3-甲基腺嘌呤可减少OGD/R诱导的PC12细胞损伤[12]。本次研究发现,OGD/R处理的PC12细胞中自噬激活,PC12细胞活性降低、细胞凋亡增加,结果提示OGD/R诱导的自噬过度激活导致PC12细胞损伤。自噬是一把“双刃剑”,参与脑缺血/再灌注损伤的发生与发展,探究自噬在脑缺血/再灌注损伤中的具体作用,明确自噬调控机制十分重要。
ZNRF2是一类膜相关的E3泛素酶,在中枢和外周神经元高度表达,在维持细胞氨基酸稳定、突触可塑性方面发挥着重要作用。有研究证实,ZNRF2抑制人骨肉瘤细胞的生长[13];在非小细胞肺癌中,上调ZNRF2可促进癌细胞增殖,抑制癌细胞凋亡[14]。最新研究表明LncRNA TTN-AS1/miR-153-3p/ZNRF2轴可以通过激活PI3K/AKT/mTOR调控癌细胞的增殖与凋亡参与乳头状甲状腺癌病理进程[15],但在神经系统疾病中研究较少。本研究结果发现,上调ZNRF2表达可以明显增加PC12细胞活力,减少PC12细胞凋亡率,从而保护OGD/R导致的PC12细胞损伤,而抑制PC12细胞中ZNRF2表达显著加剧了OGD/R导致的PC12细胞损伤。有趣的是,本研究发现上调ZNRF2表达可显著逆转OGD/R诱导的PC12细胞中LC3II/LC3I、Beclin-1蛋白表达增加伴随p62蛋白表达降低的现象,抑制PC12细胞中自噬的过度激活,而下调ZNRF2表达后,OGD/R诱导PC12细胞中自噬激活进一步加剧,PC12细胞损伤加重。结果提示,ZNRF2减轻OGD/R诱导的PC12细胞损伤,可能与抑制PC12细胞中的自噬激活相关。
哺乳动物雷帕霉素靶点(mammalian target of rapamycin,mTOR)是一类高度保守的丝氨酸/苏氨酸激酶,在多种疾病的发生发展中扮演者重要角色,是调控自噬的关键蛋白[16]。有研究发现,在非小细胞肺癌中,ZNRF2通过上调mTOR,激活下游分子促进癌细胞的增殖,抑制癌细胞的凋亡[14];且有研究通过生物信息学预测分析发现,ZNRF2与mTOR可能有直接的结合位点[17]。同时本研究发现,上调ZNRF2后,抑制自噬过度激活,而mTOR、p-mTOR(ser2448)相应上调。因此,我们推测,ZNRF2抑制OGD/R诱导的PC12细胞自噬激活,可能与上调mTOR相关,但该机制需要进一步的实验来探究。
综上所述,ZNRF2对OGD/R诱导的PC12细胞损伤有明显保护作用,其机制可能与上调mTOR, 抑制OGD/R诱导的自噬激活途径相关。ZNRF2有望成为干预脑缺血/再灌注损伤的新靶点。
| [1] |
Wu S, Wu B, Liu M, et al. Stroke in China: Advances and challenges in epidemiology, prevention and management[J]. Lancet Neurol, 2019, 18(4): 394-405. doi:10.1016/S1474-4422(18)30500-3 |
| [2] |
Kalogeris T, Baines C P, Krenz M, et al. Ischemia/reperfusion[J]. Compr Physiol, 2016, 7(1): 113-70. |
| [3] |
Galluzzi L, Baehrecke E H, Ballabio A, et al. Molecular definitions of autophagy and related processes[J]. EMBO J, 2017, 36(13): 1811-36. doi:10.15252/embj.201796697 |
| [4] |
Su J, Zhang T, Wang K, et al. Autophagy activation contributes to the neuroprotection of remote ischemic perconditioning against focal cerebral ischemia in rats[J]. Neurochem Res, 2014, 39(11): 2068-77. doi:10.1007/s11064-014-1396-x |
| [5] |
Shui M, Liu X, Zhu Y, et al. Exogenous hydrogen sulfide attenuates cerebral ischemia-reperfusion injury by inhibiting autophagy in mice[J]. Can J Physiol Pharmacol, 2016, 94(11): 1187-92. doi:10.1139/cjpp-2016-0100 |
| [6] |
Araki T, Milbrandt J. ZNRF proteins constitute a family of presynaptic E3 ubiquitin ligases[J]. J Neurosci, 2003, 23(28): 9385-94. doi:10.1523/JNEUROSCI.23-28-09385.2003 |
| [7] |
Hoxhaj G, Caddye E, Najafov A, et al. The E3 ubiquitin ligase ZNRF2 is a substrate of mTORC1 and regulates its activation by amino acids[J]. Elife, 2016, 5: e12278-96. doi:10.7554/eLife.12278 |
| [8] |
Mo Y, Sun Y Y, Liu K Y. Autophagy and inflammation in ischemia stroke[J]. Neural Regen Res, 2020, 15(8): 1388-96. doi:10.4103/1673-5374.274331 |
| [9] |
Huang Y G, Tao W, Yang S B, et al. Autophagy: Novel insights into therapeutic target of electroacupuncture against cerebral ischemia/reperfusion injury[J]. Neural Regen Res, 2019, 14(6): 954-61. doi:10.4103/1673-5374.250569 |
| [10] |
靳晓飞, 张彐宁, 周晓红, 等. 黄芪甲苷调控自噬减轻氧糖剥夺/复氧复糖PC12细胞氧化应激损伤研究[J]. 中国药理学通报, 2020, 36(1): 53-8. Jin X F, Zhang X N, Zhou X H, et al. Study of astragaloside Ⅳ alleviating oxidative stress injury of PC12 cells induced by oxygen-glucose deprivation/reoxygenation through regulating autophagy[J]. Chin Pharmacol Bull, 2020, 36(1): 53-8. doi:10.3969/j.issn.1001-1978.2020.01.012 |
| [11] |
Zhang D M, Zhang T, Wang M M, et al. TIGAR alleviates ischemia/reperfusion-induced autophagy and ischemic brain injury[J]. Free Radic Biol Med, 2019, 137: 13-23. doi:10.1016/j.freeradbiomed.2019.04.002 |
| [12] |
Jiang W W, Huang B S, Han Y, et al. Sodium hydrosulfide attenuates cerebral ischemia/reperfusion injury by suppressing overactivated autophagy in rats[J]. FEBS Open Bio, 2017, 7(11): 1686-95. doi:10.1002/2211-5463.12301 |
| [13] |
Xiao Q, Yang Y, An Q, et al. MicroRNA-100 suppresses human osteosarcoma cell proliferation and chemo-resistance via ZNRF2[J]. Oncotarget, 2017, 8(21): 34678-86. doi:10.18632/oncotarget.16149 |
| [14] |
Zhang X F, Guo Z Q, Zhao C C, et al. The role of ZNRF2 in the growth of non-small cell lung cancer[J]. Eur Rev Med Pharmacol Sci, 2016, 20(19): 4011-7. |
| [15] |
Cui Z, Luo Z, Lin Z, et al. Long non-coding RNA TTN-AS1 facilitates tumorigenesis of papillary thyroid cancer through modulating the miR-153-3p/ZNRF2 axis[J]. J Gene Med, 2019, 21(5): e3083-93. doi:10.1002/jgm.3083 |
| [16] |
Jung C H, Jun C B, Ro S H, et al. ULK-Atg13-FIP200 complexes mediate mTOR signaling to the autophagy machinery[J]. Mol Biol Cell, 2009, 20(7): 1992-2003. doi:10.1091/mbc.e08-12-1249 |
| [17] |
Yang M, Zhai Z, Zhang Y, et al. Clinical significance and oncogene function of long noncoding RNA HAGLROS overexpression in ovarian cancer[J]. Arch Gynecol Obstet, 2019, 300(3): 703-10. doi:10.1007/s00404-019-05218-5 |

