

缺血性脑血管病的高发病率、高致残率严重影响千万患者的生命健康, 但改善脑供血同时带来的脑缺血/再灌注损伤也成为缺血性脑血管病治疗的难题之一。血管内皮损伤是缺血/再灌注损伤的关键环节。氧化应激是缺血/再灌注损伤的一个主要因素[1]。核因子E2相关因子2(nuclear factor-E2-related factor 2, Nrf2)/血红素加氧酶-1(heme oxygenase, HO-1)信号轴具有抗氧化、抗炎、减少线粒体损伤、调控细胞死亡等作用, 是迄今为止发现的最重要的内源性抗氧化应激通路。因此, 有效调控Nrf2/HO-1信号通路现已成为治疗氧化应激性疾病的重要靶点[2]。
塞络通(sailuotong, SLT)是由本研究室、神威药业有限公司及澳大利亚西悉尼大学3方合作共同研制的中药6类新药, 主要由人参、银杏叶、西红花中药有效组分配伍而成, 功能为益气活血、化瘀通络, 用于治疗血管性痴呆和缺血性中风恢复期(气虚血瘀证)。本研究在体外模拟缺血/再灌注损伤模型, 建立人脑微血管内皮细胞系(human brain microvascular endothelial cell line, hCMEC/D3)氧葡萄糖剥夺/复氧(oxygen-glucose deprivation/reoxygenation, OGD/R)损伤模型, 探讨SLT对OGD/R诱导hCMEC/D3细胞损伤的抗氧化保护作用及靶点。
1 材料与方法 1.1 材料 1.1.1 主要试剂塞络通(sailuotong, SLT)由神威药业集团提供, 批号090914; ML385购自Selleck公司(S8790);内皮细胞培养基(Endothelial Cell Medium, ECM)、添加剂、胎牛血清、双抗(青霉素/链霉素, P/S)均购自上海赛百慷生物技术股份有限公司, PriMed-iCell-0016;细胞增殖-毒性检测试剂盒(CCK-8)购自上海东仁化学科技有限公司(CK04);超氧化物歧化酶(superoxide dismutase, SOD)、微量还原型谷胱甘肽(glutathione, GSH)测定试剂盒测定均购自南京建成生物工程研究所(A001-3, A006-2);人源HO-1ELISA试剂盒购自美国abcam(ab207621);HO-1小鼠单克隆抗体购自proteintech(66743-1-Ig); Nrf2小鼠单克隆抗体购自美国abcam(ab89443)。
1.1.2 仪器Olympus SH1倒置显微镜(美国奥林帕斯公司); SYNERGYTM 4多功能酶标仪(BioTek, USA); MCO175 CO2培养箱(Sanyo, 日本); 转移电泳槽(Mini Trans-Blot Transfer Cell, Bio-Rad, USA); 垂直板电泳槽(Mini Protean3 Cell, Bio-Rad, USA); Chem DocTM XRS+凝胶成像仪(Bio-Rad, USA)。
1.2 方法 1.2.1 药物配制SLT用DMSO溶解, 配制成100 g·L-1的母液, -20 ℃保存; ML385用DMSO溶解, 配制成5m mol·L-1的母液, -20 ℃保存。处理组用等体积的DMSO作对照。
1.2.2 细胞培养复苏冻存的永生化人脑微血管内皮细胞(hCMEC/D3)(上海赛百慷生物技术股份有限公司提供), 迅速置于37 ℃水浴锅中溶化, 加入6 mL内皮细胞完全培养基(内含5%胎牛血清+1%ECGS+1%双抗), 置于37 ℃, 5%CO2培养箱中培养。每2天更换1次培养液。当细胞处于对数生长期且待细胞生长融合达80%~90%时, 按1 : 3比例进行传代。
1.2.3 OGD/R诱导hCMEC/D3细胞损伤模型[3]弃去培养液, PBS洗2遍, 换成无糖DMEM或含有相应浓度药物的无糖DMEM, 将96孔板放入自制缺氧盒内或采用不通气的T25 cm2培养瓶, 通95%N2-5%CO2混合气, 流速1 L·min-1, 通气15 min后, 夹闭缺氧盒进气管和出气管或关紧培养瓶盖, 分别缺氧2, 4, 6 h后, 换成正常内皮细胞培养液, 复氧2 h, 进行细胞损伤模型条件的筛选。
1.2.4 CCK8法检测细胞活力取对数生长期hCMEC/D3细胞, 以0.5×107个·L-1细胞密度接种于96孔板中, 处理后, 每孔加入稀释的CCK8溶液100 μL(1 : 10 ECM培养基), 培养箱内孵育2 h, 酶标仪450 nm波长检测OD值。
1.2.5 WST-1法测定SOD活力按照试剂盒说明进行操作, 设定对照孔、对照空白孔、测定孔及测定空白孔, 进行各试剂的添加混匀后, 37 ℃孵育20 min, 450 nm处酶标仪读数。
1.2.6 微量酶标法测定GSH含量按照试剂盒说明进行操作, 取破碎后的细胞悬液0.1 mL, 加0.1 mL试剂一混匀, 3500 r·min-1, 离心10 min, 去上清液待测。设定空白孔、标准孔及测定孔, 进行各试剂的添加混匀后, 静置5 min, 405 nm处, 酶标仪测定各孔吸光度值。
1.2.7 ELISA检测细胞上清HO-1含量标准品按照试剂盒说明书提供的稀释方式稀释, 1 500 ng·L-1作为标准曲线最高浓度, 依次做2倍稀释。分别对应加入50 μL的标准品和样本, 再向每孔加入50 μL生物素标记的检测抗体复合物及100 μL 3, 3′, 5, 5′-四甲基联苯胺TMB底物, 摇床, 清洗, 最后加入终止液450 nm处上机检测。
1.2.8 Western blot实验配制10%分离胶, 将提取hCMEC/D3细胞蛋白样品按20 μg进行上样。蛋白经电泳及转膜结束后, 放置摇床上室温封闭60 min。封闭后放置一抗中:mouse anti-HO-1(1 : 1 000)、mouse anti-Nrf2(1 : 1 000)、mouse anti-βactin (1 : 1 000), 4 ℃孵育过夜。次日TBST洗膜5次, 每次10 min。5%脱脂奶粉封闭液再次封闭30 min, 按1 : 20 000加入羊抗鼠二抗, 室温孵育90 min后, TBST洗膜5次, 每次10 min, 采用化学发光法, 凝胶成像仪中显影。蛋白条带用Image Lab软件自动分析。
1.3 统计方法数据统计分析用SPSS16.0软件进行统计, 多组间比较用单因素方差(One-Way ANOVA)分析, 根据方差齐性检验(Homogeneity of variance test), 分别选用LSD检验或Tamhane’s检验, 数据以均数±标准差(x±s, n≥3)表示。
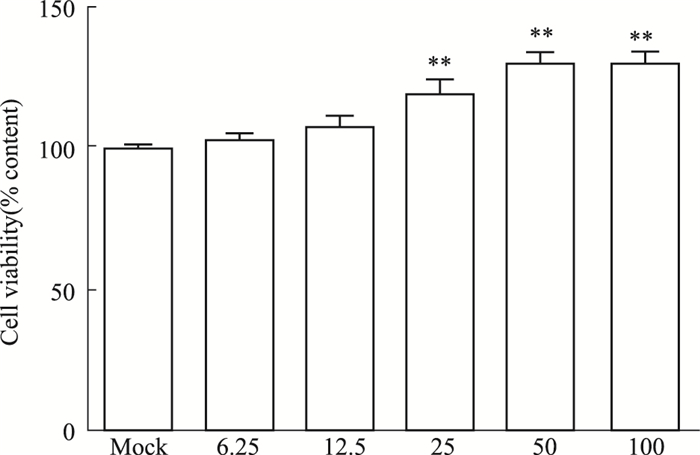
2 结果 2.1 SLT对正常培养hCMEC/D3细胞活力的影响细胞在正常培养状态下, 给与不同浓度SLT处理24h, 如Fig 1所示, 与对照组比较, 6.25、12.5 mg·L-1 SLT对细胞活力无明显影响, 25、50、100 mg·L-1 SLT对细胞活力具有升高作用, 差异有显著性(P < 0.01)见Fig 1。
|
| Fig 1 Effects of SLT on hCMEC/D3 cell viability (x±s, n=5) **P < 0.01 vs mock group. |
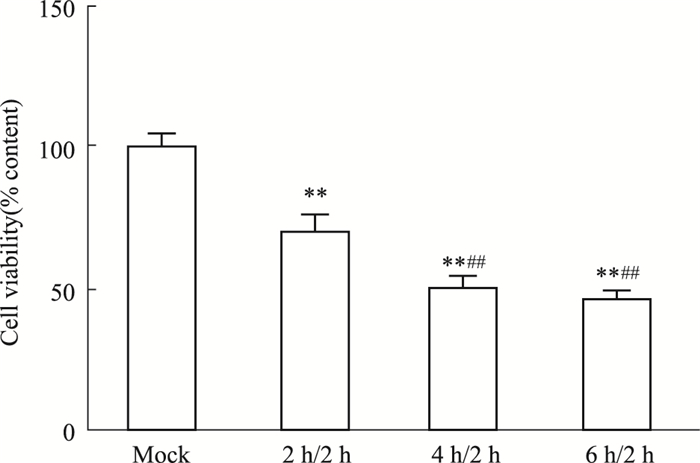
分别观察OGD2h/R2h、OGD4h/R2h、OGD6h/R2h对hCMEC/D3细胞损伤程度, 与对照组比较, OGD2h/R2h、OGD4h/R2h、OGD6h/R2h细胞明显损伤(P < 0.01);与OGD2h/R2h比较, OGD4h/R2h和OGD6h/R2h细胞明显损伤(P < 0.01)(Fig 2)。
|
| Fig 2 Effects of OGD/R injury on hCMEC/D3 cell viability (x±s, n=5). **P < 0.01 vs mock group; ##P < 0.01 vs OGD/R group (2 h/2 h). |
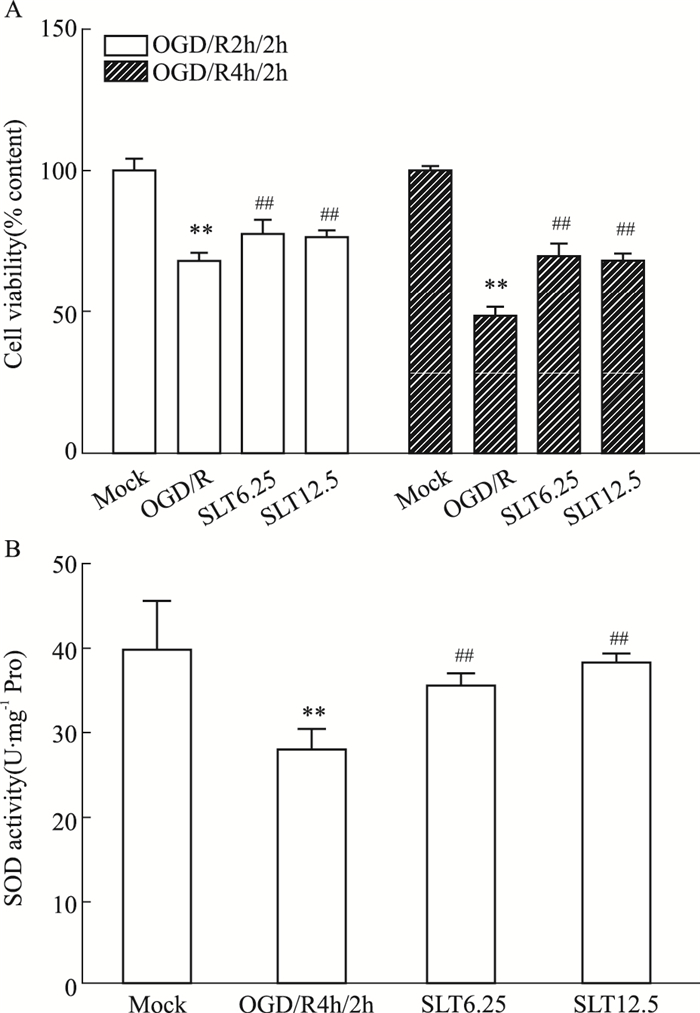
OGD2h/R2h、OGD4h/R2h, SLT分别在6.25、12.5 mg·L-1剂量下, 可明显增加细胞活力(P<0.01)。OGD4h/R2h, SLT可明显提高细胞SOD活力(P < 0.01)。表明SLT具有明显细胞保护作用(Fig 3)。
|
| Fig 3 Effects of SLT on OGD/R induced hCMEC/D3 cell injury (x±s, n=6) **P < 0.01 vs mock group; ##P < 0.01 vs OGD/R group. |
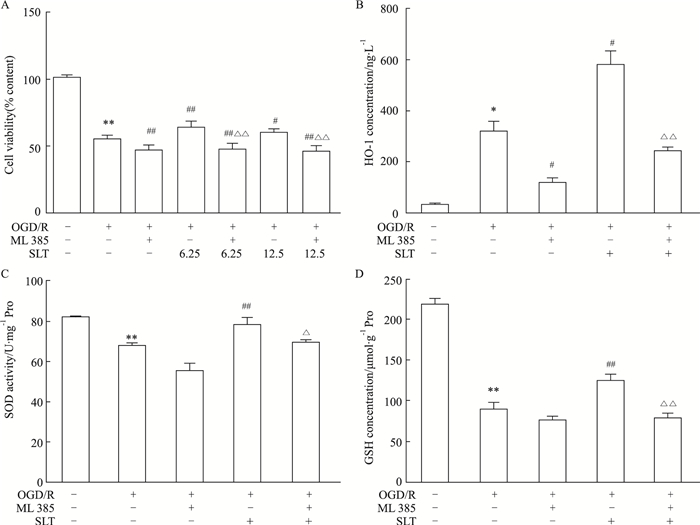
给与Nrf2抑制剂ML385(0.25 μm)干预, 细胞活力较模型组明显降低(P < 0.01);且明显降低SLT对细胞活力的保护作用(P < 0.01)(Fig 4A)。与对照组比较, OGD/R4h/2h后HO-1含量明显增加(P < 0.05), ML385干预后, 明显降低HO-1含量(P < 0.05);与模型组比较, SLT(6.25 mg·L-1)明显提高HO-1含量(P < 0.05);ML385干预后, 明显降低SLT增加HO-1含量作用(P < 0.01)(Fig 4B)。与对照比较, OGD/R4h/2h后SOD活力、GSH含量明显降低(P < 0.01);与模型组比较, SLT(6.25 mg·L-1)明显提高SOD活力、GSH含量(P < 0.01);ML385干预后, 明显降低SLT对细胞抗氧化保护作用(P < 0.05, P < 0.01)(Fig 4C, D)。
|
| Fig 4 Effects of Nrf2 inhibitor on SLT anti-oxidative injury (x±s, n=6). *P < 0.05, **P < 0.01 vs mock group, #P < 0.05, ##P < 0.01 vs OGD/R group, △P < 0.05, △△P < 0.01 vs SLT group. |
与对照组比较, OGD/R4h/2h后HO-1、Nrf2蛋白表达相对值明显增加(P < 0.01), Nrf2抑制剂ML385干预后, HO-1、Nrf2蛋白表达相对明显降低(P < 0.05, P < 0.01)。与模型组比较, SLT组(6.25 mg·L-1)HO-1、Nrf2蛋白表达相对增加(P < 0.05);ML385干预后, 明显降低SLT增加HO-1、Nrf2蛋白表达作用(P < 0.01)(Fig 5)。

|
| Fig 5 Effects of SLT on Nrf2/HO-1 signaling pathway Data are expressed as (x±s, n=3). *P < 0.05, **P < 0.01 vs mock group, #P < 0.05, ##P < 0.01 vs OGD/R group, △△P < 0.01 vs SLT group. |
缺血/缺氧性脑血管疾病发生、发展的关键环节与内皮的损伤密切相关。脑微血管内皮细胞是内覆于血管腔表面的连续单层扁平细胞, 具有合成、分泌、代谢等多种功能, 并能控制血液和脑组织之间的物质交换从而维持大脑的动态平衡[4]。脑缺血/再灌注时产生大量氧自由基使内皮细胞激活并表达多种炎症因子, 导致细胞的损伤、凋亡和坏死。hCMEC/D3细胞是永生化人脑微血管内皮细胞系, 其具备人脑内皮的大部分形态和功能特征[5]。
中医认为“气虚身中卒至, 五脏绝闭, 脉道气血不通”, 故调理气血是治疗脑中风的关键环节。在缺血性脑卒中中以Nrf2介导的氧化还原系统在某种程度上反映了气血脉失和病机特点。故本实验采用“益气活血、化瘀通络”临床有效方剂SLT以“脉”(脑微血管内皮细胞)为载体从微观层面对Nrf2介导的抗氧化通路进行干预研究。本实验室前期研究证明在双侧颈动脉结扎大鼠慢性脑低灌注模型上, SLT可明显增加SOD活性及丙二醇(malondialdehyde, MDA)含量, 具有增强清除自由基能力[6]。因此, 本研究通过建立hCMEC/D3细胞OGD/R损伤模型, 探讨塞络通对hCMEC/D3细胞的抗氧化护作用机制。通过对OGD损伤时间条件的摸索发现在缺氧4 h后, 再延长缺氧时间, 细胞的损伤并不显著升高, 故主要选择4 h作为后续实验的缺氧时间, 同时因为缺氧2 h也对细胞造成了损伤, 且程度较轻, 可以作为较轻的损伤模型, 故在部分后续实验中, 也对这种较轻模型中药物的作用进行了探讨。在OGD模型下, 最初选择了6.25、12.5、25 mg·L-1等浓度进行观察, 发现与6.25 mg·L-1比较, 12.5和25 mg·L-1并没有显示出明显的药效增加(数据未显示), 故以“同等作用下, 选择较低剂量”的原则, 在本实验中主要选择了6.25 mg·L-1作为后期药效及机制探讨的剂量。实验结果证明, OGD/R可诱导hCMEC/D3细胞损伤, SLT具有明显的细胞保护作用, 可以明显的改善细胞活力及SOD活力。
缺血性脑卒中病理机制复杂, 氧化应激是缺血性脑卒中病理过程中的一个重要因素。其中SOD活力的高低可间接反映机体清除氧自由基的能力, GSH是机体内最重要的非酶性抗氧化物, 可清除氧自由基, 故GSH亦是衡量机体抗氧化能力大小的重要物质。前期实验研究证明SLT对H2O2诱导的EA.hy926氧化应激损伤可减低ROS生成, 增加SOD活性, 通过抑制caspase-3、降低Bax/Bcl-2蛋白表达抑制细胞凋亡进而发挥对氧化损伤的保护作用[7]。本研究发现, OGD/R损伤后引起hCMEC/D3细胞SOD活力及GSH含量明显降低, SLT可以明显提高二者的含量, 进一步说明SLT具有明确的抗氧化保护能力。既往研究证实, 银杏叶提取物(ginkgo biloba extracrion, GBE)和人参皂苷(ginsenoside)可介导Nrf2/ARE信号通路发挥抗氧化应激脑保护作用。同时, 本实验结果证明在Nrf2抑制剂ML385干预下, SLT抗氧化能力被抑制, 细胞活力、SOD和GSH含量显著降低, 说明SLT可能通过Nrf2信号通路发挥抗氧化保护作用。
Nrf2/HO-1信号通路是体内的一种重要内源性的抗氧化系统。其中Nrf2属于CNC亮氨酸拉链核转录激活因子家族中活性最强的转录调节因子。在生理状态下, Nrf2与其负调控因子Kelch样环氧氯丙烷相关蛋白-1(Kelch-likeECH-associated protein, keap1)双甘酸重复DGR区域结合于细胞质中, 在keap1功能结构域BTB和IVR区参与下经Cul3/Rbx1 E3泛素化降解以保持浓度稳定。在细胞遭受氧化应激刺激时, Nrf2与keap1解偶联, 易位至细胞核中, 与其下游靶基因抗氧化反应原件(antioxidant response element, ARE)结合, 调控Ⅱ相解毒酶、SOD、过氧化氢酶(catalase, CAT)等靶基因活性, 以清除ROS等有害物质[8]。最近有证据表明, 在大鼠脑缺血/再灌注损伤模型中Nrf2表达迅速上调, 而随着再灌注时间的延长, Nrf2蛋白的表达变化不明显, 这是一种保护性应激反应, Nrf2过度活化可以减轻脑缺血损伤引起的氧化损伤, 但是反应持续时间短, 需要药物进行干预缺血/再灌注损伤[9-10]。对SH-SY5Y细胞进行Nrf2 siRNA处理, 发现HO-1蛋白表达消失, 表明HO-1的表达依赖于Nrf2[11]。HO-1是Ⅱ相解毒酶之一, HO-1所引发的下级信号通路对多脏器具有抗氧化应激的保护作用。HO-1通常在除脾脏之外的大多数组织/器官中以低水平表达, 然而, 它对于保护细胞免受氧化和炎症损伤的各种刺激具有高度诱导性[12]。HO-1是Nrf2的靶抗氧化酶, 在缺血性脑疾病中有重要保护作用[13]。在本研究中, OGD/R后的hCMEC/D3细胞上清液中的HO-1含量及细胞Nrf2、HO-1蛋白表达水平相对于对照组增加, 其可能与氧糖剥夺后的应激状态下机体自身的代偿性保护机制有关, 进而激活Nrf2及下游抗氧化酶。该实验结果与前人研究相一致, 既往体内及体外实验证明了大鼠局灶性脑缺血[9, 10, 14]和PC12氧糖剥夺后[14]及H2O2诱导的RAW264.7细胞损伤均可上调Nrf2和HO-1蛋白表达[15]。
本研究发现SLT可以明显增加OGD/R损伤后细胞Nrf2和HO-1的蛋白表达, 给与Nrf2抑制剂ML385, 发现SLT对hCMEC/D3的抗氧化保护作用被ML385部分或完全减弱, 表明SLT在OGD/R损伤hCMEC/D3模型中发挥细胞保护作用可能是通过Nrf2/HO-1信号通路介导。
| [1] |
Manzanero S, Santro T, Arumugam T V. Neuronal oxidative stress in acute ischemic stroke: sources and contribution to cell injury[J]. Neurochem Int, 2013, 62(5): 712-8. |
| [2] |
王甜甜, 陈淳媛, 杨雷, 等. Nrf2/HO-1信号轴在氧化应激性疾病中的机制[J]. 中南大学学报(医学版), 2019, 44(1): 74-80. Wang T T, Chen C Y, Yang L, et al. Role of Nrf2/HO-1 signal axis in the mechanisms for oxidative stress-relevant diseases[J]. J Cent South Univ (Med Sci), 2019, 44(1): 74-80. |
| [3] |
Zhang Y H, Liu J X, Yang B, et al. Ginkgo biloba extract inhibits astrocytic lipocalin-2 expression and alleviates neuroinflammatory injury via the JAK2/STAT3 pathway after ischemic brain stroke[J]. Front Pharmacol, 2018, 9: 518. |
| [4] |
郑华珠, 王利胜, 孟英姣. 补阳还五汤通过上调SIRT1抑制脑微血管内皮细胞氧糖剥夺再灌注诱导氧化应激损伤[J]. 中药药理与临床, 2017, 33(2): 9-13. Zheng H Z, Wang L S, Meng Y J. Effects of Buyang Huanwu Decoction against oxidative stress of rBMECs by up-regulating SIRT1[J]. Pharm Clin Chin Mater Med, 2017, 33(2): 9-13. |
| [5] |
Eigenmann D E, Xue G, Kim K S, et al. Comparative study of four immortalized human brain capillary endothelial cell lines, hCMEC/D3, hBMEC, TY10, and BB19, and optimization of culture conditions, for an in vitro blood-brain barrier model for drug permeability studies[J]. Fluids Barriers CNS, 2013, 10(1): 33. |
| [6] |
徐立, 刘建勋, 丛伟红, 等. 维脑康胶囊对慢性脑低灌注大鼠脑内胆碱能系统及清除自由基能力的影响[J]. 中国中药杂志, 2008, 33(5): 531-4. Xu L, Liu J X, Cong W H, et al. Effects of Weinaokang capsule on intracephalic cholinergic system and capability of scavenging free radicas in chronic cerebral hyoperfusion rats[J]. China J Chin Mater Med, 2008, 33(5): 531-4. |
| [7] |
Seto S W, Chang D, Ko W M, et al. Sailuotong prevents hydrogen peroxide (H2O2)-induced injury in EA.hy926 cells[J]. Int J Mol Sci, 2017, 18(1): 1-12. |
| [8] |
Krajka-Kuźniak V, Paluszczak J, Baer-Dubowska W. The Nrf2-ARE signaling pathway: An update on its regulation and possible role in cancer prevention and treatment[J]. Pharmacol Rep, 2017, 69(3): 393-402. |
| [9] |
Chen L, Wang L, Zhang X, et al. The protection by octreotide against experimental ischemic stroke: up-regulated transcription factor Nrf2, HO-1 and down-regulated NF-κB expression[J]. Brain Res, 2012, 1475: 80-7. |
| [10] |
黄娟, 廖君, 彭熙炜, 等. 脑泰方对脑缺血/再灌注大鼠海马区Nrf2、HO-1和膜铁转运辅助蛋白表达的影响[J]. 中国药理学通报, 2017, 33(10): 1467-72. Huang J, Liao J, Peng X W, et al. Effects of Naotai formula on expression of Nrf2, HO-1 and hephaestin in hippocampus of cerebral ischemia/reperfusion rats[J]. Chin Pharmacol Bull, 2017, 33(10): 1467-72. |
| [11] |
尹闻科, 石晓东, 张雄, 等. 姜黄素通过诱导Nrf-2上调SH-SY5Y细胞中HO-1的表达[J]. 中国药理学通报, 2010, 26(8): 1054-9. Yin W K, Shi X D, Zhang X, et al. Curcumins upregulate expression of HO1 via inducing Nrf2 in SH-SY5Y cells[J]. Chin Pharmacol Bull, 2010, 26(8): 1054-9. |
| [12] |
Jozkowicz A, Was H, Dulak J. Heme oxygenase-1 in tumors: is it a false friend[J]. Antioxid Redox Signal, 2007, 9(12): 2099-117. |
| [13] |
Joshi G, Johnson J A. The Nrf2-ARE pathway: a valuable therapeutic target for the treatment of neurodegenerative diseases[J]. Recent Pat CNS Drug Discovery, 2012, 7(3): 218-29. |
| [14] |
吴巍.基于Keap1-Nrf2/HO-1信号通路探讨枸杞多糖对脑缺血损伤保护作用[D].银川: 宁夏医科大学.硕士论文, 2018. Wu W. Effects of lycium barbarum polysaccharides on Keap1-Nrf2/HO-1 pathway after cerebral ischemic injury[D]. Yinchuan: Ningxia Medical University. Thesis for Application of Master's Degree, 2018. |
| [15] |
Yao Y D, Shen X Y, Machado J, et al. Nardochinoid B inhibited the activation of RAW264.7 macrophages stimulated by lipopolysaccharide through activating the Nrf2/HO-1 pathway[J]. Molecules, 2019, 24(13): 1-16. |

