

肺癌是全世界范围内发病率和死亡率较高的肿瘤之一, 据统计我国2015年新诊断的肺癌病例为73.33万, 是男性中最常见的肿瘤[1]。非小细胞肺癌(non-small cell lung cancer, NSCLC)约占肺癌病例的85%, 而80%的NSCLC患者在确诊时已失去手术等最佳治疗时机, 五年生存率仅为15%[2]。表皮生长因子受体(epidermal growth factor receptor, EGFR)基因的异常激活会促NSCLC的进展[3], EGFR的酪氨酸激酶抑制剂(tyrosine kinase inhibitor, TKIs), 如吉非替尼等疗效较好, 但一年内会产生耐药[4]。纤维蛋白原样蛋白(fibrinogen-like-protein 1, FGL1)是一种特异性的肝细胞有丝分裂活性因子, 最新发现在多种实体瘤中表达明显上调, 以肺癌中的比例最高, 尤其是NSCLC[5]。目前FGL1是否在肺腺癌中吉非替尼耐药过程中发挥作用尚不明确。因此, 本研究拟探讨吉非替尼耐药前后FGL1表达的差异, FGL1表达影响PC9/GR细胞侵袭迁移的潜在机制, 为EGFR-TKIs耐药后的治疗提供一定实验依据。
1 材料与方法 1.1 细胞和主要试剂人非小细胞肺癌吉非替尼敏感细胞株PC9(EGFR19外显子缺失突变)和人非小细胞肺癌吉非替尼耐药细胞株PC9/GR购自中国科学院上海细胞库。FGL1-siRNA重组序列、随机阴性对照序列由上海吉凯基因技术有限公司设计及合成。FGL1重组序列:F5′-GATCCTGGGAAGCAGAGT GT-3′; R5′-AACACCTTTGCCATGTTCCC-3′; 以无关通用序列为阴性对照, GAPDH序列:F5′-GCACCGTCAAGGCTGAAC-3′; R5′-TGGTGAGACGCCAGTGA-3′。DMEM高糖购自美国Hyclone公司, 货号:SH30022.01B;胎牛血清(FBS)购自杭州四季青生物科技公司, 货号:11011-8611;CCK-8试剂盒购自北京索莱宝科技公司, 货号:abs50001;Transwell小室、Matrigel基质胶购自中国康宁科技有限公司, 货号:3415和3542634;吉非替尼购自美仑生物科技有限公司, 货号:MB1112;lipofectamineTM 2000试剂盒购自美国Invitrogen公司, 货号11668-027;二喹啉甲酸(BCA)蛋白定量分析试剂盒购自北京索莱宝科技有限公司, 货号:PC0020;RT-qPCR试剂盒、RT-PCR试剂盒购自日本Takara公司货号:RR036A和RR820A, β-actin抗体购自Proteintech公司, 货号:60008-1-Ig; ZEB1抗体、E-cadherin和N-cadherin抗体购自Abcam公司, 货号:ab81972、ab184633和ab173341;DMi6000B型倒置荧光显微镜(德国Leica公司), StepOne Puls Real Time PCR仪(美国ABI公司), Stat Fax-4200酶标仪(美国Awareness公司), CheniDoc XRS凝胶成像分析系统(美国Bio-rad公司), 由安徽医科大学基础医学院免疫教研室提供。
1.2 方法 1.2.1 细胞培养PC9细胞和PC9/GR细胞培养条件:含10%胎牛血清、100 U·mL-1青霉素和链霉素的DMEM培养基, 于37 ℃, 5% CO2的温箱中常规培养, 细胞生长融合度达80%~90%时进行传代, 取对数生长期的细胞进行后续实验。
1.2.2 CCK-8法检测细胞对吉非替尼敏感性将PC9细胞和PC9/GR细胞以2.5×104个/孔接种细胞于96孔板中。24 h后更换为含不同浓度吉非替尼的培养基, 浓度梯度:0、0.125、0.25、0.5、1、2、4、8、16及32 μmol·L-1, 设阴性对照组, 5个复孔。培养48 h后加入10 μL CCK-8, 温箱孵育2 h, 于酶标仪测定570 nm处的吸光度(A)值, 计算细胞存活率。公式:细胞存活率/%=[(加药组A-阴性对照组A)/(不加药组A-阴性对照组A)]×100%, 由SPSS 22.0软件计算出半数抑制浓度(half inhibition concentration, IC50)。
1.2.3 细胞转染以1.0×108个·L-1细胞密度于6孔板中培养24 h后, 细胞融合至40%~60%时, 严格按LipofectamineTM2000试剂盒说明书进行siRNA转染。将转染FGL1-siRNA、NC-siRNA的细胞设为Fi组、NC组, 未经处理的PC9/GR细胞作为对照设为Con组, 后续试验的加药组和联合组G组和G+Fi组。转染48 h后加入TRIzol试剂, 收集细胞并提取细胞总RNA, 通过实时荧光定量聚合酶链式反应(Real-time fluorescence quantitative polymerase chain reaction, RT-qPCR)法和Westem blot法验证干扰效果。
1.2.4 划痕实验检测细胞间迁移能力划痕试验测定细胞迁移率:以5.0 ×107个·L-1细胞接种至6孔板, 培养24 h后, 用200 μL无菌枪头在6孔板划线, PBS洗去脱落细胞, 培养24 h拍照, 计算细胞迁移率。迁移率/%=(初始划痕宽度-24 h后划痕宽度)/初始划痕宽度×100%。
1.2.5 Transwell小室实验检测细胞迁移及侵袭能力迁移实验:胰酶消化5组经过药物作用48 h后细胞, 用无血清DMEM培养基调整细胞浓度为5.0×108个·L-1, Transwell小室的上室加入200 μL PC9/GR细胞悬液, 下室加入700 μL含10% FBS的DMEM培养基, 常规培养24 h后取出上室, 用棉签擦去小室上层细胞, 甲醇固定30 min, 风干, 0.1%结晶紫染色20 min, 清洗后显微镜拍照, 随机选取3个视野计数取均值。侵袭实验:Matrigel胶4 ℃放置过夜使之溶解, 用4 ℃预冷的无血清培养液1 :8稀释后取100 μL加入到Transwell小室的上室, 于37 ℃温育使胶凝固。胰酶消化5组经过药物作用48 h后细胞, 用无血清DMEM培养基调整细胞浓度为10.0×108个·L-1, Transwell小室的上室加入200 μL PC9/GR细胞悬液, 下室加入700 μL含10% FBS的DMEM培养基, 常规培养24 h后取出上室, 擦去小室上层细胞, 同上进行固定、染色、拍照和计数。
1.2.6 Western blot检测细胞沉默FGL1后Zeb1、E-cadhen及Vimentin表达变化将FGL1-siRNA和NC分别转染PC9/GR细胞, 24 h后加入终浓度为5 μmol ·L-1的吉非替尼继续常规培养48 h, 加入预冷的细胞裂解液(RIPA与PMSF比例为99 :1)将细胞重悬, 于冰上裂解30 min后, 4 ℃ 12 000 r ·min-1离心15 min, 提取总蛋白, BCA法测蛋白浓度后以同质量蛋白上样行SDS-PAGE电泳, 转膜, 10%脱脂牛奶室温封闭2 h, 再分别加入Zeb1、E-cadherin、Vimentin和GAPDH抗体, 4 ℃孵育过夜。二抗37 ℃孵育1.5 h, 应用ECL化学发光试剂盒进行显影检测、拍照。
1.3 统计学分析实验数据用SPSS 22.0统计软件进行分析, 以上实验均重复3次, 实验数据以x±s来表示, t检验用于两组独立样本均值的比较。
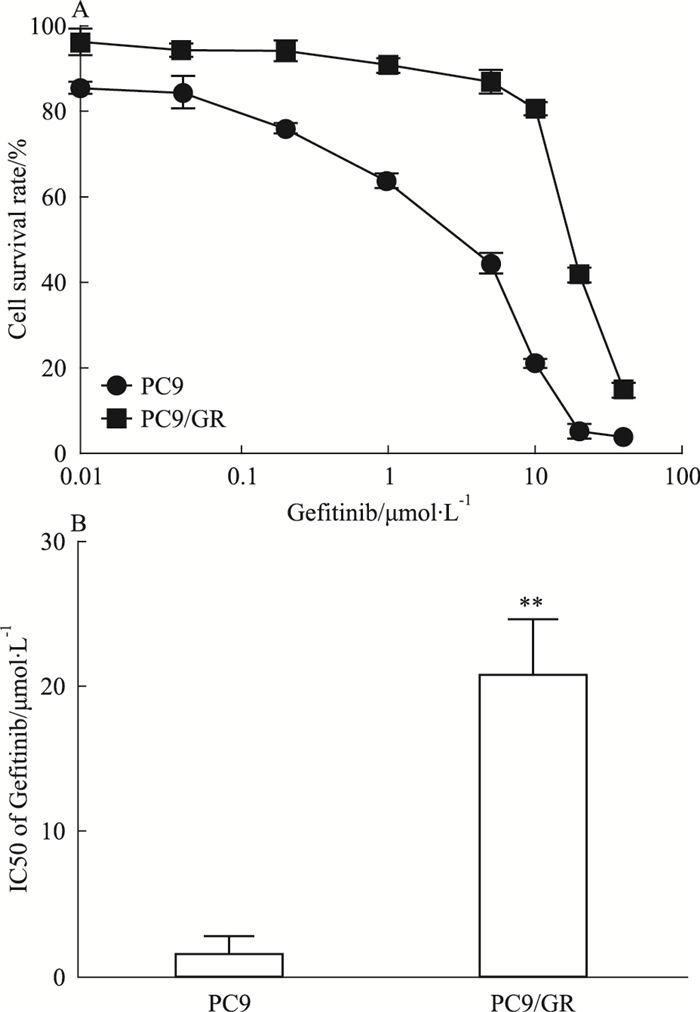
2 结果 2.1 吉非替尼对PC9细胞和PC9/GR细胞增殖的影响CCK-8结果显示, 吉非替尼对PC9细胞和PC9/GR细胞增殖的抑制作用随药物浓度增加而逐渐增强(Fig 1A); PC9细胞和PC9/GR细胞对吉非替尼的IC50值分别为(1.513 ±1.296) μmol·L-1与(19.179±1.091) μmol·L-1, 差异均有统计学意义(P<0.01)(Fig 1B)。结果提示PC9/GR细胞对吉非替尼的敏感性差。
|
| Fig 1 Sensitivity of PC9 cells and PC9/GR cells to gefitinib(x±s, n=5) A: Effect of gefitinib on proliferation of PC9 cells and PC9/GR cells; B:IC50 of PC9 cells and PC9/GR cells; **P < 0.01 vs PC9 |
Western blot结果显示PC9/GR细胞的FGL1蛋白水平明显高于PC9细胞, 差异有统计学意义(P<0.01)(Fig 2A); RT-qPCR结果显示PC9/GR细胞的mRNA水平显著高于PC9细胞, 差异有统计学意义(P<0.01)(Fig 2B)。

|
| Fig 2 Expression of FGL1 in PC9 cells and PC9/GR cells(x±s, n=5) A: Expression of FGL1 protein in PC9 cells and PC9/GR cells; B: Expression of FGL1 mRNA in PC9 cells and PC9/GR cells; **P < 0.01 vs PC9 |
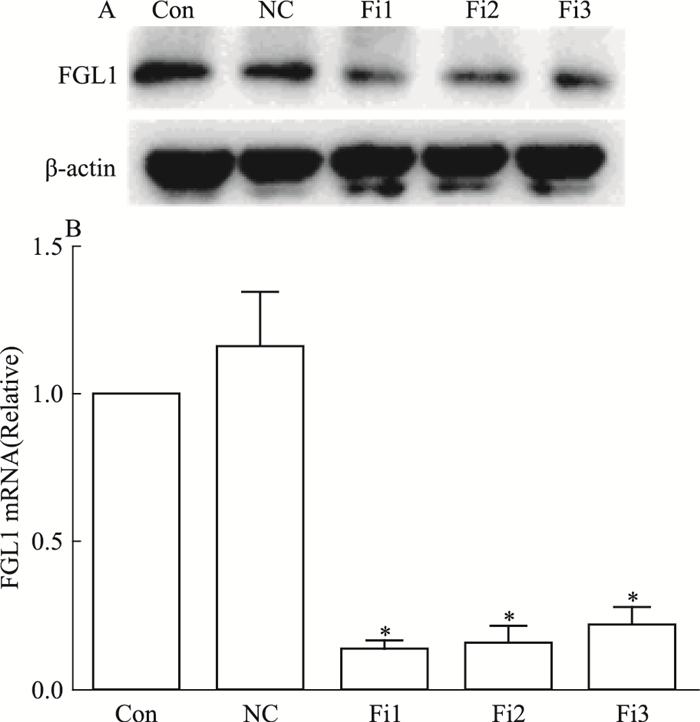
采用siRNA干扰PC9/GR细胞中FGL1的表达, Western blot结果显示3条siRNA转染细胞后, 使FGL1表达水平分别下降至Con组的(0.579±0.005)倍、(0.593±0.039)和(0.495±0.180)倍, 差异有统计学意义(P < 0.05)(Fig 3A); RT-qPCR结果显示采用3条siRNA转染细胞后, FGL1 mRNA表达水平分别下降至Con组的(0.135±0.026)倍、(0.152±0.054)和(0.217±0.052)倍, 差异有统计学意义(P < 0.05)(Fig 3B)。选取干扰效果最好最稳定的siRNA-FGL1-2序列用于后续实验。
|
| Fig 3 Effect of FGL1 interference in PC9/GR cells(x±s, n=5) A: Changes of FGL1 protein in PC9/GR cells after FGL1 interference; B:Changes of FGL1 mRNA in PC9/GR cells after FGL1 interference; *P < 0.05 vs Con |
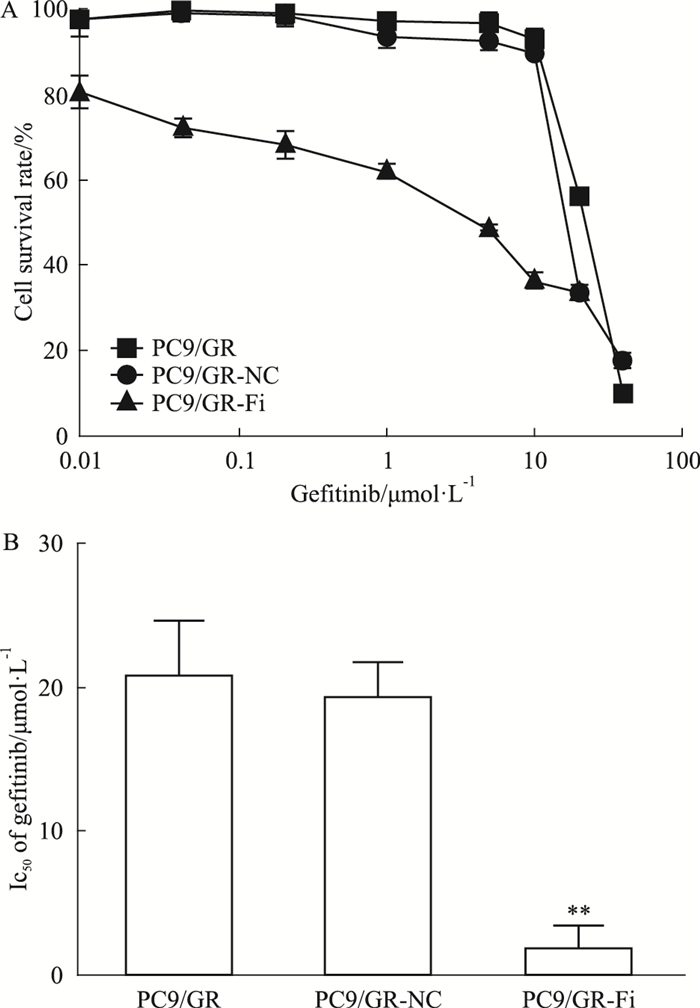
通过转染siRNA降低PC9/GR细胞中FGL1的表达水平后, 利用CCK-8法检测发现吉非替尼作用于PC9/GR细胞Con组、NC组及PC9/GR-Fi组, 对细胞增殖的抑制作用随着浓度的增加而逐渐增强(Fig 4A); Fi组、Con组与NC组对吉非替尼药物IC50分别为(1.967±1.147)μmol/L、(19.179±1.091)μmol/L和(20.754±2.735)μmol/L, 差异有统计学意义(P < 0.01)(Fig 4B), 结果提示降低FGL1表达可增加肺腺癌细胞对吉非替尼药物的敏感性。
|
| Fig 4 Sensitivity of PC9/GR cells to gefitinib(x±s, n=3) A: Effect of gefitinib on proliferation of PC9/GR cells after FGL1 knocked down; B: IC50 of PC9/GR cells after FGL1 knocked down; PC9/GR-NC:PC9/GR cells transfected with siRNA-NC; PC9/GR-Fi: PC9/GR cells transfected with siRNA-FGL1-2;**P < 0.01 vs PC9/GR |
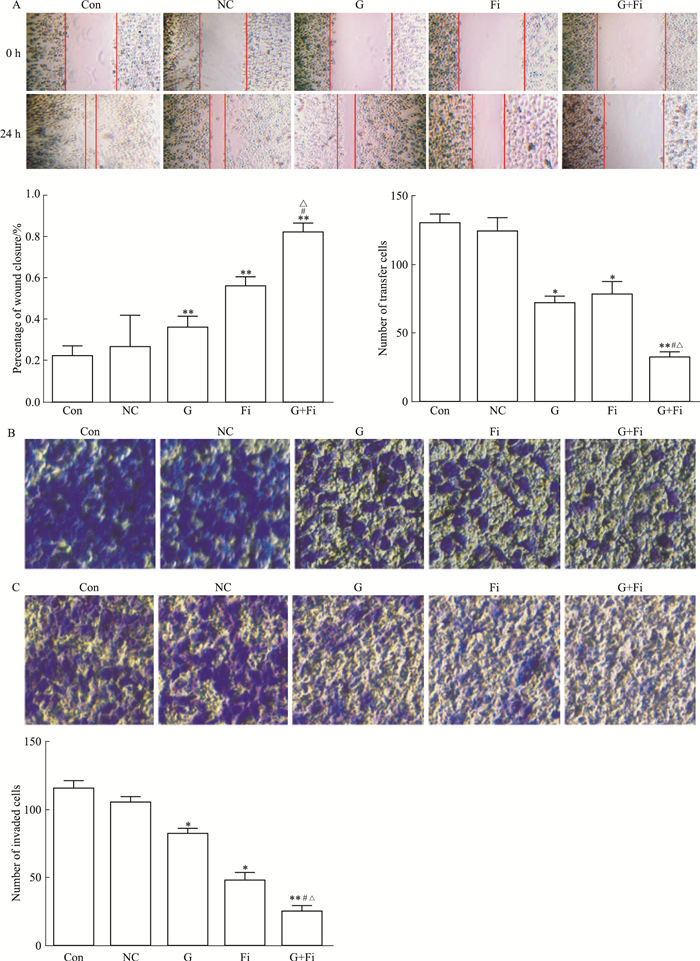
将NC-siRNA和FGL1-siRNA转进PC9/GR细胞, 于划痕24 h后观察细胞迁移能力变化。划痕实验检测结果表明Fi组与和Con组比较细胞迁移至划痕口的细胞明显减少, 划痕间隙较宽, 差异有统计学意义(P < 0.01)(Fig 5A)。G+Fi组细胞与G组、Fi组和Con组比较, 迁移至划痕口的细胞减少更加显著, 划痕间隙最宽, 差异有统计学意义(分别P < 0.01, P < 0.01, P < 0.01)。G组与Con组比较差异无统计学意义。Transwell小室迁移实验中, Fi组(78.33±9.46)与Con组(124.33±9.7)比较, 迁移在小室膜底部的细胞数减少, 差异有统计学意义(P < 0.05);G+Fi组(32.67±3.859)与Fi组(78.33±9.46)、G组(72.33±4.78)及Con组(124.33±9.7)比较, 迁移在小室膜底部的细胞数减少更加明显, 差异有统计学意义(分别P < 0.05, P < 0.05, P < 0.01)(Fig 5B)。说明沉默FGL1表达可降低PC9/GR细胞迁移能力, 联合吉非替尼后比单药组和单独沉默FGL1组对PC9/GR细胞迁移能力抑制更加明显。侵袭实验结果发现, G组(82.67±3.30)和Fi组(47.67±6.53)小室膜底部的细胞数量明显比与Con组(115.33±6.018)少, 差异有统计学意义(分别P < 0.05, P < 0.05);加入同等剂量的吉非替尼后, G+Fi组(25.33±4.03)与F组(47.67±6.53)、G组(82.67±3.30)及Con组(115.33±6.018)比较, 侵袭在小室膜底部的细胞数减少更加显著, 差异有统计学意义(分别P < 0.05, P < 0.05, P < 0.01)(Fig 5C)。说明降低FGL1表达可抑制PC9/GR细胞的侵袭能力, 联合吉非替尼后对PC9/GR细胞的侵袭能力抑制作用更加显著。
|
| Fig 5 Changes of invasion and migration of PG9/GR cells after FGL1 interference(x±s, n=3) A: Changes of wound healing ability of PG9/GR cells after FGL1 interference SP×40; B: Changes of migration ability of PC9/GR cells after FGL1 interference SP×200; C: Changes of invasion ability of PC9/GR cells after FGL1 interference SP×200; Con: blank control group; NC:siRNA-NC group; G: gefitinib group; Fi: siRNA-FGL1-2;G+Fi: gefitinib combined with siRNA-FGL1-2;*P < 0.05, **P < 0.01 vs control; #P < 0.05 vs G group; △P < 0.05 vs Fi group |
Western blot结果证实, 通过siRNA降低PC9/GR细胞FGL1的表达水平后, Fi组相对于阴性对照Con组、NC组和G组, Zeb1、Vimentin表达显著降低而E-cadherin表达明显增加, G+Fi组Zeb1、Vimentin表达降低而E-cadherin表达增加更为显著, 差异有统计学意义(P < 0.01);G组与Con组比较FGL1蛋白表达明显升高, 差异有统计学意义(P < 0.01)(Fig 6), EMT相关蛋白表达无明显变化。说明吉非替尼对PC9/GR细胞的EMT过程无影响, 而高表达的FGL1可能通过EMT过程进而促进肺腺癌细胞耐药表型产生; 抑制FGL1表达可组织PC9/GR细胞的EMT, 联合吉非替尼后对PC9/GR细胞的EMT抑制更明显。

|
| Fig 6 Changes of Zeb1, E-cadherin and Vimentin expression in PC9/GR cells after FGL1 interferences detected by Western blot(x±s, n=3) Con: blank control group; NC:siRNA-NC group; G:gefitinib group; Fi: siRNA-FGL1-2; G+Fi:gefitinib combined with siRNA-FGL1-2;*P < 0.05, **P < 0.01 vs control |
肺癌是全球死亡率较高的恶性肿瘤, 尽管EGFR-TKIs类靶向药物在伴有EGFR基因突变的NSCLC中初始疗效良好, 但9~13个月后约有65%的患者会出现获得性耐药[6]。EGFR-TKIs的获得性耐药的重要机制之一就是细胞表型转化[7], 发生EMT后上皮源性肿瘤细胞失去与基底膜的连接等上皮表型, 获得间质细胞的表型而具有较强的侵袭迁移和抗凋亡等能力[8-9]。目前, 抑制肿瘤细胞的EMT进程的是抗肿瘤治疗的一个重要研究方向。
FGL1是一种68 KD的纤维蛋白原家族成员, 作为有丝分裂生长因子调节增殖因子的表达, 促进肝脏组织再生和修复肝脏损伤[10]。研究表明骨髓间质干细胞通过调节FGL1的表达增强p-STAT/STAT3水平修复急性肝损伤[11], FGL1有丝分裂活性, 通过非受体酪氨酸激酶SRC诱导EGFR活化, 激活ERK/p-ERK通路促进L02人正常肝细胞增殖, 保护原始肝细胞和修复化学损伤的肝细胞[12]。不过FGL1在肝细胞癌中表达并不高, 其丢失可致肝癌细胞的低分化, 机制也许是肝癌中HNF1α的下调或丢失[13]; FGL1在多种实体瘤表达升高, 最新研究发现, FGL1与LKB1突变型肺腺癌的EMT和血管生成相关[14]。表明FGL1不仅在肝细胞增殖相关的通路发挥重要作用, 而且能够调节肺腺癌细胞表型转化和增殖。那么在具有EGFR突变的肺腺癌中, FGL1是否也参与了肺癌细胞的增殖、侵袭和迁移尚不明确。
本研究发现, 与吉非替尼敏感细胞系PC9比较, 吉非替尼继发性耐药细胞系PC9/GR中FGL1的mRNA和蛋白水平明显升高, 提示吉非替尼继发性耐药及耐药后的细胞恶性生物学行为可能与FGL1表达增加相关。本实验通过应用siRNA技术沉默PC9/GR细胞FGL1基因, 经RT-qPCR和Western blot证明FGL1-siRNA可明显降低PC9/GR细胞中FGL1水平, 发现在相同浓度梯度的吉非替尼的作用下, PC9/GR细胞的存活率随药物浓度增加而降低, 其IC50值也降低到原来的十分之一以下, 提示降低PC9/GR细胞FGL1表达可增加其对吉非替尼的敏感性。本实验同时发现干扰PC9/GR细胞中FGL1的表达后, 划痕实验、Transwell小室迁移和侵袭实验结果显示伤口愈合能力、迁移率和穿膜细胞数降低, 且同时加入等剂量的吉非替尼后, 伤口愈合能力、迁移率和穿膜细胞数降更加显著。以上生物学行为改变均说明抑制FGL1表达可抑制PC9/GR细胞迁移和侵袭, 其机制可能与阻断肺腺癌细胞EMT相关。为了进一步证明干扰FGL1对PC9/GR细胞侵袭和迁移的影响是通过抑制肺腺癌细胞EMT过程, 本研究检测了EMT相关分子标志物上皮性黏钙蛋白(E-cadherin)、波形蛋白(Vimentin)和E盒结合锌指蛋白1(Zincfinger E-box-binding protein 1, Zeb1)的表达情况[15]。E-cadherin常作为上皮标记基因, 其表达水平下调可促进癌细胞从原发灶脱落, 远端转移; Vimentin是中间丝的一种蛋白质, 属于间质标记基因, 其表达水平上调可促进细胞骨架重排[16]。Zeb1是胚胎发育过程中必须的转录因子, 与肿瘤血管生成、肿瘤干细胞的干性维持、肿瘤侵袭转移及肿瘤化学耐药密切相关。在本研究中, 单独沉默FGL1相对于对照组、NC组细胞E-cadherin表达上调, 加强细胞间、细胞与基质间黏附作用, Zeb1、Vinentin表达下调而降低肿瘤细胞的侵袭转移能力, 与划痕实验、Traswell小室迁移和侵袭实验结果一致, 说明抑制FGL1表达可抑制PC9/GR细胞EMT过程, 阻止肿瘤细胞的侵袭和迁移; 而吉非替尼组上述蛋白表达与对照组比较无明显变化, 但FGL1-siRNA转染联合吉非替尼作用组与对照组、NC组、吉非替尼组和单独沉默组比较, E-cadherin表达上调, Zeb1、Vinentin表达下调更明显, 说明FGL1低表达不仅可通过影响细胞EMT对PC9/GR细胞侵袭和迁移能力的抑制作用, 同时可增加细胞对吉非替尼的敏感性, 其机制可能与抑制PC9/GR细胞的侵袭和迁移过程相关。
综上所述, 本研究发现干扰FGL1表达后可明显降低PC9/GR细胞的侵袭和迁移能力, 其机制可能是抑制了PC9/GR细胞的EMT过程, 为解决EGFR- TKI获得性耐药问题提供了一定的参考依据。然而, 本实验未验证抑制PC9/GR细胞的MET过程是否增加PC9/GR对吉非替尼的敏感性, 且为体外细胞实验, 尚未建立动物模型验证, 有待后续研究。
| [1] |
Chen W Q, Zheng R, Baade P D, et al. Cancer statistics in China, 2015[J]. CA Cancer J Clin, 2016, 66(2): 115-32. doi:10.3322/caac.21338 |
| [2] |
Siegel R, Miller K, Jemal A. Cancer statistics, 2017[J]. CA Cancer J Clin, 2017, 67(1): 7-30. doi:10.3322/caac.21387 |
| [3] |
Gainor J F, Shaw A T. Emerging paradigms in the development of resistance to tyrosine kinase inhibitors in lung Cancer[J]. Clin Oncol, 2013, 31(31): 3987-96. doi:10.1200/JCO.2012.45.2029 |
| [4] |
Zhou M, Chen D M, Xia L, et al. Clinical research and drug review of epidermal growth factor receptor tyrosine kinase inhibitors in advanced non-small cell lung cancer[J]. Zhonghua Zhong Liu Za Zhi, 2019, 41(12): 949-52. |
| [5] |
Wang J, Sanmamed M, Datar I, et al. Fibrinogen-like protein 1 is a major immune inhibitory ligand of LAG-3[J]. Cell, 2019, 176(1-2): 334-47. doi:10.1016/j.cell.2018.11.010 |
| [6] |
Santarpia M, Menis J, Chaib I, et al. Dacomitinib for the first-line treatment of patients with EGFR-mutated metastatic non-small cell lung cancer[J]. Expert Rev Clin Pharmacol, 2019, 12(9): 831-40. doi:10.1080/17512433.2019.1649136 |
| [7] |
于梦迪, 王明霞, 王海东. 姜黄素逆转非小细胞肺癌分子靶向药物耐药的研究进展[J]. 中国药理学通报, 2017, 33(12): 1633-7. Yu M D, Wang M X, Wang H D. Research progress of reversion molecular targeted drug resistance in non-small cell lung cancer by curcumin[J]. Chin Pharmaco Bul, 2017, 33(12): 1633-7. doi:10.3969/j.issn.1001-1978.2017.12.002 |
| [8] |
Nagano T, Tachihara M, Nishimura Y. Mechanism of resistance to epidermal growth factor receptor-tyrosine kinase inhibitors and a potential treatment strategy[J]. Cells, 2018, 7(11): 5. |
| [9] |
She K L, Fang S H, Du W, et al. SCD1 is required for EGFR-targeting cancer therapy of lung cancer via re-activation of EGFR/PI3K/AKT signals[J]. Cancer Cell Int, 2019, 19(18): 103. |
| [10] |
Hamed N, Anal D, Valeriy D, et al. Targeted disruption of fibrinogen like protein-1 accelerates hepatocellular carcinoma development[J]. Biochem Biophys Res Commun, 2015, 465(2): 167-73. |
| [11] |
Zou Z L, Cai Y J, Chen Y, et al. Bone marrow-derived mesenchymal stem cells attenuate acute liver injury and regulate the expression of fibrinogen-like-protein 1 and signal transducer and activator of transcription3[J]. Mol Med Rep, 2015, 12(2): 2089-97. doi:10.3892/mmr.2015.3660 |
| [12] |
Gao M, Zhan Y Q, Yu M, et al. Hepassocin activates the EGFR/ERK cascade and induces proliferation of L02 cells through the Src-dependent pathway[J]. Cell Signal, 2014, 26(10): 2161-6. doi:10.1016/j.cellsig.2014.04.013 |
| [13] |
Yu H T, Yu M, Li C Y, et al. Specific expression and regulation of hepassocinin the liver and down-regulation of the correlation of HNF1 with decreased levels of hepassocin in human hepatocellular carcinoma[J]. J Biol Chem, 2009, 284(20): 13335-47. doi:10.1074/jbc.M806393200 |
| [14] |
Bie F, Wang G, Qu X, et al. Loss of FGL1 induces epithelial-mesenchymal transition and angiogenesis in LKB1 mutant lung adenocarcinoma[J]. Int J Oncol, 2019, 55(3): 697-707. |
| [15] |
Yeung K T, Yang J. Epithelial-mesenchymal transition in tumor metastasis[J]. Mol Oncol, 2017, 11(1): 28-39. doi:10.1002/1878-0261.12017 |
| [16] |
Sana R, Iain J, Mulford, et al. Targeting EGFR overcomes EMT-mediated resistance in EGFR mutant non-small cell lung cancer[J]. Oncogene, 2019, 38(37): 399-413. |

