

心肌梗死常伴有缺氧、心肌细胞凋亡和死亡, 是除脑出血外引发猝死的另一主要原因[1]。心肌梗死的治疗上也面临着较多困境, 但进入二十一世纪以来, 通过刺激血管新生改善缺血心肌血氧供应, 治疗心肌梗死的策略渐渐被人们所接受[2-3]。丹参在中医临床上治疗心肌梗死等疾病方面有着悠久的实践经历, 丹参酚酸B(salvianolic acid B, SAB)是从中药丹参中提取的水溶性酚酸类化合物, 为丹参的代表性单体成分。蛋白激酶D1(protein kinase D1, PKD1)可以抑制心肌梗死后的炎症和凋亡反应, 促血管新生, 有助于梗死心肌组织的修复[4-5]。缺氧诱导因子(hypoxia induced factor, HIF) -1α是被公认的激活后调控缺血性心脏病中氧平衡紊乱状态的关键蛋白之一[6], 血管内皮生长因子(vascular endothelial growth factor, VEGF)促缺血组织微血管的新生而改善其缺氧供应[3]。PKD1、HIF-1α和VEGF 3者通过VEGF这一联系纽带形成的通路在新生血管的形成、稳定和成熟中发挥着重要的作用[2-6]。本研究旨在探讨SAB是否通过调控PKD1-HIF-1α-VEGF通路促心肌梗死后大鼠血管新生, 保护缺血受损的心肌组织。
1 材料 1.1 实验动物40只Wistar大鼠, ♂, SPF级, 8周龄, 体质量(200±20)g, 购自北京维通利华公司, 动物生产许可证号:SCXK(京)2016-0011。
1.2 药物与试剂SAB(上海陶素公司, 批号:115939-25-8), CID755673(简称CID, 美国MCE公司, 批号:2018276); PKD1、HIF-1α、VEGF和Ⅷ因子的一抗抗体(均购自上海圣克鲁斯公司, 批号分别为:Sc-1796、Sc-1616、Sc-7269和Sc-9176);Cy3荧光标记的羊抗兔IgG二抗(武汉博士德公司, 批号:BA1032);其它试剂为国产分析纯。
1.3 仪器LSM 800激光共聚焦显微镜和ZEN 2.3 lite分析软件(德国蔡司公司); Tecnai G2 20透射电子显微镜(美国赛默飞公司); CUT6062病理切片机和MTMI全密闭自动脱水机(德国赛利公司)。
2 方法 2.1 动物造模和分组大鼠随机分为假手术组(Sham)、心梗模型组(MI)、SAB给药组(SAB)和CID阻断剂组(CID)。结扎左冠状动脉前降支复制心梗模型, Sham组除了结扎外, 其他手术程序和MI组保持一致。术后48 h开始给药, 给药方式为腹腔注射, 具体给药剂量为, SAB组:50 mg·kg-1·d-1, CID组:50 mg·kg-1·d-1 SAB+40 μg·kg-1·d-1 CID, Sham和MI组:等量生理盐水。持续14 d后, 75 mg·kg-1戊巴比妥钠深麻醉下牺牲大鼠, 进行实验指标分析。
2.2 HE染色处死后大鼠的心脏剪取左心室, 含室间隔部分, 参照之前的方法[4], 制成4 μm厚HE染色切片, 光学显微镜400×放大视野下观察分析。
2.3 Masson染色组织取材同HE染色。参照之前的方法[6], 用Masson三色染色法检测心肌纤维化程度, 胶原纤维示蓝绿色, 心肌组织示红色。胶原纤维面积用ZEN 2.3 lite软件进行分析, 其占左心室的比例用胶原容积分数(collagen volume fraction, CVF)值确定。
2.4 透射电镜(transmission electron microscopy, TEM)分析取少许麻醉后大鼠新鲜的左心室组织, 切成0.5 mm3小块后, 1 min内浸入2.5%戊二醛中, 浸泡3 h, 1%锇酸固定, 履行脱水、包埋、聚合成块、染色的操作程序后, 制成50 nm厚的组织切片, TEM 5000×视野下观察分析。
2.5 免疫组化(immunohistochemistry, IHC)染色组织取材同HE染色。参照之前的方法[6], 石蜡切片脱蜡再水化, 然后在10 mmol·L-1柠檬酸钠缓冲液(pH 6.0)中用微波炉处理20 min, 3%过氧化氢阻断内源过氧化物酶后与稀释后的一抗抗体PKD1(1 :500)、HIF-1α(1 :200)、VEGF(1 :500)或Ⅷ(1 :500)在4 ℃下孵育12 h, PBS冲洗3×3 min, 标记羊抗兔IgG二抗(1 :1 000), 室温下结合15 min, DAB染色3 min。400×视野下计数5个不重复视野的阳性染色细胞数量。
2.6 免疫荧光(immunofluorescence, IF)染色组织取材同HE染色, 切片脱蜡后微波处理15 min, PBS冲洗3×3 min后兔血清封闭切片, 加入一抗抗体PKD1(1 :50)、HIF-1α(1 :50)、VEGF(1 :100)或Ⅷ(1 :50), 4 ℃孵育过夜。次日取出, PBST冲洗后与Cy3标记的二抗抗体室温下孵育1 h, DAPI染核5 min后淬灭荧光, 封片。置入LSM 800激光共聚焦显微镜400×视野下观察, ZEN 2.3 lite分析软件计算红蓝荧光比值。
2.7 免疫印迹(Western Blot, WB)4组大鼠心脏组织在裂解缓冲液中充分浸泡后进行组织研磨, 超声裂解, 12 000 r·min-1离心15 min提取上清液, BCA测蛋白浓度后执行SDS-PAGE电泳, 4 ℃下和一抗抗体PKD1(1 :500)、HIF-1α(1 :200)或VEGF(1 :500)孵育过夜, PBS冲洗3×3 min后和二抗(1 :1 000)结合60 min, Odyssey扫描仪扫描蛋白条带, α-View SA软件计算样本蛋白/GAPDH参照蛋白的值。
2.8 统计学处理所有实验数据以x±s表示, 多组间比较用One-way ANOVA分析, 计算软件为GraphPad Prism 6.0。
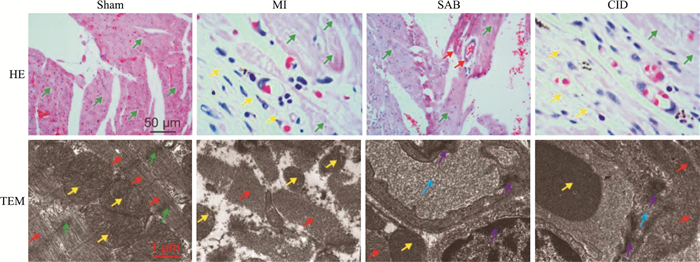
3 结果 3.1 SAB对MI大鼠心肌组织和血管形态变化的影响Fig 1的HE染色中, Sham组大鼠的心肌组织和细胞结构完整清晰(绿色箭头); MI组大鼠心肌组成以肉芽和瘢痕组织为主, 绿色箭头所示的心肌组织染色较浅, 呈疏松化, 和瘢痕组织紧邻, 黄色箭头所示的肉芽组织中可见未发育成熟的微血管、增生的炎症细胞和成纤维细胞; 和MI组相比, SAB组大鼠心肌组织红色染色加深(绿色箭头), 形态学清晰, 并可见发育较为成熟的微血管(红色箭头); CID阻断剂组大鼠心肌组织形态和MI组相似。TEM染色进一步展示了心肌组织的超微结构, Sham组大鼠的心肌组织纹理清晰(红色箭头), 闰盘结构完整(绿色箭头), 线粒体形态清晰饱满(黄色箭头); MI组大鼠心肌纹理模糊甚至消失(红色箭头), 线粒体明显萎缩, 数量减少(黄色箭头); SAB组大鼠心肌组织清晰(红色箭头), 线粒体形态饱满(黄色箭头), 微血管管腔(蓝色箭头)结构完整, 内皮细胞(紫色箭头)结构清晰; CID组大鼠心肌组织形态和MI组相似, 心肌组织(红色箭头)和线粒体(黄色箭头)结构模糊, 微血管管腔(蓝色箭头)断裂, 边缘皱缩, 内皮细胞(紫色箭头)结构模糊。
|
| Fig 1 Effects of SAB on histomorphology of myocardial infarction rats The above picture showed routine HE staining, green arrow showed myocardial tissue, red arrow showed microvascular, yellow arrow showed granulation tissue; the following figure showed TEM staining, red arrow showed myocardial tissue, green arrow showed intercalated disc, yellow arrow showed mitochondria, blue arrow showed microvasculature, purple arrow showed endothelial cells. |
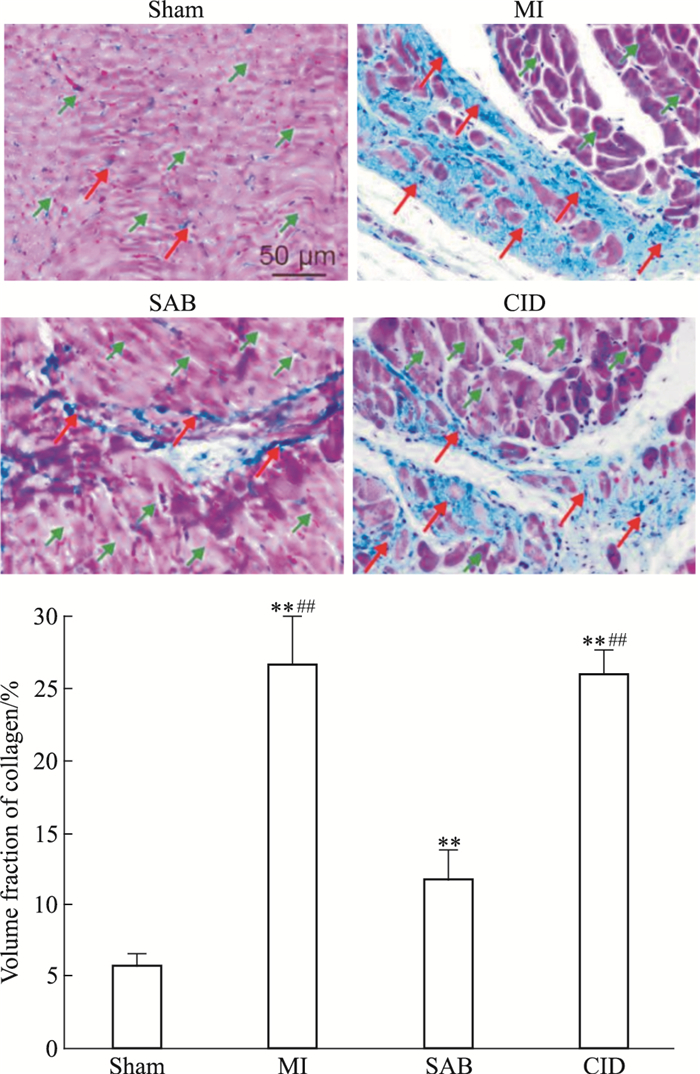
Fig 2的Masson染色中, Sham组大鼠的心肌组织以正常红色心肌组织为主, 少量胶原纤维网织其中; MI组大鼠心肌组织损伤严重, 蓝色的胶原纤维占比较Sham组明显升高(P < 0.01);SAB组大鼠心肌组织以较为完整的红色心肌组织为主, 蓝色的胶原纤维占比较MI组明显下降(P < 0.01);CID组大鼠心肌组织结构和MI组接近, 胶原纤维占比较SAB组明显升高(P < 0.01)。
|
| Fig 2 Effects of SAB on myocardial fibrosis in MI rats (x±s, n=10) The green arrow showed myocardial tissue and the red arrow showed collagen fiber.**P < 0.01 vs sham group; ##P < 0.01 vs SAB group |
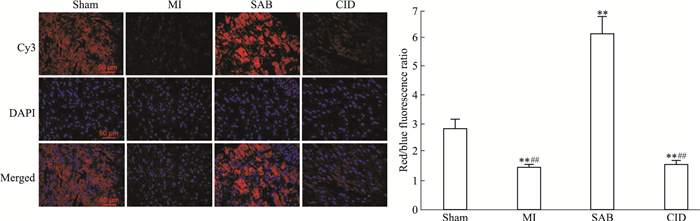
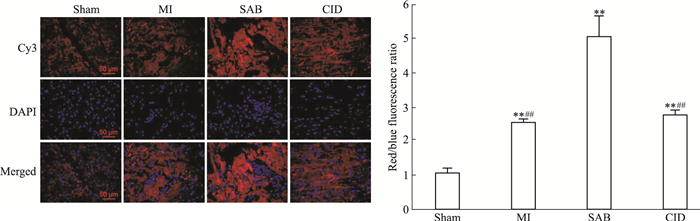
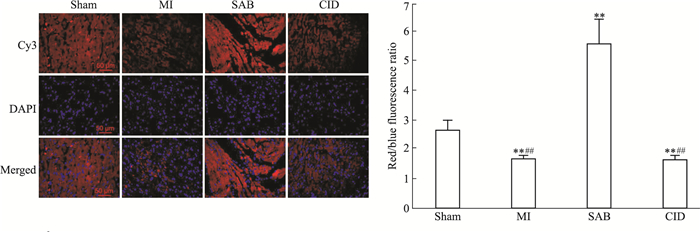
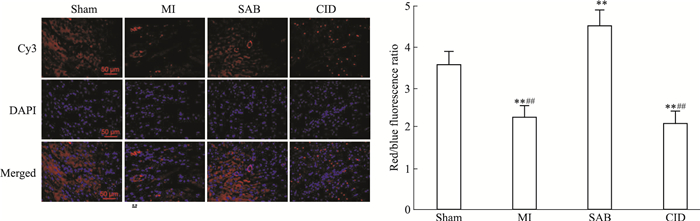
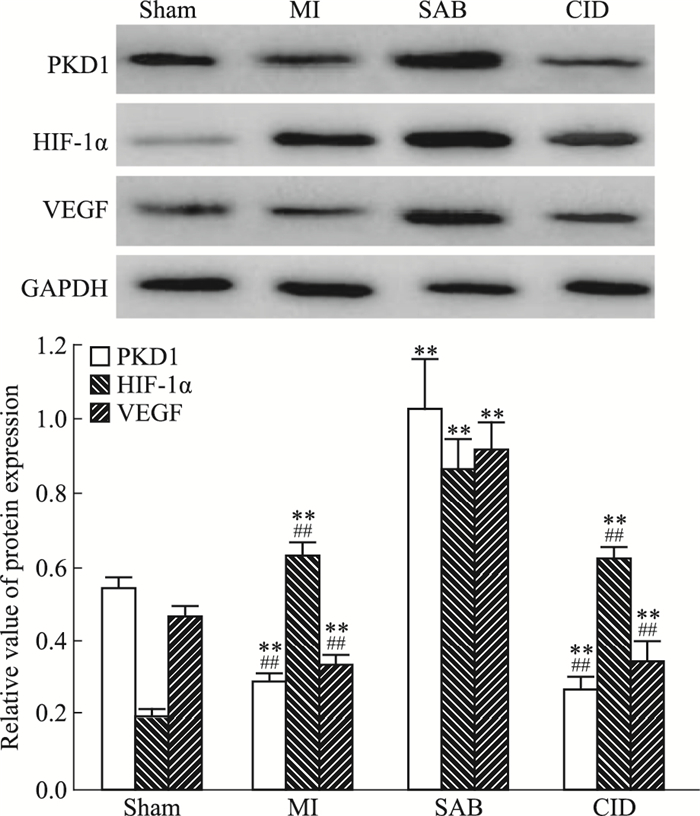
Fig 3~8分别用IHC染色和IF染色检测心肌组织中PKD1、HIF-1α、VEGF和Ⅷ因子的蛋白表达, 应用Western blot染色检测心肌组织中PKD1、HIF-1α和VEGF蛋白的表达(该方法不用于检测Ⅷ因子), 并相互印证结果。IHC染色阳性表达的蛋白呈棕黄色, IF染色阳性表达的蛋白呈红色荧光, Western blot染色阳性表达的蛋白呈灰黑色。3种检测结果呈现一致的趋势, 均表明:Sham组大鼠心肌组织中PKD1、VEGF和Ⅷ因子均有一定量的表达, HIF-1α几乎不表达; MI组大鼠心肌组织中PKD1、VEGF和Ⅷ因子表达较Sham组明显减少(P < 0.01), HIF-1α表达较Sham组明显升高(P < 0.01);SAB组大鼠心肌组织中PKD1、HIF-1α、VEGF和Ⅷ因子表达均较MI组明显升高(P < 0.01);CID组大鼠心肌组织中PKD1、HIF-1α、VEGF和Ⅷ因子表达均较SAB明显减少(P < 0.01), 接近于MI组。

|
| Fig 3 Effect of SAB on expression of PKD1, HIF-1α, VEGF and factor Ⅷ protein in myocardium of MI rats (IHC)(x±s, n=10) Green arrow showed myocardial tissue, red arrow showed protein expression.**P < 0.01 vs sham group; ##P < 0.01 vs SAB group |
|
| Fig 4 Effect of SAB on expression of PKD1(IF)(x±s, n=10) **P < 0.01 vs sham group; ##P < 0.01 vs SAB group |
|
| Fig 5 Effect of SAB on expression of HIF-1α(IF)(x±s, n=10) **P < 0.01 vs sham group; ##P < 0.01 vs SAB group |
|
| Fig 6 Effect of SAB on expression of VEGF(IF)(x±s, n=10) **P < 0.01 vs sham group; ##P < 0.01 vs SAB group |
|
| Fig 7 Effect of SAB on expression of factor Ⅷ(IF)(x±s, n=10) **P < 0.01 vs sham group; ##P < 0.01 vs SAB group |
|
| Fig 8 Effect of SAB on expression of PKD1, HIF-1α and VEGF protein in myocardium of MI rats(x±s, n=10) **P < 0.01 vs sham group; ##P < 0.01 vs SAB group |
本研究利用大鼠MI模型, 采用HE染色、Masson染色和电镜分析评价SAB在MI后心肌组织损伤中的保护作用。HE染色、Masson染色证实, MI后在没有药物干预的情况下, 坏死心肌由肉芽组织完成瘢痕修复, 胶原占比升高, 损害心脏正常的收缩和舒张功能, 进而影响机体的周身血供[4-5]。有意思的是, MI后的心肌组织中, 可以看到部分微血管, 但这些微血管属于肉芽组织的成分之一, 并不成熟, 无法提供有效的微循环血供。TEM结果进一步从超微结构上表明, MI后的心肌组织中, 除了心肌纤维本身的纹理模糊、消失外, 心肌纤维的特征性结构-闰盘也模糊、断裂甚至消失, 这表明心肌组织缺血受损严重。线粒体萎缩、消失、数量减少, 表明心肌组织的能量供应也受到了严重影响, 能量供应的不足, 可能会进一步引发炎症和凋亡反应[7-8], 从而造成心肌的进一步受损。微血管管腔边缘皱缩、断裂甚至消失, 其主要成分之一的内皮细胞结构模糊甚至消失, 进一步表明缺血的心肌组织无法提供有效的微循环血供。应用SAB干预后, 心肌组织恢复较好, 炎症细胞少见, 胶原占比下降, HE染色下可见结构轮廓清晰的微血管。TEM下, 从心肌纹理和闰盘结构看, 心肌组织恢复良好; 从线粒体形态分析, 心肌的能量供应可以保障; 并且微血管管腔形态清晰, 多个内皮细胞结构清晰。这表明, 这些微血管可能属于成熟的血管, 心肌的微循环血供从而得到保障。这表明, SAB干预可以有效保护MI后受损的心肌。应用CID后, 大鼠心肌组织形态学结构接近于MI组, 表明CID可以阻断SAB的保护作用。
本研究还应用IHC染色、IF染色和Western blot 3种不同方法检测分析了PKD1、HIF-1α和VEGF蛋白的表达, 3种检测反映的结果趋势一致。并应用IHC和IF染色检测了Ⅷ因子的表达, 两种检测方法反映的结果也比较相似。检测结果表明, Sham组心肌组织中有一定的PKD1、VEGF和Ⅷ因子的表达。这可能是PKD1和VEGF在机体的正常生理活动中发挥着一定的作用[3], PKD1是正常的胚胎发育进程中的必不可少的调控蛋白之一, PKD1的mRNA在心肌组织中高表达, 在血管内皮细胞和成纤维细胞中表达丰度也较高。Ⅷ因子反映的是血管的表达, 而正常的心肌组织中血管数量较多, 因此, IHC和IF染色均能检测出Ⅷ因子较高的表达; HIF-1α表达量极低, 这可能是由于HIF-1α的表达需要缺血缺氧环境诱导激发[9], 在正常的心肌组织中是受到阻遏表达的。
应用SAB干预后, 心肌组织中的PKD1、HIF-1α、VEGF蛋白和Ⅷ因子的表达均较MI组明显上调。PKD1是介导心血管疾病中重要的信号通路的关键蛋白之一, 涉及心肌对缺血的反应以及缺血后血管和心脏的重构进程。PKD1触发血管系统中内皮细胞(endothelial cells, ECs)对环境信号刺激的正确应答反应, 这一过程还需要VEGF激活后的协助作用, 后者可以激活磷脂酶Cγ1以及ανβ信号通路, 诱导血管生成基因的表达, 有助于微血管管腔的形成和稳定, 以及微循环的重建[10-14]。在内皮祖细胞(endothelial progenitor cells, EPCs)中, PKD1和VEGF的协同作用发挥着相似的调节功能, 而EPCs是内源性血管生成的主要细胞之一[14]。VEGF也可以通过VEGFR2/KDR-PKC信号通路反向激活PKD1, 进而激活ECs的成管作用[12]。PKD-1还通过影响一种控制心脏代谢的重要酶心脏脂蛋白脂酶的合成和分泌调节心脏的能量代谢[14]。HIF-1α在缺氧条件下稳定表达, 并控制着下游100多个基因的表达, 介导组织对缺氧/低氧的适应, 参与血管生成、葡萄糖代谢和细胞凋亡, 并在缺氧条件下维持组织和细胞的稳态[9]。缺氧的环境中, HIF-1α在血管内皮中大量集聚, 并与VEGF的启动子SENP-1结合, 诱导VEGF的表达[15]。并且, 缺氧条件下, HIF-1α的活化可将心肌细胞的氧化磷酸化代谢反应转化为糖酵解反应, 从而抑制活性氧在心肌细胞中的生成过度而损伤心肌[15]。另有文献报道, 应用转基因动物模型实现HIF-1α的过表达可以促血管新生而缩小心梗大鼠的梗死面积, 提升缺血心脏的心功能指标[13]; 而HIF-1α的敲除使小鼠的缺血心肌组织的结构破坏明显, 血管数量进一步减少, 心功能供血明显受限[9]。结合以上文献报道和本研究结果推测, SAB可能通过上调心肌组织中PKD1、HIF-1α、VEGF蛋白和Ⅷ因子的表达, 促使损伤心肌组织的血管新生, 改善心肌的微循环灌注, 进而改善心脏的能量代谢和恢复心功能。
本研究还发现, 应用了PKD1的特异性阻断剂CID后, PKD1、HIF-1α、VEGF蛋白和Ⅷ因子的表达均明显下调。这进一步表明, SAB的促心肌梗死大鼠血管新生的作用和其对PKD1-HIF-1α-VEGF信号通路的调控密切关联。
| [1] |
胡盛寿, 高润霖, 刘力生, 等. 《中国心血管病报告2018》概要[J]. 中国循环杂志, 2019, 34(3): 209-20. Hu S S, Gao R L, Liu L S, et al. Summary of the 2018 report on cardiovascular diseases in China[J]. Chin Circ J, 2019, 34(3): 209-20. doi:10.3969/j.issn.1000-3614.2019.03.001 |
| [2] |
Chen J G, Xu X M, Ji H, et al. Inhibiting miR-155 protects against myocardial ischemia/reperfusion injury via targeted regulation of HIF-1α in rats[J]. Iran J Basic Med Sci, 2019, 22(9): 1050-8. |
| [3] |
Yang L, Liu N, Zhao W, et al. Angiogenic function of astragaloside IV in rats with myocardial infarction occurs via the PKD1-HDAC5-VEGF pathway[J]. Exp Ther Med, 2019, 17(4): 2511-8. |
| [4] |
杨雷, 刘萍, 刘暖, 等. 蛋白激酶D1对心肌梗死大鼠心肌组织炎症和凋亡的影响[J]. 中国药理学通报, 2019, 35(10): 1437-42. Yang L, Liu P, Liu N, et al. Effect of protein kinase D1 on myocardial inflammation and apoptosis in rats with myocardial infarction[J]. Chin Pharmacol Bull, 2019, 35(10): 1437-42. doi:10.3969/j.issn.1001-1978.2019.10.019 |
| [5] |
杨雷, 刘暖, 毛秉豫. 蛋白激酶D1调控胶原表达逆转心肌梗死后心室重构的作用[J]. 安徽医科大学学报, 2019, 54(10): 1535-9. Yang L, Liu N, Mao B Y. Protein kinase D1 reverses ventricular remodeling after myocardial infarction through modulating collagen expression[J]. Acta Univ Med Anhui, 2019, 54(10): 1535-9. |
| [6] |
李军昌, 司静文, 刘海涛, 等. 黄芪甲苷Ⅳ对梗死小鼠心肌新生血管成熟及HIF-1α、VEGF蛋白表达的影响[J]. 心脏杂志, 2017, 29(3): 269-75. Li J C, Si J W, Liu H H, et al. Effect of astragaloside IV on angiogenesis maturity in mice with myocardial infarction[J]. Chin Heart J, 2017, 29(3): 269-75. |
| [7] |
Al-Salam S, Hashmi S. Myocardial ischemia reperfusion injury: apoptotic, inflammatory and oxidative stress role of galectin-3[J]. Cell Physiol Biochem, 2018, 50(3): 1123-39. doi:10.1159/000494539 |
| [8] |
Suthahar N, Meijers W C, Silljé H H W, et al. From inflammation to fibrosis-molecular and cellular mechanisms of myocardial tissue remodelling and perspectives on differential treatment opportunities[J]. Curr Heart Fail Rep, 2017, 14(4): 235-50. doi:10.1007/s11897-017-0343-y |
| [9] |
Cai Z, Luo W, Zhan H, et al. Hypoxia-inducible factor 1 is required for remote ischemic preconditioning of the heart[J]. Proc Natl Acad Sci USA, 2013, 110(43): 17462-7. doi:10.1073/pnas.1317158110 |
| [10] |
刘暖, 杨雷, 毛秉豫, 等. 蛋白激酶D1在大鼠骨髓源性内皮祖细胞中的促血管新生作用[J]. 中国药理学通报, 2015, 31(9): 1259-63. Liu N, Yang L, Mao B Y, et al. Angiogenesis of protein kinase D1 in bone marrow-derived endothelial progenitor cells of rats[J]. Chin Pharmacol Bull, 2015, 31(9): 1259-63. doi:10.3969/j.issn.1001-1978.2015.09.016 |
| [11] |
杨雷, 刘暖, 毛秉豫, 等. 蛋白激酶D1促血管新生的体内外实验分析[J]. 中国病理生理杂志, 2016, 32(1): 146-50, 155. Yang L, Liu N, Mao B Y, et al. Promoting angiogenesis of protein kinase D1 in vitro and in vivo[J]. Chin J Pathophysiol, 2016, 32(1): 146-50, 155. doi:10.3969/j.issn.1000-4718.2016.01.025 |
| [12] |
Ha C H, Jhun B S, Kao H Y, et al. VEGF stimulates HDAC7 phosphorylation and cytoplasmic accumulation modulating matrix metalloproteinase expression and angiogenesis[J]. Arterioscler Thromb Vasc Biol, 2008, 28(10): 1782-8. doi:10.1161/ATVBAHA.108.172528 |
| [13] |
di Blasio L, Droetto S, Norman J, et al. Protein kinase D1 regulates VEGF-A-induced alph-av-beta3 integrin trafficking and endothelial cell migration[J]. Traffic, 2010, 11(8): 1107-18. doi:10.1111/j.1600-0854.2010.01077.x |
| [14] |
Yu D, Chen W, Ren J, et al. VEGF-PKD1-HDAC7 signaling promotes endothelial progenitor cell migration and tube formation[J]. Microvasc Res, 2014, 91: 66-72. doi:10.1016/j.mvr.2013.10.006 |
| [15] |
Li S, Li S. Effects of transplantation of hypoxia-inducible factor-1α genemodified cardiac stem cells on cardiac function of heart failure rats after myocardial infarction[J]. Anatol J Cardiol, 2018, 20(6): 318-29. |

