

冠状动脉阻塞,心肌供氧不足,耗氧增加导致的心肌坏死是急性心肌梗死的基本病因。急性心肌梗死诱发因素众多,发病率逐年升高,严重威胁人类健康[1]。从来源广泛的中草药中分离高效低毒活性成分,用于防治心肌梗死,成为近年来该领域的一个研究热点[2-3]。自噬是一种保守的细胞自我降解的过程,在肿瘤、神经退行性疾病、心血管疾病等的发生发展中发挥重要的生物学效应。现代研究发现,长期严重的缺血/缺氧诱导的过度自噬会加重心肌损伤甚至引发心衰[4]。九龙藤是一种广西民族特色中草药,据报道,其提取物具有活血化瘀、抗炎、抗氧化和抗血小板聚集等多种药理作用[5]。课题组前期研究亦表明,九龙藤总黄酮(Bauhinia championii flavones,BCF)对垂体后叶素所致心肌缺血具有保护作用,并可通过激活PI3K/Akt通路调控自噬减轻心肌缺血/再灌注损伤[6-8],但BCF对心肌细胞缺血/缺氧损伤的作用尚未可知。
1 材料 1.1 H9c2大鼠心肌细胞购自上海中科院细胞库。
1.2 试剂九龙藤总黄酮:本室分离,总黄酮含量以芦丁计为82%,其分离纯化方法见文献[9]。卡托普利(Captopril,批号SLBM6819V)、氯喹(Chloroquine,CQ, 批号BCBM9716V)、3-甲基腺嘌呤(3-Methyladenine,3-MA,货号M9281)与雷帕霉素(Rapamycin,Rapa,货号R8140)购自Sigma公司;胎牛血清(货号13011-8611-100mL)、高糖及无糖DMEM(批号2044490)购自Gibco公司;Giemsa染色液(批号20190606)、DAPI染色液(批号20181030)购自索莱宝生物科技公司;CCK-8试剂盒购于东仁化学科技上海有限公司(批号KH741);cTnI试剂盒(批号W090186)与CK-MB试剂盒(批号Jun 2019)分别来自武汉华美生物公司和上海酶连生物科技公司;Ad-mRFP-GFP-LC3腺病毒(批号133F082)来自汉恒生物科技上海有限公司;TransZol UP(批号N10212)、TransScript One-Step Gdna Removal and cDNA Synthesis SuperMix(批号L20731)、GAPDH抗体(批号M21109)等购自全式金生物科技公司;PowerUpTM SYBRTM Green Master Mix(批号00684721)购自Applied Biosystems Instruments公司,引物购自Thermo Fisher Scientific公司;LC3抗体(批号DQ0262)来自Elabscience;Cathepsin D抗体(批号00058789)来自Proteintech Group;P62抗体(批号GR124843-26)来自Abcam。
1.3 仪器CO2孵箱(日本SANYO,型号MCO-15AC);厌氧培养箱(上海龙跃,型号LAI-3T);酶标仪(TECAN,型号infinite F50);正置荧光显微镜(德国ZEISS,型号Z2);超微量核酸定量仪(Thermo Scientific,型号NanoDrop One);实时荧光定量PCR仪(Bio-Rad,型号CFX96TM Real-Time System);免疫印迹化成像系统(Bio-Rad,型号ChemiDocTMXRS+)。
2 方法 2.1 细胞培养与OGD模型的建立10%胎牛血清与90%高糖DMEM配制的完全培养基用于H9c2心肌细胞的培养,并根据文献方法建立细胞OGD模型[10],将培养液换成不含血清的无糖DMEM培养基,并转移细胞至含94% N2、5% CO2、1% O2的手套培养箱中,培养24 h模拟心肌缺血/缺氧。
2.2 药物预处理与分组H9c2心肌细胞随机分组。模型组细胞按照2.1所述方法建立OGD模型,正常组细胞用高糖DMEM在正常培养条件下培养相同时间。除正常和模型组外,药物干预组细胞于造模前4 h加入相应药物。
2.3 Giemsa染色法观察H9c2心肌细胞形态对数生长期的细胞以1×105个/孔密度种于底部铺有洁净细胞爬片的6孔板中,每组设6个复孔。造模结束后,以4%多聚甲醛固定细胞,之后以PBS洗涤细胞,每孔加入400 μL Giemsa染液染色20 min,弃液后再用PBS洗涤2次,滤纸轻轻吸去多余液体,正置显微镜下观察细胞形态。
2.4 CCK-8检测细胞活力心肌细胞以104个/孔密度接种于96孔板,根据上述方法进行药物预处理和建立模型。根据试剂盒说明书于450 nm处检测OD值。
2.5 Elisa检测cTnI和CK-MB含量根据试剂盒说明书检测细胞培养上清液中cTnI、CK-MB含量。
2.6 腺病毒(Ad-mRFP-GFP-LC3)转染观察自噬体及自噬溶酶体数量H9c2心肌细胞以1×106个/孔的密度种于底部铺有细胞爬片的6孔板中,置于CO2培养箱中孵育24 h,每孔加入含15 μL腺病毒的新鲜培养基感染细胞6 h。按实验方案进行药物预处理并建立OGD模型。待造模结束,以PBS洗涤3次,4%多聚甲醛固定10分钟,根据DAPI试剂盒说明书染色,抗荧光淬灭剂封片。正置荧光显微镜下观察荧光斑点数量。在3次独立实验中,每组至少随机计算10个细胞荧光斑点数并最终取其平均值。
2.7 RT-qPCR检测基因的表达用TRIzol裂解细胞,氯仿和异丙醇等有机溶剂提取纯化总RNA,超微量核酸定量仪分析RNA的质量和纯度。根据逆转录试剂盒说明书合成cDNA,PowerUpTM SYBRTM Green Master Mix用于定量mRNA的表达。实时荧光定量PCR反应条件根据试剂盒说明书设定。用相对定量法计算基因相对表达量, 2-ΔΔCt方法用于分析实验结果。引物序列见Tab 1。
| Genes (Rat) | Sequence |
| LC3 | Forward 5′-ACCCTCTACGATGCTGGTGA-3′ |
| Reverse 5′-GCTGTCCTCAATGTCCTTCTG-3′ | |
| P62 | Forward 5′-GCTGCTCTCTTCAGGCTTACAG-3′ |
| Reverse 5′-CCTGCTTCACAGTAGACGAAAG-3′ | |
| GAPDH | Forward 5′-GACATGCCGCCTGGAGAAAC-3′ |
| Reverse 5′-AGCCCAGGATGCCCTTTAGT-3′ |
以组织、细胞高效裂解液和蛋白酶抑制剂(100 : 1)配置而成的混合液提取细胞总蛋白,以BCA试剂盒进行蛋白定量。每组取20 μg总蛋白用于SDS-PAGE凝胶电泳。以5%脱脂奶粉封闭PVDF膜,4 ℃一抗孵育PVDF膜过夜后,TBST洗膜3次并用二抗孵育1 h。用Image J分析条带灰度值。
2.9 统计学分析用SPSS 25.0进行统计学分析,两组之间比较用t检验法,以单因素方差分析法进行多组间比较。
3 结果 3.1 BCF对缺氧H9c2心肌细胞形态的影响如Fig 1所示,正常细胞为长梭形,排列较整齐且紧密;而模型组细胞生长密度低,部分细胞变不规则形状,细胞核固缩;与模型组相比,BCF干预组细胞形态明显改善,细胞脱落减少,密度增加,状态较好,与阳性药卡托普利效果相当。

|
| Fig 1 Effect of BCF on H9c2 cardiomyocytes morphology (×200) |
如Fig 2所示,模型组细胞活力明显降低(P < 0.01 vs Control);两种剂量BCF均提高OGD心肌细胞活力(P < 0.05 vs OGD),其中,低剂量组效果最好,与阳性药卡托普利相比差异无统计学意义。

|
| Fig 2 Effect of BCF on viability of H9c2 cardiomyocytes suffered OGD (x±s, n=6) **P < 0.01 vs control group; #P < 0.05, ##P < 0.01 vs OGD group; △P < 0.05 vs OGD+Captopril group |
由Tab 2可知,OGD心肌细胞上清液中cTnI与CK-MB含量明显升高(P < 0.01 vs Control),而两种剂量BCF均可减少cTnI和CK-MB含量(P < 0.05 or P < 0.01 vs OGD),减轻心肌细胞损伤,且低剂量效果更佳。据此,我们选择低剂量BCF进一步研究药物对自噬的作用。
| Group | cTnI/ng·L-1 | CK-MB/ng·L-1 |
| Control | 28.47±0.27 | 32.62±0.34 |
| OGD | 63.18±0.32** | 70.73±0.52** |
| BCF(6 mg·L-1) | 54.65±0.92## | 58.93±0.68## |
| BCF(12 mg·L-1) | 58.93±0.87# | 63.78±0.49# |
| Captopril(3 mg·L-1) | 51.65±0.92## | 54.93±0.68## |
| **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs OGD | ||
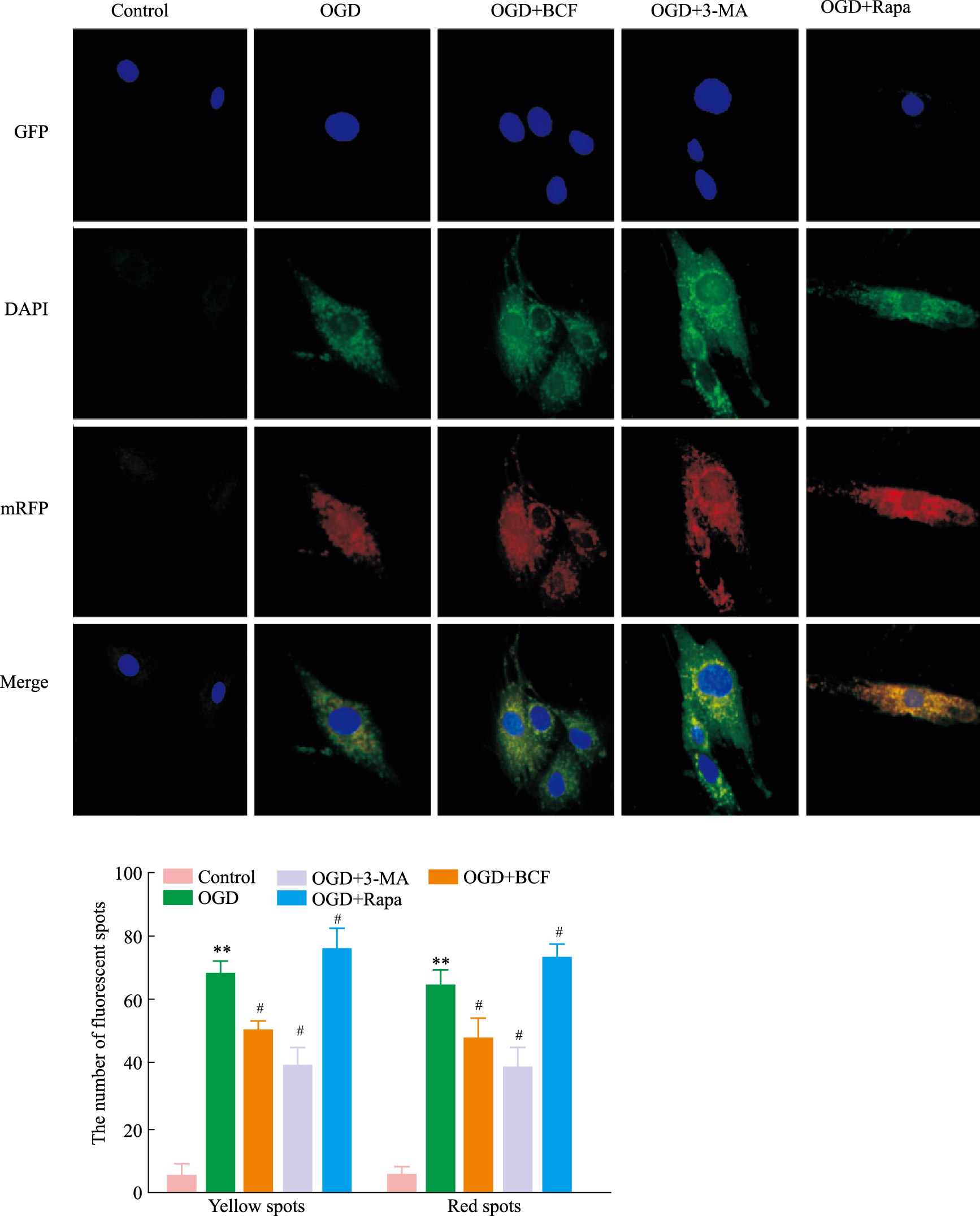
以带荧光标记LC3的腺病毒转染检测活细胞中的自噬体与自噬溶酶体[11]。当自噬形成时,LC3蛋白定位于自噬体膜上,随后LC3蛋白随自噬体与溶酶体融合,形成自噬溶酶体。由于GFP是一种酸敏感物质,溶酶体的酸性环境易淬灭GFP荧光,而mRFP在酸性环境下可稳定存在,因此GFP与mRFP荧光融合而成的黄色荧光代表自噬体,而单独的mRFP荧光斑点代表自噬溶酶体。结果如Fig 3所示,模型组与Rapa组细胞中黄色与红色荧光斑点的数量明显增加(P < 0.01 vs Control),自噬增加;而BCF与3-MA预处理的细胞中,黄色和红色荧光斑点明显减少,自噬受抑制(P < 0.05 vs OGD)。
|
| Fig 3 Number of autophagosomes and autolysosomes observed by Ad-mRFP-GFP-LC3 transfection (x±s, n=6) **P < 0.01 vs control group; #P < 0.05 vs OGD group |
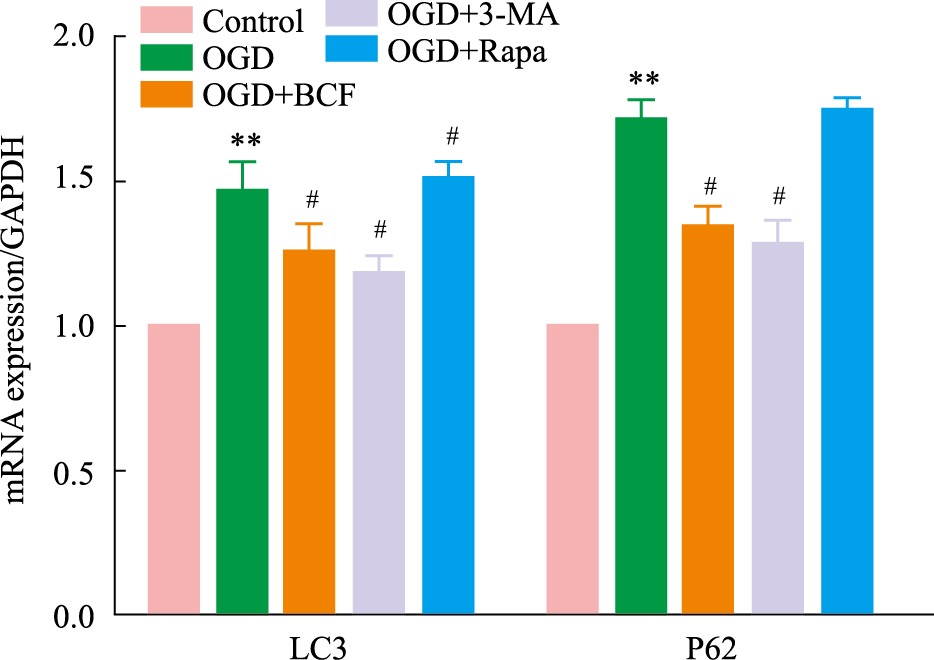
结果如Fig 4所示,与正常组相比,OGD组细胞中两种mRNA水平均明显提高(P < 0.01);经典的自噬诱导剂Rapa可上调LC3、P62 mRNA表达(P < 0.05 vs OGD);而BCF及3-MA干预明可明显降低LC3、P62 mRNA水平(P < 0.05 vs OGD)。
|
| Fig 4 Effect of BCF on mRNA expression of LC3 and P62 in OGD treatment cardiomyocytes (x±s, n=6) **P < 0.01 vs control group; #P < 0.05 vs OGD group |
为进一步研究BCF对自噬通量的影响,我们使用自噬溶酶体抑制剂—CQ作为对照。结果如Fig 5所示,CQ干预组LC3-Ⅱ/LC3-Ⅰ比值上升、P62表达增加、Cathepsin D表达减少(P < 0.05 vs OGD);而BCF干预可明显下调LC3-Ⅱ/LC3-Ⅰ蛋白比例及Cathepsin D表达,上调P62表达(P < 0.05 vs OGD)。有意思的是,与单用CQ相比,联合应用BCF与CQ可同时下调LC3-Ⅱ/LC3-Ⅰ比值及Cathepsin D蛋白表达(P < 0.05),初步提示BCF预处理可以影响自噬的发生发展,而并非只作用于其中某一环节。

|
| Fig 5 Effect of BCF on protein expression of LC3, P62 and Cathepsin D in cardiomyocytes exposed to OGD (x±s, n=6) **P < 0.01 vs control group; #P < 0.05, ##P < 0.01 vs OGD group; △P < 0.05 vs OGD +CQ group |
急性心肌梗死是以动脉供血障碍、出量减少及缺血性心肌坏死为主要病理特征的心血管常见急症,常并发心力衰竭,病情凶险、致死率高。临床主要通过手术或冠脉介入术恢复心脏血流供应,但随之而来的缺血/再灌注损伤制约着整体治疗效果。另一方面,硝酸甘油、ACEI类药物、β阻滞剂等虽可减轻心肌缺血损伤,但副作用较大[12]。近年来,从活血化瘀类中药中提取的天然活性成分在细胞、动物缺血性心脑血管疾病模型中表现出良好的治疗前景,为缺血性心脑血管疾病的防治提供了新的思路。BCF是九龙藤的主要活性物质,课题组前期报道了BCF在动物心肌缺血/缺灌注损伤与心肌梗死疾病模型中的治疗作用[6-8],本研究旨在探讨BCF对体外心肌缺血/缺氧损伤的抑制作用及潜在机制。
H9c2大鼠心肌细胞OGD模型常用于体外模拟心肌缺血/缺氧损伤[13]。cTnI和CK-MB是临床上两种最具代表性的心肌坏死血清生物标志物,其含量与心肌损伤程度呈正相关。本研究通过构建OGD模型研究BCF对心肌缺血/缺氧损伤的作用,结果发现,BCF干预可明显改善缺氧心肌细胞形态,提高细胞活力,降低细胞培养上清液中cTnI与CK-MB含量,有效减轻缺血/缺氧诱导的心肌细胞损伤。
自噬是一种高度保守的生理现象,可降解细胞内老化细胞器及受损蛋白等大分子物质。在正常情况下,细胞很少发生自噬,而饥饿、内质网应激、缺血/缺氧、细胞老化、细胞器损伤等是自噬常见的诱导因素[14-15]。有研究发现,自噬作为心脏在缺氧缺血损伤下心肌细胞的适应性反应,一定程度的自噬对心肌细胞的存活具有保护作用,而长期严重缺氧引起的过度自噬可能会加速多种缺血性心脏病的发展[16-17],因此,抑制自噬可能是治疗此类疾病的一个策略。
我们利用串联荧光标记LC3的腺病毒感染心肌细胞,观察BCF对自噬体及自噬溶酶体形成的影响[11]。在串联荧光体系中,黄色荧光斑点提示自噬体,红色荧光斑点指示自噬溶酶体。结果显示,模型组细胞中自噬体和自噬溶酶体的形成明显上升,提示OGD处理可诱导自噬的发生发展;而BCF预处理组中,两种荧光斑点数量明显减少,其中,黄色荧光斑点的减少提示BCF对自噬体的形成具有抑制作用,RT-qPCR实验结果也验证了此推断,但红色荧光的减少可能是自噬上游被抑制所导致,那么,BCF对自噬溶酶体形成有何影响?
基于此,课题组使用自噬溶酶体抑制剂—CQ为对照,进一步探究BCF对自噬通量的影响。结果显示,CQ干预组细胞中LC3-Ⅱ/I水平上升,自噬体数量增加。由于自噬是一个持续动态的过程,所以CQ组细胞中自噬体的积聚进一步证明OGD诱导了心肌细胞自噬的发生,而BCF干预使LC3-Ⅱ/I及Cathepsin D表达降低、P62增加。另一方面,BCF与CQ联用逆转了CQ导致的自噬体积聚、增强了对Cathepsin D的抑制,说明BCF可通过抑制自噬体形成及溶酶体活性等多个环节影响自噬的发生发展,具体的机制研究还有待进一步深入。
综上所述,本研究表明BCF预处理能有效改善心肌细胞形态,促进心肌细胞存活,减少cTnI、CK-MB外漏,抑制过度自噬,减轻心肌缺血/缺氧损伤。
| [1] |
Thiele H, Desch S, de Waha S. Acute myocardial infarction in patients with ST-segment elevation myocardial infarction: ESC guidelines 2017[J]. Herz, 2017, 42(8): 728-38. doi:10.1007/s00059-017-4641-7 |
| [2] |
Huang J C, Li X B, Liu P J, et al. Emodin protects H9c2 cells against hypoxia-induced injury via regulation of miR-26a/survivin and the JAK1/STAT3 pathway[J]. J Cell Biochem, 2019, 1-10. |
| [3] |
Zhang C, Liao P, Liang R G, et al. Epigallocatechin gallate prevents mitochondrial impairment and cell apoptosis by regulating miR-30a/p53 Axis[J]. Phytomedicine, 2019, 61: 152845. doi:10.1016/j.phymed.2019.152845 |
| [4] |
Liu X X, Deng Y F, Xu Y F, et al. MicroRNA-223 protects neonatal rat cardiomyocytes and H9c2 cells fromhypoxia-induced apoptosis and excessive autophagy via the Akt/mTOR pathway by targeting PARP-1[J]. J Mol Cell Cardiol, 2018, 118: 133-46. doi:10.1016/j.yjmcc.2018.03.018 |
| [5] |
Xu W, Chu K D, Li H, et al. Bauhinia championii extraction treatment ofcollagen-induced arthritisvia downregulation of the expression of TLR4, MyD88and NF-kappaB[J]. Am J Chin Med, 2013, 41(2): 379-90. |
| [6] |
Jian J, Xuan F F, Qin F Z, Huang R B. Bauhinia championii flavone inhibits apoptosis and autophagy via the Pi3K/akt pathway in myocardial ischemia/reperfusion injury in rats[J]. Drug Design, Development Therapy, 2015, 9: 5933-45. |
| [7] |
Liao P, Sun G B, Zhang C, et al. Bauhinia championii Flavone attenuates hypoxia-reoxygenation induced apoptosis in H9c2 cardiomyocytes by improving mitochondrial dysfunction[J]. Molecules, 2016, 21: 1469. doi:10.3390/molecules21111469 |
| [8] |
方瑜, 孙瑶, 简洁. 九龙藤总黄酮对垂体后叶素致大鼠急性心肌缺血的保护作用[J]. 中国药理学通报, 2013, 29(11): 1592-6. Fang Y, Sun Y, Jian J. Protective effects of Bauhinia championii flavones onpituitrin-induced acute myocardial ischemia in rats[J]. Chin Pharm Bull, 2013, 29(11): 1592-6. doi:10.3969/j.issn.1001-1978.2013.11.027 |
| [9] |
孙瑶, 李春凤, 林炜鑫, 等. 正交试验优选九龙藤总黄酮纯化工艺[J]. 中国实验方剂学杂志, 2014, 20(22): 29-32. Sun Y, Li C F, Lin W X, et al. Orthogonal design for optimizing purification process of total flavonoids from Bauhinia championii[J]. Chin J Exp Tradit Med Form, 2014, 20(22): 29-32. |
| [10] |
Jia Z Y, Lin L, Huang S J, et al. Inhibition of autophagy by berberine enhances the survival of H9C2 myocytes following hypoxia[J]. Mol Med Rep, 2017, 16(2): 1677-84. doi:10.3892/mmr.2017.6770 |
| [11] |
Wu X Q, Zheng D C, Qin Y Y, et al. Nobiletin attenuates adverse cardiac remodeling after acute myocardial infarction in rats via restoring autophagy flux[J]. Biochem Biophys Res Commun, 2017, 492(2): 262-8. doi:10.1016/j.bbrc.2017.08.064 |
| [12] |
张庆, 刘敏, 梁田, 等. 黄芪保心汤对心肌梗死后心衰大鼠心室重构及相关炎性因子影响的研究[J]. 新中医, 2019, 51(3): 8-12. Zhang Q, Liu M, Liang T, et al. Peiyingstudy on the effect of huangqi BaoXin Tang on ventricular remodeling and related inflammatory factors in rats with heart failure after Myocardial infarction[J]. Journal of New Chinese Medicine, 2019, 51(3): 8-12. |
| [13] |
梁关凤, 李素娟, 邱晓霞, 等. 激活Sonic hedgehog通路改善缺血缺氧心肌细胞DNA损伤[J]. 中国药理学通报, 2018, 34(9): 1235-42. Liang G F, Li S J, Qiu X X, et al. Activation of Sonic hedgehog signaling in ventricular cardiomyocytes exerts DNA protection against hypoxia[J]. Chin Pharm Bull, 2018, 34(9): 1235-42. doi:10.3969/j.issn.1001-1978.2018.09.011 |
| [14] |
Hoo R L, Shu L, Cheng K K, et al. Adipocyte fatty acid binding protein potentiates toxic lipids-induced endoplasmic reticulum stress in macrophages via Inhibition of janus kinase 2-dependent autophagy[J]. Sci Rep, 2017, 7: 40657. doi:10.1038/srep40657 |
| [15] |
Li Q, Dong Q T, Yang Y J, et al. AMPK-mediated cardioprotection of atorvastatin relates to the reduction of apoptosis and activation of autophagy in in-farcted rat hearts[J]. Am J Transl Res, 2016, 8(10): 4160-71. |
| [16] |
Wang Y H, Wang Q L, Zhang L, et al. Coptisine protects cardiomyocyte against hypoxia/reoxygenation induced damage via inhibition of autophagy[J]. Biochem Biophys Res Commun, 2017, 490(2): 231-8. doi:10.1016/j.bbrc.2017.06.027 |
| [17] |
Liu J B, Wu P, Wang Y L, et al. Ad-HGF improves the cardiac remodel-ing of rat following myocardial infarction by upregulating autophagy and necroptosis and inhibiting apoptosis[J]. Am J Transl Res, 2016, 8(11): 4605-27. |

