

2. 中南大学湘雅药学院药理学系,湖南 长沙 410078
2. Dept of Pharmacology, Xiangya School of Pharmaceutical Sciences, Central South University, Changsha 410078, China
糖尿病肾病(diabetic nephropathy,DN)是糖尿病常见严重的微血管并发症之一,但是有关其发病的机制尚未完全阐明。既往研究表明[1-2],炎症与DN肾脏损伤存在密切的关系。然而,有关DN肾脏损伤的细胞炎症分子调节机制以及信号传导尚不明确。因此,通过深入探究炎症的分子学机制对改善DN肾脏损伤尤为重要。
细胞焦亡(pyroptosis)是一种新的细胞炎症死亡方式,首次在沙门菌诱导的巨噬细胞死亡中被报道,后发现是由危险相关模式分子(damage-associated molecular patterns,DAMP)和/或病原相关模式分子(pathogen-associated molecular patterns,PAMP)介导caspase-1/4/5/11活化,促进IL-1β和IL-18释放,进而引起细胞强烈炎性反应的过程[3-4]。GSDMD是gasdermins(GSDMs)家族成员,为caspase-1和caspase-4/5/11的共同底物,是细胞焦亡的执行者。GSDMD由保守的两个结构域组成:C-末端抑制结构域(21 ku)和N-末端效应结构域(32 ku),其中N端具有细胞毒性,可与脂质组分结合,在细胞膜上形成孔洞,而全长结构不具有细胞毒性。GSDMD可通过caspase-1/4/5/11切割成C-端和N-端,其N-端在细胞膜上寡聚化形成非选择性孔道,释放成熟的IL-18和IL-1β,诱导细胞焦亡的发生[5-6]。其中caspase-1介导的细胞焦亡在目前研究最为广泛。caspase-1属于半胱氨酸蛋白酶家族,由半胱天冬酶募集结构域(CARD)和半胱天冬酶催化区域(CASc)组成无活性酶原。研究发现[7-8],高糖可促进caspase-1活化,上调IL-1β、IL-18表达,诱导肾小管上皮细胞和肾小球内皮细胞焦亡,进而导致DN肾脏损伤。但是,有关焦亡的执行者GSDMD表达变化以及是否参与DN未有相关报道。基于以往研究基础和不足,本实验拟通过细胞与动物实验相结合,探究GSDMD依赖性细胞焦亡在糖尿病肾病中作用及分子调控机制,即caspase-1介导GSDMD诱导的细胞焦亡途径。
1 材料 1.1 实验动物SPF级,♂,体质量(200±20)g的SD大鼠(中南大学湘雅医学院动物学部,合格证号:43004700029598)。
1.2 实验细胞人肾小管上皮细胞(human renal tubular epithelial cells,HK-2)购自美国模式菌种收集中心(ATCC)(货号:BJ0667)。
1.3 试剂与抗体DMEM低糖培养基(以色列BI公司);胎牛血清(Gibco公司);转染试剂(广州锐博公司);GSDMD siRNA(广州锐博公司);D-glucose溶液(G3285,美国Sigma公司);Caspase-1抗体(22915-1-AP,Proteintech公司);IL-1β抗体(GTX130021,美国Gene Tex公司);GSDMD抗体(sc-81868,美国Stanta Cruz公司);β-actin抗体(AF0003,江苏碧云天公司);一抗稀释液(江苏碧云天公司);二抗稀释液(江苏碧云天公司);HRP标记兔二抗(江苏碧云天公司);HRP标记鼠二抗(江苏碧云天公司);乳酸脱氢酶试剂盒(C0017,江苏碧云天公司);ELSIA试剂盒(北京中杉金桥生物技术公司);胰岛素检测试剂盒(上海酶联生物有限公司)。
1.4 主要仪器电子天平(常州万泰天平仪器公司);血糖仪(长沙三诺生物传感技术有限公司);多功能酶标仪(北京普朗医疗公司);荧光倒置显微镜(日本尼康公司);组织匀浆仪(武汉维塞尔生物科技有限公司);高速冷冻离心机(美国Beckman-Coulter公司);蛋白质免疫印迹装置(美国Bio-Rad公司);ChemiDoc XRS+成像系统(美国Bio-Rad公司);脱色摇床(江苏荣华有限公司);CO2细胞培养箱(美国Thermo公司)。
2 方法 2.1 糖尿病肾病大鼠模型建立选取SPF级,♂,体质量(200±20)g的SD大鼠40只。随机分成正常对照组(n=15)和糖尿病模型组(n=25),两组大鼠同等条件下饲养20周。通过单次大剂量腹腔注射STZ(60 mg·kg-1)构建糖尿病大鼠模型,并在注射STZ后连续3 d测定血糖。大鼠尾静脉取血,血糖值连续3 d高于16.7 mmol·L-1可认为糖尿病模型构建成功[9]。对于血糖值未达到或是连续3 d未高于16.7 mmol·L-1的大鼠视为造模失败,待大鼠血糖恢复正常水平后重新注射STZ。正常对照组大鼠腹腔注射等体积pH 4.4柠檬酸缓冲溶液。
2.2 大鼠相关指标检测① 体重:体重测定前禁食12 h,电子天平称量大鼠体质量;②血糖:大鼠尾尖取血,按照三诺生物公司血糖检测仪说明书测定血糖;③胰岛素:大鼠心脏取血,分离血浆,取上清并按照上海酶联生物公司大鼠胰岛素检测试剂盒测定胰岛素含量;④ 24 h尿蛋白:按照南京建成生物公司提供的试剂盒进行测定;⑤尿素氮:采用二乙酰肟法测定血清尿素氮含量;⑥相对肾脏重量:取大鼠左侧肾脏,电子天平称重,与体质量相比。
2.3 大鼠肾脏组织取材大鼠心脏取血完成,剪开左心耳并采用4%的多聚甲醛持续灌流直至心脏、肺呈现乳白色,随后完全打开大鼠胸腔,利用手术镊和手术剪刀剥离周围结蹄组织并剪下大鼠肾脏,采用生理盐水清洗后放置于液氮罐内保存。
2.4 苏木精-伊红(hematoxylin-eosin,HE)染色4%的多聚甲醛固定大鼠肾脏组织,石蜡切片经过烤片及脱蜡程序处理后,按以下步骤进行大鼠肾脏HE染色:①用Mayer′s苏木精浸染样本切片,脱色摇床轻摇约20 min左右将切片染色,随后蒸馏水冲洗数分钟;②染色后用0.5%盐酸酒精分化10 s;③ 75%酒精分色30 s;④蒸馏水冲洗20 min;⑤伊红酒精染色约90 s;⑥ 90%酒精脱水30 s;⑦无水乙醇脱水5 min×2次;⑧二甲苯透明5 min×3次;⑨中性树脂封片,在显微镜下观察染色结果并进行拍照保存。
2.5 细胞培养与处理HK-2细胞用含10% FBS的DMEM低糖培养基(5.5 mmol·L-1)并放置于5% CO2,37 ℃培养箱内培养,待细胞生长融合至90%时采用胰酶消化、传代、种板。待细胞生长密度达50%左右时进行同步化(0.1%的FBS)处理24 h。实验分为4组处理:①对照组(5.5 mmol·L-1 D-glucose培养48 h,Control);②高糖组(33 mmol·L-1 D-glucose处理48 h,HG);③ GSDMD无关片段+高糖组(转染GSDMD无关片段24 h后高糖处理48 h,NC+HG);④ GSDMD干扰片段+高糖组(转染GSDMD干扰片段24 h后高糖处理48 h,GSDMD siRNA+HG)。
2.6 酶联免疫吸附实验(enzyme linked immunosorbent assay,ELISA)按照北京中杉金桥生物公司提供IL-1β试剂盒说明书进行大鼠血清和HK-2细胞上清IL-1 β浓度测定。
2.7 乳酸脱氢酶(lactate dehydrogenase,LDH)检测按照江苏碧云天公司“C0017-乳酸脱氢酶细胞毒性检测试剂盒”进行LDH释放检测,操作步骤如下:① HK-2细胞总LDH释放:加入LDH释放剂,反复吹打数次混匀,置于细胞培养箱内孵育1 h,吸取各组细胞上清液120 μL;② LDH测定工作液配制:96孔板按照每孔加入20 μL乳酸溶液、20 μL稀释为1× INT溶液、20 μL酶溶液,总体积60 μL;③孵育:将LDH测定工作液加入吸取的各组细胞上清液中,避光孵育30 min;④计算:酶标仪设定490 nm波长处测定吸光度,根据吸光度值进行计算,LDH/%=(处理样品吸光度值-空白对照孔吸光度值)/(LDH全部释放量孔吸光度值-空白对照孔吸光度值)。
2.8 GSDMD siRNA转染将消化后HK-2细胞接种至6孔板内,采用完全培养基(含10% FBS)培养12~24 h后进行小干扰RNA转染。按照广州锐博公司基因siRNA转染说明书进行如下操作;①采用DEPC水稀释GSDMD siRNA和无关片段为20 μL储存液;②按照转染siRNA终浓度为5 nmol·L-1进行配置:将10× riboFECTTM CP Buffer稀释成1×(V2),后使用1× Buffer将储存液(V3)稀释并混匀;③ GSDMD siRNA转染液配置:加入锐博转染试剂Reagent(V4),混匀并置于细胞超净工作台内静置15~20 min,保证转染片段充分溶解,混合;④在细胞培养基(V1)内加入配置好的siRNA转染混合液,缓慢摇晃,混匀,并放置于细胞培养箱内培养。
2.9 Western blot① 蛋白提取:采用组织细胞裂解液对大鼠肾脏组织以及HK-2细胞进行裂解,BCA法蛋白浓度定量;②上样:按照每孔40 μg上样,电泳先将恒压80 V,后120 V恒压电泳;③湿转转膜:将PVDF膜放置甲醇槽内活化,根据Markrer指示和目的蛋白分子量大小进行切胶,252 mA恒流转膜;④封闭:采用6%的脱脂牛奶封闭caspase-1、GSDMD和IL-1β约1 h;⑤孵育一抗(caspase-1,GSDMD和IL-1β均为1 : 1 000稀释比例);⑥孵育二抗:加入对应HRP标记兔二抗(1 : 5 000)和鼠二抗(1 : 5 000),室温孵育2 h;⑦显影:采用Bio-Rad公司ChemiDoc XRS+成像系统进行显影,拍照并采用Image Lab软件进行灰度值分析。
2.10 统计学分析两组均数比较采用独立样本的Student′s t检验,多组均数比较采用ANOVA,统计分析采用SPSS 18.0软件,实验数据均采用x±s表示。
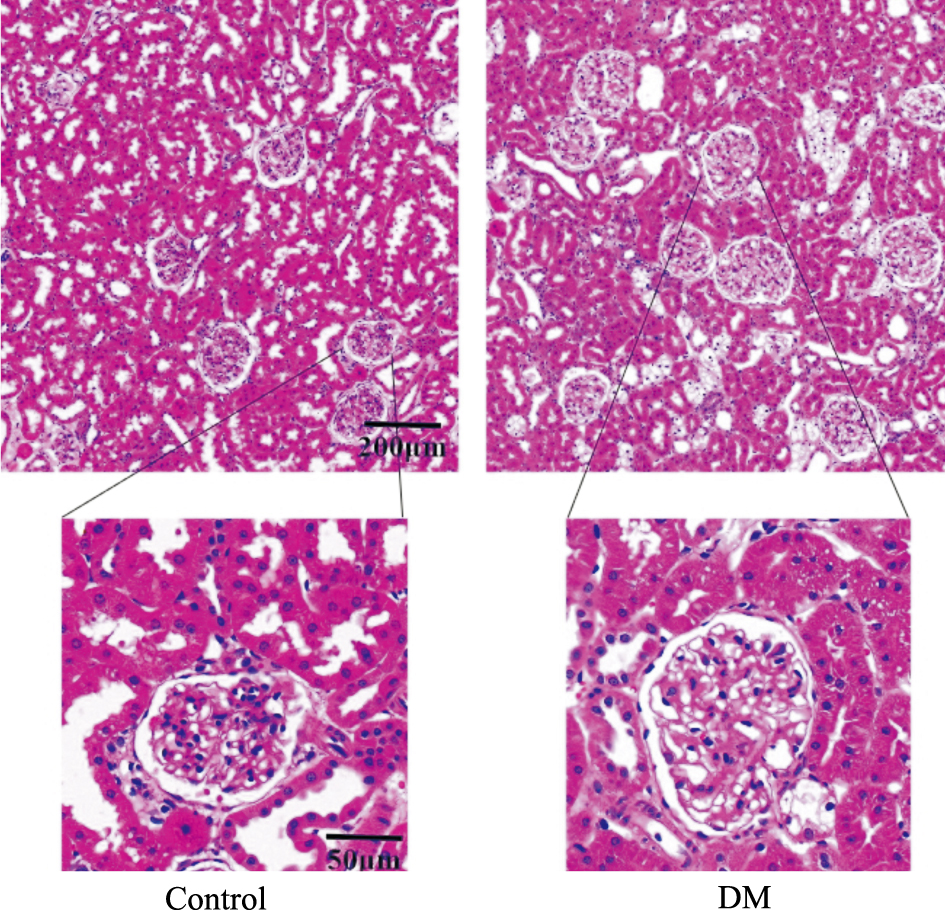
3 结果 3.1 糖尿病肾病大鼠模型建立为探究高血糖对DN肾脏损伤的影响,我们通过大鼠腹腔注射STZ造模20周构建DN模型。结果显示,糖尿病大鼠体重、血浆胰岛素含量明显降低(P < 0.01),血糖异常升高(P < 0.01)。24 h尿白蛋白含量、尿素氮浓度以及相对肾脏重量均显著增加(P < 0.01)(Tab 1)。HE染色糖尿病组大鼠肾小球明显增大,肾小囊狭窄,肾小球基底膜增厚,肾小球系膜增宽,且部分肾小管出现细胞肥大、空泡变性等(Fig 1)。以上结果表明,DN大鼠模型建立成功。
| Control | DM | |
| Weight/g | 678.52±48.40 | 237.83±25.80** |
| Blood glucose/mmol·L-1 | 4.52±0.37 | 27.53±2.72** |
| Plasma insulin/mU·L-1 | 17.06±1.53 | 6.73±1.00** |
| 24 h U-mAlb/mg·d-1 | 6.23±1.03 | 67.11±4.29** |
| BUN/mmol·L-1 | 7.04±1.38 | 22.87±4.09** |
| KW/BW/% | 3.45±1.02 | 6.89±0.69** |
| IL-1β/pg·mL-1 | 21.52±5.43 | 134.14±16.96** |
| **P < 0.01 vs control | ||
|
| Fig 1 Morphological characteristics of rat kidney HE staining was used to observe morphological characteristics of rat kidney |
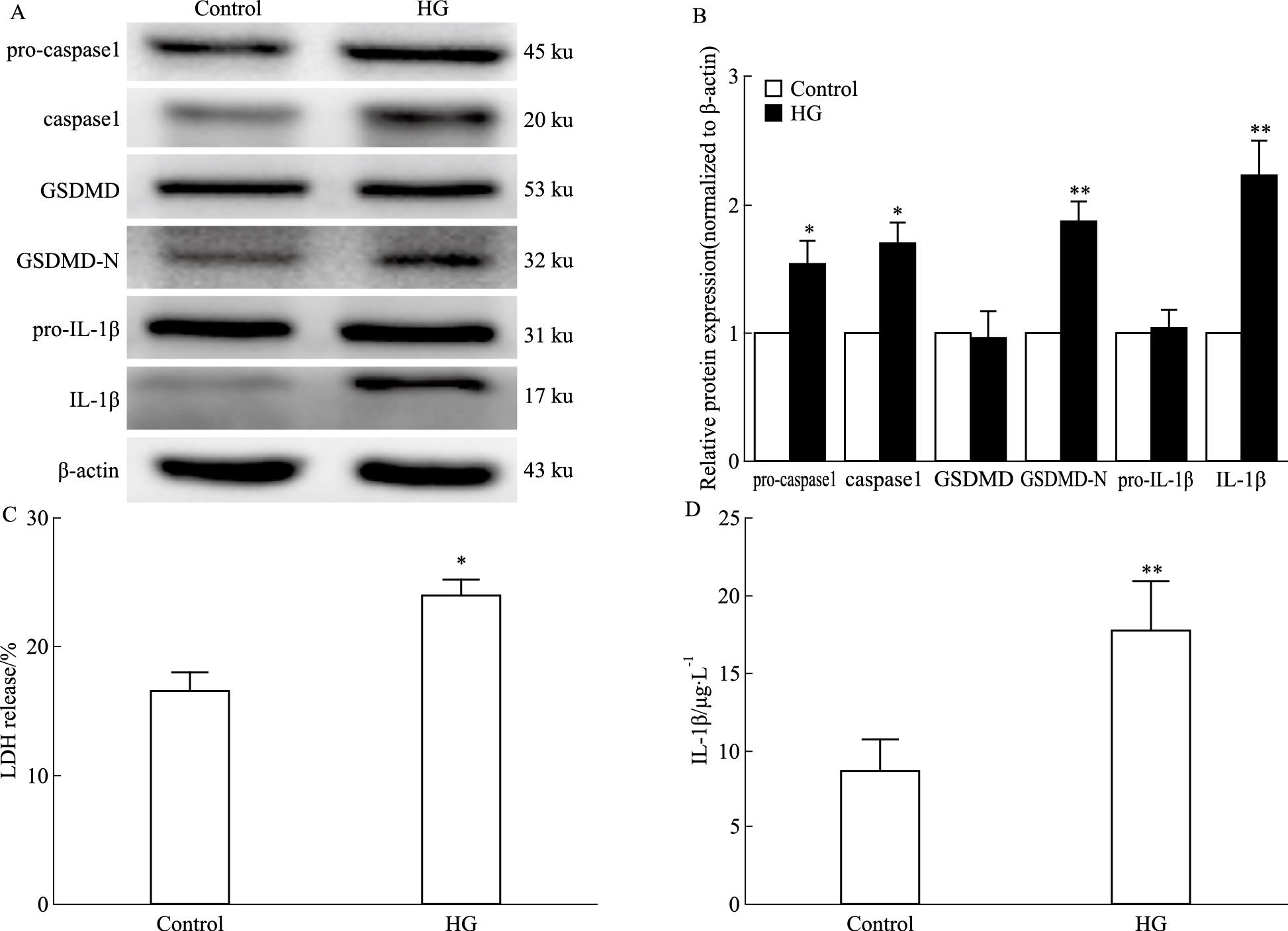
caspase-1通过促进GSDMD剪切形成细胞孔洞,诱导成熟性IL-1β通过GSDMD细胞孔释放至细胞外,进而介导细胞焦亡。为探究DN肾脏损伤时,是否涉及细胞焦亡。我们通过Western blot检测焦亡相关蛋白表达变化。结果显示,糖尿病大鼠肾脏组织GSDMD(P < 0.05),caspase-1、GSDMD-N和IL-1β表达均明显增加(P < 0.01),pro-caspase-1和pro-IL-1β表达无明显影响(Fig 2);ELISA检测糖尿病大鼠血浆IL-1β浓度明显增加(P < 0.01)(Tab 1)。

|
| Fig 2 Expression of pyroptosis-related proteins in rat kidney (x±s, n=6) A:Expression of pyroptosis-related proteins in rat kidney. B: Quantification of A.*P < 0.05, **P < 0.01 vs control |
在体动物实验证实,高血糖可诱导细胞焦亡,导致DN肾脏损伤。为进一步确证细胞焦亡对DN肾脏损伤的作用。我们通过体外细胞实验检测焦亡相关蛋白表达,LDH释放以及IL-1β浓度。结果显示,高糖可以促进pro-caspase-1、caspase-1、GSDMD-N和IL-1β表达(P < 0.05,P < 0.01),对GSDMD和pro-IL-1β表达无显著影响(Fig 3A)。高糖处理HK-2细胞可以增加LDH释放(P < 0.05)(Fig 3C)以及细胞上清IL-1β浓度(P < 0.01)(Fig 3D)。在体动物与细胞实验共同表明,高糖可以诱导GSDMD依赖性细胞焦亡,导致DN肾脏损伤。
|
| Fig 3 Effect of high glucose on HK-2 cell pyroptosis (x±s, n=3) A: Expression of pyroptosis-related proteins in HK-2. B: Quantification of B. C: The release of LDH. D: IL-1β concentration in cell supernatant.*P < 0.05, **P < 0.01 vs Control. |
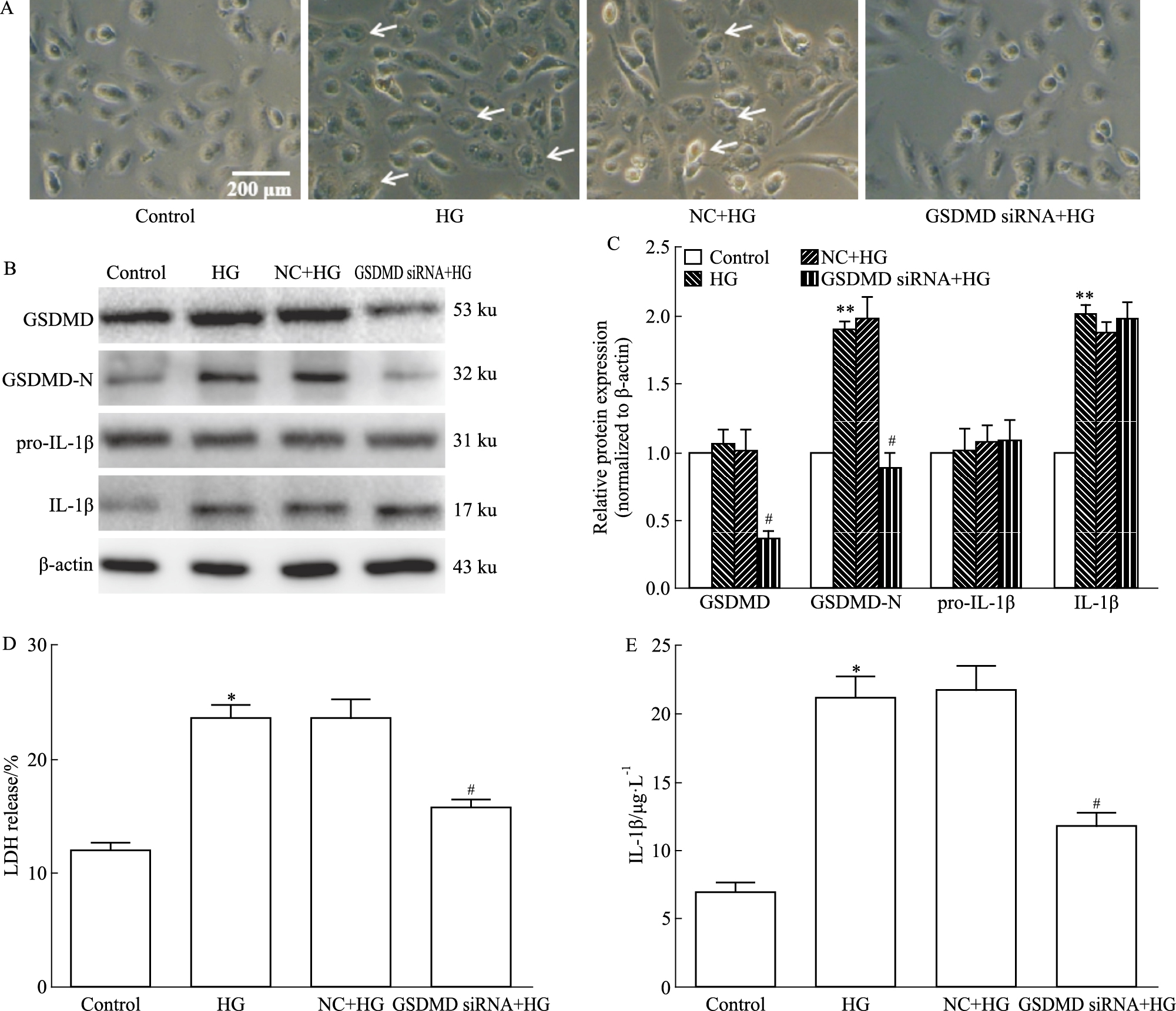
GSDMD为细胞焦亡的执行者。为确证GSDMD在高糖诱导HK-2细胞焦亡中的关键作用,我们通过转染GSDMD siRNA 24 h后,高糖处理HK-2细胞48 h。光学显微镜下观察细胞焦亡形态学变化并检测细胞上清LDH释放、IL-1β浓度以及IL-1β蛋白表达变化。结果显示,与Control组相比,HG组细胞体积显著增大,且细胞膜外围出现“灯泡样”水泡阴影,部分细胞出现细胞膜破裂。siRNA GSDMD后可以改善HG诱导的细胞焦亡形态学改变并能够显著抑制HG诱导的LDH以及IL-1β释放(P < 0.05) (Fig 4D、4E),降低GSDMD-N表达(P < 0.05)。但GSDMD siRNA对pro-IL-1β和IL-1β蛋白表达无明显影响(Fig 4B)。以上结果表明,siRNA GSDMD可以抑制细胞焦亡孔洞形成,降低高糖诱导的LDH以及IL-1β释放,缓解DN肾脏损伤。
|
| Fig 4 Effect of GSDMD siRNA on high glucose-induced pyroptosis in HK-2 cells (x±s, n=3) A: Morphological characteristics of pyroptosis. B: Effect of GSDMD siRNA on HG-induced GSDMD, GSDMD-N, pro-IL-1β and IL-1β expression. C: Quantification of B. D: Effect of GSDMD siRNA on HG-induced LDH release. E: Effect of GSDMD siRNA on HG-induced IL-1β release.*P < 0.05, **P < 0.01 vs control; #P < 0.05 vs HG. |
糖尿病为慢性代谢性疾病,易产生多种并发症,其中心血管并发症约占糖尿病患者死亡率的65%。DN是糖尿病微血管并发症之一,是糖尿病致残、致死的主要原因[10]。DN早期是以肾小球肥大,肾小球和肾小管基底膜增厚以及系膜区细胞外基质的合成增加为主要病理特征;后期肾小管和肾小球间质纤维化。临床上主要表现为肾小球滤过率降低,蛋白尿以及体液潴留等,最终导致终末期肾脏衰竭[11]。
炎症在DN发生发展中发挥重要作用。在DN大鼠模型中,IL-1β和IL-18表达明显增加[12]。外源性IL-1β处理肾小管上皮细胞,肾小球细胞可促进细胞间黏附分子-1、血管细胞黏附分子-1和E-选择素表达,增加血管通透性,损伤肾小球,导致蛋白尿的发生发展[13];IL-18亦可诱导IL-1β、TNF-ɑ和INF-γ表达增加,介导内皮细胞炎症和细胞凋亡[14]。但是有关DN肾脏损伤的炎症分子机制以及传导途径尚不完全清楚。细胞焦亡是继细胞凋亡和坏死后发现的一种新的细胞程序性、炎症性的死亡方式,参与糖尿病血管并发症的发生发展。研究发现,在糖尿病心肌病小鼠模型中,高糖可通过增加ROS产生,诱导GSDMD依赖的细胞焦亡,进而导致糖尿病心肌病心肌损伤[15];在DN大鼠模型中,焦亡相关蛋白(caspasae-1、IL-1β和IL-18)表达明显增加,抑制caspase-1可以降低肾小管细胞焦亡,缓解DN肾脏损伤[16]。以上研究提示:细胞焦亡在DN的发生发展中发挥重要作用,但是有关焦亡执行者GSDMD是否参与DN尚不完全清楚。因此,本实验通过大鼠腹腔注射STZ构建DN大鼠模型,探究GSDMD依赖性细胞焦亡在DN肾脏损伤中的分子作用机制。结果显示,糖尿病大鼠体重和血浆胰岛素均明显降低,血糖、24 h尿白蛋白含量、尿素氮浓度以及相对肾脏重量均显著增加。HE染色糖尿病大鼠肾脏出现明显肾小球、肾小管和间质病变。上述结果表明,DN大鼠模型建立成功。为探究细胞焦亡与DN肾脏损伤的关系,我们通过在体动物与体外细胞实验共同检测焦亡相关蛋白表达和指标变化。结果显示,高糖可以上调caspase-1、GSDMD-N和IL-1β表达,促进LDH和IL-1β释放,诱导肾小管上皮细胞焦亡。为进一步明确GSDMD对高糖诱导细胞焦亡的分子机制,我们通过转染GSDMD siRNA后高糖处理HK-2细胞48 h检测细胞焦亡相关指标变化。结果显示,与HG组相比,GSDMD siRNA可以明显降低LDH和IL-1β释放,改善细胞焦亡形态,但对IL-1β表达无明显影响。GSDMD作为焦亡的执行者,可诱导细胞孔的形成,进而促进LDH和IL-1β释放。既往研究证实,IL-1β和GSDMD均作为caspase-1的下游靶蛋白[5]。因此,通过干扰GSDMD对IL-1β表达无影响,但可以降低其释放。
综上所述,本研究通过探究GSDMD依赖性细胞焦亡在糖尿病肾病肾脏损伤中的作用机制。结果发现,高糖可诱导GSDMD依赖性肾小管上皮细胞焦亡,进而导致DN肾脏损伤。以上的研究结果进一步明确了细胞焦亡在DN肾脏损伤中的分子作用机制,为DN的防治提供新的理论基础。
| [1] |
曹思思, 颜苗, 张毕奎, 等. 以Nrf2为靶点防治肾脏疾病的研究进展[J]. 中国药理学通报, 2017, 33(3): 301-5. Cao S S, Yan M, Zhang B K, et al. Research on preventative role of Nrf2 in kidney diseases[J]. Chin Pharmacol Bull, 2017, 33(3): 301-5. doi:10.3969/j.issn.1001-1978.2017.03.002 |
| [2] |
Matoba K, Takeda Y, Nagai Y, et al. Unraveling the role of inflammation in the pathogenesis of diabetic kidney disease[J]. Int J Mol Sci, 2019, 20(14): pii:E3393. doi:10.3390/ijms20143393 |
| [3] |
Zhang Y, Chen X, Gueydan C, et al. Plasma membrane changes during programmed cell deaths[J]. Cell Res, 2018, 28(1): 9-21. |
| [4] |
杨祥, 开钧, 王志敏, 等. 细胞焦亡在慢性肝脏疾病中作用的研究进展[J]. 中国药理学通报, 2018, 34(12): 1638-42. Yang X, Kai J, Wang Z M, et al. Advances in role of pyroptosis for chronic liver disease[J]. Chin Pharmacol Bull, 2018, 34(12): 1638-42. doi:10.3969/j.issn.1001-1978.2018.12.003 |
| [5] |
He W T, Wan H, Hu L, et al. Gasdermin D is an executor of pyroptosis and required for interleukin-1β secretion[J]. Cell Res, 2015, 25(12): 1285-8. doi:10.1038/cr.2015.139 |
| [6] |
Jia C, Chen H, Zhang J, et al. Role of pyroptosis in cardiovascular diseases[J]. Int Immunopharmacol, 2019, 67: 311-8. doi:10.1016/j.intimp.2018.12.028 |
| [7] |
Li X, Zeng L, Cao C, et al. Long noncoding RNA MALAT1 regulates renal tubular epithelial pyroptosis by modulated miR-23c targeting of ELAVL1 in diabetic nephropathy[J]. Exp Cell Res, 2017, 350(2): 327-35. |
| [8] |
Gu J, Huang W, Zhang W, et al. Sodium butyrate alleviates high-glucose-induced renal glomerular endothelial cells damage via inhibiting pyroptosis[J]. Int Immunopharmacol, 2019, 75: 105832. doi:10.1016/j.intimp.2019.105832 |
| [9] |
梁海荣, 唐焕文, 罗皓, 等. 链脲佐菌素诱导糖尿病大鼠肾病模型的建立[J]. 应用预防医学, 2006(3): 133-5. Liang H R, Tang H W, Luo H, et al. Evaluation of experimental rat model of diabetic nephropathy induced by streptozotocin(STZ)[J]. Applied Prev Med, 2006(3): 133-5. doi:10.3969/j.issn.1673-758X.2006.03.003 |
| [10] |
Sankrityayan H, Oza MJ, Kulkarni YA, et al. ER stress response mediates diabetic microvascular complications[J]. Drug Discov Today, 2019, 24(12): 2247-57. doi:10.1016/j.drudis.2019.08.003 |
| [11] |
林子桐, 张超, 沈雪梅. 糖尿病肾病发病机制研究进展[J]. 中国药理学与毒理学杂志, 2014, 28(5): 765-73. Lin Z T, Zhang C, Shen X M. Advances in pathogenetic mechanisms of diabetic nephropathy[J]. Chin J Pharmacol Toxicol, 2014, 28(5): 765-73. doi:10.3867/j.issn.1000-3002.2014.05.013 |
| [12] |
Hameed I, Masoodi S R, Malik P A, et al. Genetic variations in key inflammatory cytokines exacerbates the risk of diabetic nephropathy by influencing the gene expression[J]. Gene, 2018, 661: 51-9. doi:10.1016/j.gene.2018.03.095 |
| [13] |
Lu X, Chen M, Shen J, et al. IL-1β functionally attenuates ABCG2 and PDZK1 expression in HK-2 cells partially through NF-κB activation[J]. Cell Biol Int, 2019, 43(3): 279-89. |
| [14] |
Yang Y, Zhang Z X, Lian D, et al. IL-37 inhibits IL-18-induced tubular epithelial cell expression of pro-inflammatory cytokines and renal ischemia-reperfusion injury[J]. Kidney Int, 2015, 87(2): 396-408. doi:10.1038/ki.2014.295 |
| [15] |
Wang X, Pan J, Liu H, et al. AIM2 gene silencing attenuates diabetic cardiomyopathy in type 2 diabetic rat model[J]. Life Sci, 2019, 221: 249-58. doi:10.1016/j.lfs.2019.02.035 |
| [16] |
Xie C, Wu W, Tang A, et al. lncRNA GAS5/miR-452-5p reduces oxidative stress and pyroptosis of high-glucose-stimulated renal tubular cells[J]. Diabetes Metab Syndr Obes, 2019, 12: 2609-17. doi:10.2147/DMSO.S228654 |

