

2. 浙江省新华医院(浙江中医药大学附属第二医院)消化内科,浙江 杭州 310005;
3. 杭州市拱墅区中西医结合医院消化(肿瘤)内科,浙江 杭州 310010
2. Dept of Gastroenterology, Zhejiang Xinhua Hospital(Second Affiliated Hospital of Zhejiang University of Traditional Chinese Medicine), Hangzhou 310005, China;
3. Dept of Gastroenterology(Oncology), Gongshu District Integrated Traditional Chinese and Western Medicine Hospital, Hangzhou 310010, China
姜黄素是从姜黄根茎中提取的具有广泛的生物学功能的活性化合物,如抗炎、抗氧化、抗凝血、抗高脂血症和抗动脉粥样硬化等[1]。近年来,姜黄素的潜在抗癌特性引起了人们的更多关注,其抗癌机制也得到了研究[2]。然而,姜黄素的抗癌机制尚未完全了解。最近的研究[3-4]表明,姜黄素通过调节表观遗传变化发挥其抗癌作用,其中包括组蛋白修饰的调节,DNA甲基转移酶的抑制等。另外,姜黄素在肿瘤中可以通过调节肿瘤相关miRNA的表达,从而发挥其抗癌作用[5]。miRNA是一类长度约19~25 nt小型非编码内源性RNA,其可通过与靶基因3′端非编码区(3′-untranslated region,3′-UTR)的碱基配对,并降解或翻译抑制转录产物,达到转录后调节靶基因表达而发挥生物学作用。miRNA作为最大类的基因调节因子之一,在人类细胞类型中含量丰富,并调节约60%的基因的表达。最近的研究表明miR-199b-5p在肾细胞癌[6]、三阴乳腺癌[7]和头颈癌[8]等肿瘤中作为肿瘤抑制因子发挥作用,但其表达和潜在的机制尚未完全阐明。在肝纤维化模型小鼠中,姜黄素能促进肝组织中miR-199b-5p表达[9]。因此,本实验观察姜黄素对结肠癌SW1116细胞增殖、迁移和侵袭中的作用,并分析姜黄素与miR-199b-5p的表达关系。
1 材料与方法 1.1 材料 1.1.1 试剂姜黄素(#78246)(Sigma公司,美国)胎牛血清(#SH30396.03)(HyClone公司,美国);L-谷氨酰胺(#A37736IN)、青霉素/链霉素(#10378016)和RPMI 1640培养基(#A1049101)(Gibco公司,美国);Lipofectamine 2000(#11668030)(Invitrogen公司,美国);5-乙炔基-2′ -脱氧尿苷(5-Ethynyl-2′-deoxyuridine,EDU)荧光染色细胞增殖试剂盒(#C10310-1)和SYBR Green RT-qPCR试剂盒(#C10220-1)(广州锐博生物生物科技有限公司);RNAiso Plus试剂盒(#9108)和PrimeScript RT试剂盒(#RR014A)(TaKaRa公司,日本);pRL-TK质粒(#E2241)(Promega Corporation公司,美国);抗P21活化蛋白激酶4(p21 activated protein kinase 4,PAK4)(#62690)、抗(丝裂原细胞外信号调节激酶(mitogen extracellular signal-regulated kinase,MEK)(#9126)、抗磷酸化MEK(phosphorylated MEK,p-MEK)(#9128)、抗细胞外调节蛋白激酶(extracellular regulated protein kinases,ERK)(#4696)、抗磷酸化ERK(phosphorylated ERK,p-ERK)(#4376)和抗β-actin抗体(#12262)(Cell Signaling Technology公司,美国)。
1.1.2 仪器蛋白电泳-电转仪(Bio-Rad公司,美国);IX73型荧光显微镜和CX41型光学显微镜(Olympus公司,日本);LightCycler 480荧光PCR系统(Roche公司,瑞士);Dual-GloⓇ荧光素酶测定系统(Promega Corporation公司,美国)。
1.2 细胞培养人结肠癌SW1116细胞购自中国科学院上海细胞库,细胞接种在含有10%胎牛血清、2 mmol·L-1 L-谷氨酰胺、100 kU·L-1青霉素和100 mg·L-1链霉素的RPMI 1640培养基中,并放置在37 ℃、含5% CO2和饱和湿度的培养箱中培养。每隔1 d对细胞换液1次,每周按照1 : 3传代1次。收集对数期细胞用于后续研究。
1.3 细胞转染miR-199b-5p模拟物(miR-199b-5p mimic)、miR-199b-5p抑制剂(miR-199b-5p inhibitor)和阴性对照(miR-NC)由广州锐博生物生物科技有限公司合成,并用Lipofectamine 2000在SW1116细胞中转染,转染试剂终浓度为50 nmol·L-1。6 h后更换含10%胎牛血清的全培养基并继续培养48 h。收集已转染的细胞,通过RT-qPCR鉴定转染效率后,用于后续研究。
1.4 细胞处理根据指定实验要求和既往文献[2]参考,采用0、5、10、15和20 μmol·L-1的姜黄素处理SW1116细胞24 h;或采用20 μmol·L-1的姜黄素处理SW1116细胞0、6、12、24和48 h;或采用20 μmol·L-1的姜黄素处理已转染miR-199b-5p inhibitor的SW1116细胞24 h。
1.5 EDU染色取对数期SW1116细胞按照5×104细胞/孔的密度接种至24孔板。细胞用无血清培养基同步化处理后,按照“1.4细胞处理”方法处理细胞后,根据EDU荧光染色细胞增殖试剂盒说明书步骤,向细胞中加入10 μmol·L-1 EdU试剂,并孵育2 h后,PBS洗掉未渗入DNA的EdU并加入4%多聚甲醛固定细胞30 min。PBS洗除固定液,加入Apollo染液室温避光孵育30 min,PBS洗除染液并用DAPI染核5 min。IX73型荧光显微镜随机获取5个视野的荧光图像,并采用Image J软件对EDU阳性细胞计数。
1.6 Transwell检测通过Transwell培养系统检测SW1116细胞的迁移与侵袭能力。按照“1.4细胞处理”方法处理细胞后,收集细胞并制成1.5×108细胞·L-1密度的细胞悬液,取100 μL细胞悬液加入Transwell的顶室中,其中检测侵袭使用涂有基质胶(2.5 g·L-1)的transwell膜,检测迁移使用不含基质胶的transwell膜。将含有10%胎牛血清的RPMI 1640培养基作为化学引诱物添加到Transwell的底室中。在细胞培养箱中孵育12 h后,擦除上Transwell膜表面细胞,用甲醇固定转移至Transwell膜下表面的细胞,用结晶紫染细胞30 min,并用CX41型光学显微镜随机获取5个视野的细胞图像,并采用Image J软件对细胞进行计数。
1.7 RT-qPCR按照“1.4细胞处理”方法处理细胞后,收集细胞并使用RNAiso Plus试剂盒提取总RNA,然后使用PrimeScript RT试剂盒进行cDNA合成。取cDNA和引物并根据SYBR Green RT-qPCR试剂盒步骤在LightCycler 480荧光PCR系统进行RT-qPCR扩增。反应条件为:95 ℃预变性15 min,然后进行40个循环(95 ℃变性10 s,55 ℃退火20 s,72 ℃延伸20 s)。引物序列为:miR-199b-5p:正向: 5′-CAGCCCAGTGTTTAGACTATC-3′,反向:5′-CAGTGCAGGGTCCGAGGT-3′;U6:正向: 5′-CGAA CGATACAGAGAAGATTAGC-3′,反向: 5′-TGGAACG CTTCACGAATTTGCG-3′。以U6为miR-199b-5p的内部参照,采用2-ΔΔCq法计算miR-199b-5p的相对表达量。
1.8 双荧光素酶报告基因测定根据TargetScan(http://www.targetscan.org)软件显示PAK4-3′UTR具有miR-199b-5p高度保守的结合位点。荧光素酶报告质粒、pRL-PAK4-3′UTR野生型(WT)和pRL-PAK4-3′UTR突变体(MUT)质粒由广州锐博生物生物科技有限公司合成并鉴定。荧光素酶报告基因实验中,SW1116细胞使用Lipofectamine 2000辅助共转染pRL-PAK4-3′UTR WT或pRL-PAK4-3′UTR MUT,miR-199b-5p mimic或NC。以pRL-TK质粒作为对照。转染48 h后,收获细胞并裂解,使用Dual-GloⓇ荧光素酶测定系统分析荧光素酶活性,并用萤火虫荧光素酶活性进行归一化。
1.9 蛋白质免疫印迹实验按照“1.4细胞处理”方法处理细胞后,收集细胞。将收集的在冰上用RIPA裂解缓冲液10 mmol·L-1 Tris(pH 8.0),150 mmol·L-1 NaCl,1% Nonidet P-40,0.1% SDS和0.5%脱氧胆酸盐]裂解30 min。在4 ℃下以14 000×g离心30 min后,收集上清液(蛋白)。蛋白经BCA法定量后,根据标准方案,每孔取等量的蛋白进行SDS-聚丙烯酰胺凝胶电泳。电泳后,蛋白经电转至PVDF膜,用含有5%脱脂奶粉的TBST溶液封闭后,室温孵育1 : 1 000稀释的一抗(抗PAK4、抗MEK、抗p-MEK、抗ERK、抗p-ERK和抗β-actin)2 h,洗涤膜后,室温孵育1 : 4 000稀释的二抗1 h。在显影室采用ECL化学发光法显影。采用Image J软件分析目的条带灰度值,并用β-actin灰度值进行归一化。
1.10 统计学分析结果表示为x±s。多组数据的比较采用单因素方差分析。
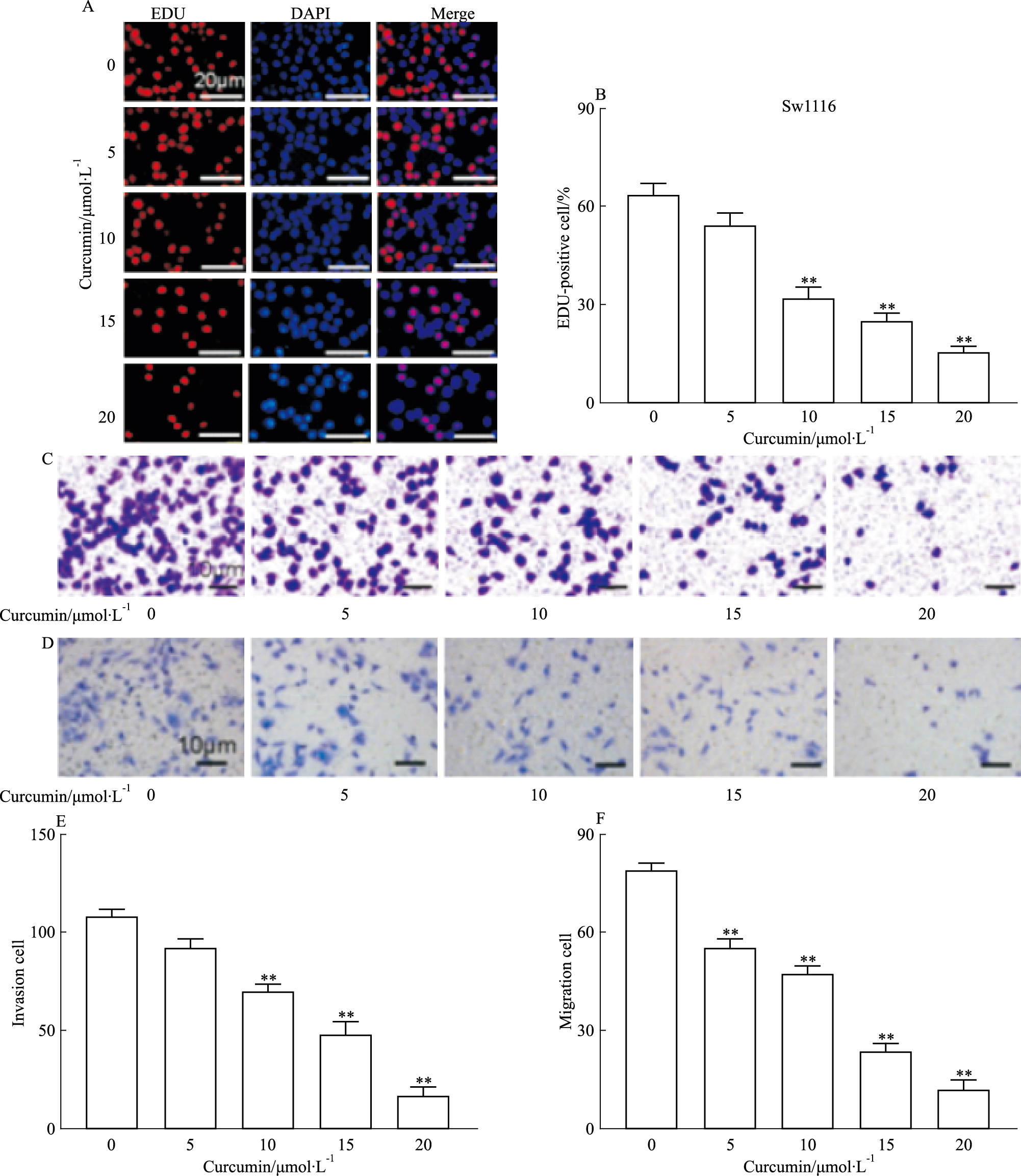
2 结果 2.1 姜黄素对SW1116细胞增殖、迁移和侵袭的影响EDU染色结果(Fig 1A和1B)显示,随着姜黄素浓度增加,EDU阳性细胞数逐渐降低,提示姜黄素浓度依赖性抑制SW1116细胞增殖。同时,transwell结果显示,随着姜黄素浓度的增加,侵袭细胞数(Fig 1C和1E)和迁移细胞数(Fig 1D和1F)均逐渐降低,提示姜黄素浓度依赖性抑制SW1116细胞的迁移与侵袭。
|
| Fig 1 Proliferation, migration and invasion in SW1116 cells inhibited by curcumin in a concentration-dependent manner A: Representative cell fluorescence images of EDU/DAPI double staining; B: Statistical results of EDU-positive cell count; C: Representative transwell images of cell invasion; D: Representative transwell images of cell migration; E: Statistical results of invasive cell count; F: Statistical results of migratory cell count(x±s, n=4).**P < 0.01 vs Control group |
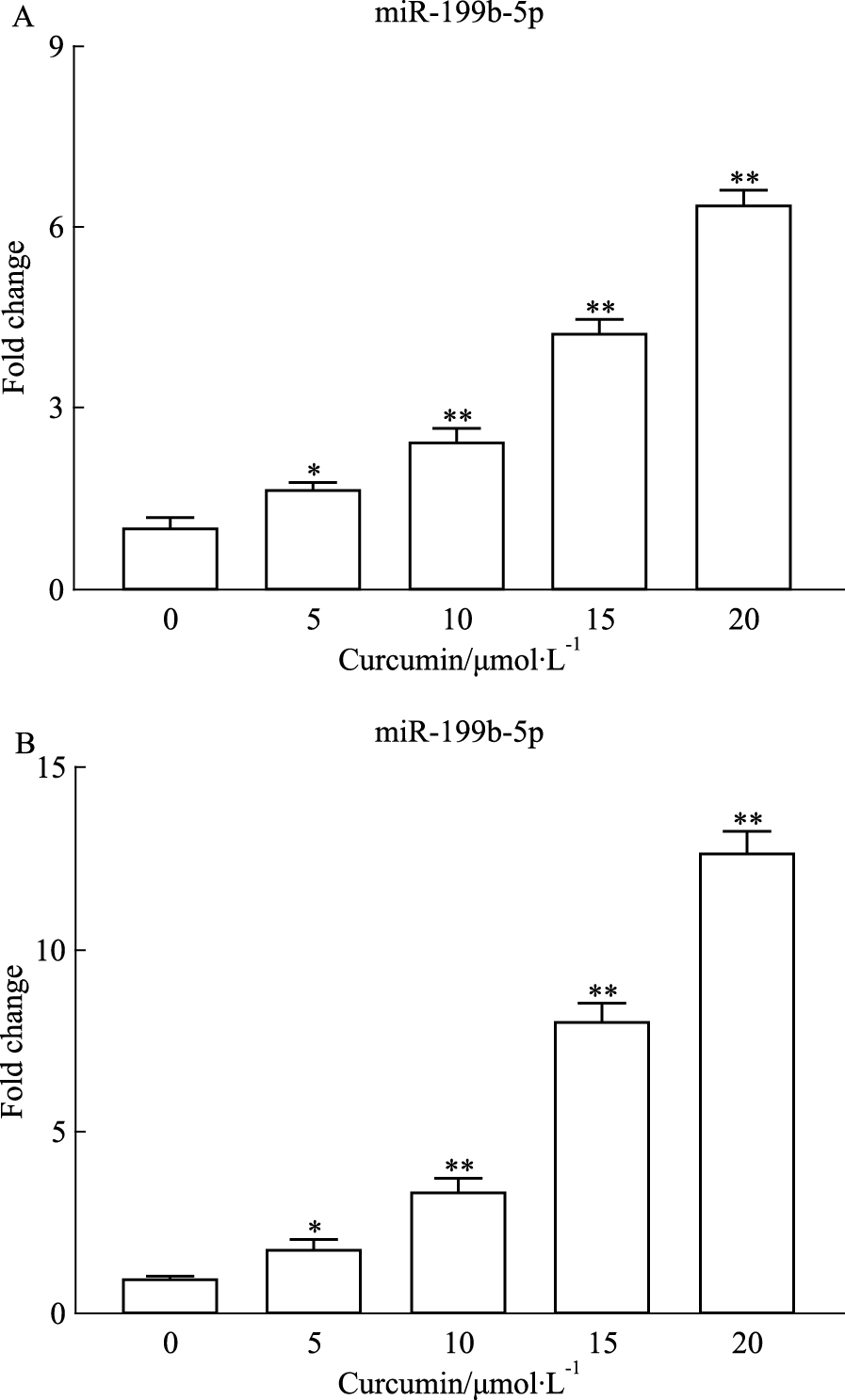
为了检测姜黄素对SW1116细胞中miR-199b-5p的影响,本实验使用不同浓度梯度和不同时间梯度的姜黄素处理细胞,并采用RT-qPCR检测miR-199b-5p的表达。Fig 2A显示,随着姜黄素浓度增加,miR-199b-5p表达逐渐增加,提示姜黄素浓度依赖性促进SW1116细胞中miR-199b-5p表达。Fig 2B显示,随着处理时间增加,miR-199b-5p表达逐渐增加,提示姜黄素时间依赖性促进SW1116细胞中miR-199b-5p表达。
|
| Fig 2 Expression of miR-199b-5p in SW1116 cells promotedby curcumin in a concentration-and time-dependent manner A: After treatment of SW1116 cells with 0~20 μmol·L-1 curcumin for 24 h, the expression of miR-199b-5p was detected by RT-qPCR; B: After treatment of SW1116 cells with 20 μmol·L-1 curcumin for 0~48 h, the expression of miR-199b-5p was detected by RT-qPCR(x±s, n=4).*P < 0.05, **P < 0.01 vs Control group |
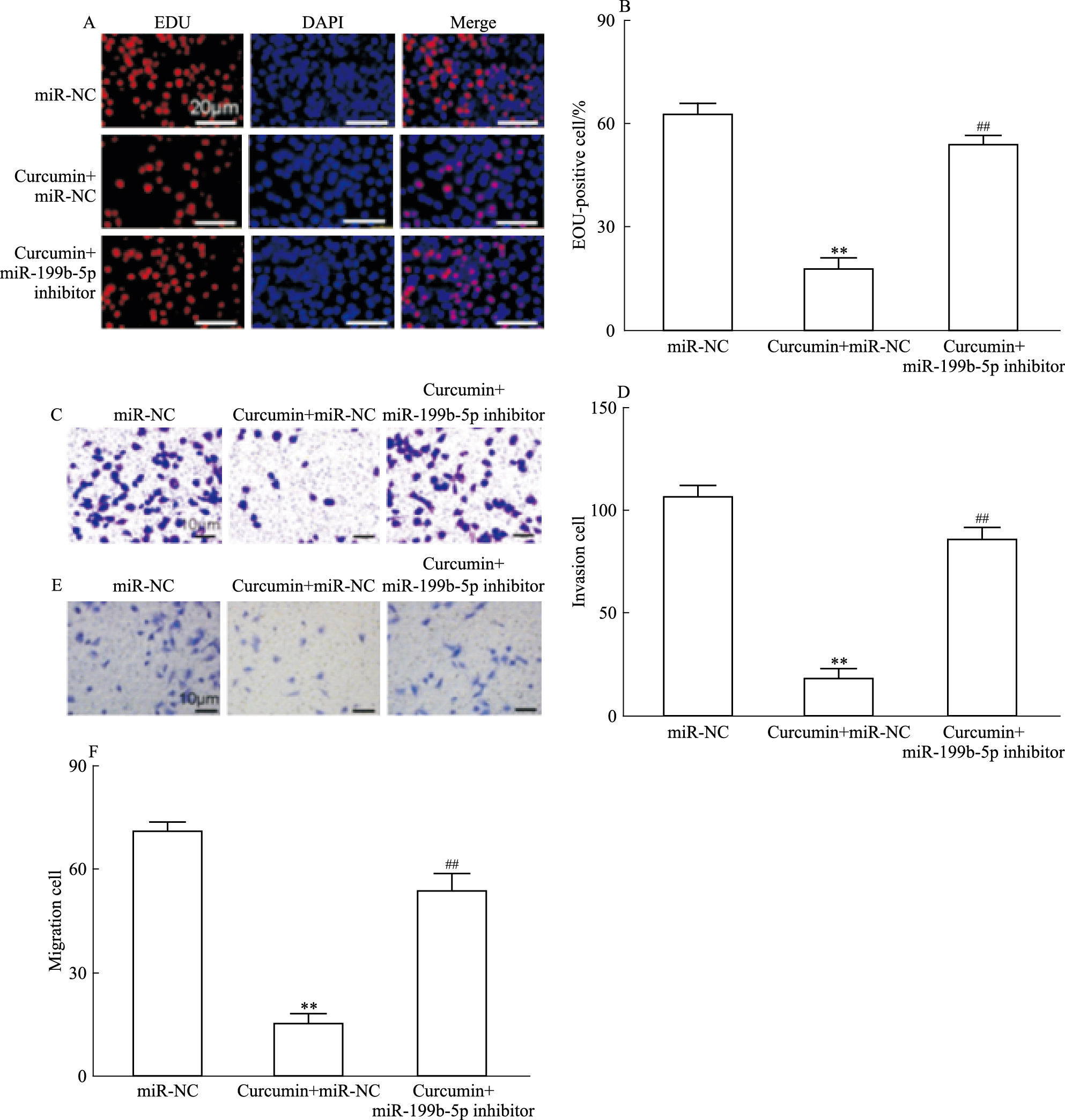
本研究进一步研究了敲减miR-199b-5p对姜黄素抑制SW1116细胞增殖和侵袭作用的影响。本研究采用20 μmol·L-1姜黄素分别处理SW1116细胞、已转染miR-199b-5p inhibitor或miR-NC的SW1116细胞24 h后,采用EDU染色和Transwell分析法分别检测细胞增殖、迁移与侵袭。EDU染色(Fig 3A和3B)结果显示,与姜黄素+miR-NC组比较,姜黄素+miR-199b-5p inhibitor组EdU阳性细胞明显增多(P < 0.01)。Transwell结果显示,与姜黄素+miR-NC组比较,姜黄素+miR-199b-5p inhibitor组侵袭细胞数(Fig 3C和3D)和迁移细胞数(Fig 3E和3F)均明显增加(P < 0.01)。提示敲减miR-199b-5p能部分逆转姜黄素对SW1116细胞增殖、迁移和侵袭的抑制作用。
|
| Fig 3 Inhibition of curcumin(20 μmol·L-1) on proliferation, migration and invasion in SW1116 cells partially reversed by knockdown of miR-199b-5p (x±s, n=4) A: Representative cell fluorescence images of EDU/DAPI double staining; B: Statistical results of EDU-positive cell count; C: Representative transwell images of cell invasion; D: Statistical results of invasive cell count; E: Representative transwell images of cell migration; F: Statistical results of migratory cell count, **P < 0.01 vs Control group; ##P < 0.01 vs Curcumin+miR-NC group |
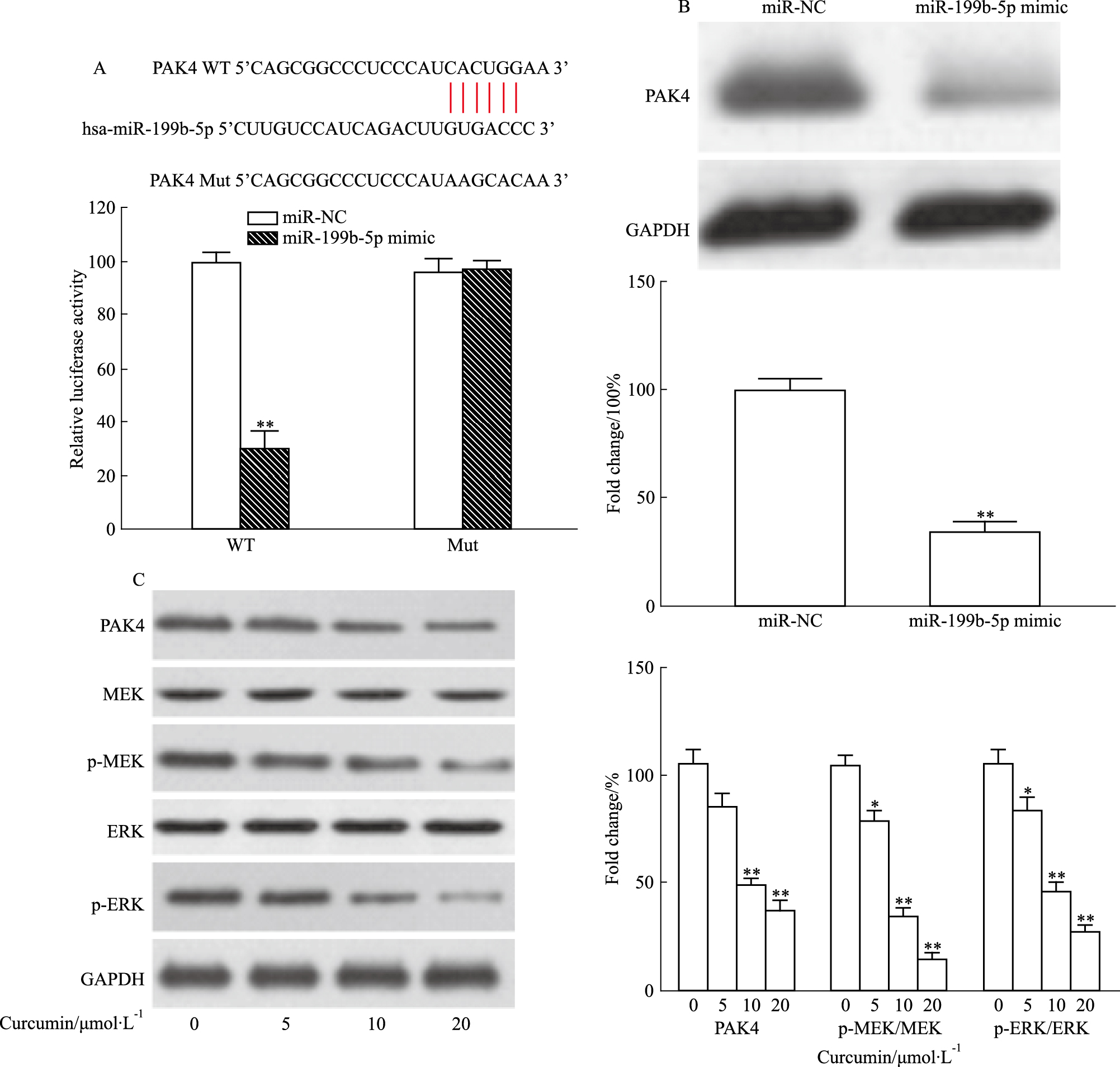
Target Scan(http://www.targetscan.org/)预测结果PAK4-3′UTR具有miR-199b-5p高度保守的结合位点(Fig 4A)。为了证实PAK4是miR-199b-5p的真正分子靶标,将pRL-PAK4-3′UTR WT或pRL-PAK4-3′UTR MUT,miR-199b-5p mimic或NC共转至SW1116细胞,双荧光素酶报告基因结果显示,miR-199b-5p显著降低了SW1116细胞中野生型PAK4的荧光素酶活性(P < 0.01),但突变体PAK4未观察到该结果(Fig 4A)。通过Western blot印迹进一步研究已转染miR-199b-5p mimic或miR-NC细胞中的PAK4蛋白表达,如Fig 4B所示,与已转染miR-NC的细胞相比,转染miR-199b-5p mimic的细胞中PAK4的蛋白表达水平明显下调(P < 0.01)。如Fig 4C所示,随着姜黄素浓度的增高,SW1116细胞中PAK4、p-MEK/MEK和p-ERK/ERK的表达均明显下降,浓度为20 μmol·L-1时下降最为明显(P < 0.01)。
|
| Fig 4 PAK4, direct target gene of miR-199b-5p and molecular mechanismof curcumin inhibiting proliferation, migration and invasion in SW1116 cells A: The binding site of PAK4-3′UTR and miR-199b-5p(upper panel) and the results of double luciferase reporter assay(bottom panel)(x±s, n=3), **P < 0.01 vs WT+miR-NC group; B: PAK4 protein expression in SW1116 cells was detected by Western blot after transfection with miR-199b-5p mimic; (x±s, n=3), **P < 0.01 vs miR-NC group; C: After treated with curcumin at different concentrations for 24 h, the expression levels of PAK4, p-MEK/MEK and p-ERK/ERK in SW1116 cells were detected by Western blot(x±s, n=4), *P < 0.05, **P < 0.01 vs Control group |
姜黄素在血液系统肿瘤、呼吸道和消化道肿瘤、泌尿生殖系统肿瘤和妇科肿瘤等多种肿瘤中发挥抗肿瘤作用[2, 6-8]。但其抑制肿瘤的具体机制尚不完全清楚。基于姜黄素的实际治疗应用的未来发展而言,对其机制细节的的研究是必不可少环节。本研究观察到,姜黄素在抑制结肠癌SW1116细胞增殖、迁移和侵袭的过程中伴随着miR-199b-5p表达上调,而通过敲减miR-199b-5p后,姜黄素的抑制作用则无法体现,这说明姜黄素是通过miR-199b-5p调控了SW1116细胞的增殖、迁移和侵袭。
随后本研究对miR-199b-5p下游抗肿瘤机制进行了探索。首先,本研究证明了PAK4是miR-199b-5p的靶基因,且过表达miR-199b-5p抑制PAK4表达。已有研究表明[10-11],PAK4是结肠癌细胞生存、生长与迁移的必须基因,过表达PAK4能促进结肠癌细胞生长与转移,而敲减PAK4抑制结肠癌细胞生长与转移。MEK/ERK通路在PAK4诱导的肿瘤细胞增殖与侵袭调控中起重要作用,下调PAK4/MEK/ERK信号通路能抑制包括结肠癌、胰腺癌和胃癌等肿瘤细胞增殖、迁移与侵袭[11-13]。我们的结果显示,miR-199b-5p通过下调PAK4/MEK/ERK信号通路抑制结肠癌细胞增殖、迁移与侵袭。提示姜黄素通过miR-199b-5p/PAK4/MEK/ERK轴抑制结肠癌细胞的增殖、迁移与侵袭。
先前的研究表明[14],miR-199b-3p在结肠癌细胞中高表达,并且在结肠癌中作为致癌基因起作用。虽然miR-199b-5p和miR-199b-3p是miR-199b的两种天然形式,但它们不仅具有不同的miRNA序列,而且还有不同的目标基因。此外,已有研究表明[15],在结肠癌SW480细胞过表达miR-199b-5p抑制细胞增殖。本研究也表明miR-199b-5p通过靶向PAK4在结肠癌中起抗癌基因的作用。这些发现表明miR-199b-5p和miR-199b-3p在结肠癌中起着相反的作用,可能是通过靶向不同的下游基因造成的。然而,其在结肠癌中相反作用的确切机制仍需进一步研究。
总之,我们的结果显示姜黄素通过miR-199b-5p下调PAK4/MEK/ERK信号传导途径抑制结肠癌细胞增殖、迁移与侵袭。另外,miR-199b-5p/PAK4/MEK/ERK轴参与调节结肠癌细胞增殖、迁移与侵袭这一项发现完善了对结肠癌发病机制的理解,并提供了结肠癌新的生物标志物和潜在治疗靶点。
| [1] |
Tsuda T. Curcumin as a functional food-derived factor: degradation products, metabolites, bioactivity, and future perspectives[J]. Food Funct, 2018, 9(2): 705-14. doi:10.1039/C7FO01242J |
| [2] |
Kunnumakkara A B, Anand P, Aggarwal B B. Curcumin inhibits proliferation, invasion, angiogenesis and metastasis of different cancers through interaction with multiple cell signaling proteins[J]. Cancer Lett, 2008, 269(2): 199-225. doi:10.1016/j.canlet.2008.03.009 |
| [3] |
Boyanapalli S S, Kong A T. Curcumin, the King of spices: epigenetic regulatory mechanisms in the prevention of cancer, neurological, and inflammatory diseases[J]. Curr Pharmacol Rep, 2015, 1(2): 129-39. doi:10.1007/s40495-015-0018-x |
| [4] |
任海玉, 孙剑经, 李多, 等. 姜黄素通过Wnt2/β-catenin通路逆转食管癌Eca-109/VCR细胞多药耐药性研究[J]. 中国药理学通报, 2018, 34(10): 1455-60. Ren H Y, Sun J J, Li D, et al. Curcumin reversed multi-drug resistance of esophageal carcinoma in Eca-109/VCR cell line through Wnt2/β-catenin pathway[J]. Chin Pharmacol Bull, 2018, 34(10): 1455-60. doi:10.3969/j.issn.1001-1978.2018.10.025 |
| [5] |
Mirzaei H, Masoudifar A, Sahebkar A, et al. MicroRNA:A novel target of curcumin in cancer therapy[J]. J Cell Physiol, 2018, 233(4): 3004-15. doi:10.1002/jcp.26055 |
| [6] |
Lai Y, Quan J, Lin C, et al. miR-199b-5p serves as a tumor suppressor in renal cell carcinoma[J]. Exp Ther Med, 2018, 16(1): 436-44. |
| [7] |
Wu A, Chen Y, Liu Y, et al. miR-199b-5p inhibits triple negative breast cancer cell proliferation, migration and invasion by targeting DDR1[J]. Oncol Lett, 2018, 16(4): 4889-96. |
| [8] |
王茜, 李光辉, 郭嘉, 等. miR-199b-5p在头颈癌细胞中的表达及对细胞增殖和侵袭能力的影响[J]. 上海口腔医学, 2018, 27(3): 265-9. Wang X, Li G H, Guo J, et al. miR-199b-5p inhibits proliferation and invasion of head and neck cancer cells[J]. Shanghai J Stomatol, 2018, 27(3): 265-9. |
| [9] |
Hassan Z K, Al-Olayan E M. Curcumin reorganizes miRNA expression in a mouse model of liver fibrosis[J]. Asian Pac J Cancer Prev, 2012, 13(11): 5405-8. doi:10.7314/APJCP.2012.13.11.5405 |
| [10] |
Zhang X, Zhang X, Li Y, et al. PAK4 regulates G6PD activity by p53 degradation involving colon cancer cell growth[J]. Cell Death Dis, 2017, 8(5): e2820. doi:10.1038/cddis.2017.85 |
| [11] |
Tabusa H, Brooks T, Massey A J. Knockdown of PAK4 or PAK1 inhibits the proliferation of mutant KRAS colon cancer cells independently of RAF/MEK/ERK and PI3K/AKT signaling[J]. Mol Cancer Res, 2013, 11(2): 109-21. doi:10.1158/1541-7786.MCR-12-0466 |
| [12] |
Tyagi N, Bhardwaj A, Singh A P, et al. p-21 activated kinase 4 promotes proliferation and survival of pancreatic cancer cellsthrough AKT- and ERK-dependent activation of NF-κB pathway[J]. Oncotarget, 2014, 5(18): 8778-89. doi:10.18632/oncotarget.2398 |
| [13] |
Zeng B, Shi W, Tan G. MiR-199a/b-3p inhibits gastric cancer cell proliferation via down-regulating PAK4/MEK/ERK signaling pathway[J]. BMC Cancer, 2018, 18(1): 34. doi:10.1186/s12885-017-3949-2 |
| [14] |
凌斌勋, 阿斯木古丽·阿不都克里木, 蔡云. 微小RNA-199b-3p靶向调控SOX6的表达及其对结肠癌细胞SW620增殖和凋亡的影响[J]. 临床肿瘤学杂志, 2017, 22(6): 505-10. Ling B X, Asimuguli A, Cai Y. Effects of miRNA-199b-3p on the targeted regulation of SOX6 and proliferation and apoptosis of colon cancer cell line SW620[J]. J Chin Clin Oncol, 2017, 22(6): 505-10. doi:10.3969/j.issn.1009-0460.2017.06.006 |
| [15] |
薛淑慧, 石萌. MiR-100-5p和miR-199b-5p靶向结合mTOR诱导结肠癌细胞自噬[J]. 贵州医科大学学报, 2018, 43(2): 179-83. Xue S H, Shi M. Autophagy of colon cancer cells by targeting miR-100-5p and miR-199b-5p combined with mTOR[J]. J Guizhou Med Univ, 2018, 43(2): 179-83. |

