

陈志武(1963-),男,博士,教授,研究方向:心脑血管药理学,博士生导师,通讯作者,E-mail:chpharmzw@163.com。
硫化氢(H2S)是继一氧化氮(nitric oxide, NO)和一氧化碳(carbon monoxide, CO)后在体内发现的第3种气体信号分子[1-2]。内源性H2S与NO一样,也可由血管内皮产生和释放,可调节着血管张力和器官血流量。RhoA-ROCK信号通路参与了许多血管床中平滑肌细胞的收缩,在血管张力调节中发挥重要的作用,是心脑血管系统的新靶点[3]。在RhoA-ROCK信号通路中,RhoA系一种小分子鸟苷酸结合蛋白,是鉴定出的Rho家族的第一个成员。Rho相关的卷曲螺旋激酶(Rho-kinase, ROCK)为丝氨酸/苏氨酸蛋白激酶家族的成员,是RhoA最重要的下游信号分子之一。RhoA被激活后可从细胞质中转位至细胞膜上,再激活其下游分子ROCK,从而参与包括细胞形状、运动、细胞收缩、增殖、血管平滑肌张力及炎症[4-5]等许多重要细胞功能的调节。ROCK有两种亚型,即ROCK1和ROCK2。我们以前研究表明,H2S可通过抑制RhoA-ROCK信号通路诱导脑血管舒张[6]。但尚不明确其抑制RhoA-ROCK信号通路的确切效应分子,即H2S是抑制RhoA,还是抑制ROCK及对其亚型有无选择性。因此,本课题利用RhoA抑制剂及siRNA干扰技术敲低ROCK表达,研究了H2S舒张大鼠脑血管作用与RhoA-ROCK信号通路中具体效应分子的关系进行了研究。
1 材料与方法 1.1 药品与试剂ROCK1-siRNA(guide:UUGCUAGAAGCUUCAUAG)及其阴性siRNA、ROCK2-siRNA(guide:GCAGCAAUGGUAAGCGUAA)及其阴性siRNA均在广州锐博生物科技有限公司购买(批号:R0824);EntransterTM in vivo-RNA,购买自北京英格恩生物科技有限公司(批号:No.18668111150825-1);C3,购买自美国Apexbio公司(批号:B4897),ROCK1(批号:ab45171)和ROCK2一抗(批号:125025),购自英国abcam公司;乙酰胆碱(acetycholine, ACh),购自Sigma公司(批号:BCBK5708V); NaHS,购自美国Sigma公司,实验前将其溶解在蒸馏水中并避光保存(批号:#SHBF1746V);生理盐溶液(physiological saline solution, PSS)成分(mmol·L-1):NaCl 118,KCl 4.7,CaCl2 1.6,KH2PO4 1.2,MgSO4 1.2,NaHCO3 25,EDTA 0.026,葡萄糖5.5,用NaOH将pH调节至7.4,并将95% O2和5% CO2的混合气体持续通入其中。
1.2 仪器DMT114P离体微血管压力直径测定系统(丹麦DMT公司);FA1004型电子天平(上海天平仪器厂);XTS-20连续变倍体式显微镜(北京泰克仪器有限公司);凝胶电泳仪、电泳槽(美国BIO-RAD公司);TGL-16H超速冷冻离心机(珠海黑马仪器有限公司)。
1.3 动物健康清洁级SD大鼠,雌雄各半,体质量(180~220) g。由安徽医科大学实验动物中心提供。实验动物合格证号:scxk(皖)2017-001。实验室内饲养温度为(22±3) ℃。所用实验动物的使用均符合安徽医科大学动物伦理委员会规定。
1.4 方法 1.4.1 血管舒张实验[7]将10%水合氯醛(3 mg·kg-1)腹腔注射入大鼠,麻醉后快速取出大脑并将其置于4 ℃的含95% O2和5% CO2混合气体预饱和的PSS液中。将大鼠脑基底动脉(cerebral basilar artery, CBA)在显微镜下小心地分离出后,将其周围的结缔组织去除后制成约3 mm的血管环,最后把血管环固定在含有5 mL的PSS液浴槽内,并用DMT114P离体微血管压力直径测定系统进行测定。在这期间,将95% O2和5% CO2的混合气体持续向槽内通入,并将浴槽内的温度维持在37 ℃。由测定系统的软件控制,在30 min内将血管环内压力从10 mmHg逐渐加压至60 mmHg后平衡1 h,并且期间每15 min更换一次槽内PSS液。然后,加入终浓度为60 mmol·L-1 KCl诱导血管环收缩(血管直径的减小)。当收缩达坪值时用PSS洗脱3次,平衡10 min后,再次用KCl诱导血管环收缩,添加ACh至终浓度10 nmol·L-1诱导血管舒张。若两次收缩坪值的差异小于10%时,则认为血管稳定性较好,若ACh诱导的舒张百分率达80%以上,则认为内皮完整,若如小于20%,则认为血管在功能上去除了内皮。最后,将血管环用PSS洗脱3次,并平衡10 min后,开始正式实验。
将内皮完整性较好的血管环随机分为对照组、C3孵育组和NaHS组。在内皮完整性较好的血管环中分别加入终浓度为1×10-5 mol·L-1 C3或等体积PSS孵育30 min后,用30 mmol·L-1 KCL诱导收缩,待血管环收缩稳定后,分别向液浴槽内加入累积终浓度为1×10-6、1×10-5.5、1×10-5、1×10-4.5、1×10-4、1×10-3.5和1×10-3 mol·L-1的NaHS来诱导血管舒张(血管直径的增大),各浓度NaHS加药间隔时间为10 min(血管舒张稳定)。按下列公式计算血管舒张的百分率:
舒张百分率=(加NaHS后CBA直径-加KCl CBA后直径) /(加KCl CBA前直径-加KCl后CBA直径)×100%[8]
1.4.2 SiRNA在体转染[9]将SD大鼠随机分为正常对照(vehicle)组、EntransterTM in vivo-RNA转染试剂(transfection reagent)组、阴性siRNA(Neg-siRNA)组和ROCK1-siRNA组,每组6只,雌雄各半。将ROCK1-siRNA或Neg-siRNA用不含RNase的去离子水溶解制成终浓度为1 g·L-1溶液,然后分别在500 μL的ROCK1-siRNA溶液、Neg-siRNA溶液及EntransterTM in vivo-RNA溶液中加入500 μL的10%葡萄糖制成各相应的转染混合物。除正常对照组大鼠静脉注射1 000 μL的10%葡萄糖外,其他3组大鼠分别静脉注射1 000 μL的ROCK1-siRNA转染混合物、阴性siRNA转染混合物及EntransterTM in vivo-RNA转染混合物。转染48 h后,麻醉处死大鼠,按前述方法取出大鼠CBA,一部分CBA匀浆后-80 ℃中保存待Western blot法检测ROCK1蛋白的表达,另一部分CBA制成血管环进行血管舒张实验。
另取一批大鼠按同样方法制备ROCK2-siRNA转染大鼠,并测定脑血管中ROCK2蛋白表达和行脑血管舒张实验。
1.4.3 Western blot法[6]将保存的大鼠CBA匀浆在蛋白酶抑制剂存在下,加入1% SDS裂解缓冲液(25 mmol·L-1 Tris-HCl pH 7.6、150 mmol·L-1 NaCl、1% NP-40和1%脱氧胆酸钠)来裂解。脑血管裂解液中的蛋白含量用BCA进行测定。在10%聚丙烯酰胺凝胶中置入将含有20 μg蛋白质的裂解液后将其电泳分离,并将分离的蛋白质转移到PVDF膜上。将膜在室温下用含有5%脱脂奶粉和0.05%吐温20的Tris缓冲盐水封闭2 h后,在4 ℃下分别与抗ROCK1抗体、抗ROCK2抗体及抗β-actin抗体孵育过夜。然后在37 ℃下,加入二抗孵育1 h后,使用增强的化学发光试剂盒使条带可视化,通过测定条带光密度,以β-actin为内标来计算ROCK1、ROCK2蛋白表达的相对强度。
1.3 统计学处理采用graphpad6软件对实验数据进行分析,所有数据均以x±s来表示。两组之间比较采用t检验,两组浓度-效应曲线之间的显著性检验用单因素方差(One-way ANOVA)来分析。
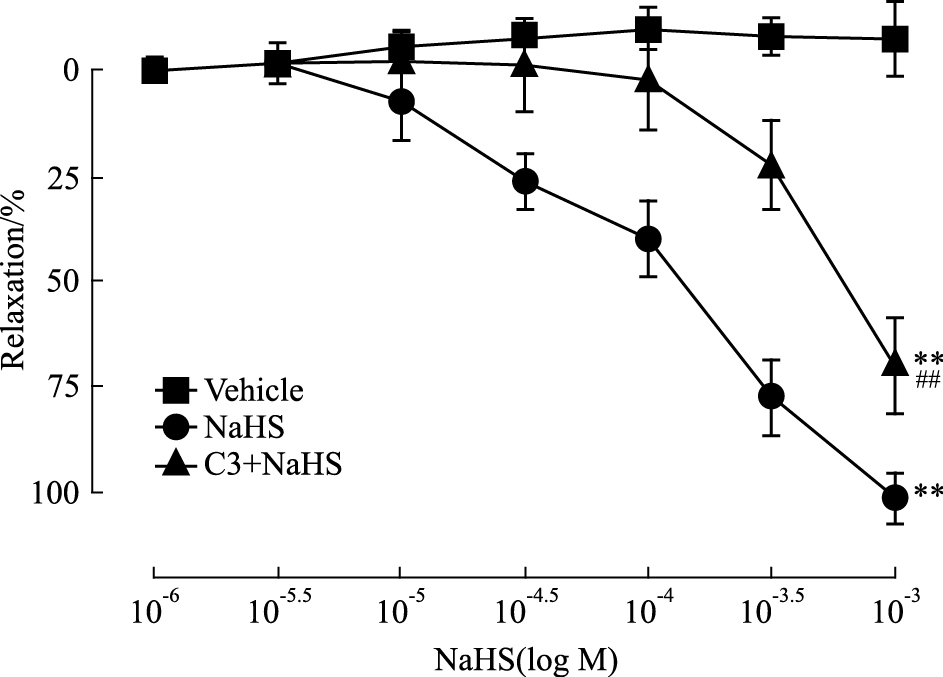
2 结果 2.1 RhoA抑制剂C3预处理对H2S诱导的大鼠CBA舒张的影响如Fig 1所示,与溶媒对照比较,H2S供体NaHS在1×10-6~1×10-3 mol·L-1范围内明显地舒张大鼠CBA(P < 0.01),并呈一定的浓度依赖性。这种舒张作用在添加血管收缩剂之前使用1×10-5 mol·L-1 C3转移酶预处理可明显地减弱NaHS诱导的大鼠CBA舒张(P < 0.01),Emax从(112.8±1.8)%降低至(64.8±1.4)%。结果表明RhoA参与了H2S诱导的大鼠BA舒张作用。
|
| Fig 1 Effect of RhoA inhibitor C3(1×10-5mol·L-1) on H2S-induced relaxation of rat cerebral basilar artery (x±s, n=6) **P < 0.01 vs vehicle; ##P < 0.01 vs NaHS |
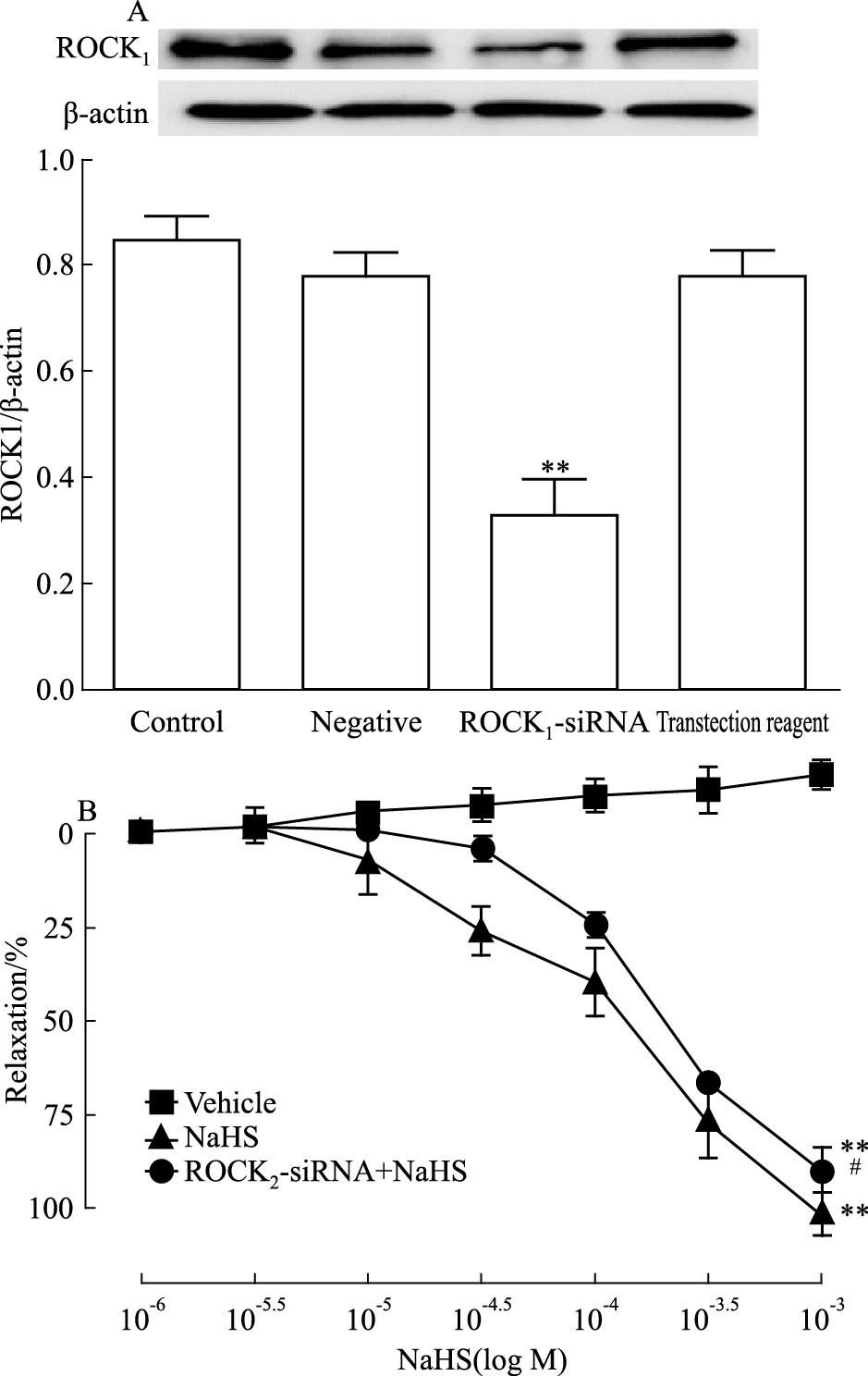
大鼠在体转染48 h后,用Western blot法测定了CBA中的ROCK1蛋白表达。如Fig 2A所示,与对照组比较,阴性siRNA组和EntransterTM in vivo-RNA转染试剂组ROCK1表达均没有明显的改变,但ROCK1-siRNA组ROCK1蛋白表达有明显的降低(P < 0.05),大约降低了60%左右。该结果表明大鼠在体转染ROCK1-siRNA可有效地减低脑血管中ROCK1蛋白的表达。
Fig 2B表明在体转染ROCK1-siRNA可明显地减弱NaHS诱导的大鼠CBA舒张(P < 0.05),Emax从(112.8±1.8)%降低至(89.7±2.4)%,提示ROCK1也参与了H2S诱导的大鼠BA舒张作用。
|
| Fig 2 Effect of transfection of ROCK1-siRNA in vivo on H2S-induced relaxation of rat cerebral basilar artery (x±s, n=6) A: Reduction in ROCK1 protein expression in the cerebral arteries from ROCK2-siRNA-transfected rats(Western blot method; B:NaHS-induced relaxations in the cerebral arteries from control rats and ROCK1-siRNA-transfected rats.**P < 0.01 vs control or vehicle; #P < 0.05 vs NaHS. |
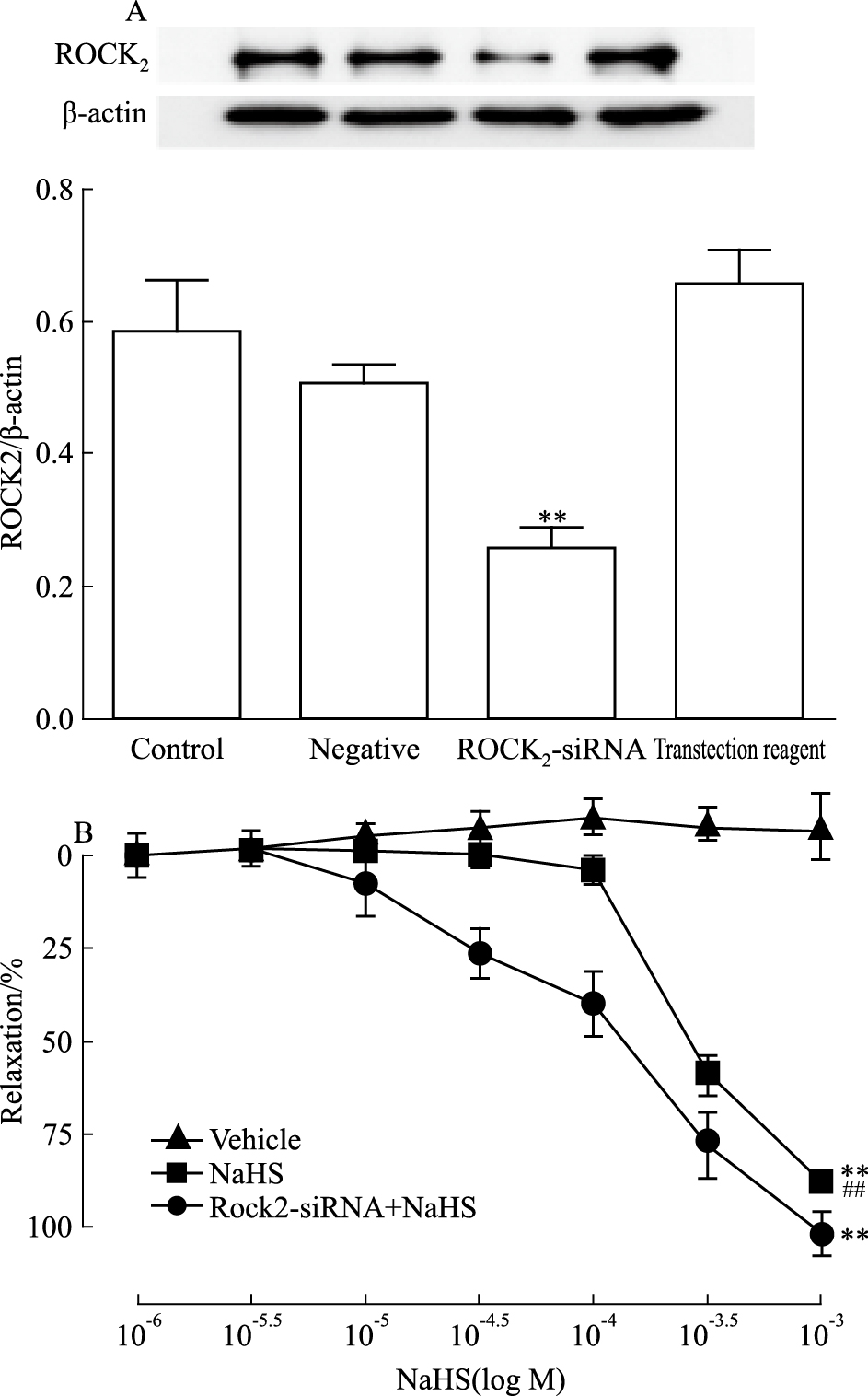
与ROCK1-siRNA转染一样,大鼠在体转染ROCK2-siRNA可有效地减低脑血管中ROCK1蛋白的表达(P < 0.01)(Fig 3A);Fig 3B表明在体转染ROCK2-siRNA也可明显地减弱NaHS诱导的大鼠CBA舒张(P < 0.01),Emax从(112.8±1.8)%降低至(87.4±2.3)%,与在转染ROCK2-siRNA转染大鼠CBA上的Emax(89.7±2.4)%无明显的差异,提示ROCK2也参与了H2S诱导的大鼠BA舒张作用。
|
| Fig 3 Effect of transfection of ROCK2-siRNA in vivo on H2S-induced relaxation of rat cerebral basilar artery A:Reduction in ROCK2 protein expression in the cerebral arteries from ROCK2-siRNA-transfected rats(x±s, n=3). B: NaHS-induced relaxations in the cerebral arteries from control rats and ROCK2-siRNA-transfected rats(x±s, n=6).**P < 0.01 vs control or vehicle; ##P < 0.01 vs NaHS. |
利用离体微血管压力直径测定法检测大鼠CBA的舒张作用,用RhoA抑制剂C3预处理后抑制RhoA活性,用siRNA转染技术在体敲低大鼠ROCK1和ROCK2表达。实验结果表明,H2S通过作用于RhoA、ROCK1和ROCK2导致RhoA-ROCK信号通路的抑制来发挥舒张大鼠脑血管作用。
3 讨论H2S对包括胸主动脉[10]、肠系膜[11]、肺[10]、肝动脉[11]及大鼠脑血管等多种血管床均有明显的舒张作用。有研究表明,H2S可通过开放ATP敏感性或钙激活钾通道,导致K+外流致平滑肌细胞发生超极化而产生血管舒张作用,但作为一种体内重要的气体信号分子,内源性H2S的血管舒张作用可能还有其他的机制。RhoA-ROCK传导通路是一种重要的细胞内信号转导机制,也参与多种血管收缩功能的调节。RhoA-ROCK传导通路的激活可使血管发生收缩,相反,该通路的抑制则可导致血管的舒张。有研究表明同样是气体信号分子的NO产生的血管舒张作用与RhoA-ROCK传导通路密切相关[11]。我们以前的研究表明,H2S也可通过抑制RhoA-ROCK传导通路来舒张大鼠脑血管[6],但其作用的确切效应分子不明确。
本研究利用RhoA抑制剂C3预处理大鼠CBA,发现NaHS的脑血管舒张作用明显地减弱,表明RhoA与H2S舒张脑血管作用有关,这与我们报道的H2S可抑制大鼠脑血管中RhoA-ROCK传导通路[6]是一致的,提示RhoA是H2S舒张大鼠脑血管作用的RhoA-ROCK传导通路抑制机制中的效应分子之一。ROCK是RhoA最主要的下游效应分子,也直接关系着RhoA-ROCK传导通路的活性。本研究通过在体转染siRNA技术,有效地降低了大鼠脑血管中ROCK1和ROCK2的表达。无论在ROCK1-siRNA转染,还是在ROCK2-siRNA转染的大鼠CBA上,NaHS舒张脑血管作用均明显地减弱,表明H2S抑制RhoA-ROCK传导通路引起的舒张脑血管作用与ROCK也有关系。
硫巯基化(S-sulfhydration)是继磷酸化、乙酰化和S-亚硝基化等之后蛋白质翻译后的一种新的修饰方式。H2S可通过对靶蛋白上的半胱氨酸残基硫巯基化修饰[12],使半胱氨酸的-SH基团转化为-SSH或过硫酸盐基团来影响靶蛋白的活性,如H2S硫巯基化KATP通道上的半胱氨酸残基可促进该通道开放[13-14]。ROCK羧基端有一个pleckstrin同源域,该域被一富含半胱氨酸残基的锌指状基序域(cysteine-rich zinc finger-like motif domain, CRD)分成两部分[15],是否H2S也可硫巯基化CRD上的半胱氨酸残基来抑制ROCK的活性?这有待于我们今后的进一步研究。
综上所述,H2S通过作用于RhoA、ROCK1和ROCK2导致RhoA-ROCK信号通路的抑制来发挥舒张大鼠脑血管作用。
| [1] |
Kamat P K, Kalani A, Tyagi N. Role ofhydrogen sulfide in brain synaptic remodeling[J]. Methods Enzymol, 2015, 555: 207-29. doi:10.1016/bs.mie.2014.11.025 |
| [2] |
Polhemus D J, Lefer D J. Emergence of hydrogen sulfide as an endogenous gaseous signaling molecule in cardiovascular disease[J]. Circ Res, 2014, 114(4): 730-37. doi:10.1161/CIRCRESAHA.114.300505 |
| [3] |
Satoh K, Fukumoto Y. Rho-kinase: important new therapeutic target in cardiovascular diseases[J]. Am J Physiol Heart Circ Physiol, 2011, 301(2): H287-96. doi:10.1152/ajpheart.00327.2011 |
| [4] |
Dongó E, Hornyák I, Benko Z. The cardioprotective potential of hydrogen sulfide in myocardial ischemia/reperfusion injury(review)[J]. Acta Physiol Hung, 2011, 98(4): 369-81. doi:10.1556/APhysiol.98.2011.4.1 |
| [5] |
Tan Z, Shi Y, Yan Y, et al. Impact of endogenous hydrogen sulfide on toll-like receptor pathway in renal ischemia/reperfusion injury in rats[J]. Ren Fail, 2015, 37(4): 727-33. doi:10.3109/0886022X.2015.1012983 |
| [6] |
Wen J Y, Gao S S, Chen F L, et al. Role of CSE-produced H2S on cerebrovascular relaxation via RhoA-ROCK inhibition and cerebral ischemia-reperfusion injury in mice[J]. ACS Chem Neurosci, 2019, 10: 1565-74. doi:10.1021/acschemneuro.8b00533 |
| [7] |
Coats P, Johnston F, MacDonald J, et al. Signalling mechanisms underlying the myogenic response in human subcutaneous resistance arteries[J]. Cardiovasc Res, 2001, 49(4): 828-37. doi:10.1016/S0008-6363(00)00314-X |
| [8] |
韩军, 程小龙, 胡坤媚. 杜鹃花总黄酮对缺血/再灌注损伤模型大鼠脑基底动脉TRPV4的作用研究[J]. 中国药理学通报, 2017, 33(5): 685-91. Han J, Cheng X L, Hu K M. Effects of rhododendron total flavonoids on TRPV4 in basal artery of rats with ischemia/reperfusion injury[J]. Chin Pharmacol Bull, 2017, 33(5): 685-91. doi:10.3969/j.issn.1001-1978.2017.05.019 |
| [9] |
Wen J Y, Wang M, Li Y N, et al. Vascular protection of hydrogen sulfide on cerebral ischemia/reperfusion injury in rats[J]. Front Neurol, 2018, 9: 779. doi:10.3389/fneur.2018.00779 |
| [10] |
Siti H N, Kamisah Y. The role of oxidative stress, antioxidants and vascular inflammation in cardiovascular disease(a review)[J]. Vascul Pharmacol, 2015, 71: 40-56. doi:10.1016/j.vph.2015.03.005 |
| [11] |
Kimura H, Shibuya N. Hydrogen sulfide is a signaling molecule and a cytoprotectant[J]. Antioxid Redox Signal, 2012, 17(1): 45-57. doi:10.1089/ars.2011.4345 |
| [12] |
Lee T M, Chung T H, Lin S Z. Endothelin receptor blockade ameliorates renal injury by inhibition of RhoA/Rho-kinase signalling in deoxycorticosterone acetate-salt hypertensive rats[J]. J Hypertens, 2014, 32(4): 795-805. doi:10.1097/HJH.0000000000000092 |
| [13] |
Kang M, Hashimoto A, Gade A. Interaction between hydrogen sulfide-induced sulfhydration and tyrosine nitration in the KATP channel complex[J]. Am J Physiol Gastrointest Liver Physiol, 2015, 308(6): G532-9. doi:10.1152/ajpgi.00281.2014 |
| [14] |
Gade A R, Kang M. Hydrogen sulfide as an allosteric modulator of ATP-sensitive potassium channels in colonic inflammation[J]. Mol Pharmacol, 2013, 83(1): 294-306. doi:10.1124/mol.112.081596 |
| [15] |
Paul B D, Snyder S H. H2S: A novel gasotransmitter that signals by sulfhydration[J]. Trends Biochem Sci, 2015, 40: 687-700. doi:10.1016/j.tibs.2015.08.007 |
| [16] |
Julian L, Olson M F. Rho-associated coiled-coil containing kinases(ROCK):Structure, regulation, and functions[J]. Small GTPases, 2014, 5(2): e29846. doi:10.4161/sgtp.29846 |

