

目前,临床上对于缺血性心脏病常用的治疗手段是恢复冠状动脉的血流,减少心肌损伤[1]。但是恢复冠状动脉血流过程其本身也会诱发心脏损伤,这一过程称为“心肌缺血/再灌注损伤”(ischemia-reperfusion,I/R)。心肌I/R损伤可能与多种因素相关,包括活性氧(ROS)的形成、细胞凋亡、钙超载与炎症反应[2]。环氧化酶(COX)又称为前列腺素内过氧化合成酶,是催化花生四烯酸转变为前列腺素的限速酶[3]。细胞膜中的磷脂在磷脂酶催化下释放花生四烯酸, 后者在环氧合酶COX催化下产生前列腺素, 分别在相应的前列腺素异构酶作用下合成PGE2[4]。目前认为,COX有两种同工酶,其中COX-2(cyclooxygenase-2)是诱导型酶,可以快速应答一系列促炎介质和细胞因子,在炎症发生的过程中扮演重要角色[5]。
硝苯地平(Nifedipine,Nif)是临床上一种常用于预防和治疗冠心病心绞痛的钙通道阻滞剂。文献报道[6],Nif对于心肌缺血再灌注损伤具有保护作用。在实验室前期研究中,我们在L-型钙通道敲除H9c2细胞上制作H/R损伤模型,通过转染COX-2-siRNA沉默COX-2基因,同时也采用COX-2特异性抑制剂NS398抑制了COX-2活性,结果表明H/R损伤明显减轻,说明COX-2参与心肌细胞H/R损伤的病理过程[7]。而关于硝苯地平是否通过抑制心脏微血管内皮细胞H/R后COX-2的高表达从而干预其损伤,目前未见有文献报道。因此,本实验通过建立CMECs H/R模型,观察Nif对COX-2所介导的细胞H/R损伤的作用及机制。
1 材料与方法 1.1 材料、试剂及主要仪器硝苯地平(Sigma-Aldrich,批号:SLBD7789V);COX-2抗体(Cayman);β-actin抗体(中杉金桥);Annexin V FITC/PI试剂盒(东仁化学,批号:NQ860);TUNEL检测试剂盒(美国Promega,批号:0000317106);IL-1βELISA试剂盒(eBioscience,批号:197250025);PGE2 ELISA试剂盒(批号:0537510);I-CAM1(Cayman,批号:P219559);流式细胞仪(Beckman);乳酸脱氢酶试剂盒(南京建成);SW-CJ-1F超净工作台(苏州净化);INVIVO2400缺氧工作站(Ruskinn);Zeiss显微镜(Beckman)。
1.2 CMECs的分离与培养采用刚出生4 d以内的SD大鼠,全身用75%乙醇进行两次全身消毒后, 仰卧位固定于操作台上(以下步骤均在超净台内完成)。开胸取心室肌,在37 ℃的条件下用眼科剪剪碎,并在0.1%的胰蛋白酶消化两到3次,每次消化5 min(在摇水浴条件下)。随后在4 ℃、1 000 r·min-1条件下离心10 min,将内皮细胞离心于离心管底部,弃上清,内皮细胞重悬于含10%胎牛血清DMEM培养基进行鉴定以及传代培养[8-9]。
1.3 内皮细胞H/R模型的建立及实验分组将离体培养的心脏微血管内皮细胞用缺氧液润洗细胞3次(缺氧液预先用高纯氮气饱和30 min),根据培养皿大小换用不同体积的缺氧液,置于Invivo 2400低氧/厌氧工作站(Ruskinn公司,英国),在1% O2、5% CO2、95% N2,37 ℃条件下制作缺氧模型,复氧时立即换用正常培养基置于细胞培养箱(5% CO2,37 ℃)条件下培养,制作H/R模型。
实验分组:H3R1组、H3R2组、H3R3组、DMSO组、Nif(10.0、1.0、0.1 μmol·L-1)组。
1.4 ELISA试剂盒、LDH试剂盒分别检测细胞上清液中IL-1β、PGE2的蛋白水平以及乳酸脱氢酶(LDH)的漏出水平将CMECs接种于6 cm的培养皿中,待细胞生长融合率达到80%以上,进行实验造模。在缺氧复氧造模结束后,使用2 mL EP管收集细胞上清复氧液,并及时放置于冰箱保存。按ELISA试剂盒说明书操作,酶联免疫吸附法测定细胞培养基中IL-1β、PGE2的蛋白水平,比色法测定LDH活性。
1.5 Annexin V-FITC/PI试剂盒检测细胞早期凋亡将CMECs传代接种6 cm的培养皿中,待细胞生长融合率达到80%以上进行造模处理。在造模结束后,用PBS洗2次,用不含EDTA的胰酶消化收集细胞于2 mL EP管, 随后在4 ℃、1 000 r·min-1条件下离心5 min,PBS冲洗2次,每次5 min,然后先加入5 μL FITC,吹打孵育,随后立即加入5 μL PI,并在室温下避光孵育10 min。使用C6流式细胞仪检测每个样本的凋亡情况。每个样本记录约10 000个细胞,使用C6检测仪自带软件对结果进行分析。
1.6 TUNEL检测细胞晚期凋亡细胞生长融合率达到80%以上时进行造模,在细胞造模结束后,首先用4%多聚甲醛(采用PBS配制)固定20 min,PBS洗3次,每次1 min;随后0.03 Triton%进行细胞打孔15分组,按照TUNEL试剂盒说明书进行染料孵育10 min。采用正置荧光显微镜(Olympus,日本)进行观察。凋亡的表达计算为随机选取的5个视野的阳性核/总核的比值。
1.7 Western blot检测细胞蛋白的表达将CMECs传代接种6 cm的培养皿中,待细胞生长融合率达到80%以上进行造模处理。在造模结束后,用PBS洗2次,每皿加入100 μL裂解液,冰上裂解30 min,随后使用离心机在12 000 r、4 ℃离心收集上清液。根据说明书,采用BCA法蛋白定量,完成后将蛋白在沸水中变性5 min,冷却后待使用。将蛋白样本进行SDS-PAGE凝胶电泳,浓缩胶跑30 min,分离胶跑75 min,随后采用湿转法将凝胶上的蛋白转移至硝酸纤维素膜,转膜时间为75 min,结束后用TBST配制5%脱脂奶粉,将条带置于奶粉中封闭1 h,封闭结束后在4 ℃条件下孵一抗过夜; d 2配置二抗在室温下孵育1 h,加入发光液,在暗室中进行曝光。Gel-pro图像分析软件分析蛋白条带的灰度值。
1.8 统计学处理采用GraphPad Prism 6软件统计分析,数据以x±s表示。组间比较采用单因素方差分析(One-way ANOVA)和t检验。
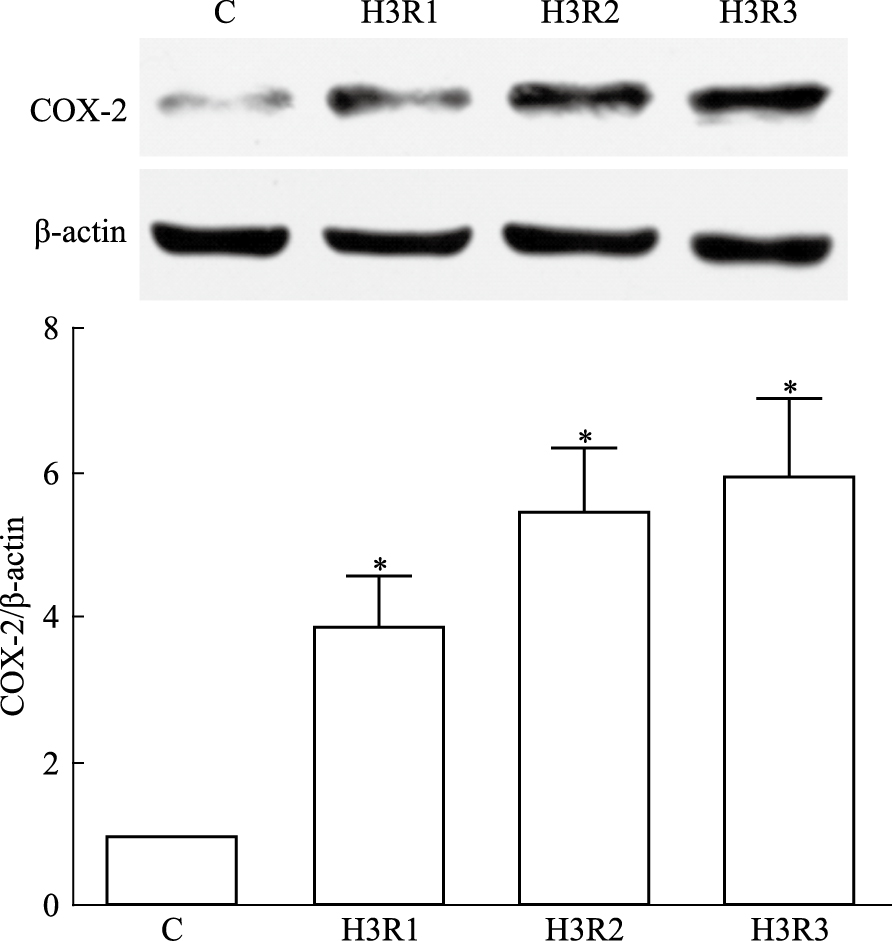
2 结果 2.1 CMECs H/R模型时间点的确立 2.1.1 CMECs H/R后COX-2蛋白表达变化如Fig 1所示,与C组相比,在H/R条件下H3h/R2h时表达最高,综合考虑CMECs在H/R不同时长下COX-2的表达趋势,确定H/R时间点为H3h/R2h。
|
| Fig 1 Changes of COX-2 proteinexpression after CMECs H/R (x±s, n=3) *P < 0.05 vs control. C: control |
如Fig 2所示,与C组相比,不同H/R时程下CMECs LDH漏出量均增高,差异具有统计学意义(P < 0.05)。

|
| Fig 2 Time effect relationship of LDHin H/R state of CMECs (x±s, n=3) *P < 0.05 vs control.C:control |
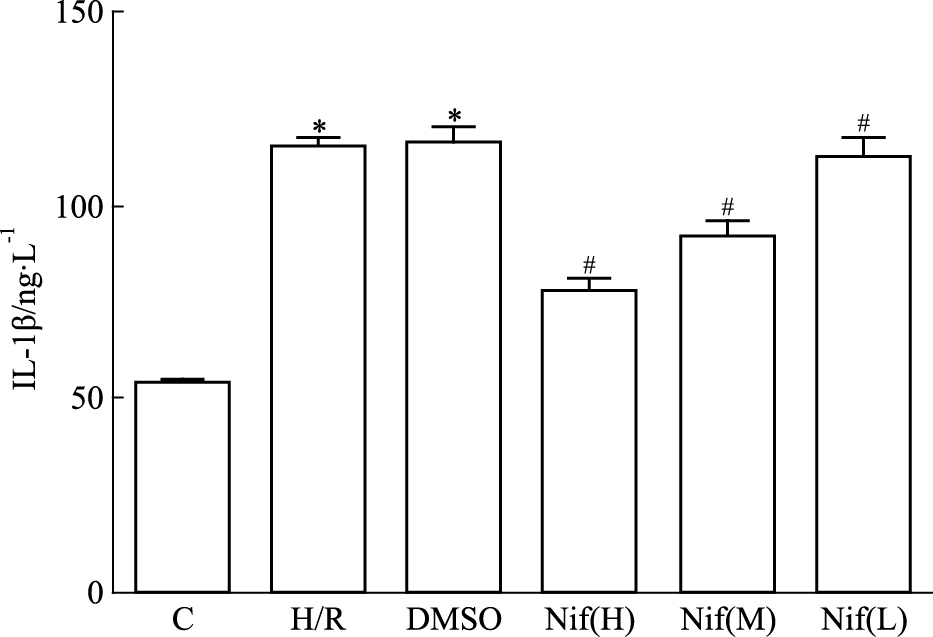
如Fig 3所示,与C组相比,造模后模型组CMECs的IL-1β的表达均增高,差异具有统计学意义(P < 0.05);与DMSO组相比,Nif(10.0、1.0、0.1 μmol·L-1)呈浓度依赖性地减少细胞的IL-1β表达,差异具有统计学意义(P < 0.05)。
|
| Fig 3 Expression of IL-1 β after H/R by Nif (x±s, n=3) C:control, H/R: hypoxia/reoxygenation; DMSO:solvent group Nif(H):Nif high concentration group, Nif(M): Nif medium concentration group, Nif(L):Nif low concentration group.*P < 0.05 vs Control group; #P < 0.05 vs DMSO group |
如Fig 4所示,与C组相比,造模后模型组CMECs的ICAM-1的表达均明显增高,差异具有统计学意义(P < 0.05);与DMSO组相比,Nif(10.0、1.0、0.1 μmol·L-1)呈浓度依赖性地减少内皮细胞的ICAM-1表达,差异具有统计学意义(P < 0.05)。

|
| Fig 4 Expression of adhesion moleculeICAM-1 after H/R by Nif (x±s, n=3) C:control, H/R:hypoxia/reoxygenation; DMSO:solvent group Nif(H):Nif high concentration group, Nif(M): Nif medium concentration group, Nif(L):Nif low concentration group.*P < 0.05 vs control group; #P < 0.05 vs H/R group |
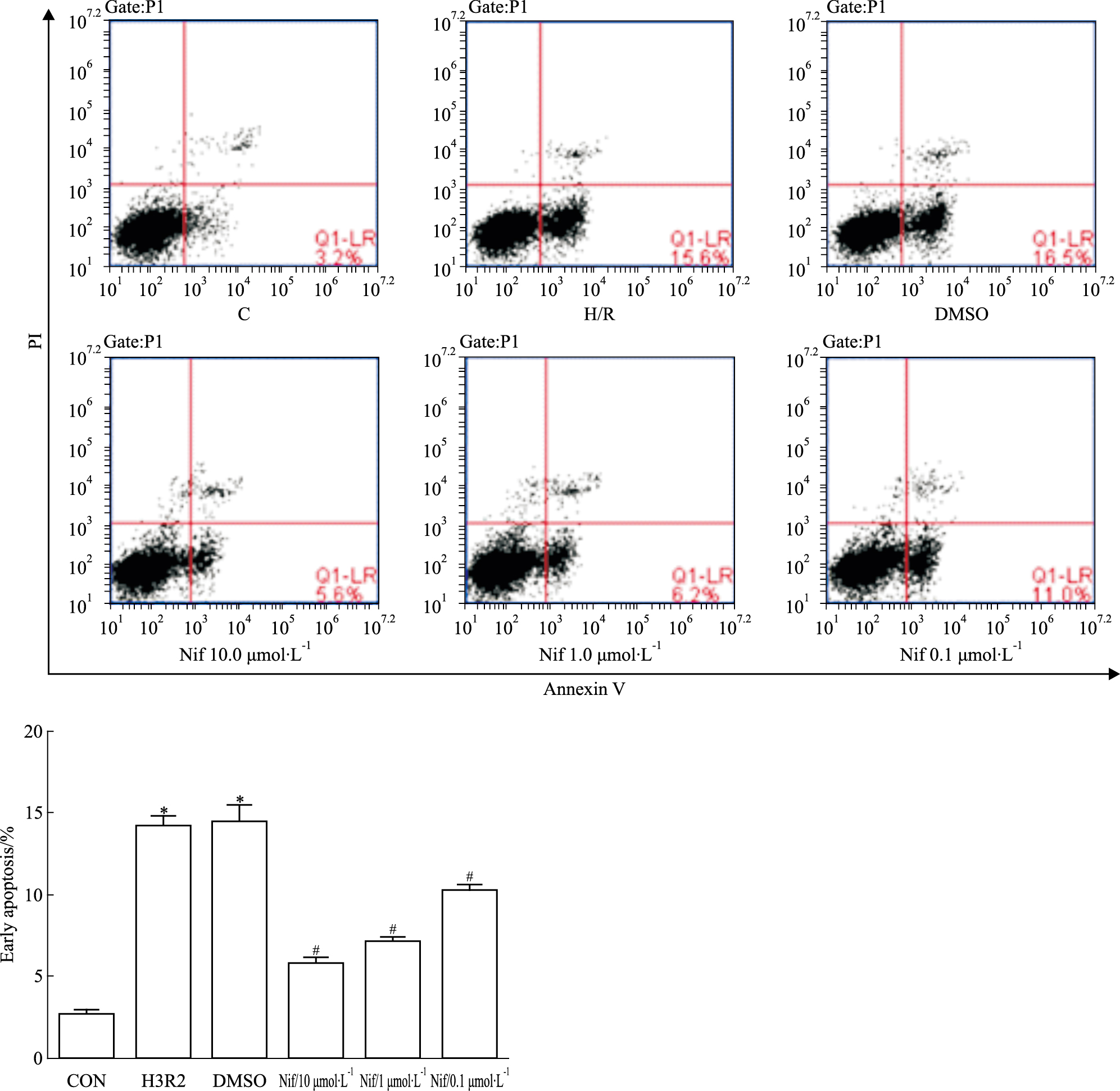
如Fig 5所示,与C组相比,H/R组与DMSO组细胞早期凋亡明显增加(P < 0.05);与DMSO组相比,Nif(10.0、1.0、0.1 μmol·L-1)呈浓度依赖地抑制细胞的早期凋亡,差异具有统计学意义(P < 0.05)。
|
| Fig 5 Annexin V FITC/PI detection of early apoptosis by flow cytometry (x±s, n=3) C:control, H/R: hypoxia/reoxygenation; DMSO:solvent group, Nif(H):Nif high concentration group, Nif(M): Nif medium concentration group, Nif(L):Nif low concentration group.*P < 0.05 vs control group; #P < 0.05 vs DMSO group |
如Fig 6所示,与C组相比,H/R组与DMSO组细胞晚期凋亡明显增加; 与DMSO组相比,Nif(10.0、1.0、0.1 μmol·L-1)呈浓度依赖性地降低细胞晚期凋亡。

|
| Fig 6 Detection of late apoptosis by TUNEL C:Control, H/R: hypoxia/reoxygenation; DMSO:solvent group Nif(H):Nif high concentration group, Nif(M): Nif medium concentration group, Nif(L):Nif low concentration group(n=1) |
如Fig 7所示,与C组相比,H/R组与DMSO组COX-2的表达明显增高(P < 0.05);与DMSO组相比,Nif(10.0、1.0、0.1 μmol·L-1)呈浓度依赖性地抑制COX-2的蛋白表达,差异具有统计学意义(P < 0.05)。

|
| Fig 7 Effect of Nif on COX-2 proteinexpression after H/R (x±s, n=3) C:control, H/R: hypoxia/reoxygenation; DMSO:solvent group Nif(H):Nif high concentration group, Nif(M): Nif medium concentration group, Nif(L):Nif low concentration group. *P < 0.05 vs control; #P < 0.05 vs DMSO group |
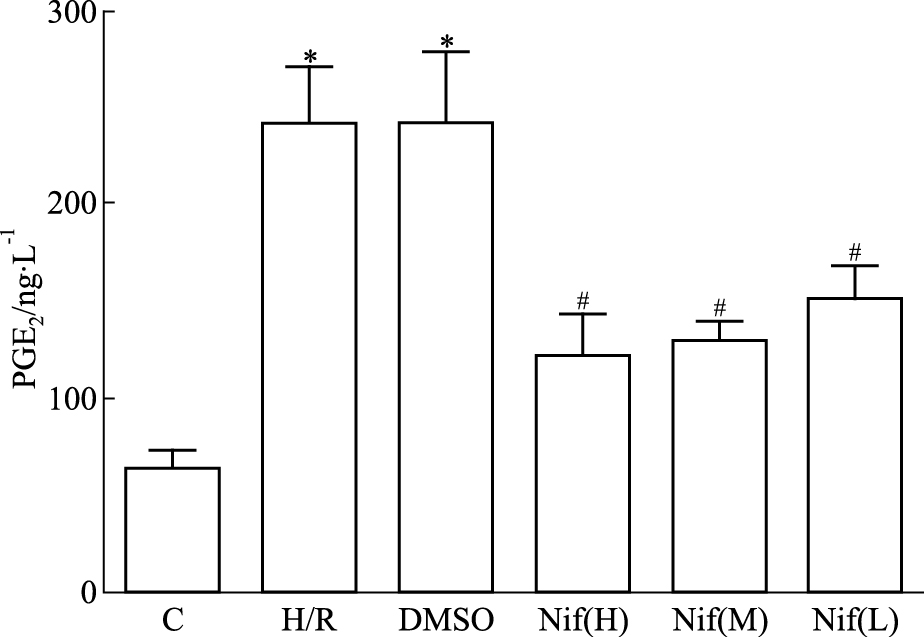
如Fig 8所示,与C组相比,H/R组与DMSO组PGE2表达明显增加(P < 0.05);与DMSO组相比,Nif(10.0、1.0、0.1 μmol·L-1)呈浓度依赖性地抑制PGE2的蛋白表达,差异具有统计学意义(P < 0.05)。
|
| Fig 8 Effect of Nif on PGE2 after H/R (x±s, n=3) C:control, H/R: hypoxia/reoxygenation; DMSO:solvent group Nif(H):Nif high concentration group, Nif(M): Nif medium concentration group, Nif(L):Nif low concentration group.*P < 0.05 vs control; #P < 0.05 vs DMSO group |
目前认为,炎性反应、凝血和血管高通透性是I/R所致心肌损伤的主要环节,在此过程中心脏微血管内皮细胞在I/R损伤中最先受累,且参与调控I/R病理生理进程。COX-2作为一个与炎症相关的经典介质,是环氧合酶COX的亚型,在大多数正常组织中表达较低,但在受到刺激时表达会明显升高[10]。根据文献报道[11],COX-2在炎症过程中主要通过前列腺素PG的合成发挥作用。其中,PGE2作为经典的促炎因子,介导的动脉扩张增强和微血管通透性增加使发炎组织的血流量增加,使炎症组织发红和水肿[12]。Nif通过抑制COX-2高表达,主要是通过减少产物PGE2的产生发挥作用,从而抑制PGE2所激发的下游瀑布式炎症效应,拮抗心肌缺血/再灌注损伤[13]。
在本实验中,我们成功分离纯化了心脏微血管内皮细胞(CMECs),通过建立CMECs H/R损伤模型,在H/R后COX-2蛋白表达明显增加,LDH漏出明显上升,细胞膜损伤加重。我们选用了缺氧3 h/复氧2 h(H3/R2)的时间点,探讨了Nif对COX-2所介导的H/R损伤发挥的作用。选用钙通道阻滞剂Nif(10.0、1.0、0.1 μmol·L-1),分别观察了内皮细胞黏附能力、炎症以及凋亡等相关指标,结果显示,Nif在H/R损伤中减轻炎症反应,减少细胞凋亡,降低COX-2的表达以及其产物PGE2的产生,拮抗H/R损伤,起到保护心肌的作用。Hempel等[14]报道,在无钙通道的内皮细胞上,Nif可通过直接抑制PKC转位减少缺血引起的内皮细胞通透性增加,保护内皮细胞缺血损伤。这也提示了Nif可能存在着非钙通道依赖地途径来发挥保护作用,而Nif是否通过非钙通道依赖地途径调节COX-2发挥保护心肌H/R损伤的作用,仍需要进一步研究及探讨。
综上所述,Nif能够保护CMECs抗心肌H/R损伤,其机制与抑制COX-2的表达有关。
( 致谢: 本文实验是在汕头大学医学院药理学教研室完成,感谢在实验过程中给予建议与帮助的老师和同学。)
| [1] |
Moran A, Forouzanfar M, Roth G, et al. The global burden of ischemic heart disease in 1990 and 2010: the Global Burden of Disease 2010 study[J]. Circulation, 2014, 129(14): 1493-501. doi:10.1161/CIRCULATIONAHA.113.004046 |
| [2] |
Ndrepepa G. Myeloperoxidase-A bridge linking inflammation and oxidative stress with cardiovascular disease[J]. Clin Chim Acta, 2019, 493(2019): 36-51. |
| [3] |
Aghaei M, Motallebnezhad M, Ghorghanlu S, et al. Targeting autophagy in cardiac ischemia/reperfusion injury: A novel therapeutic strategy[J]. J Cell Physiol, 2019, 45(3): 1-11. |
| [4] |
Abbate A, Santini D, Biondi-Zoccai G, et al. Cyclo-oxygenase-2(COX-2) expression at the site of recent myocardial infarction: friend or foe[J]. Heart, 2004, 90(4): 440-3. doi:10.1136/hrt.2003.010280 |
| [5] |
Pang L, Cai Y, Tang E, et al. Cox-2 inhibition protects against hypoxia/reoxygenation-induced cardiomyocyte apoptosis via Akt-dependent enhancement of iNOS expression[J]. Oxid Med Cell Longev, 2016, 20(16): 1-17. |
| [6] |
林朝胜, 王世贤, 孙文利, 等. 硝苯地平对缺血/再灌注心肌保护作用的病理学研究[J]. 临床与实验病理学杂志, 1996, 2(1): 19-20. Lin C S, Wang S X, Sun W L, et al. Pathological study of myocardial protective effect of nifedipine on ischemia reperfusion[J]. J Clin ExP Pathol, 1996, 2(1): 19-20. |
| [7] |
柳满, 陈润济, 蔡文峰, 等. 硝苯地平和地尔硫调控环氧合酶-2的表达和活性拮抗L型钙通道敲除H9c2细胞缺氧/复氧损伤[J]. 汕头大学医学院学报, 2019, 32(2): 70-5. Liu M, Chen R J, Cai W F, et al. Nifedipine and diltiazem ameliorate L-VDCC-/- H9c2 cells H/R injury via regulating COX-2[J]. J Shantou Univ Med Coll, 2019, 32(2): 70-5. |
| [8] |
周燕琼, 郭福晓, 贾强用, 等. 新生大鼠心脏微血管内皮细胞的分离培养及鉴定[J]. 汕头大学医学院学报, 2008, 21(3): 135-6, 139. Zhou Y Q, Guo F X, Jia Q Y, et al. Isolation, culture and identification of cardiac microvascular endothelial cellsfrom neonatal rat[J]. J Shantou Univ Med Coll, 2008, 21(3): 135-6, 139. |
| [9] |
周燕琼, 张艳美, 高分飞, 等. 碘化N-正丁基氟哌啶醇对大鼠心脏微血管内皮细胞缺氧复氧损伤保护机制的研究[J]. 中国药理学通报, 2014, 30(2): 207-11. Zhou Y Q, Zhang Y M, Gao F F, et al. N-n-butyl haloperidol iodide protects rat cardiac microvascularendothelial cells from anoxia and reoxygenation injury[J]. Chin Pharmacol Bull, 2014, 30(2): 207-11. doi:10.3969/j.issn.1001-1978.2014.02.014 |
| [10] |
Salinas G, Rangasetty U C, Uretsky B F, et al. The cycloxygenase 2(COX-2) story:it′s time to explain, not inflame[J]. J Cardiovasc Pharmacol Ther, 2007, 12(2): 98-111. doi:10.1177/1074248407301172 |
| [11] |
Sun L, Zhao M, Yang Y, et al. Acetylcholine attenuates hypoxia/reoxygenation injury by inducing mitophagy through PINK1/Parkin signal pathway in H9c2 cells[J]. J Cell Physiol, 2016, 231(5): 1171-81. doi:10.1002/jcp.25215 |
| [12] |
周巧玲, 王远航, 林泓, 等. 钙通道阻滞剂调节钙非依赖磷脂酶A2拮抗心脏微血管内皮细胞缺氧/复氧损伤的研究[J]. 中国药理学通报, 2017, 33(8): 1119-25. Zhou Q L, Wang Y H, Lin H, et al. Calcium antagonists protect cardiac microvascular endothelialcells against hypoxia/reoxygenation injury through iPLA2[J]. Chin Pharmacol Bull, 2017, 33(8): 1119-25. doi:10.3969/j.issn.1001-1978.2017.08.016 |
| [13] |
李洪涛. 环氧合酶与动脉粥样硬化[J]. 心血管病学进展, 2004, 25(1): 62-5. Li H T. The relationship between cyclooxygenase and atherosclerosis[J]. Adv Cardiovasc Dis, 2004, 25(1): 62-5. doi:10.3969/j.issn.1004-3934.2004.01.019 |
| [14] |
Hempel A, Lindschau C, Maasch C, et al. Calcium antagonists ameliorate ischemia-induced endothelial cell permeability by inhibiting protein kinase C[J]. Circulation, 1999, 99(19): 2523-9. doi:10.1161/01.CIR.99.19.2523 |

