

2. 北京中医药大学 东方医院实验中心, 北京 100078
赵永烈(1975 -), 男, 博士, 教授, 博士生导师, 研究方向:神经性疾病发病机制及药物干预, 通讯作者, E-mail:yongy3@126.com
2. Research Center ofDongfang Hospital, Beijing University ofChinese Medicine, Beijing 100078, China
偏头痛(migraine)是由神经血管系统紊乱导致的一种反复发作性神经系统疾病,属原发性头痛的一种。临床主要表现为发作性、中重度的单侧或双侧头部搏动性疼痛,一般持续4~72 h,常伴有恶心、呕吐、畏光、畏声、畏味等症状,或发作前可有先兆[1-2]。据统计,偏头痛对全世界11%成年人的身心健康造成严重损害[3]。偏头痛致残率高,2015年全球疾病负担研究报告(Global Burden of Disease studies,GBD)[4]显示,偏头痛在全球195个国家和地区的致残性疾病原因排名中位列第7位,己成为50岁以下人口的第3位致残原因。此外,偏头痛常伴发脑血管病、癫痫、抑郁等疾病,严重影响个人生活质量,制约社会经济发展。由于偏头痛病因复杂,发病机制尚不明确。近年大量研究显示降钙素基因相关肽(calcitonin gene-related peptide,CGRP)在三叉神经血管系统(trigeminal vascular system,TGVS)激活导致的偏头痛发病及病程进展过程中发挥重要作用,有望成为偏头痛治疗潜在靶点,因而受到日益关注,成为近年来偏头痛领域的研究热点。
大量研究显示[5],偏头痛与TGVS关系极为密切,TGVS的活化是偏头痛发病的关键。体内外刺激触发偏头痛启动点后,导致皮质扩散性抑制(cortical spreading depression,CSD),引发三叉神经敏化,激活TGVS,从而导致三叉神经末梢释放CGRP等血管活性物质。CGRP通过一系列级联反应介导TGVS信号转导,导致硬脑膜内肥大细胞脱颗粒和神经源性炎症,促使血管舒张,激活硬脑膜和颅内血管的三叉神经痛感神经元,引发偏头痛[6]。
CGRP是由37个氨基酸组成的神经多肽性血管活性物质,具有舒张血管,调节免疫和神经源性炎症,以及调控伤害性信息传入的功能[7-8]。因编码基因的不同,CGRP分为α-CGRP和β-CGRP两个亚型,二者功能相似。CGRP及其受体在中枢神经系统(centralnervous system,CNS)和整个TGVS中均有广泛表达[9]。CGRP受体是一种G蛋白偶联复合体,由降钙素受体样受体(calcitonin receptor-like receptor,CLR)、受体活性修饰蛋白1(receptor activity-modifying protein 1,RAMP1)和受体组分蛋白(receptor component protein,RCP)3个亚基构成[10]。
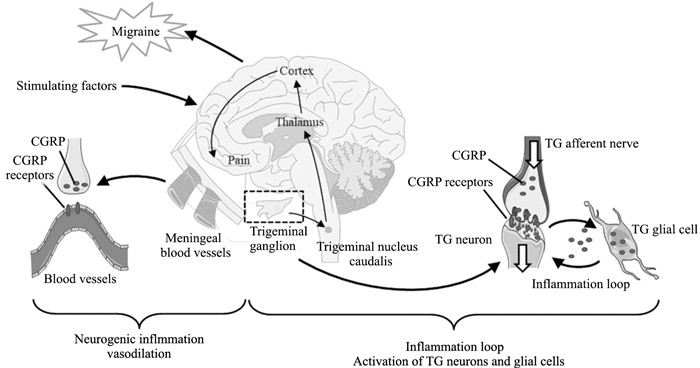
偏头痛的神经通路实现了疼痛信号从脑血管到大脑中枢的传递。体内外因素刺激后,三叉神经血管系统被激活。在脑膜中,血管(由三叉神经支配)周围传入神经释放CGRP,通过CGRP与相应受体结合发挥作用。作用于血管平滑肌CGRP受体,CGRP可介导血管舒张;作用于内皮CGRP受体,CGRP可通过介导一氧化氮(nitric oxide,NO)刺激内皮引起血管舒张;也可通过NO进一步作用于血管平滑肌细胞间接发挥舒张血管作用。在三叉神经节中,三叉神经传入神经释放CGRP,通过作用于相应受体,敏化三叉神经节神经元。三叉神经节神经元的CGRP可进一步扩散至三叉神经节胶质细胞并使其活化,神经胶质细胞反过来能够促进三叉神经节神经元中CGRP的进一步释放,形成三叉神经节中神经元-神经胶质细胞炎症环路。三叉神经节内一级神经元终末投射于三叉神经尾侧核(trigeminal nucleus caudails, TNC)。TNC神经元纤维投射到丘脑,后传递至脑的高级中枢,产生疼痛,发为偏头痛。CGRP在偏头痛三叉神经血管系统中发挥作用的机制见Fig 1。
|
| 图 1 Mechanism of CGRP in TGVS of migraine |
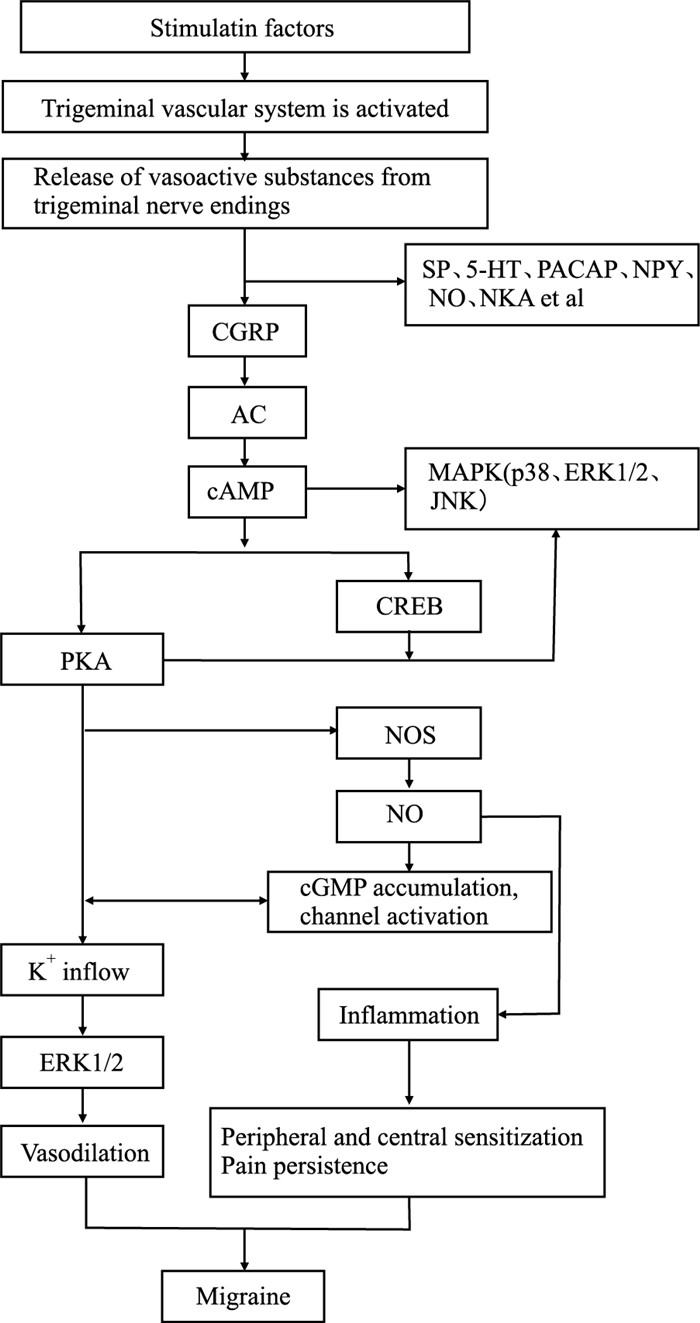
在TGVS激活导致的偏头痛中,CGRP与GTP结合蛋白α亚基(guanine nucleotide-binding protein alpha,Gαs)偶联,激活腺苷酸环化酶(adenylate cyclase, AC),上调细胞内环磷酸腺苷(cyclic adenosine monophosphate,cAMP),从而在血管平滑肌细胞、血管内皮细胞、三叉神经节神经元及神经胶质细胞中分别引发不同的信号级联反应,导致偏头痛。本文对偏头痛中CGRP在TGVS上述4种不同细胞类型中作用机制的研究进展做一综述,作用机制示意图见Fig 2。
|
| 图 2 Effects of CGRP in 4 types of cells of TGVS in migraine |
在血管平滑肌细胞中,CGRP介导cAMP表达上调后,激活蛋白激酶A(protein kinase A, PKA),从而激活ATP敏感的K+通道以增加K+内流和导致细胞外信号调节激酶1/2(extracellular regulated protein kinase 1/2,ERK1/2)活化[11]。血管内皮结构损伤时,CGRP可直接刺激血管平滑肌细胞中的AC引起cAMP升高[12]。通过对大鼠进行局部灌注α-CGRP观察基底动脉,发现CGRP能够介导cAMP激活ATP敏感性K+通道,引起血管扩张;ATP敏感性K+通道的阻滞剂可以逆转动脉平滑肌超极化,抑制α-CGRP导致的血管扩张。采用全细胞膜片钳技术研究猪冠状动脉平滑肌细胞,发现CGRP可通过促进AC、cAMP的产生与积累及PKA的活化,激活冠脉ATP敏感性K+通道,增加K+电流,引发血管扩张[13]。在临床对照研究中,Napol等[14]运用前臂灌注和体积描记技术检测血管平滑肌细胞和血管内皮细胞的反应性,结果表明CGRP介导血管内皮细胞活化后释放NO,NO直接作用于血管平滑肌细胞,诱导血管舒张。此外,血管扩张还涉及环磷酸鸟苷(cyclic guanosine monophosphate,cGMP)的活化表达。cGMP由血管平滑肌细胞产生,可导致Ca2+消耗减少和血管舒张,引起血管平滑肌细胞功能障碍,引发偏头痛患者血管反应受损[14]。
1.2 血管内皮细胞在血管内皮细胞中,CGRP介导cAMP表达上调后,激活PKA,并活化NOS,释放NO。NO一方面作用于血管内皮细胞诱导血管舒张;另一方面作用于鸟苷酸环化酶(guanylate cyclase,GC)相关的血管平滑肌细胞,导致cGMP累积和离子通道激活,促进K+内流和Ca2+外流,舒张血管[11]。在完整的血管内皮保护下,CGRP通过NO依赖机制发挥舒张血管作用[12]。通过观察CGRP对人乳腺动脉和兔冠状动脉的舒张作用,发现CGRP的血管舒张作用与内皮型NOS(endothelial nitric oxide synthase,eNOS)的激活及其NO的释放有关。Vanmolkot等[13]采用前臂灌注法对16名偏头痛患者和16名无偏头痛受试者的血管内皮细胞NO释放进行检测,发现偏头痛患者存在血管内皮功能障碍。进一步研究显示,CGRP介导人肺动脉舒张,去除血管内皮后血管舒张随之消失,表明血管舒张与血管内皮细胞释放NO具有密切关系,且呈现剂量依赖效应。此外,cAMP对eNOS的激活是由PKA介导的。cAMP能刺激eNOS活化表达,释放NO,NO进而通过作用于血管平滑肌细胞激活GC并导致cGMP表达上调,引起血管舒张[15]。
2 CGRP在三叉神经节神经细胞中的作用机制 2.1 神经元在三叉神经节神经元中,CGRP介导cAMP表达上调后,激活PKA和cAMP反应元件结合蛋白(cyclic -AMP response bin ding protein,CREB),并活化MAPK,使p38和ERK1/2表达上调[11]。有研究发现[20],向颞下颌关节注射CGRP会增加三叉神经节神经元中p38和ERK1/2的活性。Cornelison等[17]通过对成年SD大鼠脊髓上部单独注射CGRP,以及与CGRP8-37/PKA的选择性信号抑制剂KT 5720共注射, 研究CGRP在三叉神经系统内的信号传导作用及介导初级三叉神经节伤害性感受神经元的敏化过程,发现CGRP升高可促进二级神经元兴奋和神经胶质细胞激活,参与启动并维持中枢敏化和疼痛状态;CGRP升高激活PKA后,首先能够促进初级三叉神经节伤害性神经元的敏化,使三叉神经节内P-ERK升高,引发三叉神经节神经元-卫星胶质细胞偶联。Thalakoti等[18]通过将辣椒素注入大鼠颞下颌关节囊,发现辣椒素可以激活三叉神经释放CGRP,最初表现为V3神经元的激活,随后通过自分泌和旁分泌信号引起三叉神经节神经元和神经胶质细胞交叉兴奋,表现为p38MAPK表达增加;p38通路的激活又进一步促进和维持炎性疼痛。此外,通过研究辣椒素浴液激活脊髓C-纤维切片,以及通过检测新生和成年大鼠的背根神经节培养物,发现CGRP升高还可通过cAMP的活化介导CREB活化并激活CREB依赖性基因转录[19]。
2.2 神经胶质细胞在三叉神经节神经胶质细胞中,CGRP介导cAMP表达上调后,激活MAPK,p38、ERK1/2和JNK表达上调;进而增加诱导型NOS(inducible nitric oxide synthase,iNOS)的表达,导致NO的增加[11]。在中枢神经系统内,神经胶质细胞在正常情况下不表达iNOS;在缺血性、创伤性、神经毒性及炎症性损伤等各种刺激因子作用下,iNOS表达上调。研究发现[20],在神经胶质细胞富集的三叉神经节原代培养物中,CGRP能介导iNOS的活化,导致NO增加。NO还可以反过来刺激三叉神经节神经元中CGRP的活化和释放,从而形成三叉神经节神经元-神经胶质细胞炎症回路。Vause等[21]在此基础上通过检测SD大鼠的三叉神经节原代培养物,发现CGRP通过激活相应受体导致MAPK激活,并通过激活三叉神经节神经胶质细胞中CGRP受体,上调P-ERK、P-JNK和P-p38表达。此外,ERK和p38还参与了外周敏化的发展和维持。CGRP通过其受体与MAPK通路的偶联介导iNOS活化,NO及其他炎性介质的释放,其中CGRP对NO的刺激作用主要涉及p38、ERK和JNK的激活。
3 以CGRP为靶点的偏头痛治疗现状 3.1 CGRP受体拮抗剂曲普坦类药物是治疗偏头痛的一线药物,但由于其具有血管收缩作用,临床上禁用于心血管疾病患者,CGRP受体拮抗剂可以突破这一限制而具有显著优势,因而受到广泛关注,成为抗偏头痛药物研发的重要方向。CGRP受体拮抗剂能够破坏CGRP与受体的相互作用,主要用于治疗急性偏头痛,包括Olcegepant (BIBN4096BS)、Telcagepant(MK-0974)、CGRP8-37(MK-3207)、BI4370、BMS927711、Ubrogepant(MK-1602)、Rimegepant(BMS927711)、BHV-5000、CNS-penetrant(Thiazolidinones)、MK-8825、BMS-742413等。前期动物实验、Ⅰ期/Ⅱ期/Ⅲ期临床试验显示,CGRP受体拮抗剂能够有效缓解偏头痛,耐受性良好,生物利用度高。但是,Olcegepant存在制剂问题,Olcegepant、Telcagepant、MK-3207因频繁使用导致肝检异常而研发终止[22]。BI44370正在进行Ⅱ期临床试验,Ubrogepant、Rimegepant正在进行Ⅲ期临床试验。此外,BHV-5000、CNS-penetrant、MK-8825、BMS-742413均处于前期研发阶段。目前尚无CGRP受体拮抗剂正式用于临床。
3.2 针对CGRP的单克隆抗体抗CGRP单克隆抗体(CGRP mAb)可有效地对CGRP进行靶向结合,主要用于预防性治疗发作性和慢性偏头痛,因其具有明显的特异性和靶向性,是抗偏头痛治疗药物的另一个重要的研发热点。目前处于研究阶段的CGRP的单克隆抗体有LBR-101、Eptinezumab(ALD403)、Galcanezumab (LY2951742)、Erenumab(AMG334)、Fremanezumab(TEV-48125)。其中LBR-101已进行完Ⅱ期试验,其余4种均正在进行Ⅲ期试验,试验均表明CGRP mAb具有良好的耐受性,无靶外毒性,如心肝功能损害,产生的不良事件均与安慰剂组相似,是一种安全有效的预防治疗偏头痛的方法。另外,由于CGRP mAb半衰期较长,一般在20 d以上,因此给药频率低,患者依从性更高。不过,CGRP mAb在试验中未出现心肝损害,一方面可能是抗体不在肝脏中代谢的原因,另一方面可能是缺乏对心脑血管患病人群的研究[23]。而且对CGRP mAb的最佳剂量、作用部位、长期疗效以及安全性,尤其是心血管安全性,仍需要进一步研究[24],以期CGRP mAb这一重大突破减轻偏头痛带来的个人和社会负担。
综上所述,目前,偏头痛的临床药物治疗主要有非甾体类消炎药、曲坦类药物及麦角胺类药物等,但长期服用有成瘾、恶心、呕吐、胃肠道出血、心血管意外及药物性头痛等副作用,因此,以CGRP为靶点的偏头痛治疗药物可望成为未来抗偏头痛药物研发的主要方向。
| [1] |
Ashina M, Hansen J M, Do T P, et al. Migraine and the trigeminovascular system—40 years and counting[J]. Lancet Neurol, 2019, 18(8): 795-804. doi:10.1016/S1474-4422(19)30185-1 |
| [2] |
Headache Classification Committee of the International Headache Society(IHS). The international classification of headache disorders, 3rd edition[J]. Cephalalgia, 2018, 38(1): 1-211. doi:10.1177/0333102417738202 |
| [3] |
Gasparni C F, Sutherland H G, Griffiths L R. Studies on the pathophysiology and genetic basis of migraine[J]. Curr Genomics, 2013, 14(5): 300-15. doi:10.2174/13892029113149990007 |
| [4] |
Vos T, Allen C, Arora M, et al. Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990-2015: a systematic analysis for the Global Burden of Disease Study 2015[J]. Lancet, 2016, 388(10053): 1545-602. doi:10.1016/S0140-6736(16)31678-6 |
| [5] |
Iyengar S, Johnson K W, Ossipov M H, Aurora S K. CGRP and the trigeminal system in migraine[J]. Headache, 2019, 59(5): 659-81. doi:10.1111/head.13529 |
| [6] |
Kuzawińska O, Lis K, Cessak G, et al. Targeting of calcitonin gene-related peptide action as a new strategy for migraine treatment[J]. Neurol Neurochir Pol, 2016, 50(6): 463-7. doi:10.1016/j.pjnns.2016.07.012 |
| [7] |
易剑敏, 岳维, 高盼, 张伟男. rAAV9-NGF基因转染糖尿病大鼠对心脏损伤的保护作用[J]. 中国药理学通报, 2019, 35(3): 424-9. Yi J M, Yue W, Gao P, Zhang W N. Cardioprotective effect of recombinant adeno-associated virus mediated nerve growth factor gene transfection in diabetic rats[J]. Chin Pharmacol Bull, 2019, 35(3): 424-9. doi:10.3969/j.issn.1001-1978.2019.03.025 |
| [8] |
Russell F A, King R, Smillie S J, et al. Calcitonin gene-related peptide: physiology and pathophysiology[J]. Physiol Rev, 2014, 94(4): 10099-142. |
| [9] |
Miller S, Liu H, Warfvinge K, et al. Immunohistochemical localization of the calcitonin gene-related peptide binding site in the primate trigeminovascular system using functional antagonist antibodies[J]. Neuroscience, 2016, 328: 165-83. doi:10.1016/j.neuroscience.2016.04.046 |
| [10] |
张晓一, 王珍, 郭峰, 等. RCP与G蛋白偶联在静压力促血管平滑肌细胞增殖中的作用[J]. 中国药理学通报, 2017, 33(8): 1170-5. Zhang X Y, Wang Z, Guo F, et al. Interacting of receptor component protein and G protein in static pressure-induced proliferation of VSMC[J]. Chin Pharmacol Bull, 2017, 33(8): 1170-5. doi:10.3969/j.issn.1001-1978.2017.08.025 |
| [11] |
Walker C S, Hay D L. CGRP in the trigeminovascular system: a role for CGRP, adrenomedullin and amylin receptors[J]. Br J Pharmacol, 2013, 170(7): 1293-307. doi:10.1111/bph.12129 |
| [12] |
Brain S D, Grant A D. Vascular actions of calcitonin gene-related peptide and adrenomedullin[J]. Physiol Rev, 2004, 84: 903-34. doi:10.1152/physrev.00037.2003 |
| [13] |
Nelson M T, Huang Y, Brayden J E, et al. Arterial dilations in response to calcitonin gene-related peptide involve activation of K+ channels[J]. Nature, 1990, 344: 770-3. doi:10.1038/344770a0 |
| [14] |
Napoli R, Guardasole V, Zarra E, et al. Vascular smooth muscle cell dysfunction in patients with migraine[J]. Neurology, 2009, 72(24): 2111-4. doi:10.1212/WNL.0b013e3181aa53ce |
| [15] |
Butt E, Bernhardt M, Smolenski A, et al. Endothelial nitric-oxide synthase (type III) is activated and becomes calcium independent upon phosphorylation by cyclic nucleotide-dependent protein kinases[J]. J Biol Chem, 2000, 275(7): 5179-87. doi:10.1074/jbc.275.7.5179 |
| [16] |
Durham P L. Diverse physiological roles of calcitonin gene-related peptide in migraine pathology: modulation of neuronal-glial-immune cells to promote peripheral and central sensitization[J]. Curr Pain Headache Rep, 2016, 20(8): 48. doi:10.1007/s11916-016-0578-4 |
| [17] |
Cornelison L E, Hawkins J L, Durham P L. Elevated levels of calcitonin gene-related peptide in upper spinal cord promotes sensitization of primary trigeminal nociceptive neurons[J]. Neuroscience, 2016, 339: 491-501. doi:10.1016/j.neuroscience.2016.10.013 |
| [18] |
Thalakoti S, Patil V V, Damodaram S, et al. Neuror-glia signaling in trigeminal ganglion: implications for migraine pathology[J]. Headache, 2007, 47(7): 1008-25. doi:10.1111/j.1526-4610.2007.00854.x |
| [19] |
Kawasaki Y, Kohno T, Zhuang Z Y, et al. Ionotropic and metabotropic receptors, protein kinase A, protein kinase C, and Src contribute to C-fiber-induced ERK activation and cAMP response element-binding protein phosphorylation in dorsal horn neurons, leading to central sensitization[J]. J Neurosci, 2004, 24: 8310-21. doi:10.1523/JNEUROSCI.2396-04.2004 |
| [20] |
Li J, Vause C V, Durham P L. Calcitonin gene-related peptide stimulation of nitric oxide synthesis and release from trigeminal ganglion glial cells[J]. Brain Res, 2008, 1196: 22-32. doi:10.1016/j.brainres.2007.12.028 |
| [21] |
Vause C V, Durham P L. CGRP stimulation of iNOS and NO release from trigeminal ganglion glial cells involves mitogen-activated protein kinase pathways[J]. J Neurochem, 2009, 110(3): 811-21. doi:10.1111/j.1471-4159.2009.06154.x |
| [22] |
Ho T W, Connor K M, Zhang Y, et al. Randomized controlled trial of the CGRP receptor antagonist telcagepant for migraine prevention[J]. Neurology, 2014, 83(11): 958-66. doi:10.1212/WNL.0000000000000771 |
| [23] |
Tso A R, Goadsby P J. Anti-CGRP monoclonal antibodies:the next era of migraine prevention[J]. Curr Treat Options Neurol, 2017, 19(8): 27. doi:10.1007/s11940-017-0463-4 |
| [24] |
Tepper S, Ashina M, Reuter U, et al. Safety and efficacy of erenumab for preventive treatment of chronic migraine: a randomised, double-blind, placebo-controlled phase 2 trial[J]. Lancet Neurol, 2017, 16(6): 425-34. doi:10.1016/S1474-4422(17)30083-2 |

